合成水凝胶材料在组织工程中的应用
2016-04-26刘水莲李速明
刘水莲,宿 烽,李速明
(1.青岛科技大学 高性能聚合物研究院,山东 青岛266042)(2.法国蒙彼利埃二大欧洲薄膜研究院,蒙彼利埃 34095)
合成水凝胶材料在组织工程中的应用
刘水莲1,宿烽1,李速明2
(1.青岛科技大学 高性能聚合物研究院,山东 青岛266042)(2.法国蒙彼利埃二大欧洲薄膜研究院,蒙彼利埃 34095)

宿 烽
摘要:水凝胶材料因其高保湿、高吸水等特点,在组织工程、生物医药等领域具有广阔的现实意义和应用前景,特别是作为药物缓释剂、组织填充剂、酶的包埋剂、人造皮肤等方面。按原料来源分,水凝胶材料可分为天然水凝胶材料和合成水凝胶材料。尽管天然水凝胶材料的生物相容性、生物降解性优于合成水凝胶材料,但合成水凝胶材料具有相对较高的机械性能,备受研究者青睐。近年来,如何将两种类型的水凝胶材料的优点结合在一起应用成为研究热点。大量关于水凝胶材料的改性研究相继开展,并取得了一定进展。主要概述了以聚乙二醇、聚乙烯醇、聚丙烯酰胺为基础合成的水凝胶材料的研究及发展状况,并对几种水凝胶材料进行了初步生物学评价,探讨了此类水凝胶在组织工程中的应用。
关键词:合成水凝胶;生物相容性;机械性能;组织工程
1前言
水凝胶(Hydrogel)是以水为分散介质的交联聚合物,由疏水基和亲水基组成,构成一种高分子的网络体系,能吸收大量的水,但不溶解,从而保持了一定的流体形状[1]。亲水性的高分子材料通过化学或物理交联[2],均可形成水凝胶,其特点是高保湿、高吸水,被广泛应用于整容[3-4]、农业[5]、工业[6]、生物医药[7-8]、组织工程[9-11]、传感器[12-13]等领域。应用领域不同,选用的高分子原料也各异,以此满足各自的不同功用。
按原料来源不同,可将水凝胶分为天然水凝胶和合成水凝胶。天然水凝胶原料包括纤维素、壳聚糖、葡聚糖、胶原蛋白等等,以其良好的生物相容性、生物降解性受到研究者的青睐,但其力学性能较差,性能重复可靠性不好,而合成高分子水凝胶可以克服其缺点。由合成高分子制备的水凝胶不仅力学性能有很大的提高,且生物相容性也较好,近年来受到材料研究者的广泛关注。本文概述了以聚乙二醇(Poly(ethylene glycol), PEG)、聚乙烯醇(Poly(vinyl alcohol), PVA)、聚丙烯酰胺(Polyacrylamide, PAAM)为基础制备的水凝胶的研究及应用状况,探讨了此类水凝胶在组织工程中的应用。
2聚乙二醇基水凝胶
聚乙二醇(PEG)由乙二醇脱水缩聚反应得到,分子量一般在数万以下。而聚氧乙烯(Poly(ethylene oxide), PEO)则是环氧乙烷开环聚合反应制备,分子量可达数百万。二者分子链结构完全一样,仅末端基团不同。PEG末端基为羟基,而PEO末端基则取决于引发剂。PEG是一种无毒、水溶性好、生物相容性好的高分子聚合物,其末端羟基活性基团很容易发生化学反应,进行各种化学改性。由PEG制备的水凝胶,能够响应多种环境刺激(如pH、温度、磁场等的变化),被广泛应用于生物医学和药学材料等领域[14-17]。PEO水凝胶可塑性强,无免疫原性,经化学修饰后,在紫外线作用下能够从液态转为预先设定好的固态结构[18]。体内代谢研究发现该聚合物在体内能被周围组织吸收,其代谢产物经肾脏排泄出体外,是一种理想的细胞种植材料。注射植入生物体后对组织损害程度小,且治疗效果显著。Sims等[19]采用PEO水凝胶对软骨细胞进行包埋,将形成的复合物注射到裸鼠皮下培养6~12周后形成了新的软骨,说明此水凝胶的细胞相容性较好,可为细胞提供生长所需的环境。
研究者将PEG或PEO与其他高分子复合以制备性能更好的水凝胶[20-21]。PEG可以与天然高分子材料,例如壳聚糖、牛血清蛋白(BSA)、肝素等,共聚形成水凝胶。Uwe Freudenberg[22]使用星形PEG材料与肝素通过共价键交联改性,制作生物杂化水凝胶(图1)。此种水凝胶结合RGD蛋白和生长因子,可以应用于神经元细胞的替换过程,对于治疗帕金森氏病以及亨廷顿症有一定的意义。
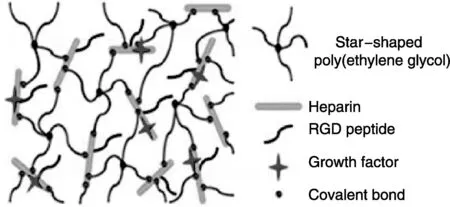
图1 以EDC/sulfo-NHS为交联剂交联星形聚乙二醇和肝素形成的生物杂化水凝胶结构示意图Fig.1 Schematic illustration of biohybrid gels formed by EDC/sulfo-NHS activated heparin with amine end-functionalized star-PEG
聚乳酸(Poly(lactic acid), PLA)是一种良好的生物可降解高分子材料,在医学上用作医用免拆外科手术缝合线、骨修复材料、人造皮肤、眼科植入材料等[23],但PLA是疏水性物质,韧性较差,研究者一般将其与其它高分子共聚成共聚物后再作研究[24-25]。李卫平等[26]以三维多孔聚乳酸/聚羟基乙酸共聚物(Poly(lactide-co-glyco-lide), PLGA)和聚氧乙烯聚丙乙烯共聚物Pluronic-F127凝胶作为支架材料,复合制备骨软骨复合物,并用裸鼠验证其可行性。2个月后有新生软骨组织形成,且形态正常、组织分布均匀,证明其可作为软骨支架材料,用于软骨组织的形成。孙俊等[27]用新型可注射温敏型聚乙二醇(PEG)、聚乳酸(PLA)和聚乙二醇(PEG),复合制备了PEG-PLA-PEG水凝胶细胞培养支架,对兔骨髓基质干细胞在体外进行三维共培养。观察细胞的形态结构,发现细胞在水凝胶中生长状况及功能检测均较为理想,细胞凋亡数目少,说明PEG-PLA-PEG水凝胶是一种良好的三维培养材料,可作为组织工程中种子细胞的载体。李宾斌[28]运用自由基共聚法接枝制备了含有IKVAV(细胞黏附多肽)的PLA/PEG水凝胶,与BMMSCs (骨髓间充质干细胞)共培养后发现,细胞的OD值呈增大趋势,细胞活力较强,说明该材料对细胞增殖有促进作用,可以作为脊髓损伤修复材料。Cui等[29]合成了聚乳酸(PLA)-聚乙二醇(PEG)-聚乳酸(PLA)立体复合物水凝胶(图2), 将这种可注射水凝胶与软骨细胞共培养后,细胞活力增强、数目增多,说明其细胞相容性好,有望成为潜在的组织工程支架材料。
尽管以聚乙二醇为基的水凝胶性质优良,但是也有其不足之处,如力学强度不够、缔合的网络结构不够稳定等,今后还需要对其进行进一步的改性研究,提高其可调控性,以期得到性能更加优良的水凝胶体系。
3聚乙烯醇基水凝胶
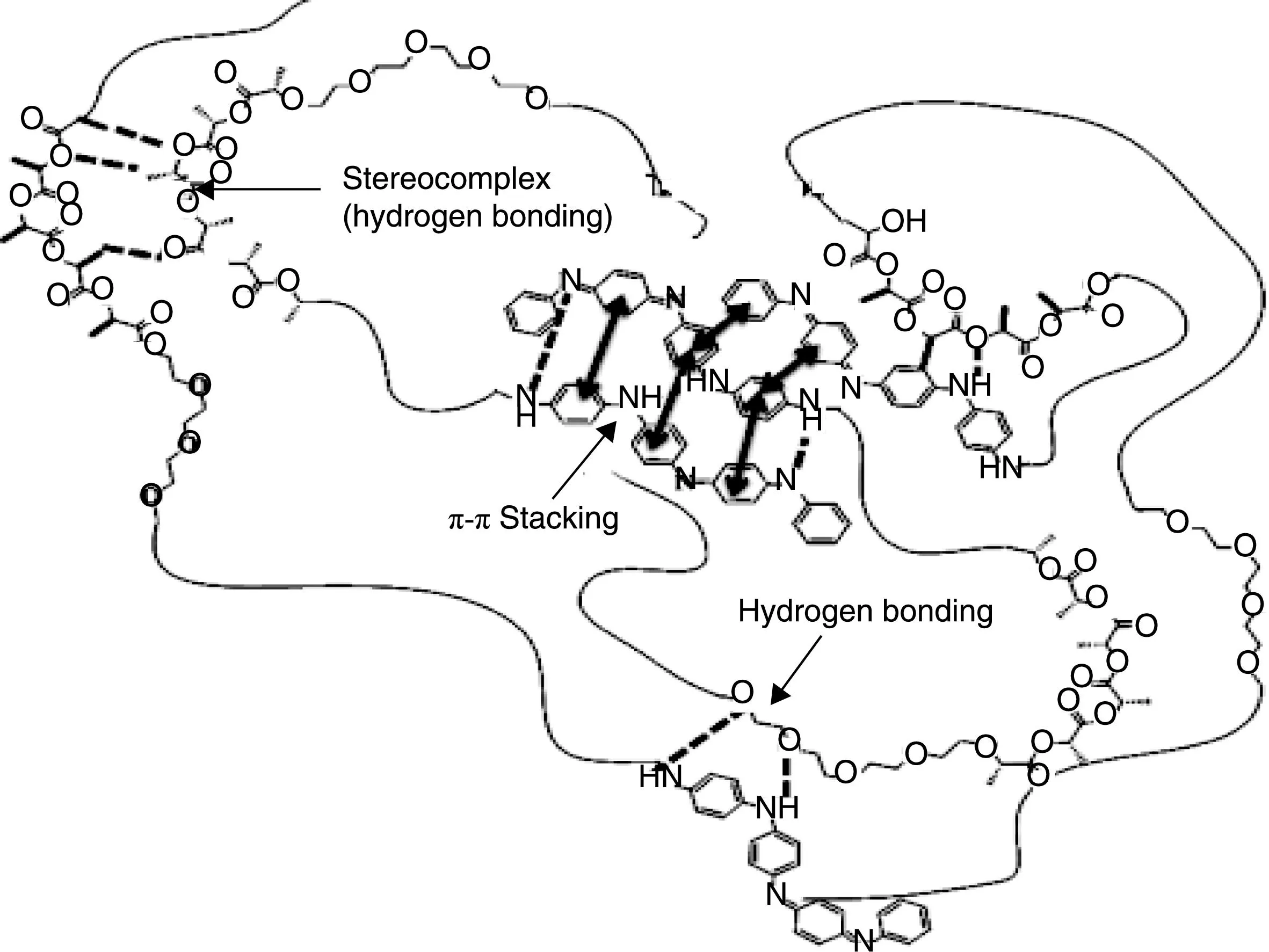
图2 共聚物分子链之间的多重交互作用示意图Fig.2 Schematic illustration of intermolecular multi-interactions between copolymer chains
聚乙烯醇(PVA)是由聚乙酸乙烯酯醇水解得到的水溶性聚合物,由于其成膜性好、乳化性高、遇热稳定等特点,被广泛应用于油田、胶粘剂、功能高分子、造纸工业等领域[30-31]。研究者利用化学交联或物理交联方法将聚乙烯醇合成水凝胶,因其具有与关节软骨相似的结构和力学性能,可作为人工软骨材料来替代病变损伤的关节软骨[32-36]。单一的PVA水凝胶力学强度低、耐用时间短,对于修复组织损伤有一定的局限性。Norihiko等[37]采用物理共混法制备了PVA/壳聚糖复合水凝胶,原有的PVA水凝胶本来就具有高弹性、高强度,由于壳聚糖的加入,复合型水凝胶具有了良好的细胞粘附性,能够促进细胞的生长。吴佳奇等[38]采用乳化发泡-冷冻干燥-去除表面活性剂工艺制备了多孔PVA、PVA/纳米羟磷灰石(Nano-hydroxyapatite, n-HA)、PVA/壳聚糖(Chitosan, CS)水凝胶,并对3种材料进行了力学性能测试、细胞毒性测试、肌肉植入实验检测材料性能和生物相容性评价,经测试,材料无细胞毒性,肌肉植入后炎症反应小且能观察到大量肌肉组织生长于材料孔隙中,而且加入n-HA和CS后材料的孔径和力学性能均有一定改变,说明这种复合水凝胶材料有望在组织工程中或作为组织填充物进一步发挥作用。Hatice等[39]用PEG作为胶凝剂,使PVA形成物理交联水凝胶网络,通过冷冻循环使AAM在PVA中聚合形成PVA-AAM半互穿网络水凝胶结构(图3),研究了其机械性能及润滑性。实验结果表明,此种水凝胶烘干物的结晶度增加,抗蠕变力加强,润滑能力提高,作为合成关节软骨的支架材料具有良好前景。为了制备修复软骨损伤的全新替代物,Shokrgozar等[40]用聚氨酯预聚物(Urethane Pre-polymer, PPU)为交联剂制备了PVA-PPU水凝胶,观察到材料与软骨细胞共培养后,细胞形态呈球形且分泌出蛋白多糖;将材料注入兔体内与自体软骨细胞培养发现,有新生软骨组织形成,结果证明在PVA-PPU上培养的软骨细胞保持了原有的形态与作用,此种水凝胶材料可以用于软骨组织工程。Jimena等[41]用冻融交联法将PVA与羟磷灰石(Hydroxyapatite, HA)交联制备了PVA/HA水凝胶,并研究了其物理、化学、机械性能,由于HA的存在,水凝胶的抗压缩强度、材料张力及硬度等性能均得到提高。结果表明,此种水凝胶可以用于修复损伤软骨。Lee等[42]采用电子束辐射交联法制备了N,O-羧甲基壳聚糖(N,O-carboxythyl Chitosan , NOCC)/PVA/PEG水凝胶支架,并对其机械性能、细胞相容性等进行了评价,该材料的孔径大小利于细胞粘附和增殖,与软骨细胞共培养后,细胞活力增强,可见NOCC的加入提高了PVA/PEG水凝胶的物理和生物两方面的特性,该材料有望作为软骨细胞生长的支架材料,应用到组织工程中。
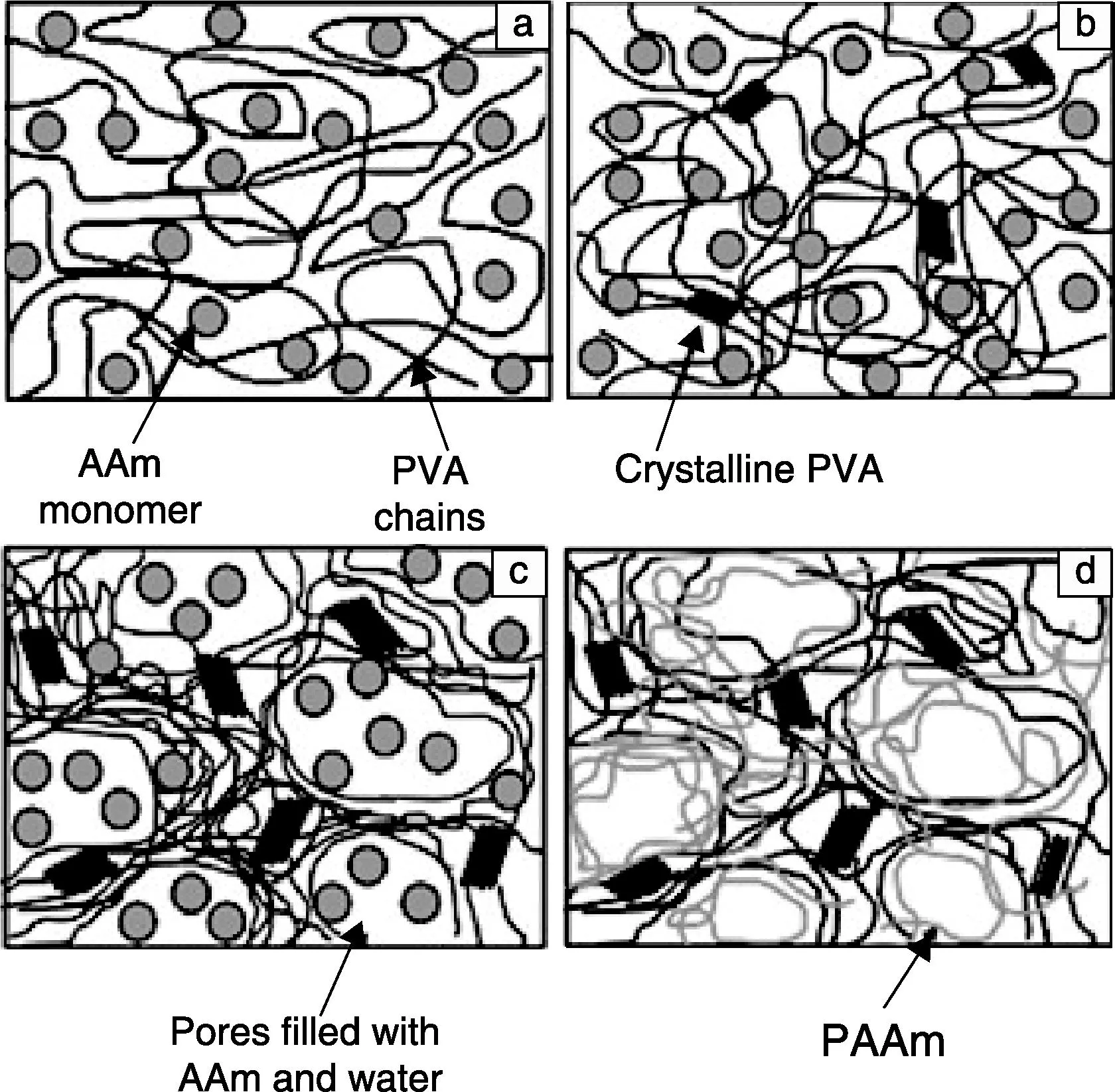
图3 PVA-AAM半互穿网络水凝胶的形成过程示意图Fig.3 Schematic illustration of PVA-AAm gel formation: (a) PVA-water mixture at 90℃ is a uniform solution, (b) as the solution is cooled down phase separation begins and forces the PVA to form crystalline domains, (c) with further cooling to near room temperature phase separation results in the formation of pores containing water and AAm monomer surrounded by PVA-rich regions and (d) the gels are heated to polymerize the PAAm in the semi-crystalline PVA host network
单一的聚乙烯醇水凝胶耐用时间短,难以满足损伤组织修复的要求,尽管研究者对聚乙烯醇做了大量改进研究,并取得一定的成果,但复合后的水凝胶的生物降解性还有待进行评价,可以通过改进制备工艺或开发新的制备技术,以便满足组织修复等临床应用的需要。
4聚丙烯酰胺基水凝胶
聚丙烯酰胺(PAAM)是丙烯腈在铜催化剂作用下,水合得到丙烯酰胺单体,然后又在引发剂K2S2O8作用下聚合而得到的水溶性高分子材料,其活性官能团较多,易通过接枝或交联得到支链或网状结构等多种改性物,被广泛应用于石油开采、水处理、造纸、医药、农业等领域[43-44]。以丙烯酰胺为单体、N, N’-二异丙基双丙烯酰胺为交联剂、过硫酸铵为引发剂交联制备的聚丙烯酰胺水凝胶,临床上作为可注射填充的硅胶材料,用于美容整形[45-46]。金宝玉等[47]对这种水凝胶材料的生物相容性进行了评价,将其与小鼠成纤维细胞株L929共培养未发现细胞溶解,细胞核膜清晰,表明无细胞毒性。将水凝胶植入豚鼠体内,短期内出现轻微炎症反应,2个月后炎症细胞明显减少,12个月后纤维细胞排列整齐,周围组织无坏死现象发生,进一步说明其组织相容性良好。由此可见,聚丙烯酰胺水凝胶是一种既安全又有效的医用可注射软组织填充材料。为了提高聚丙烯酰胺水凝胶的机械性能,拓宽其在组织工程中的应用,2012年,刘展晴[48]将聚苯胺(Polyaniline, PANI)和羧基碳纳米管(Carboxylic Multi-Walled Carbon Nanotubes, MWNTs-COOH)引入到聚(丙烯酰胺-co-甲基丙烯酸)(P(AAM-co-MAA))(图4) 网络中制备了PAAM-co-MAAPANIMWNTs-COOH新型杂合水凝胶,由于PANI的存在,此类杂合水凝胶表现出比纯聚丙烯酰胺水凝胶更好的力学性能和更强的pH敏感性(图5),有望应用于医学领域。吴贵生等[49]用共混法制备了壳聚糖/聚丙烯酰胺水凝胶,将其作为基底材料培养HepG2细胞,24 h后发现细胞粘附、正常贴壁生长,说明材料细胞相容性良好,且基底材料的硬度不同,对细胞的弹性有一定的影响,根据此种特性可以通过制备不同软硬度基底模拟体内微环境硬度变化,研究物理因素对细胞的影响,从而为临床疾病诊断提供帮助。
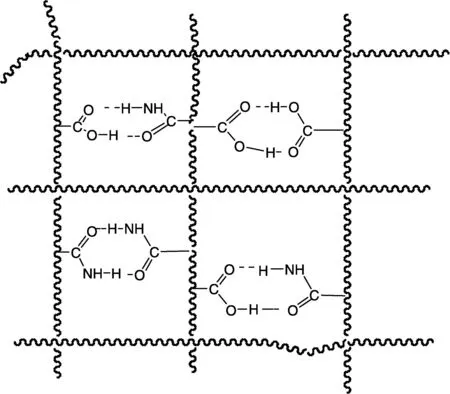
图4 PAAm和PMAA之间形成的氢键结构Fig.4 Probable structure for hydrogen bonding between PAAm and PMAA
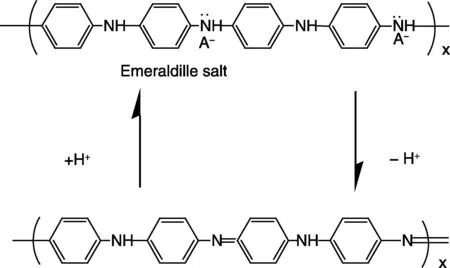
图5 PANI在酸性和碱性溶液中的质子化和去质子化机理Fig.5 Dipole-dipole interactions between PANI molecules at different acid/basic conditions
对聚丙烯酰胺进行接枝共聚后形成的水凝胶力学强度高、环境敏感性强,有望成为组织工程中的一种新型材料,从而扩展水凝胶在医学领域的应用范围。
5结语
水凝胶具有良好的生物相容性,其三维网状结构利于细胞粘附,且能促进细胞增殖分化,在修复损伤组织中起到了重要的作用。大量功能高分子经过物理或化学交联合成的水凝胶材料以其力学强度高、应用范围广泛略优于天然水凝胶材料,但是其弊端也不可避免,如生物降解速度慢,不能完全达到组织相容性等。因此,在提高水凝胶性能的同时也要考虑到其生物降解性,可以寻找性能更接近细胞外基质的材料来制备水凝胶体系。大多数研究者致力于用聚乳酸来改性材料,将水凝胶材料应用于组织工程支架、药物载体、基因载体、组织填充物等,如意大利 Pavia 大学的Asti Annalia教授[50-51]、法国蒙彼利埃二大的李速明教授[52-55]、浙江大学的高长有教授[56-58]等。生物可降解聚乳酸的加入可以明显提高材料的降解性能,使水凝胶在组织工程中发挥更好的优势,拓宽水凝胶的应用范围。随着超临界化学和点击化学的发展,水凝胶的合成速率将大幅度提升,可以在现有的基础上,继续开发利于形成水凝胶的活性官能团,利用先进的物理或化学技术诱导反应进行,通过设计优良的水凝胶合成路线,满足组织工程应用的不同需求。
参考文献References
[1]Yin Jun(殷 俊), Chen Zhaoxia(陈朝霞), Ai Shulun(艾书伦),etal.Adhesion(粘接)[J], 2013, (9): 68-73.
[2]Yu L, Ding J.ChemicalSocietyReviews[J], 2008, 37(8): 1 473-1 481.
[3]Bergeret-Galley C, Latouche X, Illouz Y G.AestheticPlasticSurgery[J], 2001, 25(4): 249-255.
[4]Lu Kaihua(鲁开化), Zhou Zhi(周 智), Cao Jingmin(曹景敏).ChineseJournalofAestheticMedicine(中国美容医学) [J], 2001, 10(1): 54-57.
[5]Yao Yue(姚 越), Wu Jinggui(吴景贵).Science&TechnologyInformation(科技信息) [J], 2012(6):19.
[6]Niladri R, Nabanita S, Takeshi K,etal.ChinaPrintingandPackaging(中国印刷与包装研究)[J], 2013, (4): 128-132.
[7]Zhang Y, Wu X, Han Y,etal.IntJPharm[J], 2010, 386(1-2):15-22.
[8]Zhang L, Wang L, Guo B L,etal.CarbohydratePolymers[J], 2014, 103: 110-118.
[9]Drury J L, Mooney D J.Biomaterials[J], 2003, 24(24): 4 337-4 351.
[10]Backdahl H, Esguerra M, Delbro D,etal.JournalofTissueEngineeringandRegenerativeMedicine[J], 2008, 2(6): 320-330.
[11]Chung T W, Yang J, Akaike T,etal.Biomaterials[J], 2002, 23(14): 2 827-2 834.
[12]Cai Z, Zhang J T, Xue F,etal.AnalyticalChemistry[J], 2014, 86(10): 4 840.
[13]Buenger D, Topuz F, Groll J.ProgressinPolymerScience[J], 2012, 37(12): 1 678-1 719.
[14]Qiao Congde(乔从德).PolymerBulletin(高分子通报) [J], 2010, (3): 23-30.
[15]Zhang Zheng(张 正).ThesisforDoctorate(博士论文) [D]. Shanghai: Fudan University, 2011.
[16]Singh N K, Lee D S.JournalofControlledRelease[J], 2014, 193: 214-227.
[17]Lee D S, Dayananda K, Kim B S. US, 08586087[P]. 2013-11-19.
[18]Zheng Xiaofei(郑小飞).ForeignMedical:BasicQuestionBookletTraumaandSurgery(国外医学: 创伤与外科基本问题分册) [J], 1999, 20(3): 129-132.
[19]Sims D C, Butler P E M, Casanova R,etal.PlasticandReconstructiveSurgery[J], 1996, 98(5): 843-850.
[20]Van Vlierberghe S, Dubruel P, Schacht E.Biomacromolecules[J], 2011, 12(5): 1 387-1 408.
[21]Ali S, Cuchiara M L, West J L. Micropatterning of Poly(Ethylene glycol) Diacrylate Hydrogels[M]//PIEL M, THERY M.MicropatterninginCellBiology,PartC. San Diego:Elsevier Academic Press Inc, 2014: 105-119.
[22]Freudenberg U, Hermann A, Welzel P B,etal.Biomaterials[J], 2009, 30(28): 5 049-5 060.
[23]Chen Youning(陈佑宁), Yang Xiaoling(杨小玲).ChemicalIntermediate(化工中间体) [J], 2009, (5): 9-12.
[24]Alexander A, Ajazuddin, Khan J,etal.JournalofControlledRelease[J], 2013, 172(3): 715-729.
[25]Hao Hong(郝 红), Wang Junlian(王君莲), Lin Genyao(林根尧).JournalofChemicalEngineeringofChineseUniversities(高校化学工程学报) [J], 2014, 28(5): 1 126-1 131.
[26]Li Weiping(李卫平), Dai Liang(代 亮), Song Bin(宋 斌),etal.China’sTissueEngineeringResearchandClinicalRehabilitation(中国组织工程研究与临床康复)[J], 2008, (27): 5 352-5 356.
[27]Sun Jun(孙 俊), Xu Hongzhen(徐红珍), Su Jiansheng(苏俭生).JournalofTongjiUniversity(MedicalEdition)(同济大学学报(医学版)) [J], 2010, 31(6): 23-27.
[28]Li Binbin(李宾斌).ThesisforDoctorate(博士论文) [D]. Wuhan: Wuhan University of Technology, 2012.
[29]Cui H T, Shao J, Wang Y,etal.Biomacromolecules[J], 2013, 14(6): 1 904-1 912.
[30]He Jianchuan(何建川), Shao Yang(邵 阳), Jiang Bo(江 波),etal.MedicalJournalofWestChina(西部医学)[J], 2009, 21(12): 2 174-2 176.
[31]Xu Ling(徐 玲), Huang Yanfei(黄妍斐), Xu Jiazhuang(徐家壮),etal.MaterialsChina(中国材料进展) [J], 2014, 33(4): 244-254.
[32]Grant C, Twigg P, Egan A,etal.BiotechnologyProgress[J], 2006, 22(5): 1 400-1 406.
[33]Oka M, Noguchi T, Kumar P,etal.ClinicalMaterials[J], 1990, 6(4): 361-381.
[34]Noguchi T, Yamamuro T, Oka M,etal.JournalofAppliedBiomaterials[J], 1991, 2(2): 101-107.
[35]Meng Haoye(孟昊业), Zheng Yudong(郑裕东), Huang Xiaoshan(黄小山),etal.JournalofBiomedicalEngineering(生物医学工程学杂志) [J], 2010, (5): 1 056-1 061.
[36]Liu Qing(刘 青).JournalofBiomedicalEngineering(生物医学工程学杂志) [J], 2003, 20(4): 742-745.
[37]Minoura N, Koyano T, Koshizaki N,etal.MaterialsScienceandEngineering:C[J], 1998, 6(4): 275-280.
[38]Wu Jiaqi(吴佳奇), Liu Yang(刘 洋), Yang Tianfu(杨天府),etal.JournalofSichuanUniversity(MedicalScienceEdition)(四川大学学报(医学版)) [J], 2007, 38(4): 705-708+724.
[39]Bodugoz-Senturk H, Macias C E, Kung J H,etal.Biomaterials[J], 2009, 30(4): 589-596.
[40]Shokrgozar M, Bonakdar S, Dehghan M,etal.JournalofMaterialsScience:MaterialsinMedicine[J], 2013, 24(10): 2 449-2 460.
[41]Gonzalez J S, Alvarez V A.JournaloftheMechanicalBehaviorofBiomedicalMaterials[J], 2014, 34: 47-56.
[42]Lee S Y, Kamarul T.IntJBiolMacromol[J], 2014, 64: 115-122.
[43]Mao Xin(毛 欣), Nie Yaling(聂雅玲).TianjinChemicalIndustry(天津化工) [J], 2007, 21(6): 39-41.
[44]Liu Jianping(刘建平), Wang Xuefang(王雪芳), Yang Xiaomin(杨小敏).ChemicalEngineer(化学工程师) [J], 2010, 179(8): 26-28+46.
[45]Jin Lanji(金兰姬), Li Jingyun(李京云), Jin Shunji(金顺吉),etal.JournalofMedicalScienceYanbianUniversity(延边大学医学学报) [J], 2002, 25(2): 127-129.
[46]Zhang Yuanlong(张元龙), Luo Qi(罗 奇).JournalofPracticalAestheticandPlasticSurgery(实用美容整形外科杂志) [J], 2002, 13(6): 308-310.
[47]Jin Baoyu(金宝玉), Cao Mengjun(曹孟君), Liu Boze(刘伯则),etal.JournalofPracticalAestheticandPlasticSurgery(实用美容整形外科杂志) [J], 2001, 12(5): 268-270.
[48]Liu Z.MaterialsReview[J], 2012, 26(7B): 73-76.
[49]Wu G, Ye Z.JournalofFunctionalMaterials[J], 2013, 44(20): 2 949-2 953.
[50]Asti A, Gastaldi G, Dorati R,etal.BioinorganicChemistryandApplications[J], 2010.
[51]Asti A, Gioglio L.IntJArtifOrgans[J], 2014, 37(3): 187-205.
[52]Wei Jia(韦 嘉), Zhang Yan(张 彦), Li Suming(李速明). 生物可吸收水凝胶的流变行为和药物释放研究[C]//ProceedingsoftheChinaPolymerScienceMeeting2007.Chengdu:2007.
[53]Hu Y, Liu Y, Qi X,etal.PolymerInternational[J], 2012, 61(1): 74-81.
[54]Li S M, Ghzaoui AE, Dewinck E.MacromolecularSymposia[J], 2005, 222(1): 23-36.
[55]Gong Yihong(龚逸鸿), Gao Changyou(高长有), He Lijuan(何丽娟),etal. 负载水凝胶聚乳酸多孔支架在软骨组织工程中的应用[C]//ProceedingsoftheSixthMemberCongressandAcademicMeetingoftheBiomedicalEngineeringSocietyofChina(中国生物医学工程学会第六次会员代表大会暨学术会议).Wuhan: 2004.
[56]Hong Y, Song H, Gong Y,etal.ActaBiomaterialia[J], 2007, 3(1): 23-31.
[57]Hong Y, Mao Z, Wang H,etal.JournalofBiomedicalMaterialsResearchPartA[J], 2006, 79A(4): 913-922.
(编辑惠琼)
《青年园地》特约撰稿人

撰稿人刘 刚
刘刚:男,1975年生,教授,博导,德国洪堡学者,西安交通大学腾飞特聘教授。2002于西安交通大学材料学院获博士学位,2003~2005在清华大学材料系进行博士后研究工作,2005年被聘为西安交通大学材料学院副教授,2008年晋升为教授,2006年入选教育部“新世纪优秀人才支持计划”,2008~2009受德国洪堡基金资助,在莱布尼兹固体材料研究所(IFW-Dresden)从事科研工作,获国家自然科学基金委优秀青年基金,陕西省中青年科技创新领军人才,西安交通大学青年拔尖人才。研究领域主要有非均质金属材料的强韧化与变形断裂,时效铝合金强韧化与微观组织调控,金属薄膜/多层膜材料的力学性能表征。已在NatureMaterials、PhysicalReviewLetters等期刊发表论文100余篇,SCI他引1 700余次。获得授权国家发明专利16项,参与编写英文书籍一部。先后主持国家自然科学基金青年和面上项目4项、国家自然科学基金优秀青年基金1项、863重点项目课题1项、973专题1项、教育部新世纪优秀人才支持项目和博士点基金博导类项目等国家级科研项目,并以研究骨干的身份参加了“973”项目以及国家自然科学基金重点项目的研究。荣获2012年度教育部技术发明一等奖1项和2013年度国家技术发明二等奖1项。主要研究方向为高性能铝合金、钼合金和金属薄膜/多层膜材料的微观组织调控和强韧化设计。

撰稿人李洪义
李洪义:男,1977年生,副教授,硕士生导师,北京工业大学金属材料系副系主任。2006年于清华大学获博士学位,在MIT做为期1年的访问学者,2015年入选首届“北京市高层次创新人才计划”青年拔尖人才。2014年入选北京市市属高等学校高层次人才引进与培养三年行动计划青年拔尖人才。兼任国家基金委通讯评审专家,美国材料研究学会(MRS)会员等,以及ChemicalSocietyReviews等期刊审稿人。主要从事金属材料表面改性的研究和教学工作,通过在种植体表面组装金属氧化物纳米管阵列,显著提高了种植体的生物相容性;在金属基柔性太阳能电池、燃料电池用新型铂电极的研究方面取得了重要进展。主持国家自然科学基金、北京市教委科技计划项目等重要课题10余项,在Biomaterials、NanoResearch等发表论文近百篇,其中SCI收录80余篇,特邀报告及SCI等他引近500次;获教育部技术发明奖1项,国家级精品课程骨干成员,申请国家发明专利30余项,已授权15项。主要研究方向:阀金属的阳极氧化;染料敏化太阳能电池、燃料电池用关键材料;种植体表面改性及生物相容性。
Applications of Synthetic Hydrogels in Tissue Engineering
LIU Shuilian1, SU Feng1,LI Suming2
(1.Institute of High Performance Polymers, Qingdao University of Science and Technology, Qingdao 266042,China)( 2.Institut Europeen des Membranes, UMR CNRS 5635, Universite Montpellier II, Montpellier 34095)
Abstract:Hydrogels have practical significance and broad application prospects in the field of tissue engineering , biomedicine, etc., especially as drug delivery agents, tissue filling agent, enzyme-embedding agent and artificial skin, because of their high moisturizing ability and high water absorption. It can be divided into two types according to their raw material source, natural hydrogels and synthetic hydrogels. Although natural hydrogels have better biocompatibility, biodegradability than synthetic hydrogels, synthetic hydrogel materials have relatively high mechanical properties that attract researchers’ eyes. In recent years, it has become a research hotpot to combine the benefits of two types. A lot of researches on modification of hydrogels have emerged one after another, and some progress has made. This paper reviews the researches, development, biological evaluation of synthetic hydrogels based on poly(ethylene glycol), poly(vinyl alcohol), and polyacrylamide. Peculiar attention is paid to the applications in tissue engineering.
Key words:synthetic hydrogel; biocompatibility; mechanical properties; tissue engineering
中图分类号:R318.0+8
文献标识码:A
文章编号:1674-3962(2016)03-0227-06
DOI:10.7502/j.issn.1674-3962.2016.03.09
通讯作者:宿烽,女,1965年生,博士,副教授,硕士生导师,Email:qdkdsufeng@hotmail.com
收稿日期:2014-11-13
第一作者:刘水莲,女,1989年生,硕士研究生
