亚硒酸盐在不同理化性质土壤中运移规律研究
2016-04-21刘冠男孙春美李德先刘新会
刘冠男,薛 薇,孙春美,李德先,刘新会
(1.中国地质科学院矿产资源研究所,北京100037;2.北京师范大学环境学院,水环境模拟国家重点实验室,北京100875;3.北京化工大学化学工程学院,北京100029)
亚硒酸盐在不同理化性质土壤中运移规律研究
刘冠男1,2,薛薇2,孙春美1,3,李德先1,刘新会2
(1.中国地质科学院矿产资源研究所,北京100037;2.北京师范大学环境学院,水环境模拟国家重点实验室,北京100875;3.北京化工大学化学工程学院,北京100029)
摘要:通过亚硒酸盐在江西丰城稻田表层0~10 cm土壤(FC1)、次表层10~20 cm土壤(FC2)、江西德兴菜地表层土壤(DC)、河北保定旱地表层土壤(BD)等几种土壤中的吸附解吸及土柱运移实验,研究了亚硒酸盐在土壤中的运移行为,探讨了亚硒酸盐在不同理化性质土壤中的运移规律。结果表明:具有较高含量活性Fe及有机质(OM)和较低pH值的FC1和FC2土壤对亚硒酸盐的吸附能力较强,其次为DC土壤和BD土壤,其最大吸附量分别为621.50、592.20、219.29、163.51 mg·kg(-1),且吸附能力最弱的BD土壤具有较高的亚硒酸盐解吸率和解吸量;亚硒酸盐在BD土壤填装土柱中运移速度最快,且在其他研究土壤中运移速度较慢,表明土壤对亚硒酸盐的吸附解吸能力控制着其在填装土柱中的运移速率。此外,江西丰城原状土柱中亚硒酸盐运移实验表明,原状土柱中亚硒酸盐的运移速度明显较填装土柱快,且其穿透曲线用HYDRUS-1D软件中双孔-两点吸附模型拟合结果较好,表明真实土壤环境中由于大孔径和优势流的存在,硒(Se)可能运移更快,进而污染地下水。
关键词:土壤;硒;吸附;解吸;运移
刘冠男,薛薇,孙春美,等.亚硒酸盐在不同理化性质土壤中运移规律研究[J].农业环境科学学报, 2016, 35(3):485-491.
LIU Guan-nan, XUE Wei, SUN Chun-mei, et al. Selenite transport in soils with various physico-chemical properties[J]. Journal of Agro-Environment Science, 2016, 35(3): 485-491.
重金属、有机污染物等有害物质在土壤中的运移可能导致地下水污染,进而对人体健康产生危害[1-3];而污染物在土壤上的吸附解吸是土壤污染物的重要环境行为,并影响其在土壤介质中的运移。因此,对污染物在土壤中的吸附解吸以及运移规律的研究,有助于了解其在土壤中的环境行为,对土壤污染防治和环境管理具有重要意义。
硒(Se)是人体所必需的微量元素之一,缺Se可能会导致一系列的疾病,如克山病、大骨节病等,并与癌症、心血管疾病、高血压等有密切关系[4-5];而摄入高含量的Se可导致Se中毒,亦会对人体造成一定的危害[4,6-7]。亚硒酸盐是Se在土壤中常见的存在形态,而以往对于亚硒酸盐在土壤中的运移研究,尤其是对其在原状土柱中的运移研究相对较少。研究亚硒酸盐在土壤中的吸附解吸以及在土壤中运移规律,对了解Se元素在实际土壤中的环境行为具有重要意义。
1 材料与方法
1.1实验材料
位于江西省中部的丰城富Se土壤资源丰富,被称为“中国生态硒谷”,实验所用土壤样品主要采集于江西丰城稻田表层0~10 cm(FC1)、次表层10~20 cm (FC2)土壤。为了比较亚硒酸盐在不同理化性质土壤中的环境行为,又采集了河北保定旱地表层土壤(BD)以及江西德兴菜地表层土壤(DC)。其中FC1、FC2和DC土壤为红壤,BD土壤为潮土。采集的土样混匀后运回实验室,自然风干,过2 mm筛,备用。用长20 cm、内径9 cm的有机玻璃柱采集江西丰城稻田原状土柱,具体操作为:将有机玻璃柱直接插入土壤中(土柱长15 cm),并用铁锹挖出,削平土柱底部,用密封袋封好,带回实验室4℃下保存。几种土壤理化性质如表1所示。
1.2几种土壤对亚硒酸盐的吸附解吸实验
对几种土壤分别进行亚硒酸盐吸附解吸实验。具体实验方法为:称取土样3 g于50 mL离心管中,加入配制好的一定量Na2SeO3溶液(1 g·L-1),并稀释到40 mL使溶液Se含量为5~400 mg·L-1。背景溶液为0.1 mol·L-1的NaCl。配置好的溶液在室温25℃下振荡24 h,然后在5000 r·min-1下离心15 min,上清液过0.45 μm的滤膜并用原子荧光光度计(AFS;AFS-9760海光仪器有限公司,北京)测定其中Se含量。吸附实验完毕后,将上清液缓慢倒掉,然后加入40 mL去离子水,在室温下振荡24 h,振荡结束后在5000 r· min-1下离心15 min,上清液过0.45 μm的滤膜并用AFS测定其中Se含量。
分别用Langmuir和Freundlich模型对等温吸附曲线进行拟合,得到相应的分配系数和吸附量等参数,具体方程为:

式中:Q为吸附量,g·kg-1;Ce为平衡浓度,mg·L-1;Qmax为最大吸附量,g·kg-1;KL为Langmuir吸附分配系数,L·kg-1;KF为Freundich吸附分配系数,Ln·mg1-n·kg-1;n 为Freundich吸附模型的指数因子。
1.3亚硒酸盐在填装土柱中的运移
称取一定重量的土样,均匀填装到直径为25 mm、长度为50 mm的色谱玻璃柱中,使土柱的容重为1.3 g·cm-3,土柱两端放有200目的尼龙滤膜防止大颗粒土壤流失。用蠕动泵(DHL-A,上海青浦沪西仪器厂,上海)提供动力,首先将背景离子强度为0.01 mol·L-1的NaCl溶液以0.05 mL·min-1的速度从土柱底部饱和土柱,然后调节土柱流速为0.2 mL·min-1,当土柱流速稳定后,将约2孔隙体积(PV,约65 mL)的含有10 mg·L-1Se的Na2SeO3从下向上冲入土柱。用部分收集器(CBS-A,上海青浦沪西仪器厂,上海)每40 mL收集一管样品,淋出液过0.45 μm滤膜后,测定其中Se含量。

表1 土壤理化性质Table 1 Soil physico-chemical properties
1.4亚硒酸盐在饱和原状土柱中的运移
原状土柱长15 cm、内径9 cm,土柱底部用200目的尼龙膜包裹,防止大颗粒土壤流失。将土柱浸泡在0.01 mol·L-1的NaCl溶液中,浸没深度为土柱的9/ 10,浸泡过夜至土柱饱和。用蠕动泵提供动力,通过模拟降雨器对土柱进行淋溶。先淋溶2 L(约4 PV)的淋溶液,其中Se浓度为10 mg·L-1,Br-浓度为8 mg·L-1,NaCl浓度为0.01 mol·L-1。淋溶速度为3 mL·min-1,每40 mL接一次溶液测定Se的浓度和Br-的浓度。Se溶液淋溶完毕后换成0.01 mol·L-1的NaCl背景溶液继续淋溶,实验共进行21 d。淋溶液中的Se用AFS进行测定;用作示踪剂的Br-通过酚红比色法测定;淋溶液中的Fe、Al、Ca、Mg含量用等离子体原子发射光谱(ICP-AES;Jarrel-ASH ICAP-9000,USA)测定;并测定淋溶液350 nm下的吸光度(Abs)、电导率(EC)和pH值。
1.5溶质运移模型
为了描述原状土柱溶液的孔隙特征以及离子扩散条件,对Br-的穿透曲线用HYDRUS-1D中的双孔-两点吸附模型(Dual-porosity with Two-Site Sorption in the Mobile Zone)进行拟合[8],然后根据Br-拟合参数对Se的穿透曲线进行拟合。双孔模型假设土壤中的水分为两部分,一部分为在裂缝或大孔径中的流动水,另一部分为在介质中的不动水。介质中的不动水可以与可动水之间发生交换。两种水中溶质的交换为一级扩散和对流扩散之和。模型溶质的运移控制公式为:

式中:θmo和θim分别为可动水和不可动水的百分比;cmo和cim分别为可动水和不可动水中溶质的浓度,M· L-3(M为物质量的单位;L为空间长度的单位);smo和sim分别为吸附在可动和不可动区域介质上溶质的浓度;fmo为可动水所接触到的吸附点位所占百分比;Dmo是溶质在可动水中的弥散系数,L2·T-1(T为时间单位);qmo是体积流量,L·T-1;φmo和φim分别为溶质可动水和不可动水中的降解/产生速率,M·L-3·T-1;ωmim为物质转移系数,T-1;Γw为可移动和不可移动区域间的水转移项;Γs为可移动和不可移动区域间的溶质转移项。
当Γw>0时,c*=cmo;当Γw<0时,c*=cim。第一个公式描述了溶质在可动水中的运移,第二个公式描述了溶质在不可动水中的物质平衡,而第三个公式描述了可动水和不可动水之间的溶质交换效率。
2 结果与讨论
2.1几种土壤对亚硒酸盐的吸附解吸
四种土壤吸附Na2SeO3的等温吸附曲线以及Langmuir和Freundlich吸附模型拟合参数如图1和表2所示。
两模型对土壤等温吸附曲线拟合均较好(Langmuir模型R2>0.902,Freundlich模型R2>0.884),前者的拟合效果较后者略好。Langmuir模型得到的Qmax大小顺序为FC2(621.50 mg·kg-1)>FC1(592.20 mg·kg-1)>DC(219.29 mg·kg-1)>BD(163.51 mg·kg-1);Freundlich模型得到的分配系数KF大小顺序为FC2(205.30 Ln· mg1-n·kg-1)>FC1(183.90 Ln·mg1-n·kg-1)>DC(102.77 Ln· mg1-n·kg-1)>BD(15.55 Ln·mg1-n·kg-1)。这表明,FC2土壤对Na2SeO3的吸附能力最大,其次为FC1,再次为DC,吸附能力最小的为BD。

图1 四种土壤对亚硒酸盐的吸附等温线Figure 1 Isotherms of selenite adsorption in four soils

表2 四种土壤吸附亚硒酸盐等温吸附曲线方程参数Table 2 Parameters of selenite adsorption equations for four soils
土壤对亚硒酸盐的吸附主要是基于SeO2-3替换土壤中的OH-官能团[6],土壤的OM含量、pH值、矿物组分等直接影响土壤对亚硒酸盐的吸附[6,9-11]。上述几种土壤中FC1和FC2对亚硒酸盐吸附量最大,而BD吸附量最低。铁锰氧化物和氢氧化物具有较强的亚硒酸盐的吸附能力[12]。BD土壤的活性Fe含量为1989 mg·kg-1;明显低于其他几种土壤的活性Fe含量。这是BD土壤具有较低吸附亚硒酸盐能力的原因之一。土壤pH值与土壤吸附亚硒酸盐能力呈负相关,土壤所带负电荷随着pH值的增加而增加,负电荷的增加会导致土壤对阴离子吸附能力减弱[6,9]。BD土壤pH值为8.06,呈碱性,而其他几种土壤均呈酸性。这是导致BD土壤具有较低亚硒酸盐吸附容量的另一个原因。有研究表明,OM也是控制土壤吸附亚硒酸盐的重要因子[6]。FC1和FC2土壤含有较高的OM,表现出对亚硒酸盐较强的吸附能力;虽然BD土壤的OM含量较DC土壤中高,但是最大吸附量却较DC土壤小,这是BD土壤中的活性氧化Fe含量远低于DC土壤中含量所导致的,因为土壤对亚硒酸盐的吸附能力是土壤多个理化性质综合作用的结果。另外,BD土壤属于高钙质土壤,钙含量明显高于其他几种土壤,但是结果表明碳酸钙含量并不明显影响土壤对亚硒酸盐的吸附。这与先前研究结果一致[6]。
几种土壤吸附亚硒酸盐实验完毕后进行亚硒酸盐的解吸实验,并计算亚硒酸盐的解吸量和解吸率。亚硒酸盐的解吸量计算公式为:

式中:Ds为解吸量,mg·kg-1;V为溶液体积,L;C为解吸平衡时溶液中Se的浓度,mg·L-1;m为离心管内的土壤质量,g。
亚硒酸盐的解吸率为解吸量与吸附量的比值。
几种土壤对亚硒酸盐解吸实验结果如图2所示。几种土壤随着对亚硒酸盐吸附量的增加,其解吸量也逐渐增加。FC1、FC2和DC三种土壤解吸量较BD土壤少,且BD土壤的解吸量与吸附量之间呈现指数上升的趋势,表现出更大的解吸量。从吸附量和解吸率来看,FC1、FC2和DC三种土壤解吸率随着吸附量的变化差异不大,均随着吸附量的增加而逐渐增加最后趋于平缓;而BD土壤解吸率很高,其值在67.97%以上,最高达到92.60%。BD土壤对亚硒酸盐吸附量较小,且解吸率较高说明BD土壤吸附亚硒酸盐主要为可逆吸附,主要是SeO2-3对土壤表面阴离子进行替换;含有较高活性Fe的FC1、FC2和DC土壤亚硒酸盐解吸能力相对较低,说明这三种土壤与SeO2-3可形成更稳定的配合物,以专性吸附为主。BD土壤较高的亚硒酸盐解吸量可能会导致其在土壤中运移速度较快。

图2 四种土壤亚硒酸盐解吸量和解吸率Figure 2 Amount and rate of selenite desorption in four soils
2.2亚硒酸盐在填装土柱中的运移
由吸附解吸实验可知,不同理化性质土壤对亚硒酸盐的吸附解吸能力明显不同。通过亚硒酸盐在填充土柱中的运移实验,进一步研究亚硒酸盐在不同理化性质填充土壤中的运移情况,运移结果如图3所示。
亚硒酸盐在填装土柱中的运移实验进行18 d左右,从图3可以得知,亚硒酸盐在BD土壤中的运移能力最强,3 h后就有Se淋出,淋出液的Se浓度在1 d左右出现了最大值,为328.17 μg·L-1。淋溶实验中亚硒酸盐初始淋溶液Se浓度为10 mg·L-1,而土壤淋溶液中Se浓度远小于初始淋溶液,说明大部分亚硒酸盐被土壤吸附。几种土壤比较显示,FC1、FC2和DC三种土壤亚硒酸盐运移速度明显较BD土壤慢。DC土壤亚硒酸盐运移速度较FC1和FC2土壤快,在第7 d左右Se被淋出,在第11 d与第12 d之间达到最大值33.38 μg·L-1,然后缓慢减小,并出现了明显的拖尾。FC1和FC2两土壤中亚硒酸盐运移速度缓慢,运移到第18 d,FC1淋出液中Se浓度达到6 μg·L-1左右,而FC2在第18 d,Se浓度仅为1 μg·L-1。与不同土壤对亚硒酸盐吸附结果相反,几种土壤中亚硒酸盐的运移能力大小依次为BD>DC>FC1>FC2。BD土壤对亚硒酸盐的吸附能力最弱,解吸能力最强,亚硒酸盐解吸率较高,因此BD土壤表现出更高的亚硒酸盐运移能力;而在具有较高亚硒酸盐吸附能力和较低亚硒酸盐解吸率的FC1和FC2土壤中,亚硒酸盐运移能力较弱。这表明,对于pH值较高且活性Fe含量相对较少的北方土壤来说,Se在土壤中的淋溶能力更强,富集能力相对较弱;而对于pH值较低且活性Fe含量较高的南方红壤来说,Se富集能力较强。

图3 亚硒酸盐在几种填充土柱中的运移Figure 3 Transport of selenite in various packed soil columns
2.3亚硒酸盐在饱和原状土柱中的运移
由亚硒酸盐在填装土柱中的实验结果可知,亚硒酸盐在FC1和FC2填装土壤中运移能力较弱;但真实土壤环境中,石子、孔洞和裂缝等普遍存在,可能会导致溶质在土壤中运移速度较填装土壤中的运移速度更快,因此原状土柱中亚硒酸盐运移的研究具有重要的现实意义。Br-和亚硒酸盐在原状土柱中的穿透曲线如图4所示,Br-穿透曲线拟合参数如表3所示。双孔-两点吸附模型对Br-的穿透曲线表现出了较好的拟合效果,R2为0.993,加权平方根差(Root mean square weighted error,RMSE)为0.016 28。

图4 原状土柱Br-和亚硒酸盐的穿透曲线及线性拟合Figure 4 Breakthrough and fitting curves of Br-and selenitetransport in intact soil column

表3 Br-原状土柱穿透曲线拟合参数Table 3 Fitting parameters of breakthrough curve of Br-in intact soil column

表4 原状土柱亚硒酸盐穿透曲线拟合结果Table 4 Fitting parameters of breakthrough curve of selenite in intact soil column
对于Se的原状土柱穿透实验,第1 d Se就被淋出,并且在第3 d左右达到最大值,其浓度达到了0.107 mg·L-1,随后明显减小,其运移速度明显较填装土柱快。这说明优势流在原状土柱Se的运移过程中起到了决定性的作用。将Br-在原状土柱中穿透曲线拟合所得到的参数应用于亚硒酸盐的穿透曲线拟合,拟合结果如图4和表4所示。表4中f1为可动水所占比例(%);KD为Langmiur-Freundlich吸附模型中的分配系数(L·mg-1);μ(L·mg-1)和β(无量纲)分别为吸附模型中的系数。两点吸附模型则将土壤对亚硒酸盐的吸附点位分为了两部分,一部分为快速吸附平衡位点,另一部分为时间控制的吸附平衡位点。f2为两点吸附模型中快速吸附点位所占比例(%);ω为溶质之间的交换系数(d-1)。拟合结果R2为0.902,RMSE为0.028,表明双孔-两点吸附模型能够较好地描述亚硒酸盐在原状土柱中的运移行为,并做出相应的预测。
亚硒酸盐在土柱中运移的过程中,土壤中一些离子也会随着淋溶液一起淋出,因而对其他离子运移和淋溶液理化性质的监测,有助于理解亚硒酸盐在土壤中的运移行为。图5为淋溶液的理化性质,图6为淋溶液中几种金属的含量。
有研究表明,土壤重金属等以胶体结合态运移是其在土壤中运移的主要方式,而胶体含量与吸光度(350 nm)有明显的线性关系[2],因此对淋溶液中的Abs进行了监测。从图5可知,淋溶液中的Abs均较低(基本小于0.02),说明在该实验条件下土壤胶体发生运移量较少,Se主要是以离子形式发生运移。胶体释放与环境条件关系密切,原状土柱中胶体运移量之所以较小,可能是因为该实验条件不利于土壤胶体的释放。当环境条件发生改变时,可能导致大量土壤胶体释放,最终致使富Se土壤胶体向深层土壤发生运移[13]。0~6 d内,淋溶液的EC基本在1200~1300 μS· cm-1之间,并在第6 d出现了明显减小,说明淋出液中离子含量逐渐减小。这可能是因为土壤中较容易被淋出的离子已经全部淋出。淋溶液pH值始终在6.5~7.0之间,且刚开始变化不大,在第6 d时出现了缓慢的增加。这可能是因为SeO2-3在运移过程中替代了土壤中的OH-,进而使更多的OH-进入土壤溶液,最终导致pH值上升[6,11]。
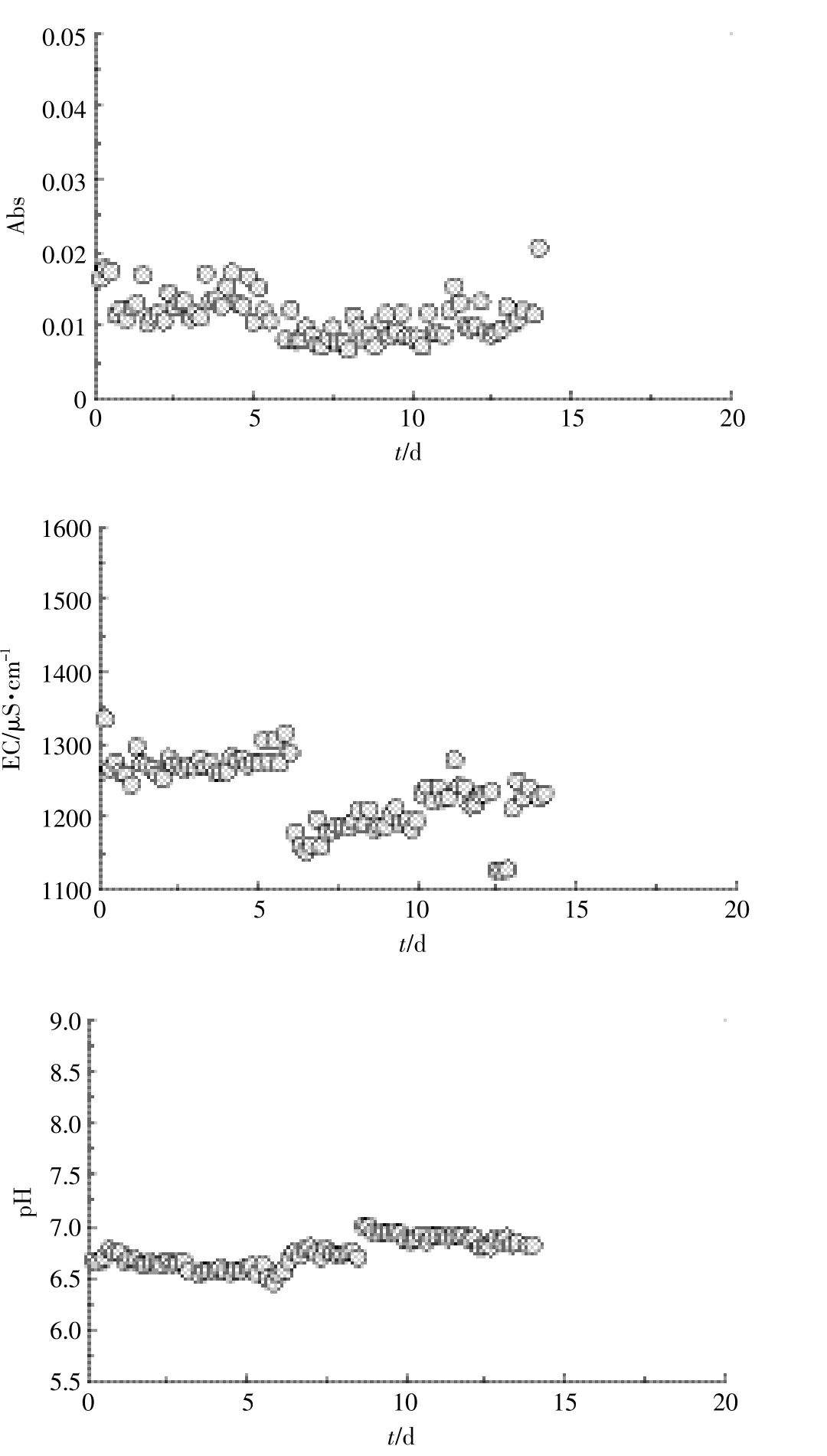
图5 淋溶液理化性质Figure 5 Physical-chemical properties of leached solutions
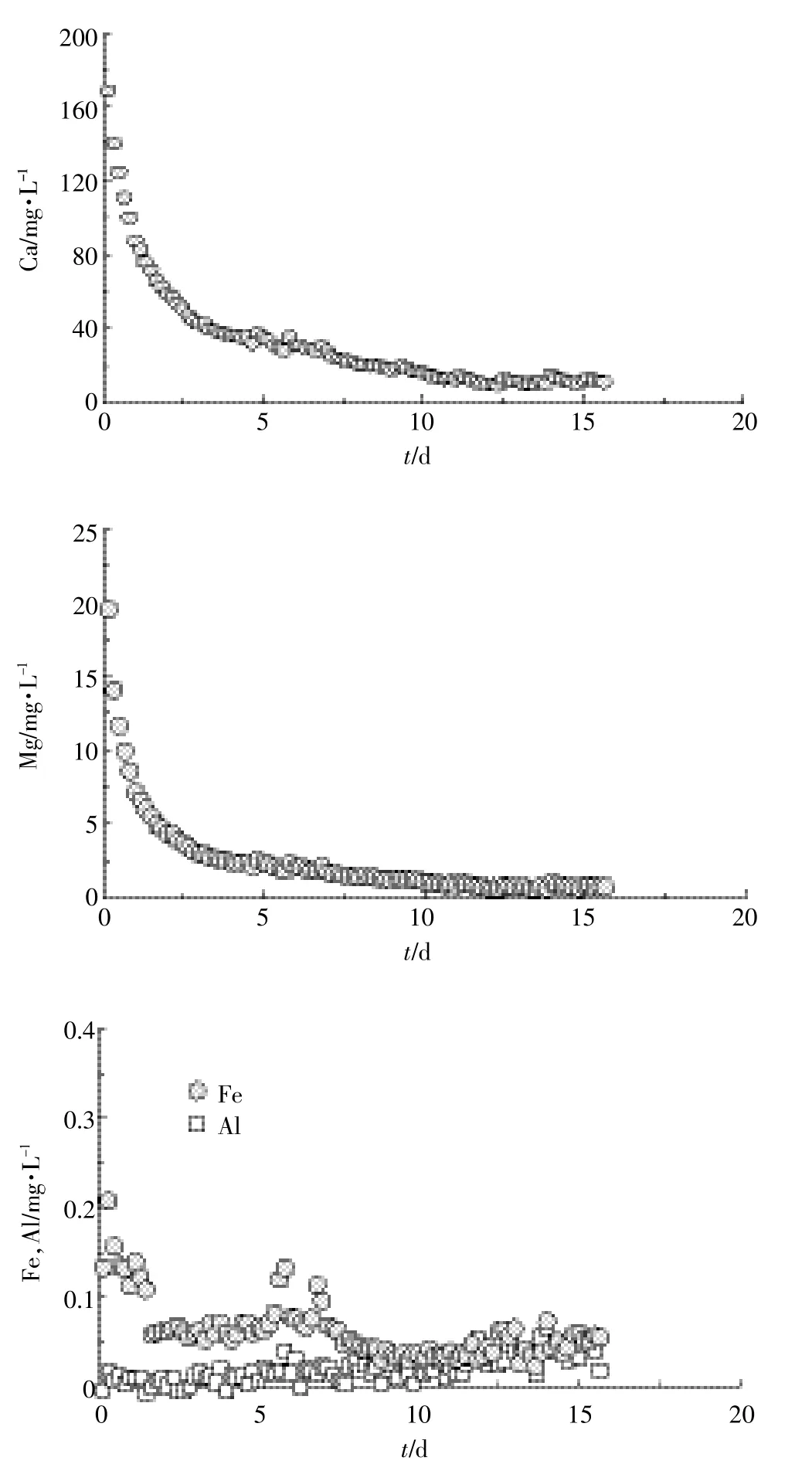
图6 淋溶液中Ca、Mg、Fe和Al离子含量Figure 6 Concentrations of Ca,Mg,Fe,and Al in leached solutions
淋溶液中Ca和Mg随着淋溶时间的增加急剧减小,并且逐渐趋于稳定。经过15 d的淋溶,淋溶液中Ca从168.96 mg·L-1降低到11.14 mg·L-1,Mg从19.50 mg·L-1降低到0.72 mg·L-1。淋溶液中Fe和Al含量较低,Al含量也随着淋溶时间的增加而减小,从0.21 mg·L-1减小到0.05 mg·L-1;Fe含量更低,平均为0.02 mg·L-1。淋溶液中Fe和Al的变化规律相似,而Ca和Mg变化规律相似。淋溶液中的Ca和Mg来源于土壤中的离子交换,说明在亚硒酸盐淋溶过程中大量的Na替换了土壤中的Ca和Mg。土壤中的Fe和Al大多以较为稳定的氧化物形式存在,大多与胶体颗粒一同淋溶下来[14],淋溶液中较低的Fe和Al含量也说明了淋溶液中胶体含量较低,在该实验条件下亚硒酸盐在淋溶过程中以胶体结合态发生运移的可能性较低。
3 结论
(1)所研究的四种土壤吸附能力大小依次为FC2 (621.50 mg·kg-1)>FC1(592.20 mg·kg-1)>DC(219.29 mg·kg-1)>BD(163.51 mg·kg-1),不同土壤对亚硒酸盐的吸附能力与土壤pH和铁铝氧化物呈正相关关系。具有较小吸附亚硒酸盐能力的BD土壤具有较高的亚硒酸盐解吸率和解吸量。
(2)亚硒酸盐在几种填装土柱中的运移速率大小依次为BD>DC>FC1>FC2;亚硒酸盐的运移能力受到土壤对其吸附解吸能力的控制。
(3)真实土壤环境中,由于大孔径和优势流的存在,亚硒酸盐的运移速率会明显增加。HYDRUS-1D软件中的双孔-两点吸附模型能够较好地预测亚硒酸盐在土壤中的运移。
参考文献:
[1] Cong W, Zhang X, Feng Y. Transport of selenium and its modeling through one dimensional saturated soil columns[J]. African Journal of Agricultural Research, 2011, 6(8):2002-2009.
[2] Yin X, Gao B, Ma LQ, et al. Colloid-facilitated Pb transport in two shooting-range soils in Florida[J]. Journal of Hazardous Materials, 2010, 177(1-3):620-625.
[3] Ngueleu S K, Grathwohl P, Cirpka O A. Altered transport of lindane caused by the retention of natural particles in saturated porous media[J]. Journal of Contaminant Hydrology, 2014, 162-163(7):47-63.
[4]陈历程,张勇.微量元素硒的研究现状及其食品强化[J].食品科学, 2002, 23(10):134-137. CHEN Li-cheng, ZHANG Yong. Status of selenium research and selenium-fortified food[J]. Food Science, 2002,23(10):134-137.
[5]牟仁祥,陈铭学,朱智伟,等.硒的形态分析方法综述[J].光谱实验室, 2004(1):27-35. MOU Ren-xiang, CHEN Ming-xue, ZHU Zhi-wei, et al. Review of the analytical methods for selenium speciation[J]. Chinese Journal of Spectroscopy Laboratory, 2004(1):27-35.
[6] Dhillon K S, Dhillon S K. Adsorption-desorption reactions of selenium in some soils of India[J]. Geoderma, 1999, 93(1/2):19-31.
[7] Qin H, Zhu J, Liang L, et al. The bioavailability of selenium and risk assessment for human selenium poisoning in high-Se areas, China[J]. Environment International, 2013, 52(2):66-74.
[8] Simunek J, Huang K, Sejna M. The HYDRUS-ET software package for simulating the one-dimentional movement of water, heat and multiple solutes in variably-saturated media, Version 1.1[M]. Bratislava:Inst. Hydrology Slovak Acad. Sci; 1997.
[9]周鑫斌,于淑慧,谢德体. pH和三种阴离子对紫色土亚硒酸盐吸附-解吸的影响[J].土壤学报, 2015, 52(5):1069-1077. ZHOU Xin-bin, YU Shu-hui, XIE De-ti. Effects of pH and three kinds of anions on selenium absorption and desorption in purple soil[J]. Acta Pedologica Sinica, 2015, 52(5):1069-1077.
[10]刘鹏,杨志辉,葛旦之,等.淹水条件下土壤硒迁移行为的研究Ⅱ.还原淋溶作用下土壤硒的迁移机理[J].湖南农业大学学报, 2000, 26(1):84-87. LIU Peng, YANG Zhi-hui, GE Dan-zhi, et al. Transport behavior of selenium in soil under water loggingⅡ. Transport mechanism in soil under reductive leaching[J]. Journal of Hunan Agricultural University, 2000, 26(1):84-87.
[11] Lee S, Doolittle J J, Woodard H J. Selenite adsorption and desorption in selected south dakota soils as a function of pH and other oxyanions[J]. Soil Science, 2011, 176(2):73-79.
[12] Chubar N, Gerda V, Szlachta M. Mechanism of selenite removal by a mixed adsorbent based on Fe-Mn hydrous oxides studied using X-ray absorption spectroscopy[J]. Environmental Science & Technology, 2014, 48(22):13376-13383.
[13]胡俊栋,沈亚婷,王学军.土壤胶体在不同饱和度土壤介质中的释放与淋溶行为研究[J].农业环境科学学报, 2009, 28(9):1829-1836. HU Jun-dong, SHEN Ya-ting, WANG Xue-jun. Release and mobilization of soil colloid in the natural soil packed column with various water saturations[J]. Journal of Agro-Environment Science, 2009, 28 (9):1829-1836.
[14] Ranville J F, Chittleborough D J, Beckett R. Particle-size and element distributions of soil colloids:implications for colloid transport[J]. Soil Science Society of America Journal, 2005, 69(4):1173-1184.
Selenite transport in soils with various physico-chemical properties
LIU Guan-nan1,2, XUE Wei2, SUN Chun-mei1,3, LI De-xian1, LIU Xin-hui2*
(1.Institute of Mineral Resources, Chinese Academy of Geological Sciences, Beijing 100037, China; 2.State Key Laboratory of Water Environment Simulation, School of Environment, Beijing Normal University, Beijing 100875, China; 3.Institute of Chemical Engineering, Beijing University of Chemical Technology, Beijing 100029)
Abstract:The transport of heavy metals in soil determines their risks to underground water and human health. However, such transport is controlled by soil properties. Here we studied the adsorption, desorption and transport of selenite in different soils:FC1(0~10 cm surface soil from Fengcheng, Jiangxi), FC2(10~20 cm subsurface soil from Fengcheng, Jiangxi), DC(surface soil in Dexing, Jiangxi)and BD(surface soil in Baoding, Hebei), to uncover the effects of soil physico-chemical properties on selenite transport in soils. Results showed that FC1 and FC2 soils, having higher amorphous iron oxide and organic matter(OM)and lower soil pH than others, had greater selenite adsorption, with the maximum adsorption capacities of 621.50 mg·kg(-1)and 592.20 mg·kg(-1), respectively. The maximum selenite adsorption was 219.29 mg·kg(-1)for DC and 163.51 mg·kg(-1)for BD. However, BD soil had the highest selenite desorption rate and amount. In packed soil column experiment, selenite transported faster in BD soil than in other soils, suggesting that the transport of selenite in soil column was influenced by the adsorption and desorption abilities of selenite in soils. In intact soil column, selenite transported quicker than in the packed soil columns. The breakthrough curve of selenite in intact soil column fitted DTSMZ(Dual-porosity with Two-Site Sorption in the Mobile Zone)model well by HYDRUS-1D software. Our results indicate the possibility of selenium pollution in groundwater due to the presence of macropore and preferential flow in the field conditions.
Keywords:soil; selenium; adsorption; desorption; transport
*通信作者:刘新会E-mail:xhliu@bnu.edu.cn
作者简介:刘冠男(1984—),男,河北保定人,博士后,主要从事土壤重金属等元素环境行为研究。E-mail:liu.guannan@126.com
基金项目:有益元素富集区多目标地球化学调查项目(12120113000100);福建省典型地区土壤重金属地质成因调查与风险评价(12120115049201)
收稿日期:2015-10-06
中图分类号:S153.6
文献标志码:A
文章编号:1672-2043(2016)03-0485-07
doi:10.11654/jaes.2016.03.011
