几种模拟土壤固相组分对平面和阻转构型PCBs的吸附作用
2016-04-20王沛然王玉军周东美方凤满
王沛然,王玉军,周东美,刘 存①,方凤满
(1.安徽师范大学国土资源与旅游学院,安徽 芜湖 241003;2.中国科学院南京土壤研究所/ 中国科学院土壤环境与污染修复重点实验室,江苏 南京 210008)
几种模拟土壤固相组分对平面和阻转构型PCBs的吸附作用
王沛然1,2,王玉军2,周东美2,刘存2①,方凤满1②
(1.安徽师范大学国土资源与旅游学院,安徽 芜湖241003;2.中国科学院南京土壤研究所/ 中国科学院土壤环境与污染修复重点实验室,江苏 南京210008)
摘要:采用批平衡试验方法,模拟了土壤的3种主要吸附活性组分〔K+饱和蒙脱石(K+-Mont)、胡敏酸-蒙脱石复合体(HA-Mont)和生物质炭(BC)〕对2种构型的一氯代联苯(PCBs)〔非共平面阻转类2-氯联苯(2-CB)和共平面类4-氯联苯(4-CB)〕的吸附特性。结果表明:线性方程均能很好地拟合3种模拟土壤固相组分对多氯联苯的吸附,2种PCBs的吸附分配系数(Kw)从大到小依次均为BC、HA-Mont和K+-Mont。通过不同温度下吸附等温线的热力学分析,发现K+-Mont对PCBs的吸附驱动力主要为表面吸附作用和疏水作用,蒙脱石矿物的层间是重要吸附域;HA-Mont对PCBs的吸附驱动力主要为分配作用;而BC对PCBs的吸附域主要为芳香性微孔表面,表面和PCB分子间的π-π作用是吸附的主要驱动力。尽管2种PCBs的疏水性相近,共平面类4-CB在3种吸附剂上的吸附量均显著大于阻转类2-CB,原因主要为非共平面的2-CB的空间位阻效应阻碍了2-CB进入纳米尺寸的蒙脱石矿物层间或BC的微孔吸附域,有机污染物分子的空间结构对污染物在土壤中的吸附迁移过程起重要作用。
关键词:多氯联苯类;黏土矿物;胡敏酸-黏土矿物复合体;生物质炭;吸附
蒙脱石具有遇水膨胀、有较强的阳离子交换量(CEC)、比表面积大以及独特的纳米尺度层间空隙等结构特点,能强烈吸附多种类型污染物,对土壤环境中的有机污染迁移和归趋有重要影响[1],由于价格低廉被广泛应用于废水处理、空气净化及垃圾防渗等领域[2]。

土壤中,SOM一般被包裹在蒙脱土表面形成复合体,表面包裹的SOM能改变黏土矿物的物理化学性质,如比表面积和层间阳离子交换量[9],进而影响有机污染物在复合体上的吸附。目前,国内外已对黏土矿物-有机质复合体进行了大量研究以模拟真实土壤对有机污染物的吸附过程,SOM能促进对三氯乙烯[10]、四氯苯[9]和抗生素[11]的吸附。GAO等[12]发现SOM不仅影响复合体对磺胺类污染物的吸附,同时也影响磺胺类在复合体上的解吸。LI等[3]发现SOM对K+饱和黏土吸附农药没有作用,但可影响其在Ca2+饱和黏土上的吸附和解吸。ZHANG等[9]发现SOM覆盖黏土表面抑制了离子偶极作用,从而限制了1,3-二硝基苯和敌草隆在蒙脱土上的吸附。
自然源和人为源的生物质不完全燃烧生成的土壤黑炭,包括炭黑、生物质炭(BC)等,尽管其在土壤中含量比蒙脱土和有机质-蒙脱土复合体少,但具有多孔性、高比表面积以及丰富的表面官能团等特点,能够很好地吸附有机污染物和某些无机金属阳离子[13]。人工制备的BC常常被施加到土壤中用于调节和修复土壤[14]。由于原材料、燃烧温度以及处理过程不同,BC的物理化学性质有很大差异,例如,随着燃烧温度的升高,BC逐渐由脂肪性过渡为芳香性,极性指数急剧降低,微孔结构被打开,比表面积逐渐增大,吸附从以分配作用为主变为以吸附作用为主[15]。BC对菲、硝基苯、多氯联苯和敌草隆等多种类型有机污染物都有很强的吸附能力,吸附机制主要为分配作用、表面吸附、π-π键和孔隙作用等[16]。

目前,关于PCBs在土壤中吸附机理研究主要集中于吸附剂的特性以及污染物的疏水性对吸附过程的影响。然而,近期的研究发现一些同分异构的PCBs尽管辛醇-水分配系数近似,在土壤上的吸附却差别很大,这可能是有机污染物的空间结构不同造成的。为此选取2-氯联苯(2-chlorobiphenyl,2-CB)和4-氯联苯(4-chlorobiphenyl,4-CB)2种构型不同的目标污染物,探讨其在土壤中的3种主要吸附剂(蒙脱土、胡敏酸-蒙脱土复合体和生物质炭)上的吸附热力学规律,以期更好地了解PCBs在土壤中的吸附规律。
1材料与方法
1.1化学药品
供试分析纯级2-CB和4-CB(表1)购自安普公司(上海),无水乙酸钠、乙酸、KCl和NaCl购自国药集团化学试剂有限公司(上海),胡敏酸(HA)购自Sigma-Aldrich公司(美国),透析膜购自联合碳化公司(美国),甲醇和正己烷购自Merck公司(德国),均为色谱纯。制备生物质炭的松针采自南京九华山公园的雪松。
表1供试多氯联苯(PCBs)的物理化学性质
Table 1Physical and chemical properties of PCBs

PCBs平面类型旋转势垒[18]/(kJ·mol-1)25℃水溶解度[19]/(mg·L-1)正辛醇-水分配系数[20](lgKow)2-CB阻转类28.805.5±0.54.464-CB共平面类8.331.2±0.34.69
1.2黏土矿物制备
供试黏土蒙脱土(SMF,FZ-10)购自丰虹公司(浙江),过0.075 mm孔径筛备用。
1.2.1钾饱和蒙脱土(K+-Mont)的制备
称量一定量黏土放入超纯水中搅拌1 d,以600 r·min-1离心(r=15.5 cm)6 min,去除瓶底直径大于2 μm的颗粒;用0.5 mol·L-1NaCl饱和3次,以4 500 r·min-1离心(r=15.5 cm)30 min,倒掉上清液,用超纯水清洗3次以去除多余Cl-;用pH值为5的0.5 mol·L-1乙酸钠缓冲液将黏土溶液pH值调节到6.8以移除碳酸盐杂质,再用0.5 mol·L-1的KCl饱和3次,重复上述步骤3次;最后,把所得黏土矿物冷冻干燥后研磨成粉末状过0.15 mm孔径筛待用[21]。通过低温外加热重铬酸钾氧化-比色法测得其w(有机质)为0.03%,可忽略不计;通过比表面积氮吸附方法(BET)测得其比表面积为98.6 m2·g-1。
1.2.2胡敏酸-蒙脱土复合体(HA-Mont)的制备
将胡敏酸在超纯水中溶解并过0.45 μm孔径滤膜制得胡敏酸(HA)溶液,把K+-Mont加入该溶液避光搅拌1周,以4 500 r·min-1离心(r=15.5 cm)30 min后倒掉上清液,再用0.5 mol·L-1的KCl饱和3次,用12 000 Da的透析袋透析1周,再用超纯水清洗至无亮棕色,以4 500 r·min-1离心(r=15.5 cm)30 min,倒掉上清液,冷冻干燥研磨过0.15 mm孔径筛待用[3]。通过低温外加热重铬酸钾氧化-比色法测得其w(有机质)为0.93%。
1.2.3BC的制备
新鲜松针样品用去离子水洗净,在80 ℃的烘箱中烘干12 h,磨碎过0.15 mm孔径筛,把样品盛入带有盖子的坩埚中,放入通少量氧气的马弗炉中热解,升温程序为100 ℃热解2 h,后以10 ℃·min-1程序升温到500 ℃,保持6 h,样品冷却至室温后取出,研磨成粉过0.15 mm孔径筛待用[22]。通过BET氮吸附方法和元素分析仪测得BC比表面积和w(C)分别为7.31 m2·g-1和67.6%。
1.3批试验方法
所有的等温吸附试验均采用批平衡方法。标准PCBs储备液用甲醇配制,溶液用超纯水稀释。在K+-Mont和HA-Mont体系中φ(甲醇)均小于1%,BC体系中采用甲醇-水混合体系,φ(甲醇)为40%~60%。
1.3.1K+-Mont和HA-Mont对PCBs的吸附试验
吸附试验在8 mL带有聚四氟乙烯垫片的安普玻璃离心瓶中进行,吸附剂浓度设定为:ρ(K+-Mont)为10 g·L-1,ρ(HA-Mont)为8 g·L-1。PCBs溶液浓度设定为:ρ(2-CB)为0.5~1.0 mg·L-1,ρ(4-CB)为0.2~0.6 mg·L-1,并加入0.01 mol·L-1KCl作为背景电解质。试验悬液分别在10、20和30 ℃条件下以200 r·min-1在恒温振荡箱中振荡平衡24 h(预试验证明在24 h内可达平衡)。平衡后以4 000 r·min-1离心(r=15.5 cm)20 min,用玻璃移液管准确移取定量上清液,用正己烷萃取。
1.3.2BC对PCBs的吸附试验
采用混合溶剂助溶-外推法精确定量计算吸附系数[23]。吸附试验在20 mL带有聚四氟乙烯垫片的安普玻璃离心瓶中进行,称取10 mg BC样品,加入15 mL含有2-CB或者4-CB的甲醇-水混合溶液,2-CB和4-CB的初始浓度ρ为5.0~12.5 mg·L-1,混匀后置入20 ℃恒温振荡箱中,以200 r·min-1振荡48 h(预试验证明在48 h内可达平衡)。平衡后以7 000 r·min-1离心(r=15.5 cm)30 min,用玻璃移液管准确移取定量上清液,用正己烷萃取。
1.4PCBs的检测方法
PCBs采用配备有Ni电子捕获检测器(μ-ECD)和自动进样器的Aglient 7890(美国)进行检测。仪器配备J&W Scientific HP-5气相毛细管柱(30 m×0.32 mm×0.25 μm)。GC色谱条件为:检测器温度为300 ℃;进样口采用不分流模式,温度为250 ℃;载气为高纯氮气,流速为1 mL·min-1,进样量为1 μL,尾吹流量为30 mL·min-1。柱箱升温程序为:从150 ℃开始,按15 ℃·min-1升温到280 ℃,保持2 min。
1.5数据分析与结果计算
K+-Mont和HA-Mont对PCBs的批平衡等温吸附试验结果均能很好地用线性方程进行拟合。
Cs=Kw×Ce。
(1)
式(1)中,Ce为吸附平衡时溶液中PCBs质量浓度,mg·L-1;Cs为吸附平衡时黏土或胡敏酸-黏土复合体中PCBs含量,mg·kg-1;Kw为线性固相-水分配系数,L·kg-1。
BC对PCBs在甲醇-水体系中的吸附等温线也能很好地用线性方程拟合,纯水中的PCBs线性吸附系数Kw可由甲醇-水体系中Km外推得到[23]。
lg(Km/Kw)=-ασfc。
(2)
式(2)中,Km为甲醇-水体系中的线性吸附系数;α为有关溶剂与吸附剂相互作用的经验常数;σ为混合溶剂间作用力;fc为甲醇在混合体系中所占体积比,%。
PCBs在土壤不同模拟固相组分上吸附的热力学参数可由上述计算得到的纯水体系中的线性吸附系数推导得到,具体计算公式如下:
ΔG=-RTlnKw,
(3)
(4)
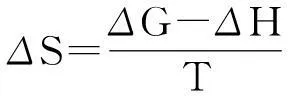
(5)
式(3)~(5)中,ΔG为吸附过程的吉布斯吸附自由能变化,kJ·mol-1;R为摩尔气体常量;T、T1、T2均为吸附试验中不同热力学温度,K;Kw,T1、Kw,T2为不同热力学温度下的吸附系数,L·kg-1;ΔH为吸附的标准焓变化,kJ·mol-1;ΔS为吸附的标准熵变化,kJ·mol-1·K-1。
有机污染物在有机质中的分配系数(lgKom)和其辛醇-水分配系数(lgKow)具有一定的线性相关性,方程为lgKom=0.904 lgKow-0.779[24]。根据表1中的lgKow值计算得到2-CB和4-CB的lgKom分别为3.25和3.46。由于PCBs在K+-Mont和HA-Mont上的吸附都是线性吸附,所以可以用简单的复合模型来预测HA和K+-Mont在整个吸附过程中的独立贡献[3]。
Kcal=fomKom+fclayKclay。
(6)
式(6)中,Kcal为胡敏酸-蒙脱土复合体的吸附系数,L·kg-1;fom和fclay分别为胡敏酸-蒙脱土复合体中的胡敏酸和黏土质量分数,%;Kom为PCBs在胡敏酸中的线性分配系数,L·kg-1;Kclay为PCBs在K+-Mont上的线性吸附系数,L·kg-1。
2结果与讨论
2.1PCBs在K+-Mont上的吸附
由图1和表2可知,不同温度下K+-Mont对PCBs的吸附均可较好地用线性模型拟合,这可能是因为不含有机质的黏土矿物对低浓度非离子型有机污染物的吸附主要是疏水作用,吸附域在黏土层间[25-26]。
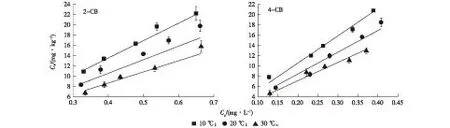
Ce为吸附平衡时溶液中PCBs质量浓度;Cs为吸附平衡时黏土或胡敏酸-黏土复合体中PCBs含量。
表2不同温度下钾饱和蒙脱土(K+-Mont)对PCBs吸附的热力学参数
Table 2Thermodynamic parameters of PCBs sorption on K+-Mont relative to temperature

PCBsT/KKw/(L·kg-1)r2ΔG/(kJ·mol-1)ΔH/(kJ·mol-1)ΔS/(kJ·mol-1·K-1)2-CB283.1533.88±0.520.9825-8.29-17.13~-14.62-0.03~-0.02293.1526.43±0.570.9805-7.98303.1521.68±0.460.9647-7.754-CB283.1552.94±0.110.9814-9.34-15.50~-12.54-0.02~-0.01293.1542.29±1.190.9680-9.13303.1535.69±0.580.9653-9.01
T为热力学温度;Kw为纯水体系中吸附系数;ΔG为吉布斯吸附自由能变化;ΔH为标准焓变化;ΔS为标准熵变化。
表2中不同温度下ΔG和ΔH均为负值,说明PCBs在K+-Mont上的吸附属于自发的放热吸附,为物理吸附[27-28]。ΔH能表征污染物分子与吸附剂表面的作用强度,在吸附PCBs的过程中,ΔH绝对值比ΔG能量绝对值大近1倍,说明2-CB和4-CB 在K+-Mont上的吸附驱动力同时包含了疏水分配和表面吸附作用。ΔS表征分子的自由度,2-CB 和4-CB的ΔS均为负值,说明所吸附的PCBs分子被固定在黏土表面或层间,自由度降低[11]。
4-CB的Kw值远大于2-CB,4-CB更易被吸附在蒙脱石上。由表1可知,2-CB和4-CB的lgKow分别为4.46和4.69,疏水性相近,单纯的疏水作用不能完全解释两者在黏土上吸附的差异。蒙脱石对有机污染的吸附域主要为黏土层间,层间表面积占黏土总比表面积的80%以上;K+-Mont的层间空隙厚度约为6Å,平面型分子易于进入黏土层间而被吸附[6-7]。2-CB的旋转势垒和二面角远大于4-CB,分子的空间尺寸阻碍了2-CB进入K+-Mont层间,而共平面型的4-CB则可自由进入K+-Mont层间。因阻转类PCBs需克服相当大的空间位阻,导致其在蒙脱石上的吸附显著低于共平面类PCBs。
2.2PCBs在HA-Mont上的吸附
由图2可知,HA-Mont对PCBs的吸附同样可以很好地用线性模型拟合。表3中HA-Mont对PCBs吸附过中的ΔG和ΔH均为负值,说明该过程仍为自发的放热的线性物理吸附过程[27]。不同温度下ΔG和ΔH大小差异不显著,说明PCBs分子主要均匀分配在HA中,与PCBs在K+-Mont表面的吸附不同[5]。从线性吸附系数Kw可知,不同温度下4-CB 在HA-Mont上的吸附是2-CB的2.09~2.18倍,表明构型因素同样影响PCBs在胡敏酸-蒙脱土复合体上的吸附。
2.3HA对K+-Mont吸附PCBs的影响
对比表2和表3发现,HA-Mont对2-CB和4-CB的吸附系数Kw值分别是K+-Mont的2.69~3.13和3.76~3.95倍。在反应温度为20 ℃时,2-CB和4-CB的Kcal值分别为42.83和68.77 L·kg-1,分别可以解释54%和41%的HA-Kont的Kw值。有学者使用X射线衍射(XRD)技术发现大部分胡敏酸分子或基团比较大,很难进入蒙脱石层间,主要包覆在蒙脱石的外表面和边面位置[3,9]。LI等[3]通过XRD分别研究了4,6-二硝基邻甲酚在K+-黏土和HA-黏土上的吸附情况,发现在有机-无机复合体中的黏土层间同样是重要的吸附域,污染物可穿透疏水的胡敏酸层进入蒙脱石层间域。由于HA吸附在边面位置,限制水分子进入蒙脱石层间,增加了黏土层间的疏水性,有更多的黏土硅氧烷疏水表面可以暴露出来,所以有机质不仅起到了分配作用,还有效地促进了蒙脱石部分对PCBs的吸附,导致胡敏酸-黏土复合体的吸附大于HA和K+-Mont单独贡献之和。
表3不同温度下胡敏酸-蒙脱土复合体(HA-Mont)对PCBs吸附的热力学参数
Table 3Thermodynamic parameters of PCBs sorption on HA-Mont relative to temperature

PCBsT/KKw/(L·kg-1)r2ΔG/(kJ·mol-1)ΔH/(kJ·mol-1)ΔS/(kJ·mol-1·K-1)2-CB283.1591.10±0.860.9926-10.62-10.92~-10.160293.1578.63±0.350.9981-10.64303.1567.83±0.320.9983-10.634-CB283.15198.95±4.110.9836-12.46-13.93~-12.060293.15167.04±5.340.9630-12.47303.15138.33±0.470.9932-12.42
T为热力学温度;Kw为纯水体系中吸附系数;ΔG为吉布斯吸附自由能变化;ΔH为标准焓变化;ΔS为标准熵变化。
2.4PCBs在BC上的吸附
由图3和表4可知,在不同甲醇-水体系下,BC对2-CB和4-CB都可用线性模型很好地拟合,可能是因为吸附剂含有较多的无定型物质且比表面积很小[29]。随着混合体系中甲醇含量的增高,BC对PCBs的吸附量随之减少,吸附系数Km与φ(甲醇)呈良好线性关系。PCBs在BC上ΔG均为负值,说明吸附过程为自发吸附。2-CB和4-CB的ΔG分别为-28.13和-34.44 kJ·mol-1,远高于PCBs在黏土矿物和有机质上的吸附自由能,说明除了疏水作用以外,存在特定的相互作用,显著促进了PCBs在BC上的吸附[27]。且BC的比表面积比K+-Mont小,说明比表面积可能不是主要影响因素,BC的微孔结构及芳香性的微孔表面可能为主要吸附域,PCBs分子的芳环与BC之间的π-π作用则是吸附的主要驱动力。对比2-CB和4-CB在BC上的吸附系数lgKw发现,4-CB比2-CB大1个数量级,这与BELES等[30]的研究结果一致,说明构型因素的影响被进一步放大,多氯联苯在炭质材料上的吸附除了受到疏水作用和π-π作用控制外还受到PCBs构型平面性的影响,共平面的疏水性有机污染物在BC上的吸附量比非平面污染物大[31].

Ce为吸附平衡时溶液中PCBs质量浓度;Cs为吸附平衡时黏土或胡敏酸-黏土复合体中PCBs浓度。
表4不同甲醇-水体系下生物质碳(BC)对PCBs的线性吸附系数及其外推纯水体系下线性吸附系数和相应的吸附自由能
Table 4Linear adsorption coefficient of PCBs on BC relative to ratio of the methanol-water solution and its derived linear adsorption coefficient and corresponding adsorption free energy in pure water

PCBsfc/%lgKmrm2ασlgKwrw2ΔG/(kJ·mol-1)2-CB403.450.98963.945.01±0.150.9890-28.13503.010.9696602.660.96264-CB404.260.99374.856.14±0.570.8973-34.44503.590.9753603.300.9492
fc为甲醇在混合体系中所占体积比;lgKm为混合体系中线性系数的对数;lgKw为外推线性系数的对数;rm2为混合体系中线性回归系数;rw2为外推体系中线性回归系数;α为有关溶剂与吸附剂相互作用的经验常数;σ为混合溶剂间作用力;ΔGw为吉布斯吸附自由能变。
3结论
(1)K+-Mont、HA-Mont和BC对PCBs的吸附均能很好地用线性方程拟合,吸附剂对PCBs的吸附量随着溶液中PCBs浓度的增加而增加。
(2)3种模拟土壤固相组分对PCBs的吸附均为自发的放热吸附过程。其中,K+-Mont和HA-Mont对PCBs的吸附属于物理表面吸附和疏水作用过程,BC对PCBs的吸附除了疏水作用外,其微孔区域的芳香性表面和PCB分子间的π-π作用是吸附的主要驱动力。
(3)共平面的4-CB在3种模拟土壤固相组分上的吸附量均大于非共平面的2-CB,主要是因为分子的空间尺寸阻碍了2-CB进入BC的微孔结构或纳米级的黏土矿物层间,导致非共平面类PCBs在蒙脱石上的吸附要显著低于共平面类PCBs。
(4)HA能促进K+-Mont对PCBs的吸附。HA一般包裹在黏土表面或边面位置,很难进入黏土的层间域,并限制了水分子的进入,加大了层间的疏水性,导致其吸附量大于HA和K+-Mont单独贡献之和。
参考文献:
[1]吴平霄,廖宗文.蒙脱石层间域的性质及其环境意义[J].地球科学进展,2000,15(2):184-189.
[2]雷绍民,郝骞,熊毕华,等.蒙脱石矿物特性及开发利用前景[J].资源环境与工程,2006,20(5):565-569.
[3]LI H,SHENG G Y,TEPPEN B J.Sorption and Desorption of Pesticides by Minerals and Humic Acid-Clay Complexes[J].Soil Science Society of America Journal,2003,67(1):122-131.
[4]KILE D E,CHIOU C T.Partition of Nonpolar Organic Pollutants From Water to Soil and Sediment Organic Matters[J].Environmental Science & Technology,1995,29(5):1401-1406
[5]CHIOU C T,SHOUP T D.Soil Sorption of Organic Vapors and Effects of Humidity on Sorptive Mechanism and Capacity[J].Environmental Science & Technology,1985,19(12):1196-1200.
[6]LH H,TEPPENB J,JOHNSTON C T,etal.Thermo Dynamics of Nitroaromatic Compound Adsorption From Water by Smectite Clay[J].Environmental Science & Technology,2004,38(20):5433-5442.
[7]LIU C,LI H,TEPPEN B J,etal.Mechanisms Associated With the High Adsorption of Dibenzo-p-Dioxin From Water by Smectite Clays[J].Environmental Science & Technology,2009,43(8):2777-2783.
[8]LI H,TEPPEN B J,LAIRD D A,etal.Effects of Increasing Potassium Chloride and Calcium Chloride Ionic Strength on Pesticide Sorption by Potassium-and- Calcium-Smectite[J].Soil Science Society of America Journal,2006,70(6):1889-1895.
[9]ZHANG J Y,ZHU D Q,YU H X.Sorption of Aromatic Compounds to Clay Mineral and Model Humic Substance-Clay Complex:Effect of Solute Structure and Exchange Cation[J].Journal of Environment Quality,2008,37(3):817-823.
[10]石钰婷.模拟有机-矿质复合体对TCE的吸附实验研究[D].北京:中国地质大学,2012.
[11]BANSALO P.Thermo Dynamics of Equilibrium Adsorption of Antibiotics by Clay Minerals and Humic Acid-Clay Complexes[J].National Academy Science Letters-India.2012,35(2):109-114.
[12]GAO J,PEDERSEN J A.Sorption of Sulfonamide Antimicrobial Agents to Humic Acid-Clay Complexes[J].Journal of Environmental Quality,2010,39(1):228-235.
[13]HALE S E,LEHMAN N J,RUTHERFOR D D,etal.Quantifying the Total and Bioavailable Polycyclic Aromatic Hydrocarbons and Dioxins in Biochars[J].Environmental Science & Technology,2012,46(5):2830-2838.
[14]MOHAN D,SARSWA T A,YONG S,etal.Organic and Inorganic Contaminants Removal From Water With Biochar,a Renewable,Low Cost and Sustainable Adsorbent:A Critical Review[J].Bioresource Technology,2014,160(Suppl:1):191-202.
[15]陈宝梁,周丹丹,朱利中,等.生物炭质吸附对水中有机污染物的吸附作用及机理[J].中国科学B辑:化学,2008,38(6):530-537.
[16]王宁,侯艳伟,彭静静,等.生物碳吸附有机污染物的研究进展[J].环境化学,2012,31(3):287-295.
[17]邢颖,吕永龙,刘文彬,等.中国部分水域沉积物中多氯联苯污染物的空间分布、污染评价及影响因素分析[J].环境科学,2006,27(2):228-234.
[18]ANDERSSON P L,HAGLUN D P,TYSKLIND M.The Internal Barriers of Rotation for the 209 Polychlorinated Biphenyls[J].Environmetal Science & Pollutant Research,1997,4(2):75-81.
[19]SHIU W Y,MACKA Y D.A Critical Review of Aqueous Solubilities,Vapor Pressures,Henry Law Constants,and Octanol-Water Partition Coefficients of the Polychlorinated Biphenyls[J].Journal of Physical and Chemical,1986,15(2):911-929.
[20]HAWKER D W,CONNELL D W.Octanol-Water Partition Coefficients of Polychlorinated Biphenyl Congengers[J].Environmental Science & Technology,1988,22(4):382-387.
[21]ARROYOL L J,LI H,TEPPEN B J,etal.A Simple Method for Partial Purification of Reference Clays[J].Clays and Clay Minerals,2005,53(5):511-519.
[22]FANG G D,ZHU C Y,DIONYSIOS D,etal.Mechanism of Hydroxyl Radical Generation From Biochar Suspensions:Implications to Diethyl Phthalate Degradation[J].Bioresource Technology,2015,176:210-217.
[23]NKEDI-KIZZA P,RAO P S C,HORNSBY A G.Influence of Organic Cosolvents on Sorption of Hydrophobic Organic Chemicals by Soils[J].Environmental Science & Technology,1985,19 (10):975-979.
[24]CHIOU C T.Partition and Adsorption of Organic Contaminants in Environmental Systems[M].New Jersey,USA:John Wiley & Sons,2002:133-138.
[25]SU Y H,ZHOU Y G,SHENG G Y,etal.Linear Adsorption of Nonionic Organic Compounds From Water on Hydrophilic Minerals:Silica and Alumina[J].Environmental Science & Technology,2006,40(22):6969-6954.
[26]MADER B T,GOSS K U,EISENREICH S J.Sorption of Nonionichydrophobic Organic Chemicals to Mineral Surfaces[J].Environmental Science & Technology,1997,31(4):1079-1086.
[27]SEKI Y,YURDAKOC K.Adsorption of Promethazine Hydrochloride With KSF Montmorillonite[J].Adsorption,2006,12(1):89-100.
[28]YU Y,ZHUANG Y Y,WANG Z H.Adsorption of Water Soluble Dye Onto Functionalized Resin[J].Journal of Colloid and Interface Science,2001,242(2):288-293.
[29]周丹丹.生物碳质对有机污染物的吸附作用及机理调控[D].杭州:浙江大学,2008.
[30]BELES S B,RIFAI H S,RODRIGUES D F.Efficiency of Carbonaceous Materials for Sorbing Polychlorinated Biphenyls From Aqueous Solution[J].Environmental Science & Technology,2014,48(17):10372-10379.
[31]CORNELISSEN G,GUSTAFSSON O.Sorption of Phenanthrene to Environmental Black Carbon in Sediment With and Without Organic Matter and Native Sorbates[J].Environmental Science & Technology,2004,38(1):148-155.
(责任编辑: 陈昕)
Adsorption of Co-Planar and Non-Planar Chlorobiphenyls on Simulated Soil Components.
WANGPei-ran1,2,WANGYu-jun2,ZHOUDong-mei2,LIUCun2,FANGFeng-man1
(1.College of Territorial Resources and Tourism, Anhui Normal University, Wuhu 241003, China; 2.Key Laboratory of Soil Environment and Pollution Remediation/ Institute of Soil Science, Chinese Academy of Sciences, Nanjing 210008, China)
Abstract:Characteristics of the adsorption of ortho-substituted non-planar 2-chlorobiphenyl (2-CB) and non-ortho-substituted co-planar 4-chlorobiphenyl (4-CB) on three major simulated sorptive soil components: K+ saturated montmorillonite(K+-Mont), humic acid-clay mineral complexes(HA-Mont) and biochar(BC) were studied through batch equilibration experiments. Results show that the linear eqatio could be used to fit the adsorption isotherms of PCBs on all the three absorbents with the adsorption coefficient Kw being in the order of BC>HA-Mont>K+-Mont. Thermodynamic analysis of the adsorption isotherms as a function of temperature indicated that both surface adsorption and hydrophobic effect were the driving forces of the PCBs sorption on K+-Mont, while partition was the major one of the PCBs sorption on HA-Mont, for the interlayer spaces of montmorillonite are the major adsorption area, and the aromatic nanoporous surface of BC and the π-π effect between PCB molecules were the major driving forces, for the surface was the major adsorption area of BC. The sorption of 4-CB was higher than that of 2-CB on all the three absorbents despite that 2-CB and 4-CB are similar in hydrophobicity, which suggests that steric effect of the non-planar structure prevents 2-CB from accessing nano sized interlayer spaces of montmorillonite or nanopores on the surface of BC. All the findings in this study indicate that the three dimensional structures of organic pollutant molecules play an important role in their sorption and translocation in the soil.
Key words:polychlorobiphenyl;clay minerals;humic acid-clay mineral complex;biochar;adsorption
作者简介:王沛然(1989—),男,河北邢台人,硕士生,主要从事有机污染物吸附与控制方面的研究。E-mail: wangpr1432@163.com
DOI:10.11934/j.issn.1673-4831.2016.02.020
中图分类号:X131.3
文献标志码:A
文章编号:1673-4831(2016)02-0302-07
通信作者①E-mail: liucun@issas.ac.cn ②E-mail: ffm1974@mail.ahnu.edu.cn
基金项目:国家自然科学基金青年基金(41301535);国家自然科学基金面上基金(41371480);江苏省自然科学基金青年基金(BK20131042)
收稿日期:2015-06-03
