肺癌切除术后肺内孤立性转移复发灶的射频消融治疗效果分析
2016-04-18陈松宽杨光钊胡叶明陆海华
陈松宽 杨光钊 胡叶明 陆海华
浙江省立同德医院放射科,浙江杭州310012
肺癌切除术后肺内孤立性转移复发灶的射频消融治疗效果分析
陈松宽 杨光钊▲胡叶明 陆海华
浙江省立同德医院放射科,浙江杭州310012
目的探究分析肺癌切除术后肺内孤立性转移复发灶的射频消融治疗效果。方法随机选取我院2013年10月~2014年8月收治的95例肺癌切除术后肺内孤立性转移复发灶患者,将所选患者分为观察组(n=48)和对照组(n=47),对照组患者采用常规放疗化疗治疗,观察组患者采用射频消融术治疗,观察两组患者术后并发症及治疗效果,随访6个月调查两组患者的生存质量。结果观察组患者的射频消融过程均顺利完成,其术后并发症发生率为12.50%,经对症治疗后均逐渐消失,对照组患者的并发症发生率为23.40%,高于观察组(P<0.05);随访结果中观察组患者的生存质量显著优于对照组,两组比较差异具有统计学意义(P<0.05)。结论射频消融治疗肺癌切除术后肺内孤立性转移复发灶的临床疗效确切。
肺癌;肺切除;孤立性转移;射频消融;复发;生存质量
肺癌是临床诊疗中较为常见的恶性肿瘤之一,临床上常采用外科手术进行治疗,但是部分早期非小细胞肺癌患者在接受肿瘤切除后仍然会出现局部复发,导致临床治疗无效[1]。近年来,射频消融术以其高效的治疗效果成为肺癌切除术后局部复发患者的主要治疗手段,临床上关于射频消融术治疗肺内孤立性转移复发灶的研究及相关报道少之又少[2]。本文选取在我院治疗的95例肺癌切除术后肺内孤立性转移复发灶患者为研究对象,进一步探讨射频消融的治疗效果。现报道如下。
1 资料与方法
1.1 一般资料
研究对象均为2013年10月~2014年8月期间到我院肺癌切除术治疗的患者,入选标准[3]:①所选患者均在CT引导下行皮肺穿刺活检检查确诊;②经临床影像学诊断为肺内孤立性转移与局部复发;③患者肺部检查无其他并发病灶;④患者能够接受并自愿接受射频消融术治疗。排除标准:①患者身体素质较差不能耐受射频消融术;②患者出现肿瘤病灶合并远处转移;③患者肿瘤病灶复发时间与手术之间<6个月。按照随机数表法将所选95例患者分为两组。其中观察组48例患者中男25例,女23例,年龄22~64岁,平均(42.15±7.36)岁,经临床病理检查,腺癌22例,鳞癌26例。对照组47例患者中男24例,女23例,年龄23~67岁,平均(36.19±7.33)岁,临床病理检查结果显示,腺癌23例,鳞癌24例。两组性别、年龄、临床病理类型等一般资料比较,差异无统计学意义(P>0.05),具有可比性。
1.2 方法
1.2.1 对照组对照组患者在经临床检查确诊肿瘤复发局部病灶后,给予相应的放疗、化疗治疗。患者保持仰卧位,在负压真空体模立体定位体架上,双手上举置于前额部,抽空负压真空体模,让患者的身体相对固定,患者的体表以及定位架上的标记相对应,使用CT扫描,对患者制定三维适形放疗方案。以患者身体为放射治疗的中心,采用4~7个适形野,使用放射剂量激进型治疗。放射剂量为4Gy/次,3次/周,先进行10次,然后进行重新定位,再进行7次放射治疗,同期化疗治疗方案为1~3个周期VP-16 100 mg静脉滴注,在第1~3天,CDDP 40mg静脉滴注,化疗在患者放射治疗的第1周、4周、7周进行。
1.2.2 观察组观察组患者采用射频消融术治疗,首先实施局部麻醉后,在CT引导下,采用“四步法”整形穿刺定位,靶温度设置在90℃,采用250W射频发生器和射频针,消融时间控制在30~60 min,平均消融时间(37.92±8.39)min。其次,射频消融处理后,再经CT扫描检查确认肺癌病灶没有出现气胸、出血等并发症,可安排患者返回病房休息。术后给予患者预防性抗菌素治疗,并对后期出现咳血、发热等患者采取对症治疗。
1.3 观察指标
两组患者在接受治疗后均进行随访调查,观察两组患者的术后并发症情况及生存质量。
1.4 评价标准
1.4.1 术后并发症评估依据美国介入放射学会(Society of Interventional Radiology,SIR)分级标准[4],其中死亡病例需要经临床检测确定死亡原因,并说明与射频消融术治疗的关系;严重并发症患者出现致残现象,应增加住院时间,采取输血、胸腔闭式引流术等临床处理;轻微并发症包括肿瘤种植、气胸等;副作用包括肺内出血、胸腔积液、疼痛、血痰、胸膜反应以及射频消融综合征等,常伴随射频消融治疗出现,但是较少造成患者的实际损害。
1.4.2 生存质量评定采用SF-36健康调查问卷对患者进行生存质量的评定[5],该量表分为8个维度,即躯体功能(PF)、日常活动功能(RP)、身体疼痛(BP)、活力(VT)、社会交往功能(SF)、精神活动功能(RE)、心理健康(MH)、总体健康(GH)。数据收集过程中采用双盲法,每个维度分值范围0~100分,分值越高,表示患者的生存质量越好。
1.5 统计学分析
采用SPSS18.0统计学软件进行处理,计量资料采用均数±标准差(±s)表示,组间比较采用t检验,多组间数据对比采用ANOVA方差分析,计数资料用率(%)表示,采用χ2检验,检验标准α=0.05,P<0.05为差异有统计学意义。
2 结果
2.1 射频消融术治疗过程中的CT扫描结果
射频消融后经CT扫描可观察到肿瘤病灶呈现结节样(图1)或者空洞样(图2)。
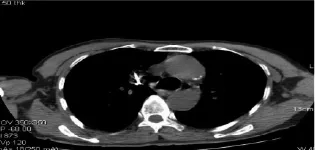
图1 CT引导下射频消融术中扫描右肺上叶转移灶
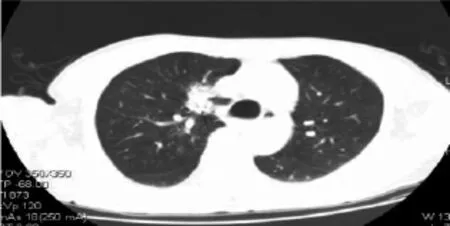
图2 射频消融后转移灶周围见磨玻璃样影覆盖
2.2 两组患者并发症比较
术后分别采用不同的护理干预,两组患者均出现不同程度的高烧不退、恶心呕吐、呼吸道感染等并发症,其中观察组患者的并发症发生率为12.50%,远远低于对照组的23.40%,观察组患者半年生存率为97.92%,对照组半年生存率为93.62%,两组比较差异无统计学意义(P>0.05)。见表1。
2.3 两组患者的生存质量比较
治疗前,两组生存质量的各维度指标比较,差异无统计学意义(P>0.05);随访6个月发现,观察组患者生存质量的8个维度评分与对照组比较,差异具有统计学意义(P<0.05)。见表2。

表1 两组患者术后并发症比较[n(%)]
表2 两组患者生存质量比较(±s,分)
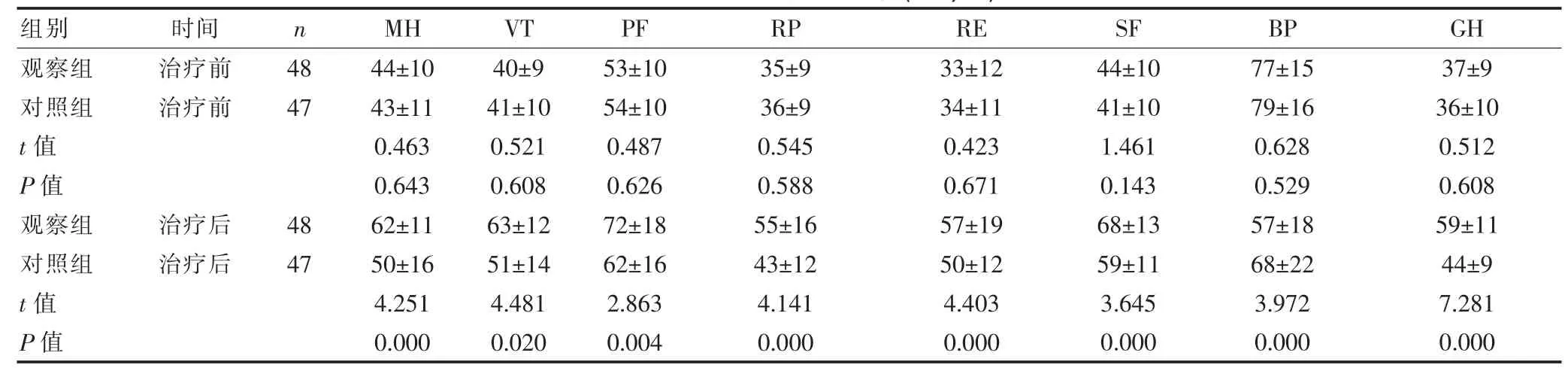
表2 两组患者生存质量比较(±s,分)
组别时间n MH VT PF RP RE SF BP GH观察组对照组t值P值观察组对照组t值P值治疗前治疗前48 47治疗后治疗后48 47 44±10 43±11 0.463 0.643 62±11 50±16 4.251 0.000 40±9 41±10 0.521 0.608 63±12 51±14 4.481 0.020 53±10 54±10 0.487 0.626 72±18 62±16 2.863 0.004 35±9 36±9 0.545 0.588 55±16 43±12 4.141 0.000 33±12 34±11 0.423 0.671 57±19 50±12 4.403 0.000 44±10 41±10 1.461 0.143 68±13 59±11 3.645 0.000 77±15 79±16 0.628 0.529 57±18 68±22 3.972 0.000 37±9 36±10 0.512 0.608 59±11 44±9 7.281 0.000
3 讨论
近年来,随着肿瘤热疗学的研究发展,射频消融术开始使用在肿瘤治疗中,临床研究发现射频消融术治疗肺部恶性肿瘤效果较好。此外,临床上采用的化疗方式也常因肿瘤耐药性而治疗失败,而射频消融术能够有效治疗肺部恶性肿瘤,加强对肿瘤转移的控制,具有较好的临床价值[6-8]。肿瘤病灶局部区域组织在射频消融后出现的相关病变征象是否完全覆盖肿瘤病灶,是临床上判断射频消融术是否成功的重要依据[9]。
国内外研究报道显示[10-12],射频消融术对早期肺癌切除术后复发、无法耐受手术患者等均具有较好的治疗效果。经CT引导下射频消融治疗能够减少患者的痛苦,提高患者生存质量,同时能够有效抑制周围残留癌组织,增强术后化疗敏感性。但是很多研究也发现CT引导下经皮穿刺射频消融治疗容易产生多种并发症,如气胸、感染等。是由于射频消融技术作用范围远远超过肿瘤病灶范围,再加上射频消融处理区域组织的成分较为复杂,在进行射频消融处理之前应先行CT扫描,初步判断肿瘤复发区域,以此提高手术治疗结果的准确性[13-15]。为了增加肿瘤抑制的效果,本研究中的手术治疗效果评价以术后1个月的CT增强扫描作为临床依据。本组研究中观察组患者术后的生活质量显著优于对照组,说明观察组患者采用射频消融治疗的效果良好,能够显著改善患者的肿瘤病灶治疗效果,提高生活质量。且对照组放化疗过程采用的化疗药物对机体具有一定的毒副作用,术后并发症发生率较高,容易产生呕吐、恶性等症状,也在一定程度上影响了患者的生活质量。另外,考虑到穿刺活检在临床病理检测中的重要作用,肿瘤病灶的复发也可依据肺癌患者的穿刺活检进行合理预估判断[16]。射频消融治疗,相对于手术切除以及放化疗治疗而言,其创伤小、安全性高,患者的可承受性高,射频消融可以对病灶进行清除,并最大限度地减轻对正常肝组织的损伤,完成射频消融之后,肿瘤组织可以吸收入血,形成一种内源性肿瘤抗原,激发患者机体的抗肿瘤免疫反应。射频消融治疗,患者的住院时间短,术后恢复好,创伤小,安全性高,且可以降低术后并发症等[17-20]。对于射频消融治疗的远期复发及预后需要进行长期跟踪调查,本组研究对其远期肿瘤复发率暂不作详述。
综上所述,肺癌切除术后肺内孤立性转移复发灶采用射频消融治疗的效果显著,能够明显提高患者的生活质量,但是如何从影像学上判断及时疗效并采取合理的粒子植入、靶向药物等联合治疗,是临床上治疗肺癌肿瘤病灶的关键,也是今后射频消融技术治疗的研究方向之一。
[1]赵洪伟,刘福全,岳振东,等.DSA旋转重建技术引导下射频消融治疗肺门区恶性肿瘤的临床疗效分析[J].实用医学杂志,2013,29(5):779-782.
[2]Schlijper RCJ,Grutters JPC,Houben R,et al.What to choose as radical local treatment for lungmetastases from colo-rectal cancer:Surgery or radiofrequency ablation?[J]. Cancer Treatment Reviews,2014,40(1):60-67.
[3]章丽,严志芳,王蕾,等.射频消融辅助肝细胞肝癌切除术6例的手术配合[J].中国乡村医药,2012,19(8):63-64.
[4]刘宝东,支修益.影像引导射频消融治疗肺部肿瘤专家共识(2015年版)[J].中国肺癌杂志,2015,18(5):251-259.
[5]伍时佐.CT引导经皮肺穿刺锚状电极高温射频消融治疗肺部肿瘤临床研究[J].中国实用医药,2015,9(13):108-109.
[6]张康,张鲁昌,张广敬,等.CT引导下射频消融治疗肺癌36例临床分析[J].山东医药,2015,14(5):77-79.
[7]陈仕林,许林,张勤,等.CT导向射频消融治疗肺部恶性肿瘤[J].中国癌症防治杂志,2014,10(3):271-274.
[8]周爱芽,马萍,许怿靓,等.房颤射频消融术后抗凝治疗的观察与护理[J].中国乡村医药,2015,22(19):73-74.
[9]赖全图,顾萍,陈卫群,等.超声引导射频消融治疗肺肿瘤的临床观察[J].实用癌症杂志,2013,28(6):768-769.
[10]杨福奎,陈德路.CT引导下肿瘤四维立体定位精确穿刺弓箭射频消融治疗肺癌[J].中国肿瘤外科杂志,2014,6(3):153-157.
[11]Modesto A,Giron J,Massabeau C,et al.Radiofrequency ablation for non-small-cell lung cancer in a single-lung patient:Case report and review of the literature[J].Lung cancer:Journal of the International Association for the Study of Lung Cancer,2013,80(3):341-343.
[12]Angela C Tramontano,Lauren E Cipriano,Chung Yin Kong,et al.Microsimulationmodel predicts survival benefit of radiofrequency ablation and stereotactic body radiotherapy versus radiotherapy for treating inoperable stage inon-small cell lung cancer[J].AJR:American Journal of Roentgenology:Including Diagnostic Radiology, Radiation Oncology,Nuclear Medicine,Ultrasonography and Related Basic Sciences,2013,200(5):1020-1027.
[13]杨宇辉,陈仲武,林征宇,等.CT引导下射频消融治疗肺部恶性肿瘤的疗效评价[J].中国介入影像与治疗学,2015,11(2):77-79.
[14]Simon TG,Beland MD,MacHan JT,et al.Charlson Comorbidity Index predicts patient outcome,in cases of inoperable non-small cell lung cancer treated with radiofrequency ablation[J].European Journal of Radiology,2012,81(12):4167-4172.
[15]刘宝东,刘磊,李岩,等.射频消融治疗100例肺部肿瘤的远期疗效[J].中国肺癌杂志,2011,14(4):335-339.[16]韩景奇,李涌,陈明,等.CT引导结直肠癌肺内孤立性转移灶的射频消融治疗[J].中国医师进修杂志,2015,38(5):342-345.
[17]祝明华,江寅芳,杨运海,等.肝癌术后孤立性肺转移灶切除术的临床应用[J].医学研究杂志,2013,42(5):117-119.
[18]龚柳.射频消融术治疗肺部恶性肿瘤的临床观察[D].浙江大学医学院,2009.
[19]罗君,邵国良,郑家平,等.CT引导下射频消融治疗33例肺癌的回顾性分析[J].介入放射学杂志,2015,11(6):530-533.
[20]郭俊,王海江,尹永厚,等.动脉化疗联合射频消融术治疗中晚期肺癌的临床观察[J].中国医药指南,2015,9(24):58-59.
Effect analysis on radiofrequency ablation of pulmonary solitary metastasis recurrent fociafter lung cancer resection
CHEN Songkuan YANGGuangzhao HU Yeming LU Haihua
Department of Radiology,Zhejiang Provincial Tongde Hospital,Hangzhou 310012,China
Objective To discuss and analyze the effect of radiofrequency ablation(RFA)on pulmonary solitarymetastasis recurrent foci after lung cancer resection.M ethods 95 patientswith pulmonary solitarymetastasis recurrent foci after lung cancer resection treated in our hospital from October 2013 to August 2014 were selected and divided into observation group(n=48)and control group(n=47).Patients in the control group were given routine radiotherapy and chemotherapy,while those in the observation group were given RFA.The postoperative complications and treatment effectswere observed in both group,and the patientswere followed up for 6months to evaluate their quality of life.Results RAF were all successfully conducted in the observation group,with an incidence rate of 12.50%as to the postoperative complications,which were all resolved after symptomatic treatment.And the incidence rate of complicationswas 23.40%in the control group,which was significantly higher than that in the observation group(P<0.05).The results of follow up showed that the life quality was significantly higher in the observation group than in the control group(P<0.05).Conclusion RFA has definite effects in treatment of pulmonary solitary metastasis recurrent foci after lung cancer resection.
Lung cancer;Pulmonary resection;Solitary metastasis;Radiofrequency ablation;Recurrence;Quality of life
R734.2
A
1673-9701(2016)18-0023-04
2016-03-05)
浙江省医药卫生科技计划A类基金项目(2013 KYA036)
▲通讯作者
