氧化受损甘氨酸分子内质子迁移的机理
2016-04-11孟祥军杨笑春贾俊芳唐山师范学院化学系河北唐山063000
孟祥军,石 瑾,杨笑春,贾俊芳,杨 静(唐山师范学院化学系,河北唐山063000)
氧化受损甘氨酸分子内质子迁移的机理
孟祥军*,石 瑾,杨笑春,贾俊芳,杨 静
(唐山师范学院化学系,河北唐山063000)
摘要:采用M06,B3LYP和CCSD方法,在6-31++G(**)基组水平研究了氧化受损甘氨酸分子的构象异构化机理,探讨了甘氨酸氧化受损后的性质变化和溶剂化效应.找到7个甘氨酸阳离子稳定构型和9个过渡态,发现甘氨酸阳离子构象异构化过程存在质子迁移反应,质子从羧基迁移到氨基的能垒为15.2 kJ/mol,从α-C迁移到羰基O的能垒为138.6 kJ/ mol;最稳定甘氨酸构象失去一个电子的垂直电离势为878.0 kJ/mol;N5原子失电子最多(超过0.4),其他各原子失去电荷不多(均低于0.1);电荷变化导致迁移质子所在化学键显著被削弱.溶剂化效应能显著增高质子迁移反应能垒.
关键词:氧化损伤;甘氨酸阳离子;质子迁移;反应机理;量子化学
氨基酸是重要的生命物质,参与众多生理过程;氨基酸分子结构和性质的研究[1-2]是深入探讨其在生化反应中变化情况的基石,也是理解复杂生物分子(如多肽和蛋白质等)结构和功能的基础.近年来蛋白质氧化损伤现象成为自由基生物学研究的热点之一[3],人们发现许多病理过程中酶的失活都与肽链上氨基酸的氧化受损有关[4].
甘氨酸(glycine)在20种天然氨基酸中结构最简单,所以它是实验和理论研究的首选测试对象.对于甘氨酸构象和稳定性的认识已经比较清晰:量子化学理论研究[5-10]得到8种甘氨酸分子稳定构象,电子衍射技术[11]、基质隔离红外光谱技术[12]、振动拉曼光谱技术[13]实验观测得到3种稳定构象;理论结果和实验结果存在的差异也得到了合理的解释[14].氧化受损产生的甘氨酸自由基的结构、性质和解离过程也有较多文献报道[15-19],然而有关甘氨酸阳离子结构和性质的文献比较缺乏.2000年Rodríguez-Santiago等采用B3LYP和BHLYP等理论方法研究了4种甘氨酸阳离子构象,并发现分子内能够发生质子迁移反应[20]; 2005年Simon等采用B3LYP/6-31++G(d,p)方法研究了甘氨酸阳离子最稳定构象的裂解产物[21];2012 年Lee采用B3LYP/6-31++G**方法研究了丙氨酸阳离子分子内质子迁移反应机理[22].
通过比较甘氨酸和甘氨酸阳离子的相关文献,我们认识到:1)甘氨酸阳离子构象的研究尚不全面;2)甘氨酸阳离子构象间的异构化机理不清楚; 3)氧化对甘氨酸结构和性质的影响仍不清楚;4)缺乏溶剂化效应方面的认识.本文针对上述问题,采用量子化学理论方法系统地研究了甘氨酸阳离子构象间的异构化机理.
1 计算方法
本文采用B3LYP/6-31+ +G**方法和M06/6-31++G**方法[23]对甘氨酸阳离子结构进行全梯度优化.找出稳定态构象后,采用QST2方法寻找构象间转化的过渡态结构.再对各构象进行振动频率计算,对过渡态进行反应内禀坐标(IRC)计算来验证各结构的正确性.然后对M06/6-31++G**方法下的各构象采用CCSD/6-31++G**方法计算单点能,并对能量进行了零点能(ZPE)校正;采用相对能ΔE(ΔE =E-Emin,其中Emin是最稳定构象的能量)表示各构象的能量大小.最后采用极化连续介质(PCM)模型计算了CCSD∥M06/6-31++G**方法下的溶剂化效应.所有计算任务均使用Gaussian 09程序完成.
2 结果与讨论
2.1稳定构象
本文找到7种甘氨酸阳离子稳定构象,示于图1.构象间转化的过渡态有9个,过渡态的名称由对应的反应物和产物名称组合得到.为了便于讨论构象转化机理,先统一不同构象中相应原子的编号(见图1中的构象Ⅰ),再将这些构象按照转化途径进行排列.
各构象能量数据(ΔE、异构化正反应的活化能Ea和逆反应活化能Ea')列于表1,其中υ1和υ2分别是M06/6-31++G**方法下的第一和第二振动频率,υ1为正表明构象是稳定态,υ1为负而υ2为正则表明构象是过渡态.在CCSD/6-31++G**方法下,构象稳定性顺序为Ⅶ>Ⅰ>Ⅱ>Ⅲ>Ⅳ>Ⅴ>Ⅵ,ΔE分别为0,80.3,94.3,103.6,124.4,141.3,147.0 kJ/mol,最稳定构象Ⅶ为二醇形式.
在过渡态中:Ⅰ-Ⅲ由相应构象旋转C1—N5键得到,CCSD/6-31++G**方法下ΔE为104.1 kJ/mol,构象Ⅰ转化为Ⅲ的Ea为23.8 kJ/mol,Ea'为0.4 kJ/ mol;Ⅱ-Ⅲ和Ⅴ-Ⅵ都对应于C1—C2键的旋转,ΔE不超过11.8 kJ/mol;Ⅱ-Ⅵ和Ⅲ-Ⅴ是C2—O4键旋转的过渡态,Ea分别为63.5和49.2 kJ/mol,Ea'分别为10.8和11.5 kJ/mol;Ⅳ-Ⅵ是质子从羧基迁移到氨基的过渡态,Ea和Ea'分别为37.8和15.2 kJ/mol;Ⅰ-Ⅱ和Ⅲ-Ⅱ是质子在2个羧基O原子间的迁移,ΔE高于170.5 kJ/mol;Ⅱ-Ⅶ是α-H迁移到羰基O的过渡态,Ea为138.6 kJ/mol.

图1 甘氨酸阳离子的构象及转化途径Fig.1 The stable conformers of glycine cations and the isomerization reaction paths
2.2构象转化机理
甘氨酸阳离子构象间转化的途径和能级变化示于图2.2个羧基O原子间质子迁移的ΔE高于170.5 kJ/mol,反应难以发生;构象Ⅶ是α-H迁移的产物, ΔE达162.6 kJ/mol,该反应也难以发生;而质子从羧基迁移到氨基变为兼性离子Ⅳ的ΔE只有15.2 kJ/mol,该反应容易发生.因此我们重点介绍由构象Ⅰ转变为兼性离子Ⅳ的机理,转化途径为:Ⅰ↔Ⅰ-Ⅲ↔Ⅲ↔Ⅲ-Ⅴ↔Ⅴ↔Ⅴ-Ⅵ↔Ⅵ↔Ⅳ-Ⅵ↔Ⅳ.
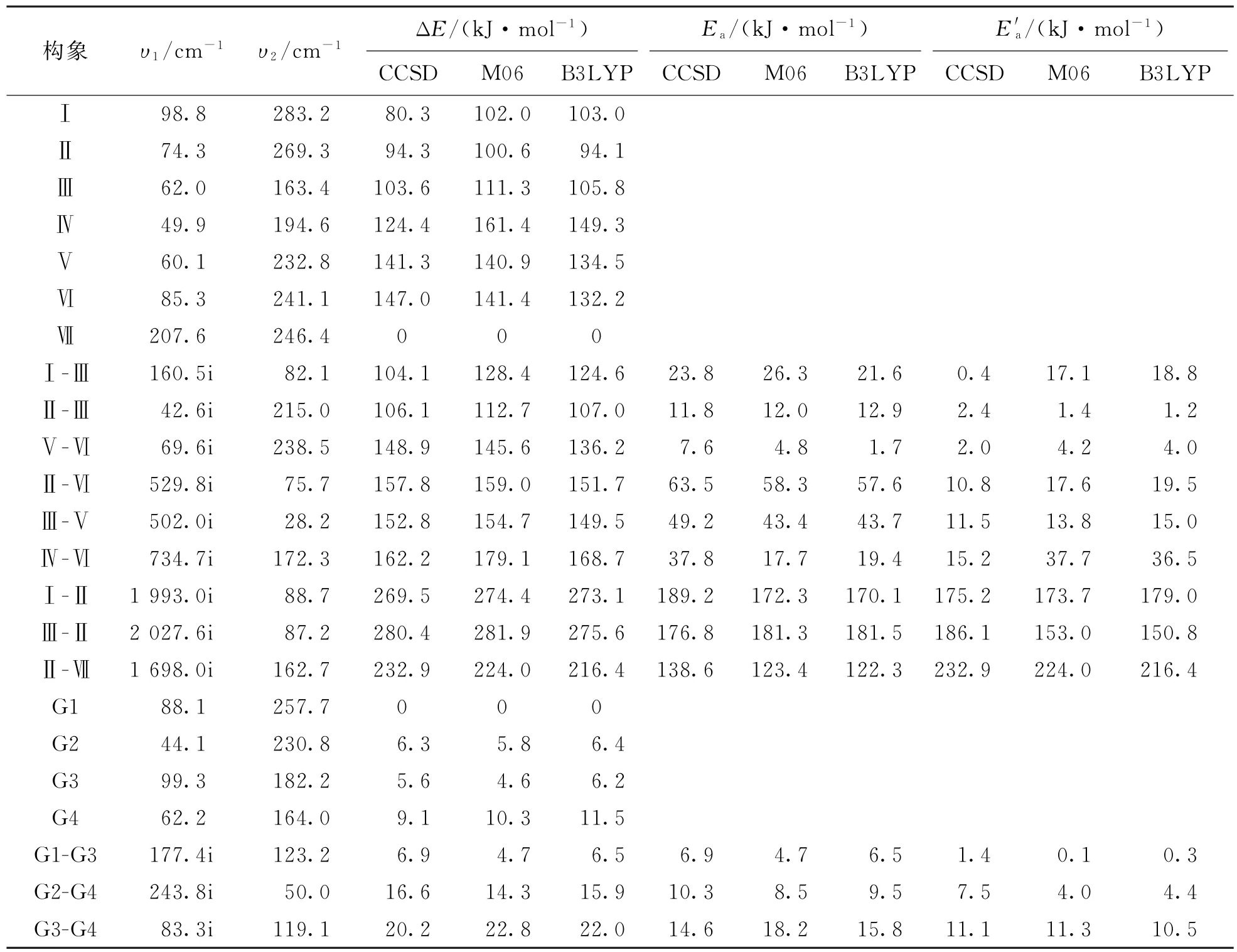
表1 构象的振动频率和能量数据Tab.1 The vibration frequency variations and energy data of each conformer

图2 CCSD∥M06/6-31++G(d,p)方法下的甘氨酸阳离子构象转化能级图Fig.2 The energy level diagram of isomerization reaction of glycine cations by CCSD∥M06/6-31++G(d,p)
构象Ⅰ经C1—N5键的旋转变为过渡态Ⅰ-Ⅲ(二面角Φ(H7—N5—C1—C2)由180.0°变为118.0°),能量升高23.8 kJ/mol;C1—N5键继续旋转(Φ(H7—N5—C1—C2)变为87.2°),得到构象Ⅲ,能量降低0.4 kJ/mol.
构象Ⅲ经C2—O4键的旋转变为过渡态Ⅲ-Ⅴ(Φ(H6—O4—C2—C1)由-179.3°变为-86.8°),能量升高49.2 kJ/mol;C2—O4键继续旋转(Φ(H6—O4—C2—C1)变为-3.6°),得到构象Ⅴ,能量降低11.5 kJ/mol.
构象Ⅴ经C1—C2键的旋转变为过渡态Ⅴ-Ⅵ(Φ(N5—C1—C2—O4)由148.3°变为52.4°),能量升高7.6 kJ/mol;C1—C2键继续旋转(Φ(N5—C1—C2—O4)变为0°),得到构象Ⅵ,能量降低2.0 kJ/mol.
构象Ⅵ经质子迁移变为构象Ⅳ.构象Ⅵ中H6质子距离O4原子97.4 pm,距离N5原子230.6 pm. H6质子远离O4原子,距离N5原子130.2 pm时(此时距离O4原子122.8 pm),得到过渡态Ⅳ-Ⅵ,能量升高15.3 kJ/mol;H6质子继续靠近N5原子到104.8 pm时(此时距离O4原子188.8 pm),得到构象Ⅳ,能量降低37.9 kJ/mol.
2.3甘氨酸氧化受损后的性质变化
按照垂直电离的概念,图3中甘氨酸最稳定3种构象G1、G2和G3(能量数据见表1)经垂直电离相应地得到甘氨酸阳离子Ⅲ、Ⅱ和Ⅰ.G3→Ⅰ、G2→Ⅱ和G1→Ⅲ的垂直电离势分别为849.2,862.4和878.0 kJ/mol,G1异构化为G3的能垒为6.9 kJ/mol,所以甘氨酸阳离子Ⅰ比最稳定甘氨酸分子G1的能量高856.1 kJ/mol.
甘氨酸失去一个电子变为阳离子,从表2中甘氨酸各位点ΔQ数据可知:N5原子失电荷最多,超过0.41;除C1原子外,其他原子电荷均有缺失,但是幅度较小,不超过0.1;C1原子电荷有增有减,变化不大,低于0.08.从ΔR(O4—H6)和Δυ(O4—H6)数据可知:氧化损伤导致迁移质子所在化学键(O4和H6原子间的化学键)的键长增加0.5 pm以上,导致该键振动的红移超过64.1 cm-1,迁移质子所在化学键被削弱,可见氧化损伤有利于甘氨酸羧基H迁移到氨基上.
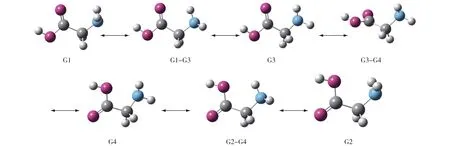
图3 CCSD∥M06/6-31++G(d,p)方法计算的甘氨酸构象转化途径Fig.3 Conformational isomerization paths of glycine calculated with the CCSD∥M06/6-31++G(d,p)
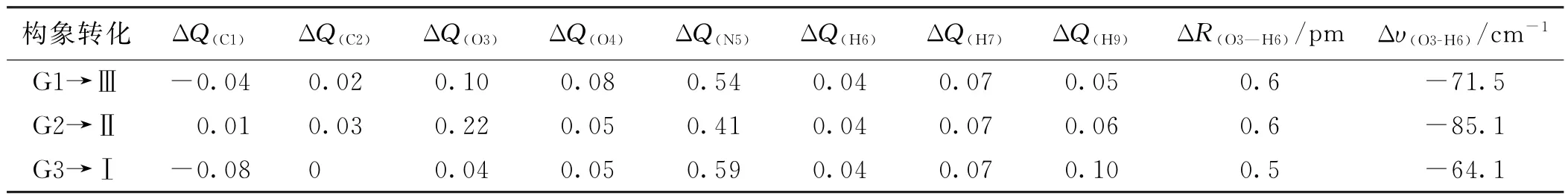
表2 氧化损伤后甘氨酸中各位点的电荷、键长和振动频率的变化值(ΔQ、ΔR(O4—H6)和Δυ(O4—H6))Tab.2 The differences of charge,bond length and vibration frequency after oxidation of glycine
2.4甘氨酸阳离子异构化的溶剂化效应
采用PCM模型,在CCSD∥M06/6-31++G**方法下考查甘氨酸阳离子异构化的水溶剂化效应.考虑水溶剂的作用后,图1中大部分构象的结构并未发生明显变化(如PCM模型下的[Ⅰ]与气相模型的Ⅰ结构相近),图1仍可作为构象异构化途径和机理的参照.溶剂化效应引起的主要结构变化如下:1)构象Ⅲ经全优化后氨基发生旋转(氨基H最终与分子骨架共面),得到的稳定构象[Ⅲ]与[Ⅰ]结构相同(二者区别是H7和H8位置互换),[Ⅲ]与[Ⅰ]转化的过渡态是[Ⅰ-Ⅲ](结构与Ⅰ-Ⅲ相近);2)Ⅰ-Ⅱ和Ⅲ-Ⅱ收敛为同一过渡态[Ⅰ-Ⅱ](结构与Ⅰ-Ⅱ相近);3)Ⅲ、Ⅲ-Ⅴ和Ⅴ3个构象的氨基旋转至与分子骨架共面,对应变为[Ⅲ]、[Ⅲ-Ⅴ]和[Ⅴ].
表3列出了PCM模型下各构象的能量数据.依据CCSD∥M06/6-31++G**方法,各构象的稳定性次序为[Ⅶ]>[Ⅰ]=[Ⅲ]>[Ⅱ]>[Ⅴ]>[Ⅵ]>[Ⅳ], ΔE分别为0,71.9,71.9,81.5,90.2,122.1,129.7 kJ/mol,可见最稳定构象还是二醇形式的[Ⅶ],但是溶剂化效应使构象[Ⅳ]的相对稳定性变差;此外,溶剂化效应显著地增高了质子迁移反应的能垒,如构象[Ⅳ-Ⅵ]反应能垒增高54.0 kJ/mol(即表3中ΔE值91.8 kJ/mol与表1中对应的Ea值37.8 kJ/mol之差,下同),[Ⅰ-Ⅱ]和[Ⅱ-Ⅶ]的反应能垒分别增高34.9和77.1 kJ/mol.
3 结 论
本文采用M06/6-31++G**方法和B3LYP/6-31 ++G**方法研究了甘氨酸阳离子构象异构化反应机理,并探讨了甘氨酸氧化受损后的性质变化和溶剂化效应,得到如下结论:
1)甘氨酸阳离子稳定构象有7个,甘氨酸阳离子构象异构化过程存在质子迁移反应,质子从羧基迁移到氨基的能垒为15.3 kJ/mol,质子从α-H迁移到羰基O的能垒为138.6 kJ/mol;
2)最稳定甘氨酸构象变为甘氨酸阳离子的垂直电离能为878.0 kJ/mol;
3)甘氨酸失去一个电子变为阳离子,N5原子失电子最多(超过0.4),其他各原子失去的电荷不多(均低于0.1),变为阳离子后利于质子从羧基迁移到氨基;
4)溶剂化效应显著增高了质子迁移反应能垒.
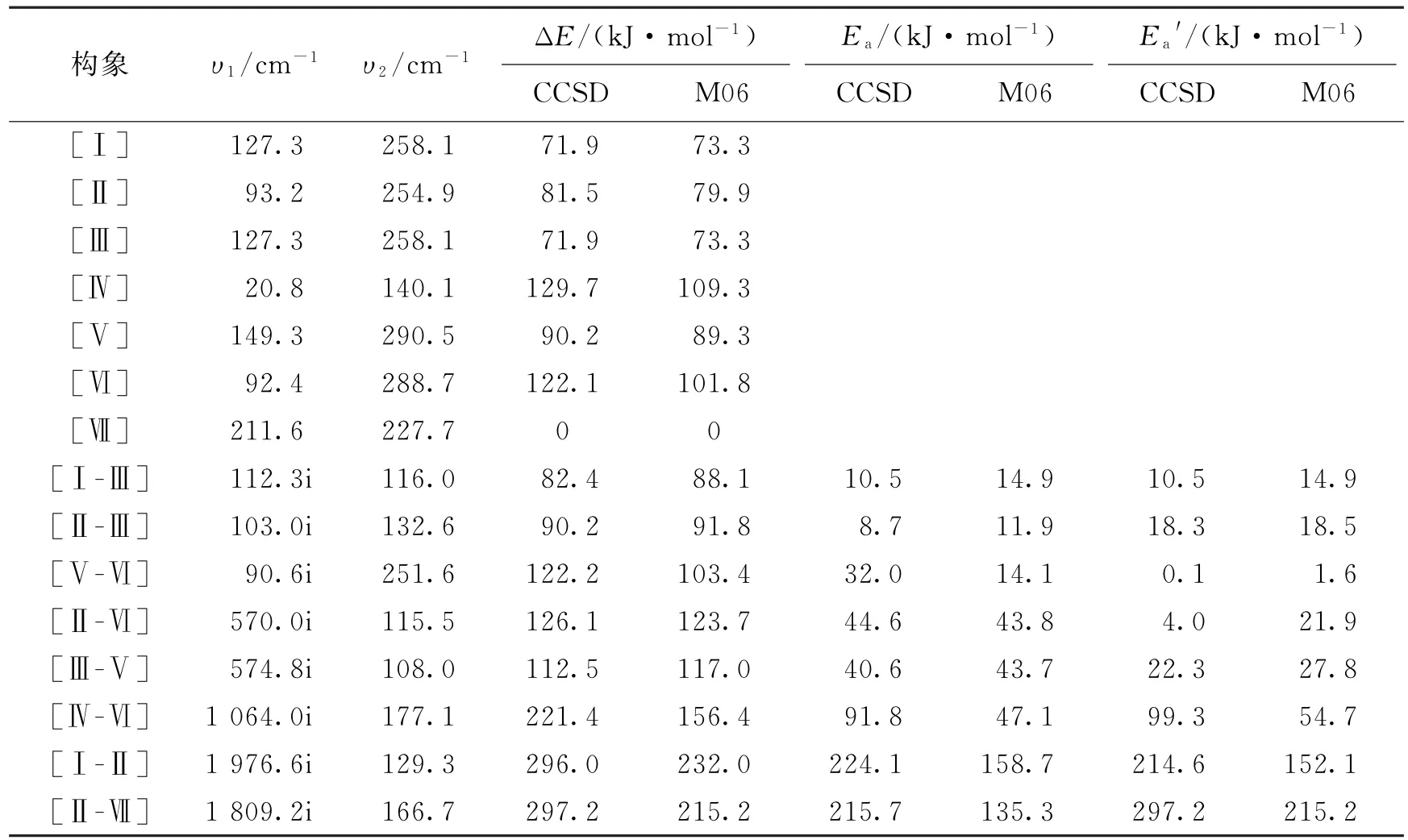
表3 PCM模型下各构象的振动频率和能量数据Tab.3 The vibration frequency variations and energy data of each conformer by PCM model
参考文献:
[1] 田善喜.氨基酸分子构象稳定性与光电离解离动力学的氢键效应[J].化学进展,2009,21(4):601-605.
[2] 钟亮,胡勇军,邢达,等.生物分子的微溶剂化过程[J].化学进展,2010,22(1):1-7.
[3] RAUK A,YU D,ARMSTRONG D A.Oxidative damage to and by cysteine in proteins:an ab initio study of the radical structures,C—H,S—H,and C—C bond dissociation energies,and transition structures for H abstraction by thiyl radicals[J].J Am Chem Soc,1998,120(34): 8848-8855.
[4] STADMAN E R.Oxidation of free amino acids and amino acid residues in proteins by radiolysis and by metal-catalyzed reactions[J].Annu Rev Biochem,1993,62(7): 797-821.
[5] JENSEN J H,GORDON M S.Conformational potential energy surface of glycine:a theoretical study[J].J Am Chem Soc,1991,113(21):7917-7924.
[6] CSASZAR A G.Conformers of gaseous glycine[J].J AmChem Soc,1992,114(24):9568-9575.
[7] AIKENS C M,GORDON M S.Incremental solvation of nonionized and zwitterionic glycine[J].J Am Chem Soc, 2006,128(39):12835-12850.
[8] KE H W,RAO L,XU X,et al.Theoretical study of glycine conformers[J].J Theor Comput Chem,2008,7 (4):889-909.
[9] BALABIN R M.Conformational equilibrium in glycine: focal-point analysis and abinitio limit[J].Chem Phys Lett,2009,479(4/5/6):195-200.
[10] HIDENORI M,MISAKO A.Ab initio QM/MM-MC study on hydrogen transfer of glycine tautomerization in aqueous solution:helmholtz energy changes along watermediated and direct processes[J].Chem Lett,2013,42 (6):598-600.
[11] IIJIMA K,TANAKA K,ONUMA S.Main conformer of gaseous glycine:molecular structure and rotational barrier from electron diffraction data and rotational constants[J].J Mol Struct,1991,246(3/4):257-266.
[12] STEPANIAN S G,REVA I D,RADCHENKO E D,et al.Matrix-isolation infrared and theoretical studies of the glycine conformers[J].J Phys Chem A,1998,102 (6):1041-1054.
[13] BALABIN R M.Experimental thermodynamics of free glycine conformations:the first Raman experiment after twenty years of calculations[J].Phys Chem Chem Phys,2012,14(1):99-103.
[14] 孟祥军.甘氨酸构象异构化机理的密度泛函理论研究[J].南开大学学报(自然科学版),2013,46(3):15-22.
[15] TUREˇCEK F,CARPENTER F H.Glycine radicals in the gas phase[J].J Chem Soc Perkin Trans,1999,2 (11):2315-2323.
[16] GIL A,SIMON S,SODUPE M,et al.Gas-phase protontransport self-catalysed isomerisation of glutamine radical cation:the important role of the side-chain[J]. Theor Chem Account,2007,118(3):589-595.
[17] YANG G,ZU Y G,ZHOU L J.Deprotonation and radicalization of glycine neutral structures[J].J Phys Org Chem,2008,21(1):34-40.
[18] PHILIPPE C,ALAIN D,ILARIA C,et al.Vibrational analysis of glycine radical:a comparative ab initio static and dynamic study[J].Phys Chem Chem Phys,2009, 11(21):4375-4384.
[19] SYLVAIN M,DARIUSZ G P,RUDY D,et al.Stability of the glycine cation in the gas phase after interaction with multiply charged ions[J].Eur Phys J D,2014,68 (6):149-156.
[20] RODRÍGUEZ-SANTIAGO L,SODUPE M,OLIVA A, et al.Intramolecular proton transfer in glycine radical cation[J].J Phys Chem A,2000,104(6):1256-1261.
[21] SIMON S,GI L A,SODUPE M,BERTRAN J. Structure and fragmentation of glycine,alanine,serine and cysteine radical cations.A theoretical study[J].J Mol Struct,2005,727(1/2/3):191-197.
[22] LEE G.Structure and intramolecular proton transfer of alanine radical cations[J].Bull Korean Chem Soc,2012, 33(5):1561-1565.
[23] 孟祥军.取代基效应对水分子催化甘氨酸质子迁移反应的影响[J].厦门大学学报(自然科学版),2014,53(3): 390-396.
Intramolecular Proton-transfer Mechanism of Oxidized Glycine Molecule
MENG Xiangjun*,SHI Jin,YANG Xiaochun,JIA Junfang,YANG Jing
(Department of Chemistry,Tangshan Normal University,Tangshan 063000,China)
Abstract:M06,B3LYP and CCSD methods were applied at the 6-31++G(**)basis set level to investigate the isomerization mechanism of glycine cations.In addition,property differences caused by oxidation and solvation effect were discussed.7 stable minimums and 9 transition states of glycine cations were obtained.It is found that the carboxyl proton can transfer to amino by stepping over a 15.2 kJ/mol energy barrier during the isomerization reactions,andα-H can transfer to carbonyl O over a 138.6 kJ/mol energy barrier.Vertical ionization potential of the most stable glycine conformation is 878.0 kJ/mol.More than 0.4 charge was lost on N5 atom in ionization process,while on other atoms less than 0.1 charge was lost.The charge variation is conducive to the reaction of proton transfer,while solvation effect greatly increases the energy barriers of proton transfer reactions.
Key words:oxidation damage;glycine cation;proton-transfer;reaction mechanism;quantum chemistry
*通信作者:xjmeng_1974@126.com
基金项目:河北省高等学校科学技术研究青年基金(QN2014312);唐山师范学院科学研究重点项目(2015B04)
收稿日期:2015-05-28 录用日期:2015-08-29
doi:10.6043/j.issn.0438-0479.2016.02.004
中图分类号:O 641
文献标志码:A
文章编号:0438-0479(2016)02-0168-06
引文格式:孟祥军,石瑾,杨笑春,等.氧化受损甘氨酸分子内质子迁移的机理[J].厦门大学学报(自然科学版),2016,55(2): 168-173.
Citation:MENG X J,SHI J,YANG X C,et al.Intramolecular proton-transfer mechanism of oxidized glycine molecule[J]. Journal of Xiamen University(Natural Science),2016,55(2):168-173.(in Chinese)
