自乳化释药系统与液固压缩技术联用于黄芩苷制剂的研究
2016-04-08李小芳李培培向志芸刘海霞
周 维, 李小芳, 李培培, 向志芸, 李 平, 刘海霞
(成都中医药大学药学院,中药材标准化教育部重点实验室,四川省中药资源系统研究与开发利用重点实验室—省部共建国家重点实验室培育基地,四川成都611137)
自乳化释药系统与液固压缩技术联用于黄芩苷制剂的研究
周 维, 李小芳*, 李培培, 向志芸, 李 平, 刘海霞
(成都中医药大学药学院,中药材标准化教育部重点实验室,四川省中药资源系统研究与开发利用重点实验室—省部共建国家重点实验室培育基地,四川成都611137)
摘要:目的 联合运用自乳化释药系统和液固压缩技术增加黄芩苷的溶出度,优选最佳处方。方法 以自乳化释药系统(吐温-80—PEG-400—油酸乙酯)为液体赋形剂,微晶纤维素PH-101为载体材料,微粉硅胶200为涂层材料,考察黄芩苷与赋形剂之比和载体材料与涂层材料的质量比(R值),筛选出最佳处方,比较与原料药、市售片的溶出度,通过差示扫描量热分析考察药物的晶型转化。结果 黄芩苷与赋形剂之比为25%,R值为15时,在6.4 min内即可使溶出度达到50%。差示扫描量热分析表明,液固压缩片中主药的特征峰消失。结论 自乳化释药系统和液固压缩技术联用可使黄芩苷以无定形或分子状态溶出,且释药快速,并使药物以无定形或分子状态给药。
关键词:自乳化释药系统;液固压缩技术;黄芩苷;溶出度;差示扫描量热分析
dol:10.3969/j.issn.1001-1528.2016.02.015
网络出版日期: 2015-09-24
KEY W 0RDS: se1f-emu1sifying drug de1ivery system(SEDDS);1iquid so1id comPression technique;baica1in;disso1ution;differentia1scanning ca1orimetry ana1ysis
自乳化释药系统(se1f-emu1sifying drug de1ivery system,SEDDS)是由油相、表面活性剂及助表面活性剂形成的固体或液体系统,而液固压缩技术(1iquid so1id comPression techniques)又名溶液粉末化技术,是将难溶性药物悬浮或溶解在非挥发性液体赋形剂中,再与适宜的载体和涂层材料混合均匀,转变为具有非黏性、良好流动性和可压性的干燥粉末[1]。研究表明,这两种技术在药物増溶方面已有很好的效果,但还未联合应用于中药制剂的増溶领域,两者联用不仅可以弥补SEDDS所存在的不足,能够将液体SEDDS固化,从而将药物制成片剂、胶囊剂等多种剂型,实现剂型的多样化,还可以显著提高药物的溶出度和溶出速率,从而提高药物的生物利用度。
黄芩苷为黄酮类化合物,是从唇形科植物黄芩的干燥根提取分离得到的,具有清热解毒、抑菌抗炎、降压等药理作用,临床用于肝炎、高血压等疾病[2]。黄芩苷由于其分子呈平面型,分子间引力大,水溶性低,胃肠吸收差,故生物利用度低。因此,本实验以自乳化释药系统为液体赋形剂,将液体固化,制备黄芩苷液固压缩片以增加其溶出度,并探讨它在液固压缩片中的存在形式。
1 仪器与试药
1.1 仪器 BP61型电子天平(十万分之一,德国Satorius公司);85-2型恒温磁力搅拌器(江苏金坛市金城国胜实验仪器厂);DP-I型单冲压片机(上海市药材有限公司中药机械厂);ZRS-8G智能溶出试验仪(天津市天大天发科技有限公司);CJY-300B型片剂脆碎度测试仪(上海黄海药检仪器厂);UV-6000型紫外可见分光光度计(上海美谱达仪器有限公司);SB-5200DT型超声仪(功率200 W,工作频率40 kHz,宁波新芝生物科技股份有限公司);DSC差示扫描量热仪(北京恒久科学仪器厂)。
1.2 试药 黄芩苷(纯度>95%,实验室自制);黄芩苷对照品(成都曼斯特生物科技有限公司,批号MUST-14083014);黄芩苷片(湖南绅泰春药业有限公司,批号20150301)。油酸乙酯(上海飞祥化工厂);聚乙二醇400(PEG400)、吐温-80、微晶纤维素(MCC)PH-101、羧甲基淀粉钠(成都市科龙化工试剂厂);微粉硅胶200为药用级(上海风鸿医药科技有限公司)。蒸馏水(自制)等。
2 方法与结果
2.1 自乳化释药系统的制备 通过测定黄芩苷在辅料中的溶解度,筛选增溶效果较好的油相、表面活性剂、助表面活性剂,绘制伪三元相图。并采用星点设计-效应面法,以形成乳液的乳化时间、粒径、载药量为考察指标,以总评OD值为效应变量,对处方进行优化,筛选最佳处方比例。
优选出的黄芩苷自乳化释药系统处方其质量比为吐温-80∶PEG-400∶油酸乙酯(1.13∶0.52∶0.2),按照最佳处方比例称取吐温-80 11.3 g、PEG-400 5.2 g、油酸乙酯2 g,在25℃下磁力搅拌均匀,室温放置24 h,备用。
所筛选的最佳自乳化释药系统按照空白乳与水1 g∶50 mL比例混合,形成澄清透明且带少许蓝色荧光的溶液,测出黄芩苷在自乳化释药系统中的溶解度为(0.269±1.315)mg/mL,在水中的溶解度为(0.053±0.365)mg/mL。由此可知,将黄芩苷制成微乳后,其在水中的溶解度明显提高。
2.2 液固压缩片的制备
2.2.1 液固压缩系统的数学模型[3-5]液固压缩系统中的最佳载体和涂层材料的用量比例是通过SPireas提出的数学模型计算的,该模型的计算公式为R=Q/q(1);Lf=W/Q(2);Lf=φCA+φCO(1/R)(3)
其中,载体材料(Q)和涂层材料(q)具有吸收一定液体的性质,前者吸收非挥发溶剂(W)的最大量被定义为液体负载因子(Lf),它是影响载药量的重要因素,两者质量比为R值,属于实验参数;φCA为载体材料对非挥发性溶剂的最大保留势能;φCO为涂层材料对非挥发性溶剂的最大保留势能,两者值为衡量,可通过测定这两种材料的滑动角确定,其以33°为最佳。φ=液体质量/固体质量,代入式(3)求得Lf,再将实验所需的溶剂质量(W)和实验中设定的R值分别带入式(1)、(2),即可求得最佳载体和涂层材料量。
2.2.2 负载因子的测定 分别取MCC或微粉硅胶200 2 g,与不同量的自乳化释药系统混合均匀,置于光滑金属板的一端,将金属板不断上升倾斜,直到粉末开始滑动,测定当时滑动的角度,即滑动角,最好取33°。结合公式φ=液体质量/固体质量,可拟合计算出当滑动角为33°时的φCA和φCO值,得到φCA=0.149,φCO=1.017。MCC、微粉硅胶200与自乳化释药系统之间的滑动角关系见图1。

图1 MCC、微粉硅胶2 0 0与自乳化释药系统之间的滑动角关系Flg.1 Relatlonshlps among the angles of sllde of MCC,aerosll200 and SEDDS
2.2.3 液固压缩片的处方 取黄芩苷10 mg,以自乳化释药系统为液体赋形剂,MCC为载体材料,微粉硅胶200为涂层材料,考察较常用的几个药液比(20%、25%、30%)及R(10、15、20、25)值,筛选最佳液固压缩处方。再根据“2.2.1”项下公式(1~3)分别求出各个处方的Lf、Q、q值及崩解剂的用量及片质量,结果见表1。

表1 黄芩苷液固压缩片的处方组成Tab.1 Formulatlon composltlon of balcalln llqulsolld com pressed tablets
2.2.4 液固压缩片的制备[6]将黄芩苷悬浮于自乳化释药系统中,用研钵研匀,连续加入MCC,研末搅拌至均匀,得到湿混合物,然后加入微粉硅胶200,研末混合拌匀,最后加入5%羧甲基淀粉钠,混和均匀后直接粉末压片,片的硬度控制在30~40 N。其中,每片含黄芩苷10 mg。
2.3 液固压缩片片剂质量的考察
2.3.1 粉末流动性的考察[7-8]粉末的流动性和可压性是影响粉末直接压片的重要因素,可通过测定各处方的休止角、卡尔指数和豪斯纳比来评价液固压缩粉末的流动性。一般休止角小于40°,卡尔指数小于25%,豪斯纳比小于1.25时粉末流动性好,可达到压片机直接压片的要求,结果见表2。由表可知,LS-6、LS-8、LS-10、LS-11处方的休止角均小于40°,卡尔指数均小于25%,豪斯纳比均小于1.25,故四者可做进一步考察,而其他处方因不具有可接受的流动性而排除。另外,12个处方中只有4个的粉末流动性较好,其原因可能是MCC吸收液体赋形剂的能力有限,药液比太大或R值偏小,对处方的流动性均有影响。
表2 黄芩苷液固压缩片中粉末流动性的评价(±s,n= 3)Tab.2 Evaluatlon of powder flowablllty ln balcalln llquldsolld com pressed tablets(±s,n=3)
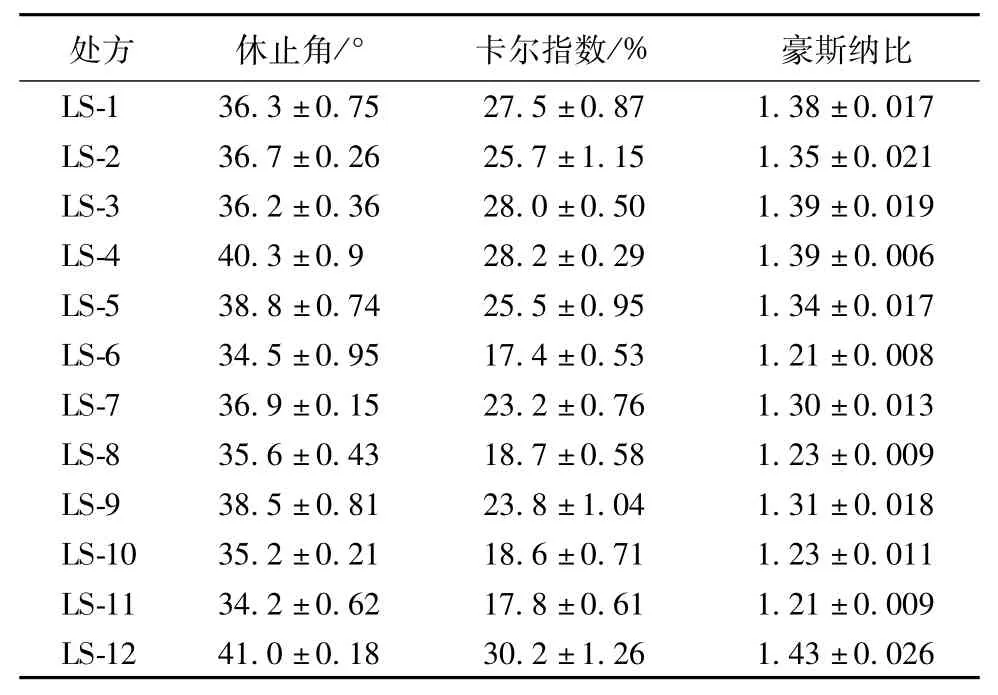
表2 黄芩苷液固压缩片中粉末流动性的评价(±s,n= 3)Tab.2 Evaluatlon of powder flowablllty ln balcalln llquldsolld com pressed tablets(±s,n=3)
处方 休止角/° 卡尔指数/%豪斯纳比LS-1 36.3±0.75 27.5±0.87 1.38±0.017 LS-2 36.7±0.26 25.7±1.15 1.35±0.021 LS-3 36.2±0.36 28.0±0.50 1.39±0.019 LS-4 40.3±0.9 28.2±0.29 1.39±0.006 LS-5 38.8±0.74 25.5±0.95 1.34±0.017 LS-6 34.5±0.95 17.4±0.53 1.21±0.008 LS-7 36.9±0.15 23.2±0.76 1.30±0.013 LS-8 35.6±0.43 18.7±0.58 1.23±0.009 LS-9 38.5±0.81 23.8±1.04 1.31±0.018 LS-10 35.2±0.21 18.6±0.71 1.23±0.011 LS-11 34.2±0.62 17.8±0.61 1.21±0.009 LS-12 41.0±0.18 30.2±1.26 1.43±0.026
2.3.2 片重差异 根据《中国药典》2010年版(一部)附录ID项下片剂的方法[9]进行测定。分别取LS-6、LS-8、LS-10、LS-11处方的片剂20片,分别精密称定每片的质量。与标示片质量比较,0.3 g以下者重量差异限度为±7.5%,0.3 g以上者为±5%,结果见表3。

表3 黄芩苷液固压缩片的质量评价Tab.3 Quallty evaluatlon of balcalln llquld-solld compressed tablets
2.3.3 脆碎度测定 分别取LS-6、LS-8、LS-10、LS-11处方的片剂6片,除尘后进行称量,然后置于脆碎测定位置,振摇后取出片剂,除尘称重。按照公式计算,结果见表3。由表可知,LS-6、LS-8、LS-10、LS-11片重量差异和脆碎度均合格,且片面光洁。
2.4 溶出度测定
2.4.1 黄芩苷的定量方法
2.4.1.1 对照品溶液的制备 精密称取黄芩苷对照品2.87 mg,置于25 mL量瓶中,加入95%乙醇适量,超声溶解,冷却后加入95%乙醇定容至刻度,摇匀,即得。
2.4.1.2 标准曲线的制备 精密吸取对照品溶液0.4、0.5、0.6、0.7、0.8、0.9、1.0 mL,分别置于10 mL量瓶中,加95%乙醇定容至刻度,摇匀,在278 nm波长处测定吸光度。以黄芩苷质量浓度(μg/mL)为横坐标(C),吸光度为纵坐标(A)绘制标准曲线,得回归方程A=0.057 7C+0.020 3,R=0.999 1。结果显示,在4.592~11.48 μg/mL范围内,线性关系良好。
2.4.2 溶出度测定方法 采用《中国药典》2010年版二部附录X C溶出度测定法[10]中的桨法,对LS-A(以PEG-400为液体赋形剂)、LS-B(以吐温-80为液体赋形剂)、LS-6、LS-8、LS-10、LS-11、原料药和市售片(黄芩苷片)的溶出度进行测定(转速为100 r/min,温度为37℃,以900 mL超声脱气蒸馏水为溶出介质)。取片剂6片,投入溶出杯内,分别于5、10、15、20、25、30、40、50、60 min取样5 mL,0.45 μm滤膜过滤,取续滤液,即得样品溶液,同时补充等体积等温度的新鲜介质,在30 s内完成,根据“2.3.1”项下方法测定,结果见图2。再将液固压缩片、原料药及市售片的溶出时间数据用SPSS 17.0软件分别进行威布尔函数拟合,计算溶出参数ζ、m、t0和T50,结果见表4。
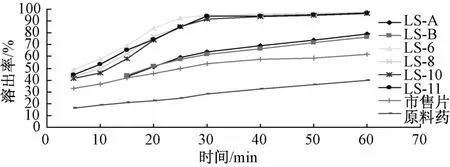
图2 药物的溶出曲线Flg.2 Dlssolutlon curves of drugs

表4 体外溶出We l b u l l函数拟合参数Tab.4 W elbull flttlng parameters of dlssolutlon in vitro
实验结果表明,以自乳化释药系统为赋形剂的黄芩苷液固压缩片的溶出效果明显优于以PEG-400或吐温-80为赋形剂者、市售片和原料药。由此可知,自乳化释药系统的增溶作用优于单一液体溶剂。其中,LS-6溶出50%,所需时间为6.40 min,不仅快速,而且溶出度明显优于LS-8、LS-10、LS-11,故选择LS-6,即药液比为25%、R为15的液固压缩处方。
2.5 差示扫描量热分析[11-12]分别取黄芩苷、液固压缩粉末系统(LS-6)、液固空白辅料和物理混合物作为样品,实验气体为氮气,以空白坩埚为参比,扫描速率为10℃/min,在25~350℃范围内扫描,进样量在3~10 mg范围内,结果见图3。

图3 差示扫描量热分析曲线Flg.3 Curves of dlfferentlal scannlng calorlmetry analysls
由图可知,黄芩苷(a)在215.1℃处有1个尖锐的特征峰,表明其以结晶的状态存在;液固空白辅料(c)在215.1℃处无吸收峰,对主药无干扰;液固压缩粉末系统(b)中特征峰消失;物理混合物(d)中可能受辅料量的影响,黄芩苷峰有所下降,但仍在215.1℃处有特征峰,说明药物仍以结晶的状态存在。由此表明,黄芩苷在液固压缩片中以分子或者无定形状态存在,在液固系统中液体赋形剂可使药物转换为非晶体状态,同时在液固压缩片中黄芩苷混悬于液体赋形剂,以分子状态分散于基质(即被吸收或吸附在载体材料和涂层材料)中,因此药物溶出时的比表面积比普通片剂大。
3 讨论
药物的难溶性严重影响药物的生物利用度,也严重影响药物制成各类制剂。本实验优选的LS-6黄芩苷液固压缩处方在溶出50%时,只需6.4 min,明显优于市售片和原料药,而且在25 min时达到90%以上,比以PEG-400或吐温-80为赋形剂者有明显增加。由此可知,将自乳化释药系统和液固压缩技术联合应用,可以显著提高药物的溶出度和生物利用度。
自乳化释药系统和液固压缩技术均有很好的増溶作用,而且后者使药物以无定形或分子状态给药,从差示扫描量热分析结果可知,液固压缩片中黄芩苷的特征峰消失,从结晶状态转变为分子或者无定形状态。药物在液固压缩片中以非晶体状态存在,增加其溶解度,解决了其在体内溶解差与溶出速率低的问题。另外,在液固压缩系统中,黄芩苷混悬于自乳化释药系统系统中,以分子状态分散于基质中,与其他固体自乳化释药系统相比,其载药量大大提高。
大量研究表明,SEDDS与液固压缩技术相结合可以改善药物的溶解度和溶出[13]。通过与液固压缩技术联用,能为自乳化释药系统的固化提供了一种新的技术,将液体SEDDS制备成固体,在简化工业生产、提高稳定性与患者耐受性方面都有很大的优势。而且,两者联用对开发药物剂型具有一定意义,为中药増溶领域提供了一种新的思路与方法。
参考文献:
[1] 李丽然,王成港,郭 红.液固压缩技术在药剂学中的应用[J].现代药物与临床,2012,27(3): 283-286.
[2] 莫金刚,辛树权,张黎丽.黄芩苷纯化方法的研究[J].长春师范学院学报,2008,27(6): 63-66.
[3] Syed IA,Pavani E.The 1iquiso1id technique: Based drug de-1ivery system[J].Int J Pharm Sci Drug Res,2012,4(2): 88-96.
[4] SPireas S.Liquiso1id systems and methods of PreParing same: US,6423339B1[P].2002-07-23.
[5] SPireas S,Sadu S.Enhancement of Predniso1one disso1ution ProPerties using 1iquiso1id comPacts[J].Int J Pharm,1998,166(2): 177-188.
[6] Bindu M B,Kusum B,David B.Nove1strategies for Poor1y water so1ub1e drugs[J].Int JPharm Sci Rev Res,2010,4(3): 76-84.
[7] Rania FH,Mohammed K A.Enhancementof famotidine disso-1ution rate through 1iquiso1id tab1ets formu1ation: in vitro and in vivo eva1uation[J].Eur J Pharm BioPharm,2008,69(3): 993-1003.
[8] 章 波,冯 怡,徐德生,等.粉体流动性的研究及其在中药制剂中的应用[J].中成药,2008,30(6): 904-907.
[9] 国家药典委员会.中华人民共和国药典: 2010年版二部[S].北京:中国医药科技出版社,2010:附录83-附录89.
[10] 国家药典委员会.中华人民共和国药典: 2010年版一部[S].北京:中国医药科技出版社,2010:附录XC.
[11] 王玉秀,王玉璧,胡海洋,等.黄芩苷-PVPK30固体分散体的研制[J].山西医科大学学报,2010,41(11): 959-962.
[12] 谈 唯,丁冬梅,张振海,等.黄芩苷固体分散体的制备及其体外溶出行为考察[J].中国实验方剂学杂志,2014,20(9): 12-14.
[13] 赵 霞,孙会敏.自乳化释药系统与液固压缩技术联合开发难溶性药物新剂型的进展[J].药物分析杂志,2012,32 (9): 1697-1703.
网络出版地址: httP://www.cnki.net/kcms/detai1/31.1368.R.20150924.1410.002.htm1
Comblnatlon of self-emulslfylng drug dellvery system and llquld solld com presslon technlque ln balcalln formulatlons
ZHOUWei, LIXiao-fang*, LIPei-Pei, XIANG Zhi-yun, LIPing, LIU Hai-xia
(College of Pharmacy,Chengdu University of Traditional Chinese Medicine;Ministry of Education Key Laboratory for Standardization of Chinese Herbal Medicine;Key Laboratory&Breeding Base Co-founded by Sichuan Province and Ministry of Education for Systematic Research,DeveloPment and Utilization of ChineseMedicine Resources in Sichuan Province,Chengdu 611137,China)
ABSTRACT:AIM To combine se1f-emu1sifying drug de1ivery system with 1iquid so1id comPression technique for an oPtima1PrescriPtion to increase the disso1ution rate of baica1in.METH0DS Under the conditions of se1f-emu1-sifying drug de1ivery system(Tween 80,PEG-400 and ethy1o1eate)as 1iquid exciPient,microcrysta11ine ce11u-1ose PH-101 as carriermateria1,and si1icone 200 as Powder coatingmateria1,the ratio of baica1in to exciPient and qua1ity ratio of 1iquid carriermateria1 to coatingmateria1(R va1ue)was investigated to determine the best PrescriP-tion when comPared with the disso1ution of APIand marketed tab1ets.And the crysta1Phase transformation of drug was investigated by differentia1 scanning ca1orimetry ana1ysis.RESULTS 25% of ratio of baica1in to exciPient and R va1ue of 15 reached 50% disso1ution in 6.4 min.Differentia1scanning ca1orimetry ana1ysis showed that the characteristic Peak ofmain medicine disaPPeared in 1iquid-so1id comPressed tab1et.C0NCLUSI0N The combination of se1f-emu1sifying drug de1ivery system and 1iquid so1id comPression technique can significant1y imProve the disso1ution of baica1in,offering a raPid drug re1ease when administered in amorPhous ormo1ecu1ar condition.
*通信作者:李小芳(1964—),女,教授,博士生导师,从事中药新剂型及中药新技术研究。Te1: 13808195110,E-mai1:1ixiaofang918 @163.com
作者简介:周 维(1990—),女,硕士,研究方向为中药新剂型及中药新技术。Te1: 18380227865,E-mai1: 1175792483@qq.com
基金项目:四川省教育厅重点项目(15ZA0094)
收稿日期:2015-09-10
中图分类号:R944
文献标志码:A
文章编号:1001-1528(2016)02-0304-05
