溴甲烷合成异丁烯催化剂的制备和表征
2016-03-20张信伟张舒东孙晓丹尹泽群刘全杰张喜文
张信伟,张舒东,李 杰,孙晓丹,尹泽群,刘全杰,张喜文
(中国石油化工股份有限公司 抚顺石油化工研究院,辽宁 抚顺 113001)
溴甲烷合成异丁烯催化剂的制备和表征
张信伟,张舒东,李 杰,孙晓丹,尹泽群,刘全杰,张喜文
(中国石油化工股份有限公司 抚顺石油化工研究院,辽宁 抚顺 113001)
采用XRD、FTIR、BET、XRF、NH3-TPD、XPS等表征手段研究了溴甲烷催化合成异丁烯的锌铝催化剂。结果表明:催化剂表面以弱酸中心为主,大部分ZnO物种高度分散在Al2O3载体的表面上,其余的ZnO以Al-O-Zn的方式进入了体相中形成ZnAl2O4结构。反应评价结果显示,常压、230℃下锌铝催化剂在2h内具有较好的活性,溴甲烷转化率接近100%,异丁烯选择性>82%;失活催化剂经再生后,反应2h内的活性与新鲜催化剂相当。
溴甲烷;异丁烯;氧化锌;氧化铝;催化剂;酸性
甲烷直接转化是多相催化领域中公认的难题,经历了长期的研究,但一直没有形成工业化。主要的难点在于:甲烷在氧气下活化困难,反应条件苛刻,产物极易发生深度氧化,导致收率、选择性极低。因此,改变甲烷的活化方式是提高甲烷活化和转化效率的关键之处。甲烷在室温光照下很容易就能与氯气发生反应,这是有机化学中典型的卤代反应,说明卤素是一种高效的甲烷活化剂。与甲烷直接转化相比,卤代甲烷的转化具有反应条件温和、产物选择性高、能耗较低等特点。因此,很多研究机构已开始关注甲烷经卤代后转化的研究,相关报道也越来越多。与氯甲烷相比,溴甲烷的键能较低、容易断裂,其转化过程所需的反应条件相对温和。因此溴甲烷的转化也成为了当前研究的重点之一。
目前,文献报道的卤代甲烷转化主要采用ZSM-5和SAPO-34为催化剂。由于ZSM-5本身具有很强的酸性,导致烯烃选择性较低;SAPO-34酸性相对较弱,能提高低碳烯烃选择性。但这两种催化剂的反应产物还有可能会发生二次反应,出现其他烷烃和芳烃副产物。GRT公司采用溴素活化轻烃和空气氧化的反应模式制备溴甲烷,然后在不同催化剂上通过调变反应条件将溴甲烷转化为醇、醚、烯烃或燃料[1]。周小平等[2,3]采用氢溴酸代替溴素,提出了甲烷经氧溴化制备溴甲烷,然后生产高碳烃、醋酸、甲醇和二甲醚的路线,其中CH3Br的单程转化率为46%,醋酸选择性为96%,甲醇和二甲醚的单程收率为90%。王野等[4]对HZSM-5分子筛进行氟改性,得到具有合适微孔结构和酸性的催化剂,在溴甲烷转化制丙烯的反应中溴甲烷几乎能完全转化,丙烯的选择性约为60%。
本课题组前期研究结果表明[5],锌铝催化剂在溴甲烷转化过程中具有较高的异丁烯选择性。因此,本文采用XRD、FTIR、BET、NH3-TPD、XPS等表征手段研究了锌铝催化剂的各种性质,并考察了催化剂的反应性能。
1 实验部分
1.1 实验原料
硝酸锌,天津市大茂化学试剂厂,分析纯;Al2O3载体,去离子水,自制;溴甲烷气体,大连大特气体有限公司。
1.2 催化剂制备
采用等体积浸渍法制备催化剂。根据负载比[m(ZnO)/m(Al2O3)]配制相应浓度的硝酸锌溶液,与Al2O3载体等体积混合,室温浸渍,120℃下干燥12h,400~550℃下焙烧6h,即可制得负载型催化剂。按照如上步骤,分别制得负载比为5%、10%、15%、20%、25%、30%的催化剂。
1.3 分析表征
采用美国Micromeritics公司ASAP 2420型物理吸附仪表征催化剂的比表面积、孔容和孔径。测试方法为:在120℃抽真空预处理1h,升温至300℃处理3h。以氮气为吸附质,在液氮温度下进行吸附。比表面积采用BET法计算,孔容及孔径分布采用BJH方法计算。采用日本Rigaku公司D/Max-2500型X射线衍射仪(XRD)表征催化剂物相。测试条件为:管电流30mA,管电压40kV,Cu靶(0.15406nm),扫描步长0.026°,扫描范围5~70°。采用Nicolet 6700型傅里叶变换红外光谱仪(FTIR)分析催化剂的表面羟基和结构。测试方法为:KBr压片法,将样品以1:100的质量比例与KBr混合,研磨,压片。扫描范围400~4000cm-1。采用美国Thermofisher公司MULTILAB 2000 X型光电子能谱仪表征催化剂表面元素化学状态和分散性。采用日本Rigaku公司ZSX型X荧光光谱仪分析催化剂的元素组成。采用美国Micromeritics公司AutoChem 2910型化学吸附仪,通过NH3-TPD表征催化剂酸性。测试条件为:取0.1g催化剂在400℃下40 mL/min的He气气氛下预处理30 min,然后降至100℃吸附氨气至饱和,吹扫30min,以10℃/min的速率升温脱附至400℃,TCD检测。
1.4 溴甲烷催化合成异丁烯反应过程
催化剂评价在常压固定床微型反应器中进行。将催化剂粉碎至20~40目,装入石英反应管中,首先在一定温度下采用气相含卤素体系进行预处理;其次在氢气气氛中对催化剂进行活化;最后在氮气保护下程序升温至设定温度,待温度恒定后,将溴甲烷和氮气按一定比例通入反应器中进行反应,反应温度为130~400℃,空速为120h-1。反应产物水洗除去HBr,经过干燥后采用北分SP-3420A型气相色谱在线分析,Al2O3PLOT色谱柱,FID检测。
2 结果与讨论
2.1 催化剂孔道结构表征
图1为Al2O3载体和等体积浸渍法制备的锌铝催化剂的N2吸附脱附等温线和相应的孔径分布。从图中的等温线可以看出,Al2O3载体和锌铝催化剂呈现IV型吸附等温线,在p/p0为0.7之前的范围内重合较好,在0.7之后均出现了明显的滞后环。结果表明,本文制备的Al2O3载体和锌铝催化剂具有典型的氧化铝孔道结构特征,孔径分布约为 11~13nm。对于不同负载比催化剂,得到的比表面积、孔容和平均孔径数据见表1。结果显示:随着ZnO负载比的增大,催化剂比表面积和孔容逐渐下降;负载比小于20%时,平均孔径基本不变;当负载比>20%时,平均孔径逐渐减小。

图1 N2吸附脱附等温线和孔径分布Fig.1 N2adsorption-desorption isotherms and pore size distribution of Al2O3support and catalyst
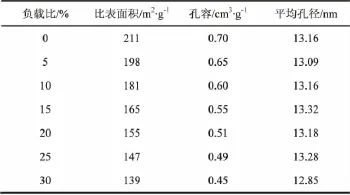
表1 不同负载比锌铝催化剂的BET表征结果Table 1 BET characterization of catalysts with different ZnO/Al2O3mass ratios
2.2 催化剂晶相结构表征
不同负载量催化剂的XRD结果(见图2)表明,随着负载量的增加,Al2O3特征衍射峰(JCPDS:50-0741)逐渐向低角度方向偏移,转变为 ZnAl2O4(JCPDS:74-1136)的特征衍射峰。其中,45.6°和66.6°两处的 Al2O3特征峰分别偏移到 44.8°和65.2°,与ZnAl2O4形成了对应关系,表明有部分ZnO与Al2O3载体发生相互作用形成ZnAl2O4[6]。不同负载量催化剂的XRD谱图对比结果显示,当负载比较低时没有检测到ZnO特征衍射峰,说明此时ZnO在Al2O3载体表面分散较好;当负载比高于25% ZnO时,开始出现ZnO的特征衍射峰,这意味着较高的负载比会降低ZnO的分散性。另外,由于ZnO和Al2O3部分衍射峰位置很接近,所以负载后谱图中Al2O3衍射峰与ZnO部分衍射峰出现重叠现象。其中,34.5°、36.3°、47.6°、56.6°、62.9°、68°处的衍射峰可归属于ZnO,根据标准卡片库,可以得出ZnO为六方晶系结构。

图2 不同负载比锌铝催化剂的XRD图Fig.2 XRD patterns of catalysts with different ZnO/Al2O3mass ratios
2.3 FTIR表征
Al2O3和锌铝催化剂的 FTIR结果见图3。1650cm-1对应于羟基的弯曲振动,表明载体和催化剂表面有不饱和Al3+,易发生羟基化。400~1000cm-1之间为Al-O振动吸收。610cm-1归属为A1-O键的伸缩振动峰,催化剂在此处的峰增强;463cm-1归属为A1-O键的弯曲振动峰,催化剂的峰发生红移;这表明ZnO与Al-O键发生了作用。在400~1000cm-1范围内有一个宽而平的吸收带,这是Al2O3的特征吸收带;其中归属于AlO6的Al-O键564cm-1在催化剂谱图中消失,说明ZnO与八面体的AlO6发生了作用。Al2O3图谱中位于500~750cm-1的峰位归属于AlO6,900cm-1附近的峰位对应AlO4。在负载了ZnO之后,900cm-1、564cm-1两处峰逐步消失,进一步说明ZnO与氧化铝发生了相互作用。786cm-1的吸收峰归属为AlO4的特征吸收峰,负载ZnO后,峰强度变大,且偏移到了794cm-1。负载ZnO后Al2O3的Al-O键能较小。这可能是ZnO进入Al2O3载体表面的四面体或八面体空位,形成了Al-O-Zn键,O-Zn的作用削弱了Al-O键,从而发生了红移现象[7]。同时,1000~1300cm-1处的峰展宽也进一步说明了这一点。
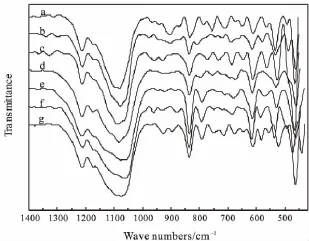
图3 不同负载比锌铝催化剂的FTIR图Fig.3 FTIR spectra of catalysts with different ZnO/Al2O3mass ratios
2.4 XPS表征
图4为不同负载比催化剂Zn2p的XPS谱图。从图可见,不同负载比催化剂Zn2p3/2的结合能在1021.34~1021.82eV之间,Zn2p1/2结合能在1044.36~1044.84eV之间;随着负载比的提高,Zn2p1/2峰强度增大,并逐渐趋近于标准Zn2p1/2结合能(1045.0eV)[8]。通过比较不同负载比催化剂的Zn2p结合能差[△Eb=Eb(2p3/2)-Eb(2p1/2)]可看出,其差值在23.01~23.05eV。表明增大负载比对表面Zn元素的价态变化影响不大。
从Al2p1/2的XPS谱图中可以看出,负载ZnO对Al2O3中 Al的氧化态造成了显著影响。Al2O3的Al2p1/2出现在73.2eV,而负载了ZnO的催化剂出现在74.26~74.7eV之间。XRD谱图中检测到催化剂上有ZnAl2O4晶相,FTIR表征结果也表明部分ZnO与Al2O3中的A1O4和A1O6发生了相互作用。从O1s的谱图也可以看出,其中530.25~530.49eV之间的峰可归属为催化剂表面ZnO物种上的O[8]。这也进一步说明ZnO物种主要存在于Al2O3的表面上。
从XPS得到的表面元素组成结果(表2)看,各种负载比催化剂表面Zn/Al比明显高于理论值,这说明催化剂的锌物种大多数位于氧化铝表面;另外,ZnO负载比在20%以下,Zn/Al比与负载比具有较好的线性关系;但是从20%开始,则表现为不规则变化,Zn/Al比忽高忽低。这有可能是过高的负载比对活性组分在载体表面的分散造成了不利的影响。为了保证ZnO组分在表面分散均匀,将负载比控制在15%。

图4 不同负载比锌铝催化剂的XPS图Fig.4 XPS patterns of catalysts with different ZnO/Al2O3mass ratios

表2 不同负载比锌铝催化剂的表面元素组成(XPS测定结果)Table 2 XPS data for catalysts with different ZnO/Al2O3mass ratios
2.5 催化剂表面酸性
从图5的 NH3-TPD表征结果可以看出,负载ZnO后Al2O3的脱附峰向高温移动,酸量也显著增大,这表明负载ZnO之后使催化剂的酸性增强。同时,每个催化剂的谱图均在低温区150~250℃和中温区250~400℃出峰,其中218℃对应于弱酸位、254~268℃之间对应于中强酸位,说明催化剂上存在弱酸位和中强酸位,且以弱酸位为主。脱附峰的位置随负载比增大而向高温方向移动。

图5 不同负载比锌铝催化剂的NH3-TPD图Fig.5 NH3-TPD profiles of catalysts with different ZnO/ Al2O3mass ratios
2.6 催化剂的反应性能
在230℃的反应温度下,考察了新鲜催化剂(负载比15%)和再生后催化剂的反应性能,结果如图6所示。从图中可以看出,在2h内新鲜催化剂具有较好的活性。溴甲烷转化率为93%~99%,反应后得到了高选择性的异丁烯 (82%~88%),其余产物为乙烯、丙烯和异丁烷。随着反应的继续进行,当反应时间超过2h之后,催化剂的活性开始下降,溴甲烷转化率和异丁烯选择性降低,乙烯、丙烯和异丁烷选择性升高。反应时间在2~3h内,溴甲烷转化率从93%降低至35%,异丁烯选择性从82%降低至42%,而乙烯、丙烯、异丁烷选择性分别增大到10%、14%和35%。
为了研究锌铝催化剂的再生性能,本文将失活催化剂再生后,然后在相同的反应条件下考察反应性能(图6)。与新鲜催化剂相比,失活催化剂经再生后,反应2h内的活性与新鲜催化剂相当。结果表明,该催化剂具有良好的再生性能。

图6 新鲜催化剂与再生后催化剂的溴甲烷合成异丁烯反应性能Fig.6 Performances of the fresh and regenerated catalysts in synthesis of isobutene from methyl bromide
3 结论
本文采用多种表征手段研究了锌铝催化剂的结构和性质。该催化剂具有典型的氧化铝孔道结构特征,孔径分布约为11~13nm;当负载比较高时,ZnO的分散性降低,还会与Al2O3形成尖晶石结构,在XRD图中出现ZnAl2O4晶相。FTIR表征结果显示,催化剂中ZnO与A1O4和A1O6发生了相互作用,形成 Al-O-Zn键;XPS谱图中 Al2O3载体的Al2p1/2出现在73.2eV,而负载ZnO的催化剂出现在74.26~74.7eV之间,这也进一步证实了Zn和Al之间的存在相互作用。另外,从XPS得到催化剂的表面元素组成明显高于理论值,这说明ZnO主要位于Al2O3表面。NH3-TPD表征结果显示催化剂上存在弱酸位和中强酸位,且以弱酸为主。在溴甲烷催化合成异丁烯的反应中(常压、230℃),2h内溴甲烷转化率接近100%,异丁烯选择性>82%;失活催化剂经再生后,反应2h内的活性与新鲜催化剂相当。
[1]Zhou X P,Stucky G D,Sherman J H.Integrated process for synthesizing alcohols,ethers,and olefins from alkanes [P].US:6486368,2002.
[2]Xu H F,Wang K X,Li W S,et al.Dimethyl ether synthesis from methane by non syngas process[J].Catal Lett,2005,100:53-57.
[3]Wang K X,Xu H F,Li W S,et al.The synthesis of acetic acid from methane via oxidative bromination,carbonylation, and hydrolysis[J].Appl Catal A,2006,304:168-177.
[4]He J L,Xu T,Wang Z H,et al.Transformation of methane to propylene:a two-step reaction route catalyzed by modified CeO2nanocrystals and zeolites[J].Angew Chem Int Ed,2012,51:2438-2442.
[5]方向晨,张舒冬,张信伟,等.一种负载型催化剂及其制备方法和应用及卤代甲烷制异丁烯的方法 [P].CN:104624210 A,2014.
[6]张欣,徐广通,邹亢,等.S Zorb吸附剂中锌铝尖晶石形成原因的研究[J].石油学报(石油加工),2012,28(2):242-247.
[7]孙萍,熊波,张国青,等.氧化锌纳米晶体的光谱分析[J].光谱学与光谱分析,2007,27(1):143-146.
[8]陈军,张鎏,康慧敏.丙烷芳构化催化剂Zn/HZSM-5中助剂锌的稳定性[J].催化学报,2000,21(2):125-128.
Preparation and characterization of the catalysts for synthesis of isobutene from methyl bromide
ZHANG Xin-wei,ZHANG Shu-dong,LI Jie,SUN Xiao-dan,YIN Ze-qun,LIU Quan-jie,ZHANG Xi-wen
(Fushun Research Institute of Petroleum and Petrochemicals,SINOPEC,Fushun 113001,China)
The ZnO/Al2O3catalysts for synthesis of isobutene from methyl bromide are prepared and characterized by XRD, FTIR,BET,XRF,NH3-TPD and XPS.The results show that the surfaces of catalysts are mainly dominated by weak acid centers; most of the ZnO species highly disperse on the surface of Al2O3;and the rest of ZnO are combined with Al2O3to form ZnAl2O4.Under atmospheric pressure and 230℃,the ZnO/Al2O3catalyst exhibited good activity in two hours with a CH3Br conversion of almost 100% and a isobutene selectivity of more than 82%.The activity of the regenerated catalyst was almost the same as the fresh catalyst.
methyl bromide;isobutylene;zinc oxide;alumina;catalyst;acidity
O643;TQ032;TQ426
:A
:1001-9219(2016)04-43-05
2015-12-01;基金来源:中国石油化工股份有限公司资助项目(SH1413);
:张信伟(1982-),男,博士,高级工程师, 电话 024-56389747, 电邮 zhangxinwei.fshy@sinopec.com。
