一种基于细胞计数技术的羊肚菌单孢子菌种分离方法*
2016-03-14邹振平王婷婷袁通阔楼莹莹王一东
邹振平,王婷婷,袁通阔,楼莹莹,王一东
(长春理工大学生命科学技术学院,吉林 长春 130022)
一种基于细胞计数技术的羊肚菌单孢子菌种分离方法*
邹振平,王婷婷,袁通阔,楼莹莹,王一东**
(长春理工大学生命科学技术学院,吉林 长春 130022)
为了获取羊肚菌(Morchella esculenta)单孢子菌种,利用经无菌处理的羊肚菌孢子悬液,经细胞计数板计数后稀释至每100微升含2个、1个、0.5个孢子,分别加入96孔细胞培养板培养孔中,镜检观察各孔中的孢子数并标记出含单个孢子的培养孔。室温下培养,待单孢子孔中孢子萌发的菌丝生长至培养孔底部边缘时,将菌丝转移至PDA平板中培养,对培养得到的菌丝进行ELISA鉴定,确定分离得到羊肚菌单孢子菌种,然后将菌种进行编号,扩大培养并保存。利用该方法分离得到3株羊肚菌单孢子菌种,分别编号为LG-01、LG-02、LG-03。
羊肚菌;单孢子菌种;细胞计数;酶联免疫吸附法 (ELISA)
羊肚菌 [Morchella esculenta(L.)Pers.]是一种以美味著称的珍稀食用菌,具有较高的营养和保健价值[1]。目前羊肚菌还无法实现稳定的大规模人工栽培,价格一直居高不下,这与人们对羊肚菌的生活史并不十分了解有关[2-3]。为加深人们对羊肚菌生活史的了解,开展人工栽培实践,迫切需要在羊肚菌单孢子菌种的分离、单孢子菌丝的萌发、菌丝生长发育,以及能否出菇方面展开研究。与传统的孢子菌种分离(如:划线分离、稀释涂布、显微镜下单孢直接挑取等)方法不同[4-5],本文介绍一种借鉴动物细胞培养中单克隆细胞操作,进而演化的羊肚菌单孢子菌种分离方法[6],该方法具有操作简便、易于观察的特点,结合免疫学的ELISA鉴定[7],可以保证分离菌种的可靠性。目前还未见其相关的研究报道。该方法为羊肚菌生活史研究及羊肚菌人工栽培的开展提供技术支撑。
1 材料与方法
1.1 材料
1.1.1 标准菌株和羊肚菌孢子
羊肚菌(Morchella esculenta)菌株(51589号),购于中国农业微生物菌种保藏中心。
黑木耳(Auricularia auricula) 菌种,购于吉林农业大学菌物研究所。
野生羊肚菌子实体于2006年5月中旬采自吉林省吉林市丰满区旺起镇,在实验室无菌环境下收集吸附于打印纸上的子实体自然弹射孢子,4℃保存于冰箱。
1.1.2 主要试剂
孢子洗脱液:含双抗(青霉素100 IU·mL-1、链霉素100 μg·mL-1)、0.05%Toween-20无菌水溶液;孢子萌发液:水1 000 mL、葡萄糖20 g、磷酸二氢钾1 g、硫酸镁0.5 g,121℃灭菌20 min;PDA培养基:马铃薯200 g、葡萄糖20 g、磷酸二氢钾1 g、硫酸镁0.5 g、蛋白胨3 g、琼脂粉20 g,水1 000 mL,121℃灭菌20 min;PDB培养基:不添加琼脂粉的PDA液体培养基;HRP标记山羊抗兔IgG(H+ L),购于北京中杉金桥生物技术有限责任公司;TMB,Sigma公司产品;抗羊肚菌单克隆抗体(C6A8株腹水)、抗羊肚菌多克隆抗体(兔高免血清),由长春理工大学生命科学技术学院制备并保存[8]。其他试剂为国产分析纯化学试剂。
1.1.3 主要材料、仪器及设备
96孔细胞培养板,康宁公司;XB.K.25细胞计数板,上海求精生化试剂仪器有限公司;超净工作台;80-2B飞鸽牌离心机,上海安亭科学仪器厂;XD30倒置显微镜,宁波舜宇公司;HZQ-QX型全温震荡器,东联电子技术开发有限公司;MDF-192型低温冰箱,SANYO公司;ELx800TM酶标仪,美国伯腾仪器有限公司;微量移液器;高压灭菌锅等。
1.2 方法
1.2.1 羊肚菌孢子悬液制备及孢子计数
在超净工作台中,剪取约2 cm×2 cm载有羊肚菌孢子的打印纸于小烧杯中,加入15 mL孢子洗脱液并用镊子轻轻搅动纸片洗下孢子,制成孢子悬液。将孢子悬液移至15 mL离心管中,1 500 r·min-1离心5 min,弃上清;加入适量孢子萌发液吹打重悬后,相同转速离心,重复3次上述离心操作。加入10 mL孢子萌发液吹打重悬,并用细胞计数板在100×显微镜下进行孢子计数。
1.2.2 有限稀释法获得羊肚菌单孢子及其萌发情况观察
根据计数得出孢子浓度,用孢子萌发液做适当倍数的稀释,用无菌微量移液器吸取含130个孢子体积的孢子悬液,移入孢子萌发液中并使终体积为6.5 mL。此时的孢子悬液浓度为20个·mL-1,100 μL·孔-1加入细胞培养板A、B、C三行;余下2.9 mL孢子悬液补加2.9 mL孢子萌发液,此时的孢子悬液浓度为10个·mL-1,100 μL·孔-1加入D、E、F三行;余下2.2 mL孢子悬液补加2.2 mL孢子萌发液,此时的孢子悬液浓度为5个·mL-1,100 μL·孔-1加入G、H两行。在100×倒置显微镜下观察加入孢子的96孔细胞培养板各孔,记录各孔中所含的孢子数,并对含有单个孢子的培养孔进行标记,室温下培养,定时观察孢子萌发情况。记录孢子的萌发总数,计算孢子萌发率。
1.2.3 羊肚菌单孢子菌种的获取及鉴定
待含单个孢子的培养孔中萌发的菌丝生长至培养孔底部边缘时,在无菌条件下将其转接到PDA平板中培养并编号,初步得到了羊肚菌单孢子分离菌种。
菌种鉴定:待上述平板中的菌丝生长后,按编号无菌挑取适量菌丝接种至PDB培养基中,22℃、120 r·min-1培养,4 d后收集菌丝球,将收集的菌丝球放入研钵中,加入适量的海沙及pH7.4的磷酸盐缓冲液(PBS)充分研磨破碎,收集研磨液3 000 r·min-1离心20 min,取上清10 000 r·min-1离心5 min,所得上清即为待测抗原原液。用同样的方法制备、处理标准阳性抗原(51589号)、阴性抗原(木耳菌丝),对待测抗原进行ELISA夹心法检测,以检测样品的OD值与阴性样本OD值的比值(P/N)大于等于2.1,判定为羊肚菌的菌丝,检测过程参照文献[7]。
2 结果与分析
2.1 孢子计数及悬液稀释结果
取少量无菌处理后的孢子悬液进行计数,孢子悬液浓度为4×104个·mL-1,用无菌微量移液器取出100 μL孢子悬液于10 mL孢子萌发液中吹打均匀(稀释100倍),从中取出325 μL悬液并补充孢子萌发液至6.5 mL,得到浓度为20个·mL-1的孢子悬液。
2.2 孢子分离结果与孢子萌发情况
镜检96孔细胞培养板中,各培养孔中孢子分布结果见表1。
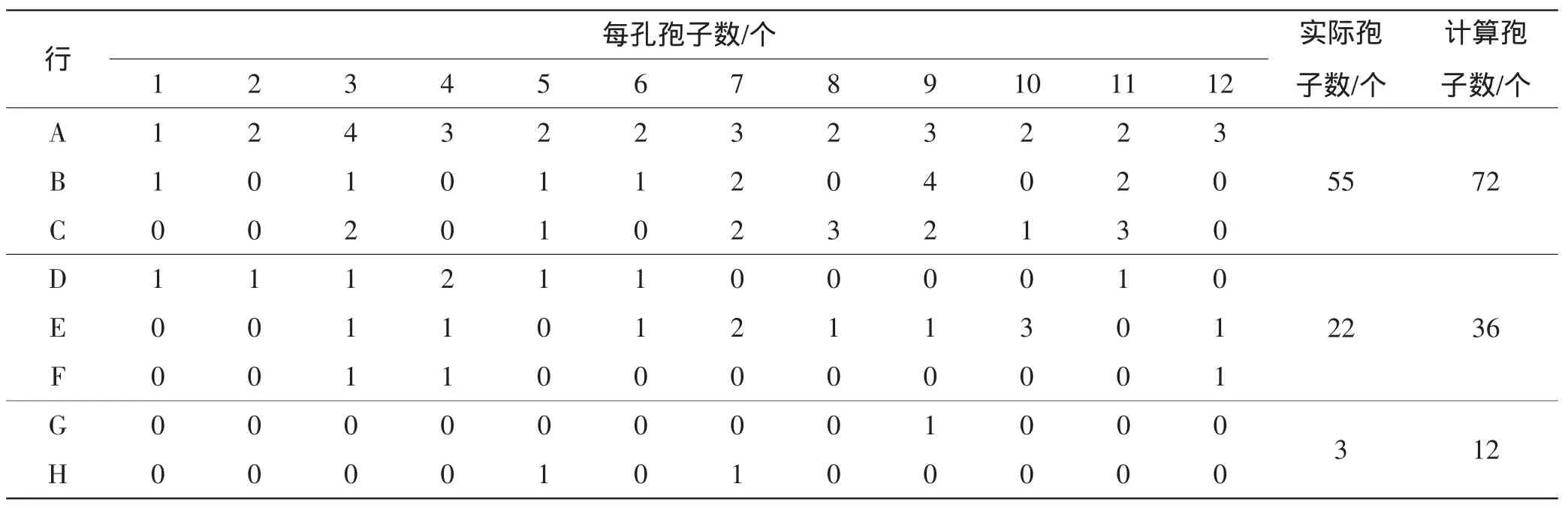
表1 96孔细胞培养板中的孢子分布Tab.1 Distribute of the spores in 96-well cell culture plate
3 d~5 d时陆续观察到10个孢子萌发,5 d后则未发现有孢子继续萌发,孢子萌发率为12.5%(萌发率为萌发的孢子数除以孢子总数乘以100%),10个萌发的孢子中,D6、E6、G9萌发前即为分离得到的单个孢子,待菌丝生长至培养孔底部边缘时,将其转移至PDA平板中培养,编号LG-01、LG-02、 LG-03。为了保证单孢子分离的准确性,实验舍弃了非单孢子培养孔中孢子萌发的菌丝。
2.3 ELISA夹心法鉴定羊肚菌单孢子菌株及分离结果
利用ELISA夹心法对待测抗原进行检测,以P/ N比≥2.1判定为阳性,结果见表2。

表2 ELISA夹心法检测分离菌株结果Tab.2 Results of isolated strains detection by sandwich ELISA
由表2可以看出,以标准羊肚菌抗原(51589号)为阳性对照,木耳菌丝为阴性对照,PBS缓冲液为试剂空白,进行了多次的ELISA夹心法检测。结果显示LG-01、LG-02、LG-03均表现为阳性(以P/N大于2.1为阳性),确定为羊肚菌菌丝,并对分离得到的3株羊肚菌单孢子菌株进行扩大培养并保存。
3 讨论
传统的分离羊肚菌单孢子菌种的划线法、稀释涂布法,具有操作简单的特点,但其分离的是肉眼可见的单菌落,而无法保证是单孢子萌发的菌落,可靠性较差;显微镜下的单孢子直接挑取法虽分离准确,但操作复杂,需经过专门训练,且在挑取过程中易污染。本文提出的羊肚菌单孢子菌种分离方法则具有操作便捷、不易污染的特点,并可在显微镜下观察到单孢子萌发,配合ELISA方法鉴定分离的菌种,为羊肚菌单孢子菌种分离提供了准确性与可靠性双重保障。此种方法进行羊肚菌单孢子分离操作的关键在于对悬液孢子浓度的准确计数及稀释。
本实验使用的羊肚菌孢子的萌发率相对于新鲜羊肚菌孢子的萌发率较低[9],并且在萌发时间方面存在差异,推测原因或与孢子长时间4℃保存有关(保存10年)。考虑到常用的乙醇做灭菌处理或许会对孢子造成伤害,在本试验中我们使用了较温和的低浓度青霉素与链霉素(双抗)处理孢子,效果较为理想。
通过对羊肚菌单孢子菌种的分离、单孢子菌丝的萌发、菌丝生长发育以及能否出菇进行了研究,将有助于人们了解羊肚菌生活史,而对羊肚菌生活史了解的深入程度将直接影响到人工栽培实践的成败。同时,单孢子菌种分离技术也是食用菌杂交育种的前提之一[10]。本文介绍的这种便捷的羊肚菌单孢子分离方法,或许能为上述目的实现提供一定的支撑。
[1]兰进,曹文芩,徐锦堂,等.中国羊肚菌属真菌资源[J].资源科学,1999,21(2):56-61.
[2]陈向东,朱戎,兰进,等.羊肚菌研究进展[J].食用菌学报,2002,9(2):56-61.
[3]Volk Thomas J,Lenard Thomas J.Cytology of the life-cycle of Morchella[J].Mycological Research,1990,94(3):339-406.
[4]肖江勇,何秀霞,王丹,等.ELISA鉴别条件下的野生羊肚菌菌种分离方法 [J].中国食用菌,2015,34(3):11-14.
[5]张昊,张争,许景升,等.一种简单快速的赤霉病菌单孢分离方法--平板稀释画线分离法[J].植物保护,2008,34(6):134-136.
[6]周珍辉.动物细胞培养技术[M].北京:中国环境科学出版社,2006:231.
[7]张红艳,孙伟虹,熊博宇,等.羊肚菌菌丝标识性抗原C6A8在菌丝不同发育阶段含量的变化规律[J].菌物研究,2015,13(3):160-163,167.
[8]王一东,刘健.一株抗羊肚菌单克隆抗体及其制备方法:中国,200910218152.8[P].2010-06-09.
[9]林彬,贾身茂.粗腿羊肚菌的显微形态观察[J].食用菌,1994(1):13-14.
[10]张树强,卫彩红,胡建伟,等.鸡腿菇单孢分离和单孢杂交的研究[J].新疆农业科学,2012,49(1):190-194.
A Separation Method for Morchella Monospore Strains Based on Cell Count Technology
ZOU Zhen-ping,WANG Ting-ting,YUAN Tong-kuo,LOU Ying-ying,WANG Yi-dong
(Changchun University of Science and Technology,School of Life Science and Technology,Changchun 130022,China)
In order to obtain monospore strains of Morchella esculenta,M.esculenta spore suspension processed by sterile were diluted to 2,1,0.5 spores per 100 μL after it counted by cell counting plate,which were added to 96-well cell culture plate respectively,and the spore number were observed using microscope and the well with a single spore were marked.The spore were cultured at room temperature,when the spore germination hyphae grew to culture wells,edge in the well with single spore,the hyphae was moved to the PDA plates,which were identified by ELISA to ensure that the Morchella strains were isolated from single spores,then the monospore strains were numbered,expanded and saved.Using this method,three M.esculenta single spore strains were isolated,named LG-01,LG-02 and LG-03.
Morchella;monospore strains;cell count;enzyme linked immunosorbent assay (ELISA)
S646.9
A
1003-8310(2016)05-0006-04
10.13629/j.cnki.53-1054.2016.05.002
长春理工大学大学生创新创业训练计划项目(2015S054、2016S093);吉林省教育厅“十三五”科学技术研究项目(吉教科合字[2016]第384号)。
邹振平(1995-),男,在读本科,主要研究方向为食用菌实验技术。E-mail:zouzp82465@163.com
**通信作者:王一东(1962-),男,本科,高级实验师,主要从事食品与卫生检验研究。E-mail:wyd@cust.edu.cn
2016-07-10
