改进HPLC法测定注射用多种维生素(12)中维生素B12的含量
2016-03-11徐家根刁岩忠南京大学医学院附属口腔医院药学部南京10008南京优科生物医药集团股份有限公司南京10009
徐家根,刁岩忠(1.南京大学医学院附属口腔医院药学部,南京 10008;.南京优科生物医药集团股份有限公司,南京 10009)
改进HPLC法测定注射用多种维生素(12)中维生素B12的含量
徐家根1*,刁岩忠2(1.南京大学医学院附属口腔医院药学部,南京 210008;2.南京优科生物医药集团股份有限公司,南京 210009)
目的:改进高效液相色谱法测定注射用多种维生素(12)中维生素B12的含量。方法:采用高效液相色谱法。色谱柱为Kromasil 100-5 C18,流动相为水(用10%稀磷酸调节pH为4.5)-乙腈(梯度洗脱),流速为1.2 ml/min,检测波长为361 nm,柱温为35Ⅱ,进样量为50 μl。结果:维生素B12检测进样量线性范围为15.03~45.09 ng(r=0.999 9);精密度、稳定性、重复性试验的RSD<1%;回收率为99.31%~100.90%(RSD=0.42%,n=9)。结论:该方法简便、准确、灵敏度高、重复性好,可用于注射用多种维生素(12)中维生素B12的含量测定。
注射用多种维生素(12);维生素B12;含量测定;高效液相色谱法;方法改进
维生素B12(Vitamin B12)又称氰钴胺素(Cyanocobalamin)[1],是人体必需的水溶性维生素之一[2],参与体内多种代谢,还可有效预防恶性贫血、老年痴呆、抑郁症等疾病,对保持人体健康起着重要作用[3]。维生素B12原料药及单方制剂标准在《中国药典》《美国药典》《欧洲药典》《日本药典》中均有收载,但均采用紫外-可见分光光度法测定含量,该方法专属性差,干扰因素多。国内外上市的注射用复合维生素制剂有注射用水溶性维生素、注射用12种复合维生素、注射用多种维生素(12)、多种维生素注射液(13)[4-5]等。这些制剂的标准均为国家药品注册标准[6-8],尚无药典标准;国家药品注册标准及相关文献[9]中,均
1 材料
1.1 仪器
LC-20AB型HPLC仪,包括CBM-20A系统控制器、DGU-20A3真空脱气机、SPD-M20A二极管阵列检测器、LC-20AB输液单元、SIL-20AC自动进样器、CTO-20AC柱温箱、LabSolutions色谱工作站(日本岛津公司);XS205型电子分析天平(瑞士梅特勒-托利多公司)。
1.2 药品与试剂
注射用多种维生素(12)(南京优科制药有限公司,批号:20130201、20130202、20130203,规格:复方);维生素B12对照品(中国食品药品检定研究院,批号:100248-200802,纯度:95.5%);乙腈(色谱纯,美国Sigma公司);磷酸为分析纯,水为超纯水。
2 方法与结果
2.1 色谱条件
色谱柱:Kromasil 100-5 C18(250 mm×4.6 mm,5 μm);流动相:水(用10%稀磷酸调节pH为4.5)(A)-乙腈(B),梯度洗脱(0 min,91.5%A;25.00 min,91.5%A;30.00 min,20.0%A;40.00 min,20.0%A;40.01 min,91.5%A);流速:1.2 ml/min;检测波长:361 nm;柱温:35Ⅱ;进样量:50 μl。
2.2 溶液的制备
2.2.1 对照品溶液 取维生素B12对照品约12 mg,精密称定,置于100 ml量瓶中,加水溶解并稀释至刻度,摇匀,精密量取1 ml,置于200 ml量瓶中,加水稀释至刻度,摇匀,制成每1 ml约含维生素B120.6 μg的对照品溶液。
2.2.2 供试品溶液 取样品内容物约650 mg,置于10 ml量瓶中,加水溶解并稀释至刻度,摇匀,即得。
2.2.3 阴性对照溶液 按样品的配方比例取不含维生素B12的空白制剂(含处方中的其他维生素主成分及所有辅料)约650 mg,置于10 ml量瓶中,加水溶解并稀释至刻度,摇匀,即得。
2.3 系统适用性试验
精密量取“2.2”项下对照品溶液、供试品溶液、阴性对照溶液各适量,按“2.1”项下色谱条件进样测定,记录色谱,详见图1。由图1可知,在该色谱条件下,维生素B12与其他维生素主成分及辅料之间均能达到基线分离,分离度>2.0;理论板数以维生素B12峰计为12 395,保留时间为22.6 min。结果表明,辅料及其他维生素主成分对维生素B12的测定无干扰。
2.4 破坏性试验
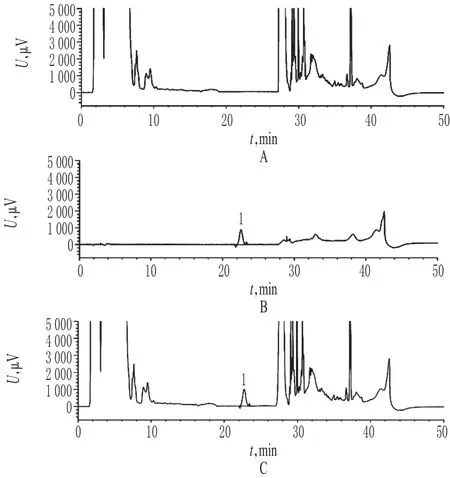
图1 系统适用性试验高效液相色谱图A.阴性对照;B.对照品;C.供试品;1.维生素B12Fig 1 HPLC chromatograms of system suitability testA.negative control;B.reference substance;C.test sample;1.vitamin B12
为验证降解产物与维生素B12主峰的分离度情况,对本品进行破坏性试验。(1)酸破坏溶液:取样品内容物约650 mg,精密称定,置于10 ml量瓶中,加1 mol/L盐酸溶液1 ml,于室温下放置4 h后用1 mol/L氢氧化钠溶液调节pH至中性,加水溶解并稀释至刻度,摇匀,即得;(2)碱破坏溶液:取样品内容物约650 mg,精密称定,置于10 ml量瓶中,加1 mol/L氢氧化钠溶液1 ml,于室温下放置2 min后用1 mol/L盐酸溶液调节pH至中性,加水溶解并稀释至刻度,摇匀,即得;(3)氧化破坏溶液:取样品内容物约650 mg,精密称定,置于10 ml量瓶中,加30%过氧化氢溶液1 ml,于室温下放置2 h后加水溶解并稀释至刻度,摇匀,即得;(4)高温破坏溶液:取样品内容物约650 mg,精密称定,置于10 ml量瓶中,加水1 ml,于80Ⅱ水浴加热10 min后取出,放冷,加水溶解并稀释至刻度,摇匀,即得;(5)光照破坏溶液:取样品内容物约650 mg,精密称定,置于10 ml量瓶中,加水1 ml,于室温下在5 000 lx强光下照射4 h后,加水溶解并稀释至刻度,摇匀,即得。取各破坏溶液适量,按“2.1”项下色谱条件进样测定,记录色谱,详见图2。由图2可知,本品在酸、碱、氧化、高温及光照破坏条件下均有不同程度的破坏,维生素B12含量均有下降;其中,碱破坏条件降解幅度最大,其次为氧化、光照和酸破坏,各降解产物峰与维生素B12峰分离度均符合要求。
2.5 线性关系考察
取维生素B12对照品约12 mg,精密称定,置于100 ml量瓶中,加水溶解并稀释至刻度,摇匀,精密量取5 ml,置于50 ml量瓶中,用水稀释至刻度,摇匀,作为对照品贮备液。精密量取对照品贮备液适量,分别加水稀释制成每1 ml中约含维生素B120.30、0.48、0.60、0.72、0.90 μg的系列线性工作溶液。精密量取上述溶液各适量,按“2.1”项下色谱条件进样测定,记录峰面积。以维生素B12进样量(x,ng)为横坐标、峰面积(y)为纵坐标进行线性回归,得维生素B12的回归方程为y=952.2x+ 243.2(r=0.999 9)。结果表明,维生素B12检测进样量线性范围为15.03~45.09 ng。
2.6 定量限与检测限考察
取“2.2.1”项下对照品溶液适量,等倍逐步稀释,按“2.1”项下色谱条件连续进样测定6次,记录峰面积。当信噪比为10∶1时,得定量限为4.355 ng;当信噪比为3∶1时,得检测限为1.452 ng。
2.7 精密度试验
精密量取“2.2.1”项下对照品溶液适量,按“2.1”项下色谱条件连续进样测定6次,记录峰面积。结果,维生素B12峰面积的RSD=0.21%(n=6),表明仪器精密度良好。
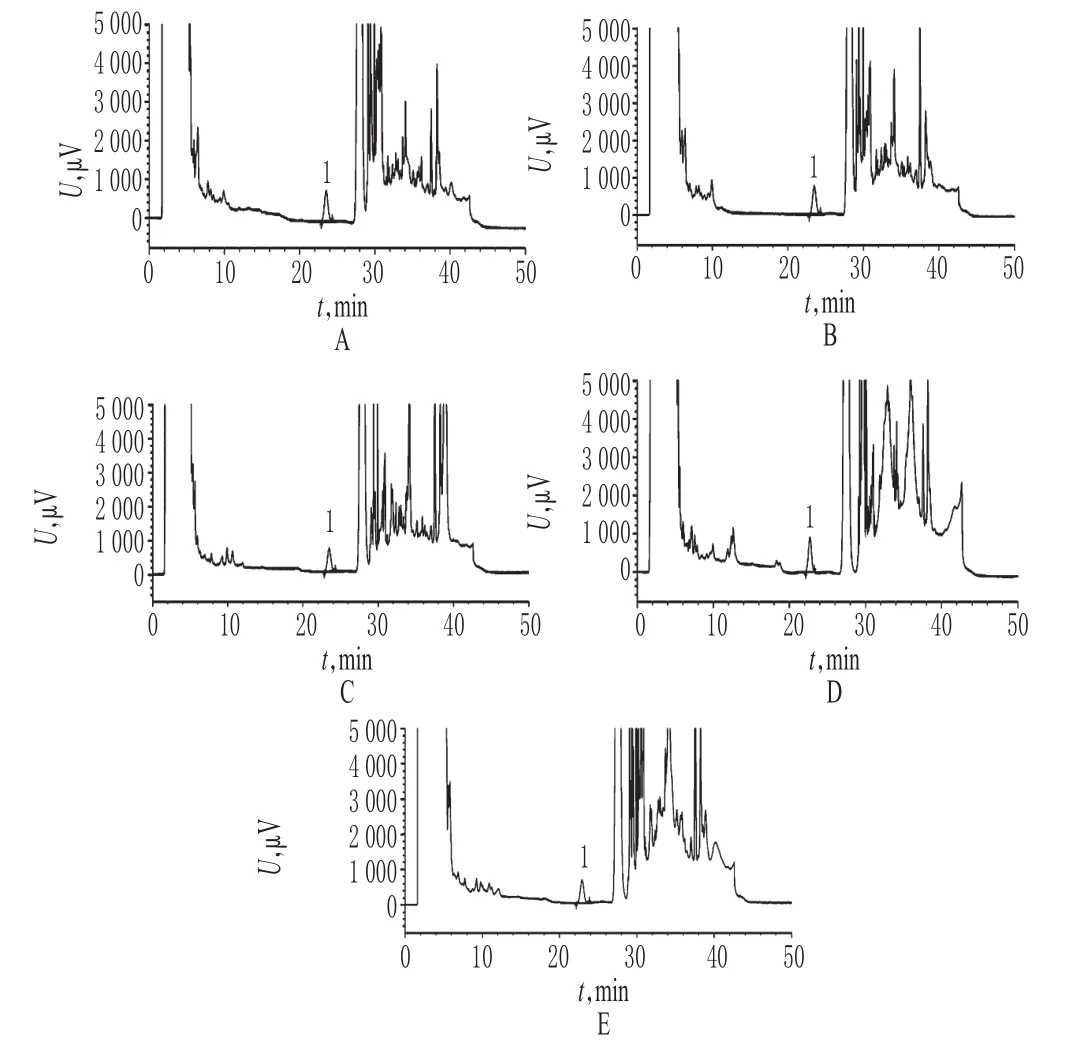
图2 破坏性试验高效液相色谱图A.酸破坏;B.碱破坏;C.氧化破坏;D.高温破坏;E.光照破坏;1.维生素B12Fig 2 HPLC chromatogram of destructive testsA.destructed by acid;B.destructed by alkali;C.destructed by oxidation;D.destructed by high temperature;E.destructed by light;1.vitamin B12
2.8 稳定性试验
取同一供试品溶液(批号:20130201)适量,分别于室温下放置0、2、4、6、8、12 h时按“2.1”项下色谱条件进样测定,记录峰面积。结果,维生素B12峰面积的RSD=0.31%(n=6),表明供试品溶液在室温下放置12 h内稳定性良好。
2.9 重复性试验
取“2.2.2”项下供试品溶液(批号:20130201)适量,共6份,分别按“2.1”项下色谱条件进样测定,记录峰面积。结果,维生素B12峰面积的RSD=0.29%(n=6),表明本方法重复性良好。
2.10 回收率试验
取“2.2.3”项下阴性对照溶液适量,加入一定质量的维生素B12对照品,按“2.2.2”项下方法制成80%、100%、120%的低、中、高质量浓度的溶液。取上述溶液适量,按“2.1”项下色谱条件进样测定,记录峰面积并计算维生素B12的回收率,结果见表1。试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算维生素B12的含量。结果,3批样品(批号:20130201、20130202、20130203)中维生素B12的含量分别为100.4%、100.7%、100.1%(n=3)。
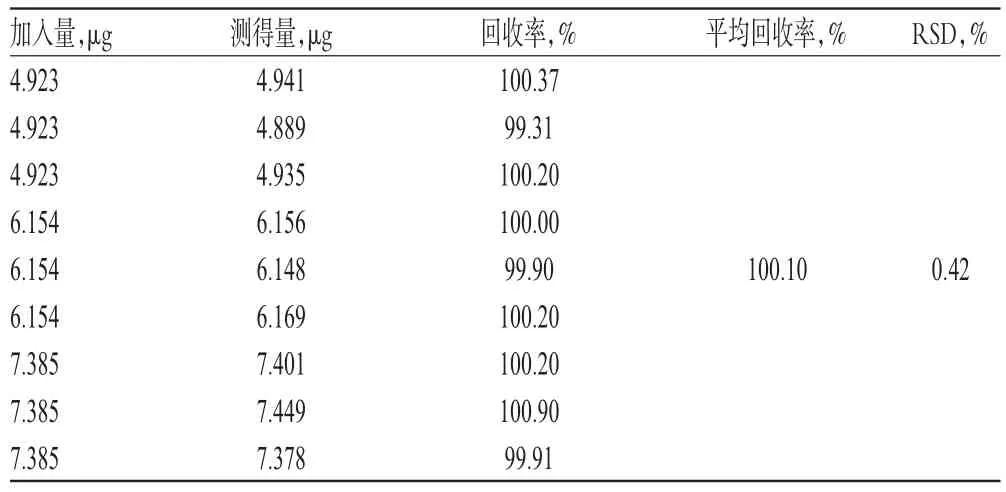
表1 回收率试验结果(n=9)Tab 1 Results of recovery test(n=9)
3 讨论
3.1 流动相的选择
有文献[6]采用0.001 5 mol/L己烷磺酸钠-甲醇(83∶17,V/V)为流动相,而该系统中的离子对试剂对HPLC仪有损伤,且重复性差。也有文献[9]采用0.02 mol/L磷酸氢二钠溶液(用磷酸调节pH为3.5)-甲醇(74∶26,V/V)为流动相,或采用0.05 mol/L磷酸二氢钾溶液(用磷酸调节pH为6.4)-乙腈(90∶10,V/V)为流动相[10],而这些系统中的缓冲盐可缩短色谱柱的使用寿命,同时易造成HPLC仪的堵塞。为延长色谱柱的使用寿命,减少对HPLC仪的损伤,降低检验成本,本试验采用水(用10%稀磷酸调节pH为4.5)-乙腈(梯度洗脱)为流动相,可缩短分析时间,且各色谱峰的分离度均较好。
3.2 检测波长的选择
取“2.2.1”项下对照品溶液适量,进行全波长紫外扫描。结果,维生素B12在278、361、550 nm波长处有最大吸收,但在361 nm波长处的吸收值最大。结合各国药典中维生素B12含量测定项下检测波长,最终确定本试验的检测波长为361 nm。
综上所述,本方法简便、准确、灵敏度高、重复性好,可用于注射用多种维生素(12)中维生素B12的含量测定。
[1] 刘惠,张颖,薛稚明,等.食物中维生素B12的测定方法研究进展[J].中国卫生检验杂志,2013,23(11):2 556.
[2] 秦尚.浅谈维生素与人体健康[J].中国医药指南,2015,13(28):294.
[3] 冯晓葶.维生素B12缺乏与相关疾病的关系[J].中国实用神经疾病杂志,2014,17(1):96.
[4] 白靖,何朝星,向柏,等.维生素制剂学研究[J].中国医院药学杂志,2010,30(16):1 396.
[5] 中华医学会肠外肠内营养学分会,北京医学会肠外肠内营养学分会.维生素制剂临床应用专家共识[J].中华外科杂志,2015,53(7):481.
[6] 国家食品药品监督管理局.国家药品标准YBH06412009 [S].2009.
[7] 国家食品药品监督管理局.国家药品标准YBH36742005 [S].2009.
[8] 国家食品药品监督管理局.国家药品标准WS-784(X-629)-2001(2)[S].2009.
[9] 宋新康,姚海燕,陈彤.HPLC法测定维生素B12片含量及含量均匀度[J].中国药师,2014,17(9):1 598.
[10] 宋金春,陆迅,曾俊芬,等.HPLC测定注射用13种复合维生素中维生素H、叶酸及维生素B12含量[J].中国药学杂志,2007,42(17):1 345.
(编辑:刘 柳)
2.11 样品含量测定
取3批样品内容物各适量,分别按“2.2.2”项下方法制备供
Improvement of the Method for Content Determination of Vitamin B12in Multivitamin for Injection(12)by HPLC
XU Jiagen1,DIAO Yanzhong2(1.Dept.of Pharmacy,Stomatological Hospital Affiliated to Medical College of Nanjing University,Nanjing 210008,China;2.Nanjing YOKO Pharmaceutical Group Co.,Ltd.,Nanjing 210009,China)
OBJECTIVE:To improve the method for the content determination of vitamin B12in Multivitamin for injection(12).METHODS:HPLC was performed on the column of Kromasil 100-5 C18with mobile phase of water(adjusted to pH4.5 with 10%diluted phosphoric acid)-acetonitrile(gradient elution)at a flow rate of 1.2 ml/min,the detection wavelength was 361 nm,column temperature was 35Ⅱ,and injection volume was 50 μl.RESULTS:The linear range of vitamin B12was 15.03-45.09 ng(r=0.999 9);RSDs of precision,stability and reproducibility tests were no lower than 1%;recovery was 99.31%-100.90%(RSD=0.42%,n=9).CONCLUSIONS:The method is simple,accurate,sensitive,reproducible,and can be used for the content determination of vitamin B12in Multivitamin for injection(12).
Multivitamin for injection(12);Vitamin B12;Content determination;HPLC;Method improvement
R917;R927.2
A
1001-0408(2016)36-5159-03
2016-05-25
2016-09-27)
DOI10.6039/j.issn.1001-0408.2016.36.38
*副主任药师。研究方向:医院药学。电话:025-83620369。E-mail:Xjg.234@163.com采用高效液相色谱法(HPLC),以等度洗脱的方式测定上述制剂中维生素B12的含量,但由于其流动相中含有大量缓冲盐和离子对试剂,对色谱柱和仪器损伤较大,同时大部分脂溶性主成分及辅料会在色谱柱中残留,累积产生污染,导致方法准确度、重复性差。另有文献[10]介绍了同时测定多种维生素的方法,但在试验中发现其他维生素主成分对维生素B12含量测定有明显干扰。为消除测定干扰,延长色谱柱使用寿命,减少对HPLC仪的损伤,缩短分析时间,降低检验成本,笔者对注射用多种维生素(12)中维生素B12的含量测定方法进行了改进,采用HPLC法以梯度洗脱的方式进行测定。
