一测多评法同时测定保肾乙丸中5种蒽醌类成分的含量
2016-03-11常志惠胡军华万亚菲孙雷雷王铀生南京中医药大学附属连云港市中医院药学部江苏连云港00江苏康缘药业股份有限公司江苏连云港000南京博大肾科医院南京0000
常志惠,胡军华,万亚菲,孙雷雷,王铀生(.南京中医药大学附属连云港市中医院药学部,江苏连云港00;.江苏康缘药业股份有限公司,江苏连云港 000;.南京博大肾科医院,南京 0000)
一测多评法同时测定保肾乙丸中5种蒽醌类成分的含量
常志惠1*,胡军华2,万亚菲1,孙雷雷3,王铀生3(1.南京中医药大学附属连云港市中医院药学部,江苏连云港222002;2.江苏康缘药业股份有限公司,江苏连云港 222000;3.南京博大肾科医院,南京 210000)
目的:建立同时测定保肾乙丸中芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚5种蒽醌类成分含量的方法。方法:采用高效液相色谱法,以大黄素为基准峰,分别计算其与芦荟大黄素、大黄酸、大黄酚、大黄素甲醚的相对校正因子(RCF),通过RCF计算保肾乙丸中上述5种蒽醌类成分的含量。色谱柱为Waters Symmetry C18,流动相为甲醇-0.1%磷酸溶液(70∶30,V/V),流速为1.0 ml/min,检测波长为254 nm,柱温为30Ⅱ,进样量为10 μl。结果:芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚检测质量浓度线性范围分别为5.83~186.6 μg/ml(r=0.999 7)、9.39~300.5 μg/ml(r=0.999 5)、9.55~305.6 μg/ml(r=0.999 9)、10.23~327.4 μg/ml(r=0.999 9)、4.01~128.4µg/ml(r=0.999 4);定量限分别为364.4、880.2、596.9、319.7、501.3 ng,检测限分别为109.3、293.4、179.1、95.91、150.4 ng;精密度、稳定性、重复性试验的RSD<2.0%;加样回收率分别为96.38%~100.90%(RSD=1.62%,n=6)、97.72%~101.75%(RSD=1.44%,n=6)、97.66%~102.34%(RSD=1.63%,n=6)、97.33%~101.91%(RSD=1.75%,n=6)、97.78%~100.74%(RSD=1.19%,n=6)。大黄素与芦荟大黄素、大黄酸、大黄酚、大黄素甲醚间的RCF分别为1.217 7、1.153 4、1.424 2、1.034 5。结论:该方法准确可靠、操作简便快捷,可用于同时测定保肾乙丸中芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚5种蒽醌类成分的含量。
保肾乙丸;一测多评法;蒽醌类成分;高效液相色谱法
保肾乙丸是在临床治疗经验基础上优选的组方,具有补肾健脾、活血和络、泄浊利水的功效,主治慢性肾脏病所致的慢性肾衰竭(代偿期、失代偿期和衰竭期)非透析患者、气阴两虚兼湿浊证患者出现的面黄乏力、食少纳呆、口干腰酸、大便干结、下肢水肿等,具有保护肾功能,降血肌酐、血尿素氮、血尿酸、尿蛋白,消水肿等作用。该处方主要由菟丝子、何首乌、黄芪、怀牛膝、大黄、陈皮等中药材组成,其中君药何首乌的主要成分为蒽醌类成分,使药大黄的主要成分亦为蒽醌类成分。蒽醌类成分具有多种生理活性,主要表现在降血糖、降胆固醇、利尿通便、抗氧化和抗衰老等方面。蒽醌类成分主要包括芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚等,目前对该类成分的测定多采用外标法(ESM),所需对照品繁杂,且费时费力。因此,本研究采用一测多评法(QAMS)[1-4]建立了同时测定保肾乙丸中芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚含量的方法,旨在为保肾乙丸的质量控制提供参考。
1 材料
1.1 仪器
1260型高效液相色谱(HPLC)仪,包括MWD紫外检测器(美国Agilent公司);H1650型台式高速离心机(湖南湘仪实验室仪器开发有限公司);AE-240型电子分析天平(瑞士Mettler-Toledo公司);BP211D型电子分析天平(德国Sartorius公司);Milli-Q型超纯水仪(美国Millipore公司)。
1.2 药品与试剂
保肾乙丸(江苏康缘药业股份有限公司,批号:120905、120906、120907、120909、131001、131002、131003、141201、141202、141203,规格:6 g/瓶);芦荟大黄素对照品(批号:110795-201007,纯度:98.0%)、大黄酸对照品(批号:110757-200206,纯度:100%)、大黄素对照品(批号:110756-201410,纯度:100%)、大黄酚对照品(批号:110796-201017,纯度:99.5%)、大黄素甲醚对照品(批号:110758-201013,纯度:99.8%)均购自中国食品药品检定研究院;甲醇为色谱纯,其余试剂均为分析纯,水为超纯水。
2 方法与结果
2.1 原理
在一定范围内成分的量(质量或浓度)与仪器响应值成正比,即:f=W/A(f表示相对校正因子,W表示成分的量,A表示仪器响应值)。在对保肾乙丸中5种蒽醌类成分进行质量控制时,以大黄素(s)为内参物,建立大黄素(s)与芦荟大黄素、大黄酸、大黄酚、大黄素甲醚之间的相对校正因子(RCF):
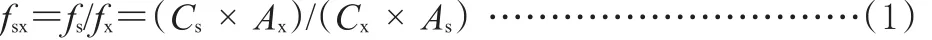
式中,fsx代表内参物与待测成分之间的成分RCF;Cs、Cx分别代表内参物与待测物成分浓度;As、Ax分别代表内参物与待测成分的仪器响应值。
通过RCF计算芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚的量,同时采用ESM法计算上述成分的量:

式中,AE代表待测成分的仪器响应值;a、b分别代表本公式的斜率和截距;CE代表ESM法计算所得待测成分的浓度进行同步测定,以验证计算值的准确性和可行性[5-8]。
2.2 色谱条件
色谱柱:Waters Symmetry C18(250 mm×4.6 mm,5 μm);流动相:甲醇-0.1%磷酸溶液(70∶30,V/V);流速:1.0 ml/min;检测波长:254 nm;柱温:30Ⅱ;进样量:10 μl。
2.3 溶液的制备
2.3.1 混合对照品溶液 分别精密称取芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚对照品适量,置于同一100 ml量瓶中,加甲醇制成1 ml含芦荟大黄素40 μg、大黄酸60 μg、大黄素60 μg、大黄酚60 μg、大黄素甲醚25 μg的混合对照品溶液。
2.3.2 供试品溶液 取样品适量,研细,取约2.5 g,精密称定,置于250 ml圆底烧瓶中,精密加入甲醇100 ml,称定质量,加热回流1 h,放冷,再次称定质量,加甲醇补足减失的质量,滤过,滤液蒸干,残渣加2.5 mol/L的硫酸溶液25 ml,微热使溶解,加三氯甲烷40 ml,水浴回流1 h,分取三氯甲烷层,剩余溶液再加三氯甲烷萃取3次,每次20 ml,合并上述三氯甲烷液,水洗至中性,回收三氯甲烷,残渣加甲醇使溶解并定容至10 ml量瓶中,作为供试品溶液。
2.3.3 阴性对照溶液 按样品的处方比例和制备工艺制备缺何首乌和大黄的阴性样品,再按“2.3.2”项下方法制备阴性对照溶液。
2.4 系统适用性试验
精密量取“2.3”项下混合对照品溶液、供试品溶液和阴性对照溶液各适量,按“2.2”项下色谱条件进样测定,记录色谱,详见图1。由图1可知,在该色谱条件下,各成分均能达到基线分离,分离度均>1.5;理论板数以大黄素峰计为19 872,保留时间为23.478 min。结果表明,其他成分对测定无干扰。

图1 高效液相色谱图A.混合对照品;B.供试品;C.阴性对照;1.芦荟大黄素;2.大黄酸;3.大黄素;4.大黄酚;5.大黄素甲醚Fig 1 HPLC chromatogramsA.mixed reference substance;B.test sample;C.negative control;1.aloe emodine;2.rhein;3.emodin;4.chrysophanol;5.physcion
2.5 线性关系考察
精密称取芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚对照品各适量,置于同一50 ml量瓶中,加甲醇溶解并定容,摇匀,得各待测成分质量浓度分别均为186.6、300.5、305.6、327.4、128.4µg/ml的系列混合对照品溶液。取上述系性溶液各适量,按“2.2”项下色谱条件进样测定,记录峰面积。以待测成分质量浓度(x,µg/ml)为横坐标、峰面积(y)为纵坐标进行线性回归,回归方程与线性范围见表1。

表1 回归方程与线性范围Tab 1 Regression equations and linear ranges
2.6 定量限与检测限考察
取“2.3.1”项下混合对照品溶液适量,等倍逐步稀释,按“2.2”项下色谱条件进样测定,记录信噪比。当信噪比为10∶1时,得定量限(LOQ);当信噪比为3∶1时,得检测限(LOD)。结果,芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚的LOQ分别为364.4、880.2、596.9、319.7、501.3 ng;LOD分别为109.3、293.4、179.1、95.9、150.4 ng。
2.7 精密度试验
取“2.3.1”项下混合对照品溶液适量,按“2.2”项下色谱条件连续进样测定6次,记录峰面积。结果,芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚峰面积的RSD分别为1.13%、1.12%、0.51%、0.73%、0.94%(n=6),表明仪器精密度良好。
2.8 稳定性试验
取“2.3.2”项下供试品溶液(批号:120905)适量,分别于室温下放置0、2、4、8、10、12 h时按“2.2”项下色谱条件进样测定,记录峰面积。结果,芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚峰面积的RSD分别为0.75%、1.11%、0.83%、0.95%、1.57%(n=6),表明供试品溶液在室温下放置12 h内稳定性良好。
2.9 重复性试验
取样品(批号:120905)2.5 g,精密称定,共6份,按“2.3.2”项下方法制备供试品溶液,再按“2.2”项下色谱条件进样测定,记录峰面积并计算含量。结果,芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚的平均含量分别为0.18、0.46、0.35、0.21、0.11 mg/g,RSD分别为1.24%、0.71%、1.12%、1.08%、1.64%(n=6),表明本方法重复性良好。
2.10 加样回收率试验
取已知含量的样品(批号:120905)6份,每份1.25 g,分别置于250 ml锥形瓶中,精密加入一定质量的芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚对照品,按“2.3.2”项下方法制备供试品溶液,再按“2.2”项下色谱条件进样测定,记录峰面积并计算加样回收率,结果见表2。

表2 加样回收率试验结果(n=6)Tab 2 Results of recovery tests(n=6)
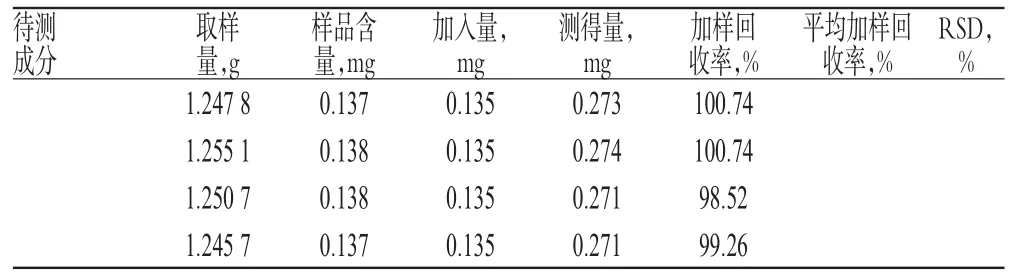
续表2Continued tab 2
2.11 RCF的计算和待测成分色谱峰的定位
以大黄素为内参物,按“2.1”项下公式(1),结合“2.5”项下系列混合对照品溶液所得峰面积数据,计算大黄素与芦荟大黄素、大黄酸、大黄酚、大黄素甲醚的RCF。结果,大黄素与芦荟大黄素、大黄酸、大黄酚、大黄素甲醚的RCF分别为1.217 7、1.153 4、1.424 2、1.034 5。
利用色谱峰相对保留值(其他成分保留时间与内参物保留时间的比值)定位:由色谱峰相对保留值和内参物的保留时间计算出目标峰相对保留时间,再根据峰形及光谱吸收变化趋势,即能够在一定程度上准确判断目标峰的位置。结果,芦荟大黄素、大黄酸、大黄酚、大黄素甲醚相对保留时间的RSD分别为0.75%、0.60%、0.45%、0.44%(n=5),表明利用色谱峰相对保留值进行目标峰的定位是可行的。
2.12 RCF的耐用性考察
本试验考察了不同色谱柱(Waters Symmetry C18、Kromasil C18、Phenomenex Luna C18)、不同仪器(Aglient 1200、Aglient 1260、Waters 2695)、不同柱温(25、28、30、32、35Ⅱ)、不同流速(0.8、1.0、1.2 ml/min)对蒽醌类成分含量测定结果的影响及对RCF和相对保留值的影响。结果,不同色谱柱、仪器、柱温、流速下测定的芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚含量的RSD分别为1.35%、2.14%、0.37%、1.68%、0.85%;芦荟大黄素、大黄酸、大黄酚、大黄素甲醚RCF的RSD分别为2.14%、1.71%、1.23%、1.46%,相对保留值的RSD分别为1.89%、2.79%、2.31%、2.10%。结果表明,不同色谱柱、仪器、柱温、流速对芦荟大黄素、大黄酸、大黄酚、大黄素甲醚的RCF无明显影响。
2.13 样品含量测定
取10批样品各适量,按“2.3.2”项下方法制备供试品溶液,再按“2.2”项下色谱条件进样测定,记录峰面积并分别采用ESM法和QAMS法测定保肾乙丸中5种蒽醌类成分的含量[相对误差(RE)=(QAMS法测得含量-ESM法测得含量)/ESM法测得含量×100%],结果见表3。
3 讨论

表3 样品含量测定结果(n=2,mg/g)Tab 3 Results of contents determination of samples(n=2,mg/g)
本研究选用性质稳定、价廉易得的大黄素为内参物,建立了该成分与其他4种蒽醌类成分的RCF,分别采用ESM法与QAMS法测定10批保肾乙丸中5种蒽醌类成分的含量。结果表明,ESM法测定结果与QAMS法测定结果无显著差异,说明QAMS法能够准确测定保肾乙丸中5种蒽醌类成分的含量。同时,QAMS法所用对照品种类较少,操作简单、方便,具有实用价值。
综上所述,本方法准确可靠、操作简便快捷,可用于同时测定保肾乙丸中芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚5种蒽醌类成分的含量。
[1] 国家药典委员会.中华人民共和国药典:四部[S].2015年版.北京:中国医药科技出版社,2015:59. 2] 王智民,钱忠直,张启伟.一测多评法建立的技术指南[J].中国中药杂志,2011,36(6):657.
[3] 张锴镔,冯伟红,王智民,等.一测多评法与外标法测定新清宁片中大黄蒽醌类成分含量[J].中国实验方剂学杂志,2012,18(11):61.
[4] 王钰莹,冯伟红,杨菲,等.“一测多评”法测定三黄片中的大黄蒽醌类成分[J].中国中药杂志,2012,37(2):212.
[5] 李爱红,陈伟健,胡文军.一测多评法测定银杏叶胶囊中总黄酮醇苷的含量[J].中国药房,2012,23(36):3 446.
[6] 刘晖晖,张辉,莫结丽,等.一测多评法测定黄连配方颗粒中4个成分的含量[J].中国药业,2012,21(10):39.
[7] 刘志辉,顾玮,常星洁,等.“一测多评”法测定麦贞花颗粒中不同类型成分的含有量[J].中成药,2012,34(12):2 342.
[8] 韩海红,陈翔.一测多评法测定大败毒胶囊中的蒽醌类成分[J].中国药学杂志,2013,48(23):2 039.
(编辑:刘 柳)
Simultaneous Determination of 5Anthraquinones in Baoshenyi Pill by QAMS
CHANG Zhihui1,HU Junhua2,WAN Yafei1,SUN Leilei3,WANG Yousheng3(1.Dept.of Pharmacy,Lianyungang Hospital of Traditional Chinese Medicine Affiliated to Nanjing University of Chinese Medicine,Jiangsu Lianyungang 222002,China;2.Jiangsu Kanion Pharmaceutical Co.,Ltd.,Jiangsu Lianyungang 222000,China;3.Nanjing Boda Nephrological Hospital,Nanjing 210000,China)
OBJECTIVE:To establish a method for the simultaneous determination of 5 anthraquinones(aloe emodin,rhein,emodin,chrysophanol and physcion)in Baoshenyi pill.METHODS:HPLC was conducted,using emodin as reference peak,the relative correction factors(RCFS)between emodin and aloe emodin,rhein,chrysophanol and physcion were calculated to calculate the contents of above-mentioned 5 anthraquinones.The column was Waters Symmetry C18with mobile phase of methanol-0.1% phosphoric acid solution(70∶30,V/V)at a flow rate of 1.0 ml/min,the detection wavelength was 254 nm,column temperature was 30Ⅱand injection volume was 10 μl.RESULTS:The linear range was 5.83-186.6µg/ml for aloe emodine(r=0.999 7),9.39-300.5µg/ml for rhein(r=0.999 5),9.55-305.6µg/ml for emodin(r=0.999 9),10.23-327.4µg/ml for chrysophanol(r=0.999 9)and 4.01-128.4µg/ml physcion(r=0.999 4);the limits of quantification were 364.4,880.2,596.9,319.7,501.3 ng,limits of detection were 109.3,293.4,179.1,95.9,150.4 ng;RSDs of precision,stability and reproducibility tests were lower than 2.0%;recoveries were 96.38%-100.90%(RSD=1.62%,n=6),97.72%-101.75%(RSD=1.44%,n=6),97.66%-102.34%(RSD=1.63%,n=6),97.33%-101.91%(RSD=1.75%,n=6)and 97.78%-100.74%(RSD=1.19%,n=6).The RCFs of emodin to aloe emodine,rhein,chrysophanol and physcion were 1.217 7,1.153 4,1.424 2 and 1.034 5,respectively.CONCLUSIONS:The method is reliable,simple and fast,and can be used for the simultaneous determination of aloe emodin,rhein,emodin,chrysophanol and physcion in Baoshenyi pill.
Baoshenyi pill;QAMS;Anthraquinones;HPLC
R284.1;R927
A
1001-0408(2016)36-5156-04
2016-06-01
2016-08-01)
*副主任中药师。研究方向:中药制剂。电话:0518-85572867。E-mail:zhchang66@sohu.com
DOI10.6039/j.issn.1001-0408.2016.36.37
