一种钇(Ⅲ)酰腙配合物的合成及抑菌性研究
2016-03-04张国春刘永亮周春生
高 霞,张国春,刘永亮,周春生
(商洛学院 陕西省尾矿资源综合利用重点实验室/化学工程与现代材料学院,商洛 726000)
一种钇(Ⅲ)酰腙配合物的合成及抑菌性研究
高 霞,张国春,刘永亮,周春生
(商洛学院 陕西省尾矿资源综合利用重点实验室/化学工程与现代材料学院,商洛 726000)
以3-甲氧基苯甲酰肼和丙酮酸为原料,采用乙醇为溶剂,在油浴加热条件下,通过缩合反应得到丙酮酸-3-甲氧基苯甲酰腙(PMBH).以自制的丙酮酸-3-甲氧基苯甲酰腙为配体,采用溶液法,与稀土金属盐YCl3·6H2O作用,合成了一种新的钇(Ⅲ)酰腙配合物:{Y(PMBH)3}·3H2O.利用元素分析、红外光谱、热分析等分析手段对配合物的组成、结构和性质进行研究.采用菌落直径法研究了配体及配合物对腐皮镰刀真菌的抑菌性,结果表明配体及配合物对腐皮镰刀真菌的生长都具有一定的抑制作用,且配合物对腐皮镰刀真菌的抑制作用较配体更强.
配合物;钇(Ⅲ);酰腙;抑菌性
酰腙化合物分子结构中活性基团-CO-NH-N=CH-的存在,使得此类化合物不仅可以与多种金属离子进行配位形成相应的金属有机配合物,而且具有良好的生物和药理活性,如抗菌、抗癌、抗肿瘤、抗氧化、抗病毒,消炎、除草等,在农药、医药等众多领域有着广泛的应用[1-11].作为一类具有较高医学和生物学价值的化合物,酰腙类化合物及其配合物在生物、催化、光学等领域应用十分广泛,其研究是化学和生物学领域的前沿领域之一.稀土金属离子具有未填满的4f电子层结构,这种结构的存在使得其在光、电、磁等方面具有独特的性质.有关稀土元素生物活性的研究始于二十世纪初期,随后的大量研究结果表明,稀土是具有生理活性的化学元素,其可以影响植物光合作用等一系列植物生理活动[12].
由酰腙化合物与稀土金属离子配位形成的稀土酰腙配合物,不仅具有抗炎、抗菌、抗癌等生理活性,而且在发光、荧光免疫分析及生物传感器等领域的研究和应用备受研究人员的广泛关注[13-26].Julio课题组的研究表明对氯苯甲酰肼与水杨醛希夫碱及其金属配合物具有良好的抑制杀虫作用[13].杨正银课题组研究了系列苯甲醛苯甲酰腙类稀土配合物其抗肿瘤和抗氧化活性,结果表明其均有一定的抗肿瘤和抗氧化活性[14].何水样等人对水杨醛缩水杨酰腙稀土金属配合物的研究,表明其对各类细菌普遍具有十分显著的抑制作用[15].杨锐等人在水和乙醇的混合体系中首次得到2-羰基丙酸水杨酰腙稀土金属Dy(III)配合物,并对其发光性能进行测试,结果表明配合物具有较好的荧光性能[16].罗飞华等人研究了邻氧乙酸苯甲醛缩水杨酰腙过渡金属Cu(Ⅱ)、Ni(Ⅱ)和Zn(Ⅱ)配合物的抗真菌活性和除草活性,测试结果表明其对受体均表现出了不同程度的选择性[19].但目前关于苯甲酰腙类稀土配合物生物活性研究的报道还不是很多,绝大多数是过渡金属配合物的相关报道.由于酰腙化合物所具有的良好的生物活性和多样的配位能力,结合稀土元素本身所具有的独特性质,本研究利用丙酮酸与3-甲氧基苯甲酰肼的缩合反应,设计合成了一种新的丙酮酸-3-甲氧基苯甲酰腙配体及其稀土金属钇(Ⅲ)配合物,利用菌落直径法初步测定了其在室温下的抑菌活性.
1实验部分
1.1 药品试剂及仪器
3-甲氧基苯甲酰肼,分析纯,梯希爱化成工业发展有限公司;丙酮酸,分析纯,宏大化工有限公司;YCl3·6H2O,分析纯,上海倍卓生物科技有限公司;二甲基亚砜(DMSO)和无水乙醇均为分析纯,天津市天力化学试剂有限公司;电子天平,JA-2003型,上海恒平科学仪器有限公司;显微熔点测定仪,X-5型,北京泰光仪器有限公司;电热鼓风干燥箱,202-1-AB型,上海一恒科学仪器有限公司;旋转蒸发器,R系列,上海申生科技有限公司;电子显微镜XT2-D型,重庆光电仪器有限公司;热重分析仪,NETSCHZSTA-449C型,美国TA公司;红外光谱仪,Nicolet Avatar 360型,尼高力公司;元素分析仪,Vario EL III型,德国元素分析系统公司;LDZX 40CI型立式自动电热电压蒸汽灭菌锅;SNCJ 1BU型无菌操作台;恒温生化培养箱;微量移液器;定量滤纸(直径6 mm);培养皿;三角瓶;酒精灯;接种环;打孔器;涂布器.
1.2 PMBH配体的合成
在250 mL三颈烧瓶中加入3-甲氧基苯甲酰肼(1.66 g,10 mmol)和无水乙醇(40 mL),混合均匀,置于装有冷凝管的磁力搅拌油浴锅中加热搅拌回流.称取丙酮酸(1.23 g,14 mmol),加入10 mL无水乙醇稀释,配制得丙酮酸乙醇溶液.待油浴锅温度达到75 ℃时,将丙酮酸乙醇溶液用恒压滴液漏斗缓慢地、逐滴地滴加至3-甲氧基苯甲酰肼溶液中.待滴加结束后开始计时,加热回流2 h,取出反应瓶.用旋转蒸发器蒸出适量无水乙醇,得白色沉淀,加入少量无水乙醇润洗,得黄色油状粗品,用甲醇重结晶,干燥得纯品.红外光谱吸收峰(KBr压片,cm-1):3 506(s),3 402(m),3 278(m),2 913(w),2 848(w),1 722(s),1 675(s),1 591(s),1 513(s),1 422(s),1 357(s),1 272(s),1 213(s),1 142(s),1 031(s),842(s),747(s).PMBH配体的合成路线如图1所示.
1.3 {Y(PMBH)3}·3H2O的合成
将PMBH(0.28 g,1.2 mmol)和YCl3.6H2O(0.18 g,0.6 mmol),分别溶于30 mL甲醇和30 mL蒸馏水中,得到PMBH甲醇溶液和YCl3·6H2O水溶液.量取甲醇和蒸馏水各15 mL,配制得30 mL缓冲溶液以供备用.用针管吸取YCl3·6H2O水溶液、缓冲溶液、PMBH甲醇溶液各5 mL,依次沿试管壁缓慢地注射到同一试管中,待出现明显分层现象后,用保鲜膜封口贴上标签,置于试管架静止.待过一个星期左右,试管壁上出现白色菱形晶体,经过滤,甲醇洗,真空干燥除去晶体表面的可溶性杂质,得到更纯净的晶体.红外光谱吸收峰(KBr压片,cm-1):3 434(m),3 187(m),2 952(w),2 829(s),1 617(w),1 532(m),1 487(s),1 364(s),1 311(s),1 213(s),1 135(s),1 037(s),861(s),738(s).

图1 PMBH配体的合成路线图
1.4 生物活性测试
1) 腐皮镰刀真菌菌种是由上海宝录生物科技有限公司提供.称取马铃薯400 g,切成小块放入烧杯中,加蒸馏水1 000 mL,加热至沸腾后持续加热30 min,用纱布趁热滤去马铃薯块,得滤液.将滤液转入1 000 mL烧杯中,加蒸馏水至最大标线,加入葡萄糖20 g,琼脂20 g,在石棉网上小火加热,同时用玻璃棒不断搅拌.待完全溶解后将培养液分装到6个锥形瓶中,分装结束后向锥形瓶口塞上棉塞,并用橡皮筋扎好,以免杂菌污染。将装有培养液的锥形瓶放入电热电压蒸汽灭菌锅中,在压力为0.1 MPa的高温蒸汽下灭菌.待30 min后取出,置无菌操作台上,转入直径为9 cm的培养皿中,制成培养基平板,凝固后备用.
2) 在无菌操作台上,取0.2 mL的腐皮镰刀菌菌液,注入制好的培养基平板上,用涂布器涂抹均匀,静置2 h后,倒置放入28 ℃恒温生化培养箱中,培养3 d,称取配体和配合物各5 mg分别加入100 mL的锥形瓶中,在无菌操作条件下向每个锥形瓶中加入10 mL葡萄糖琼脂培养液配成溶液,溶解过程中需要加入3滴DMSO溶剂.取配好的样品溶液10 mL,转入直径为9 cm的培养皿中,制成实验所需浓度的含样品平板.取培养3 d并经纯化的腐皮镰刀真菌,在无菌操作台中,使用直径为7 mm的打孔器切取菌饼,并接种于含样品平板的中央.然后倒置于28 ℃恒温生化培养箱中,培养5 d后观察抑菌效果,测量菌落的生长直径,每个样品对腐皮镰刀真菌平行试验3次,取其平均值.
3) 采用经典的十字交叉法测定空白对照样和样品的菌落直径,计算6次测量的直径平均值(每次试验记录两个数据)作为测定结果,计算样品对腐皮镰刀真菌生长的抑菌率.抑菌率计算公式如下:抑菌率 = [(空白对照菌落直径-样品处理菌落直径)/(空白对照菌落直径)]×100%.
2 结果与讨论
2.1 元素分析
由表1 可见,配体和配合物分别按化学式C11H12N2O4和Y(C11H11N2O4)3·3H2O计算,其测定值与理论值基本相吻合.因此,由元素分析数据结果推测配合物的组成为{Y(PMBH)3}·3H2O.
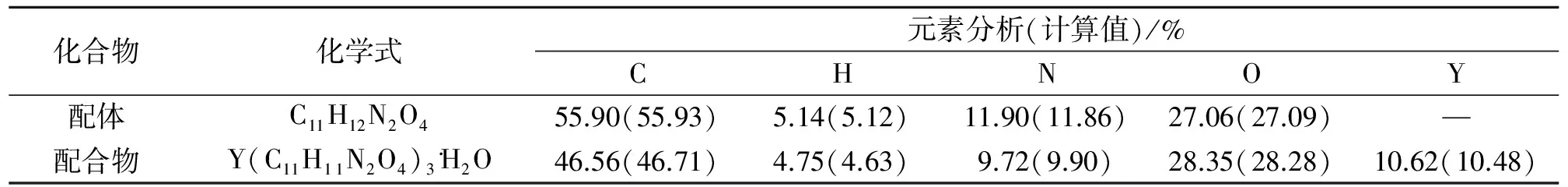
表1 配体和配合物的元素分析数据
2.2 红外光谱
以溴化钾为压片,在400~4 000 cm-1红外区域范围内测定了配体及其稀土金属钇配合物的红外光谱,红外光谱图如图2所示.与配体相比,配合物的红外光谱图中的某些吸收峰发生了明显的偏移,吸收强度也有较大的改变,说明稀土金属盐氯化钇与配体发生了反应.配体在1 513 cm-1处的吸收归属为C=N双键的伸缩振动,在配合物中,C=N双键的伸缩振动吸收峰蓝移到了1 532 cm-1处,伸缩振动强度也较配体弱.同时,配体在3 402 cm-1处的吸收归属为N-H单键的伸缩振动吸收峰,但配合物在3 402 cm-1处的吸收消失,表明配体中的亚氨基氮参与了金属键的配位.配体中的另外一个特征基团C=O在1 675 cm-1处出现了明显的伸缩振动,而配合物的伸缩振动吸收峰红移到了1 617 cm-1的位置,说明羰基变为C-O的伸缩振动,伸缩强度明显减弱,从以上现象可以推断出羰基上的氧原子参与金属键的配位.配合物在3 434 cm-1处出现宽的水的吸收峰,说明配合物中有水.根据以上分析,推测配合物中配体以图4的三齿形式与稀土钇离子配位形成两个五元环的稳定结构.

图2 配体和配合物的红外光谱图
2.3 热分析
配合物的TG和DTA曲线见图3,其热分解数据见表2.
配合物的理论失重率是根据化学式Y(C11H11N2O4)3·3H2O计算得到.热分析结果表明配合物在25~1 000 ℃范围内的失重过程分为两个阶段进行.配合物的框架结构可以稳定到大约250 ℃,当温度进一步升高后,配合物开始连续分解失重,该过程一直持续到大约850 ℃.第一阶段在25~250 ℃之间发生,相应的失重率为6.18%,约相当于失去配合物中3个水分子的阶段(理论失重率为6.35%).第二阶段分解温度在250~850 ℃之间,对应于配合物中配体的分解,相应的失重率为82.80%(理论失重率为83.21%),表明配合物的逐渐失重,并伴随着能量的放出.在250 ℃时开始有明显的失重现象,表明晶体结构发生了坍塌,850 ℃时的残余率为11.02%(理论残余率为10.44%),最终残余物为金属钇的氧化物.
2.4 配合物可能的结构
由元素分析数据结果推测配合物的组成为{Y(PMBH)3}·3H2O,由红外光谱分析推测配合物中配体中的C=N双键、亚氨基氮和羰基上的氧原子参与了金属键的配位,配体以图4的三齿形式与稀土钇离子配位形成两个五元环的稳定结构.通过以上分析,我们推测出配合物的可能结构如图4所示.

表2 配合物的热分解数据

图3 配合物的TG/DTA曲线图
2.5 抑菌活性
抑菌试验采用菌落直径法,受试菌种为腐皮镰刀真菌.配体和配合物对于腐皮镰刀真菌的抑菌实验数据见表3.由表3 可以看出,配体和配合物对所测试的菌种均有不同程度的抑菌活性,并且在相同的条件下,配合物对腐皮镰刀真菌的抑制作用呈现明显高于配体的趋势,如配体的抑菌率为18.6%,而相应的配合物为45.7%.这是由于稀土金属钇离子参与配位形成相应的配合物后,导致分子的共轭面增大,分子的脂溶性增加,对细菌细胞膜的穿透能力增强,从而引起细胞不能进行正常的新陈代谢,因此配合物的抑菌能力强于配体.

图4 配合物可能的结构

样品菌落生长直径/mmⅠⅡⅢ平均值抑菌率/%465049配体2930273245.7353735空白60555759—626058
2.6 抑菌机理分析
由表3 的实验数据可以看出,配体和配合物对腐皮镰刀真菌都具有一定的抑菌作用,配合物可能的抑菌作用机理[28]是:① 配体本身可以显示抑菌作用,当其与稀土金属离子进行配位形成配合物后,产生的配位作用会使得稀土金属离子的极性减小.同时形成的配合物为输送稀土金属离子通过细胞膜提供了合适的形式,在细胞膜内,稀土金属离子对生物大分子必需功能基团的发挥起到抑制作用,从而导致细胞凋亡;② 配体与稀土金属离子配位形成配合物后,鳌合作用的存在可以增大分子的共轭面和配体的亲油性,使其对细菌细胞膜的穿透能力增强,从而破坏了细胞壁的完整性,改变了细胞膜的通透性,最终导致细胞凋亡.
3 结 论
利用传统溶液法,以甲醇和蒸馏水为溶剂,成功合成了一种未见文献报道的丙酮酸-3-甲氧基苯甲酰腙钇(Ⅲ)配合物.采用菌落直径法测定了丙酮酸-3-甲氧基苯甲酰腙配体及其稀土金属钇(Ⅲ)配合物在室温下的抑菌活性.结果表明,配合物对腐皮镰刀真菌的抑制作用较配体更强,为该类配合物进一步的生物活性研究和应用提供有价值的参考.
[1] WU Wangting,HE Shuiyang,HU Huaiming,et al.Crystal structure and fluorescence of the supramolecular complex [Dy(H2L)(HL)(H2O)3]·0.5 dipy.2H2O[J].Journal of Coordination Chemistry,2007,60(2):125.
[2] CAROLINA D D,JORGE L M T,DANIEL I L,et al.Synthesis,Pharmacological Evaluation and Electrochemical Studies of Novel 6-Nitro-3,4-Methylenedioxyphenyl-N-Aylhydrazone Derivatives:Discovery of LASSBio-881,a New Ligand of Cannabinoid Receptors[J].Bioorganic & Medicinal Chemistry,2007,15:2421.
[3] 叶英,赵志刚,刘兴利,等.吲哚-6-酰腙类化合物的微波合成及其抗菌活性研究[J].有机化学,2009,29(6):993.
YE Ying,ZHAO Zhigang,LIU Xingli,et al.Microwave-Assisted Synthesis of Indole-6-Acylhydrazone and Their Antibacterial Activities[J].Chinese Journal of Organic Chemistry,2009,29(6):993.
(in Chinese)
[4] MORADI A,NAVIDPOUR L,AMINIETM.Design and Synthesis of 2-Phenoxy-Nicotinic Acid Hydrazides as Anti-Inflammatory and Analgesic Agents[J].Arch Pharm Chem Life Science,2010,343(9):509.
[5] 倪振杰,薛思佳,王静,等.1-取代哌啶-4-酮芳甲酰腙的合成及其抗白血病活性[J].有机化学,2011,31(2):222.
NI Zhenjie,XUE,Sijia,WANG Jing,et al.Synthesis and Anti-Leukemia Activity of 1-SubstitutedPiperidin-4-One Arylformylhydrazones[J].Chinese Journal of Organic Chemistry,2011,31(2):222.(in Chinese)
[6] JIN Yanxdxian,ZHONG Aiguo,ZHANG Yujian,et al.Synthesis,Crystal Structure,Spectroscopic Properties,Antibacterial Activity and Theoretical Studies of a Novel Difunctionalacylhydrazone[J].Journal of Molecular Structure,2011,1002:45.
[7] PAOLA H,MAURICIO C,MARíA L L,et al.Discovery of New Orally Effective Analgesic and Anti-Inflammatory Hybrid Furoxanyl N-Acylhydrazone Derivatives[J].Bioorganic & Medicinal Chemistry,2012,20:2158.
[8] XING Man,ZHAO Tingting,REN Yujia,et al.Synthesis,Biological Evaluation,and Molecular Docking Studies of Pyrazolyl-Acylhydrazone Derivatives as Novel Anticancer Agents[J].Medicinal Chemistry Research,2014,23:3274.
[9] LIU Yongxian,SONG Hongjian,HUANG Yuanqiong,et al.Design,Synthesis,and Antiviral,Fungicidal,and Insecticidal Activities of Tetrahydro-β-arboline-3-Carbohydrazide Derivatives[J].Journal of Agricultural and Food Chemistry,2014,62:9987.
[10] RICARDOAUGUSTO M S,JOSE E G,FELIPE P S,et al.Design,Synthesis and Biological Evaluation of Hybrid Bioisoster Derivatives of N-Acylhydrazone and Furoxan Groups with Potential and Selective Anti-Trypanosoma Cruzi activity[J].European Journal of Medicinal Chemistry,2014,82:418.
[11] YU Xifang,SHI Liqiao,KE Shaoyong.Acylhydrazone Derivatives As Potential Anticancer Agents:Synthesis,Bio-Evaluation and Mechanism of Action[J].Bioorganic & Medicinal Chemistry Letters,2015,25:5772.
[12] 何跃君,薛立.稀土元素对植物的生物效应及其作用机理[J].应用生态学报,2005,16(10):1983.
HE Yuejun,XUE Li.Biological Effects of Rare Earth Elements and Their Action Nechanisms[J].Chinese Journal of Applied Ecology,2005,16(10):1983.
(in Chinese)
[13] JULIO B,ALINE C Q,ISABELC.Newoxidovanadium(IV) N-Acylhydrazone Complexes:Promising Antileishmanial and Antitry Panosomal Agents[J].EuropeanJournal of Medicinal Chemistry,2013,62(1):20.
[14] 杨正银,杨汝栋.邻羧基苯甲醛苯甲酰腙稀土配合物的合成和抗氧化活性[J].中国稀土学报,2002,20(4):366.
YANG Zhengyin,YANG Rudong.Synthesis of 2-Carboxybenzaldehyde Benzoyl Hydrazone Rare Earth Complexes and Their Antioxidative Activity[J].Journal of the Chinese Rare Earth Society,2002,20(4):366.(in Chinese)
[15] 何水样,陈军利,杨锐,等.水杨醛水杨酰腙及其稀土配合物的合成、波谱研究及生物活性[J].有机化学,2003,23 (12):1387.
HE Shuiyang,CHEN Junli,YANG Rui,et al.Synthesis,Spectrum Study and Biological Activity of SalicylaldehydeSalicylhydrazone Complexes with Rare Earth[J].Chinese Journal of Organic Chemistry,2003,23 (12):1387.(in Chinese)
[16] 杨锐,何水样,武望婷,等.镝(Ⅲ)与酰腙及1,10-菲啰啉多元配合物的晶体结构及荧光性质[J].化学学报,2004,62(20):2040.
YANG Rui,HE Shuiyang,WU Wangting,et al.Crystal Structure,Fluorescence Characterization of Dysprosium(III) Multicomponent Complex with Acylhydrazone and 1,10-Phenanthroline[J].ActaChimica Sinica,2004,62(20):2040.(in Chinese)
[17] ZHANG Dong,ZANG Zhipeng,ZHOU Xiaoyan,et al.A Selective Fluorescence Probe for Yttrium(III) Based on Acylhydrazone Schiff Base[J].Inorganic Chemistry Communications,2009,12:1154.
[18] MARKUS A,YENI Y,ANNA E,et al.1∶1 vs.2∶1 Coordination of Pentadentatehydrazone-Type Ligands to Lanthanide(III) oIns.Formation of Cationic as Well as Dicationic Complexes[J].Dalton Transactions,2009,(36):7421.
[19] 罗飞华,杨莉,张萍,等.邻氧乙酸苯甲醛缩水杨酰腙及其配合物的合成与生物活性研究[J].化学研究与应用,2010,22(10):1315.
LUO Feihua,YANG Li,ZHANG Ping,et al.Synthesis,Biological Activity of 2-(2-formyl phenoxy) acetic acid-2-hydroxybenzohy Drazone and Its Complexes[J].Chemical Research and Application,2010,22(10):1315.(in Chinese)
[20] XUE S F,ZHAO L,GUO Y N,et al.A Series of Tetranuclear Lanthanide Complexes Comprising Two Edge-Sharing Triangular Units with Field-Induced Slow Magnetic Relaxation for Dy4Species[J].Dalton Transactions,2011,40:8347.
[21] XUE H F,ZHAO L,GUO Y N,et al.A Novel Windmill-Type DyIII[2 ×2] Grid Exhibiting Slow Magnetic Relaxation[J].Cite this:Dalton Transactions,2012,41:351.
[22] XU Min,ZHANG Yucui,XU Zhihong,et al.Crystal Structure,Biological Studies of Water-Soluble Rare Earth Metal Complexes with an Ofloxacin Derivative[J].Inorganica Chimica Acta,2012,384:324.
[23] XUE Shufang,GUO Yunnan,ZHAO Lang,et al.Molecular Magnetic Investigation of a Family of Octanuclear [Cu6Ln2] Nanoclusters[J].Inorgnic Chemistry,2014,53:8165.
[25] STANISLAV S B,SERGEY I L,LEONID D P,et al.Crystal Structure and Magnetic Properties of Binuclear Dy(III) Complexes with 4-substituted 2,6-diformylphenol Bis(Acylhydrazones)[J].Mendeleev Communications,2014,24:219.
[26] XU Zhouqin,MAO Xianjie,JIA Lei,et al.Synthesis,Characterization and Anticancer Activities of Two Lanthanide(III) Complexes with a Nicotinohydrazone Ligand[J].Journal of Molecular Structure,2015,1102: 86.
[27] ZHANG Li,ZHANG Peng,ZHAO Lang,et al.Anions Influence the Relaxation Dynamics of Mono-μ-3- OH- Capped Triangular Dysprosium Aggregates[J].Inorgnic Chemistry,2015,54:5571.
[28] 宋玉民,马俊怀,张玉梅.姜黄素苯胺希夫碱稀土配合物的抑菌性研究[J].化学试剂,2013,35(12):1069.
SONG Yumin,MA Junhuai,ZHANG Yumei.Antibacterial Properties of Complexes of Curcumin Aniline Schiff Base with Rare Earth[J].Chemical Reagents,2013,35(12):10169.(in Chinese)
(责任编辑、校对 肖 晨)
Synthesis and Antibacterial Activity of an Y(Ⅲ) Acylhydrazone Complex
GAOXia,ZHANGGuochun,LIUYongliang,ZHOUChunsheng
(Shaanxi Key Laboratory of Comprehensive Utilization of Tailings Resources,Department of Chemical Engineering & Modern Materials,Shangluo University,Shangluo 726000,China)
A new acylhydrazone ligand of pyruvate-3-methoxy benzoylhydrazone (PMBH)was synthesized under the condition of conventional oil bath heating with pyruvate and 3-methoxy benzoyl hydrazine as the raw materials and ethanolas as the solvent.The conventional solution reaction of the ligand with YCl3·6H2O generated a novel rare earth Y(III) complex,namely,{Y(PMBH)3} 3H2O.Its composition,structure and properties were studied by means of elemental analysis,fourier-transform infrared spectroscopy and thermogravimetric analysis.In addition,the antibacterial activity of the ligand and its complex against fusarium solaniwere were studied by the colony diameter method.The results show that they possesse certain antibacterial activities against the fungus and that the complex is much more resistant to the fungus than the ligand.
complex;Y(III);acylhydrazone;antibacterial activity
10.16185/j.jxatu.edu.cn.2016.11.004
2016-07-13 基金资助:国家自然科学基金项目(21273171);陕西省自然科学基础研究计划项目(2016JM2026); 商洛学院科研基金项目(14SKY002);国家级创新训练项目(201511396706)
高 霞(1983-),女,商洛学院讲师,博士研究生,主要研究方向为新型功能配合物的合成与性能研究. E-mail:xiagao2007@163.com.
O634
A
1673-9965(2016)11-0876-07
