超声提取/固相萃取测定固体介质中合成麝香及有机磷酸酯阻燃剂/增塑剂
2016-02-23曾祥英于志强盛国英傅家谟
刘 静,曾祥英,于志强,盛国英,傅家谟
(1.中国科学院广州地球化学研究所,有机地球化学国家重点实验室,广东省环境资源利用与保护重点实验室,
广东 广州 510640;2.中国科学院大学,北京 100049)
超声提取/固相萃取测定固体介质中合成麝香及有机磷酸酯阻燃剂/增塑剂
刘静1,2,曾祥英1*,于志强1,盛国英1,傅家谟1
(1.中国科学院广州地球化学研究所,有机地球化学国家重点实验室,广东省环境资源利用与保护重点实验室,
广东广州510640;2.中国科学院大学,北京100049)
摘要:基于超声提取与固相萃取技术,建立了沉积物和污泥中合成麝香与有机磷酸酯增塑剂/阻燃剂联合前处理方法,并采用气相色谱-质谱对目标化合物进行定性定量分析。考察了不同溶剂对目标化合物萃取效率的影响,确定以丙酮与乙腈-水(1∶3)的组合作为超声萃取溶剂。研究了基质效应和老化效应对目标化合物回收率的影响。结果表明,不同加标浓度下,4种常见合成麝香和9种常用有机磷酸酯的回收率为(27%±12%)~(117%±9%)。
关键词:有机磷酸酯;合成麝香;超声提取;固相萃取;气相色谱-质谱
有机磷酸酯(Organophosphate esters,OPs)是磷酸基团被取代而形成的一类化合物。这类化合物表现出良好的阻燃性和延展性,常作为阻燃剂或阻燃性增塑剂被大量添加在塑料制品、纺织品、电子设备、建筑材料以及家具装饰材料等产品中。由于取代基不同,OPs的理化性质,如水溶解度、挥发性等有显著差异(表1),用途也有所不同[1-2]。 随着五溴联苯醚和八溴联苯醚的逐步禁用,有机磷酸酯阻燃剂/增塑剂的产量用量逐步攀升[3]。 由于OPs是以物理添加而非化学键合方式添加于产品中,因此极易在产品的生产、使用和回收等过程中逃逸和挥发进入周围环境[1]。目前,在环境各介质中均检出OPs,包括大气[4-5]、污水污泥[6-7]、表层水和沉积物[6,8],甚至生物体[8-9]及人体样品[5]。由于磷酸酯尤其是氯代磷酸酯的毒理效应显著[1],其在环境介质中的分布、赋存、迁移转化以及毒副作用研究已成为环境领域的研究热点[10]。
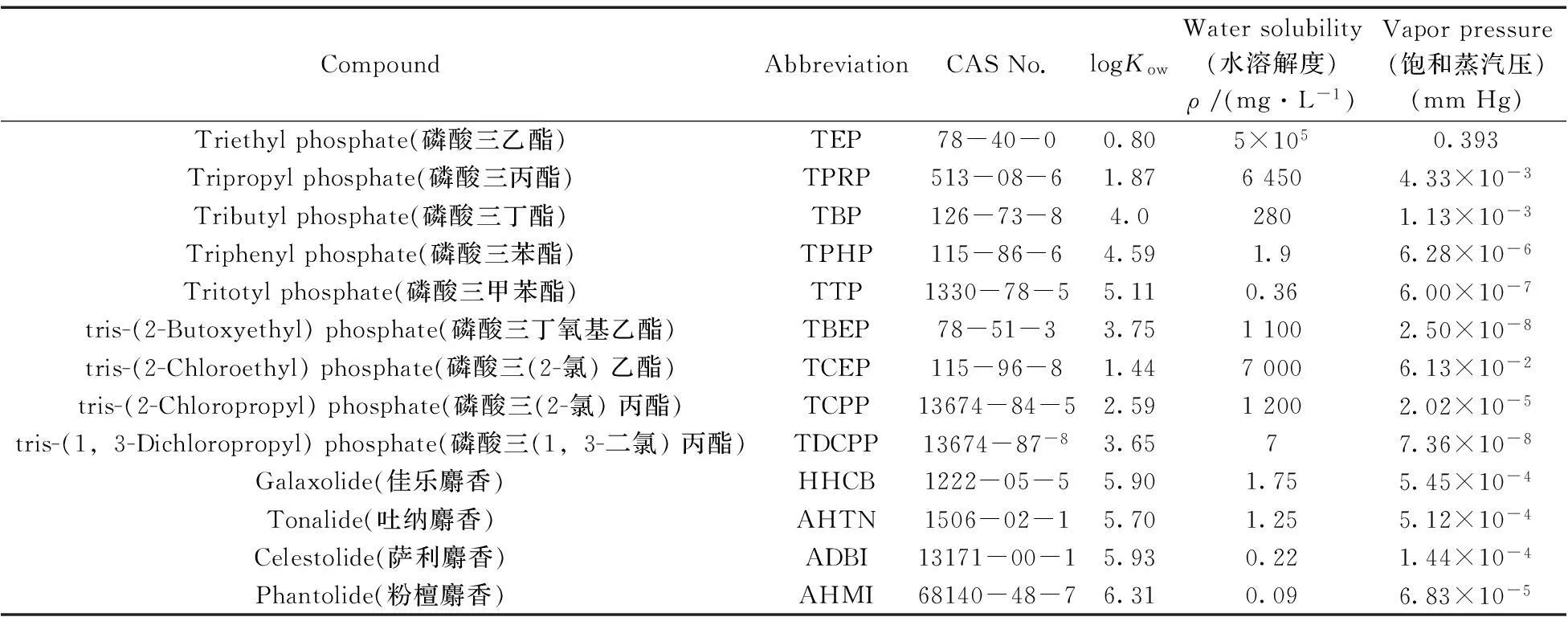
表1 13种目标化合物的相关信息[20]
合成麝香是人工合成的香料物质,取代天然麝香广泛添加在洗涤用品、日化产品、化妆品等产品中,使用后主要通过工业废水和生活污水持续排放进入环境,并可在食物链中富集和放大[11-12]。这类化合物不仅自身会对生物体和人体产生毒性(如抑制水生生物的生长和发育、雌激素活性等[13-14]),还能抑制生物体中多药外流载体的活性(Multixenobiotic resistance,MXR),从而促进有机体对其它污染物的吸收和富集[15]。目前,合成麝香被认定为新型污染物,其在环境中的分布赋存、迁移转化和毒性效应等研究已成为环境领域研究的热点之一。
本课题组在前期研究中建立了水环境中7种常见OPs的富集、分离和分析方法[16];此外,也对污泥和沉积物中的OPs分布进行了初步研究[17-19]。研究发现,利用乙腈-水(1∶3)作溶剂,对亲水性较好的OPs提取效果较好,如磷酸三丁酯(TBP)、磷酸三(2-氯乙基)酯(TCEP)、磷酸三(2-氯丙基)酯(TCPP)。但对于疏水性较强的两种芳基磷酸酯的提取效率不甚理想[18],尤其是基质复杂、总有机碳(TOC)含量较高的污泥样品,回收率很差[17]。
本文在前期研究基础上[17,19],筛选和优化提取溶剂,并将目标化合物扩展为目前环境介质中检测频率较高的9种OPs,同时将新型污染物合成麝香[14]纳入研究范畴,拟建立固体介质(包括沉积物和污泥)中常见OPs和合成麝香的快速联合前处理方法,并初步探讨基质效应以及老化效应对目标化合物提取效率的影响。
1实验部分
1.1仪器、材料与试剂
Oasis HLB(200 mg,6 mL)固相萃取小柱购于美国Waters公司;2300T超声仪(上海安普科学仪器有限公司);Anke-GL-10B离心机(上海安亭科学仪器厂)。
所用试剂均为色谱纯:乙酸乙酯(北京百灵威公司),丙酮(美国Burdick & Jackson公司),甲醇、正己烷、乙腈(德国Merck Co.公司)。9种OPs标样(美国Sigma-Aldrich公司):TEP(99.8%),TPRP(99%),TBP(99%),TPHP(99%),TCEP(97%),TBEP(94%),TTP(90%),TDCPP(97%)和TCPP(99.5%)。4种磷酸酯回收率指示物:d15-TEP(99.1%)、d27-TBP(98%)、d15-TPHP(98%)和d12-TCEP(98%)购于加拿大C/D/N Isotopes公司,合成麝香及回收率指示物d15-MX(97.5%)和内标六甲基苯(HMB,99.5%)购于德国Ehrenstofer-Schäfer Bgm-Schlosser实验室。实验用水为超纯水(锐思捷科学仪器有限公司的实验室超纯水系统制备)。
1.2样品前处理
待测样品置于50 mL聚四氟乙烯管中,依次加入5种回收率指示物和萃取溶剂,超声萃取30 min,控制水浴温度为(25±2)℃;3 000 r/min离心10 min,合并上层清液并置换溶剂为甲醇-水(1∶99),采用水环境中OPs分析方法完成富集、净化和洗脱回收[16]。方法如下:Oasis HLB小柱依次用3 mL洗脱溶剂、3 mL甲醇、3 mL甲醇-水(1∶99)活化;上述提取液通过大流量采样管载入SPE小柱,控制过柱速度为5~10 mL/min;上样结束后用3 mL甲醇-水(1∶99)洗涤小柱,抽干;再用洗脱溶剂洗脱目标化合物,洗脱液在柔和氮气下吹至近干后用正己烷定容,加入内标六甲基苯,待GC-MS分析。
1.3仪器分析条件
岛津2010 GC-MS,色谱柱为TG-5 MS(Thermo Scientific,30 m×0.25 mm×0.25 μm)。EI源,离子源温度220 ℃,进样口和接口温度分别为290 ℃和300 ℃。不分流模式进样,进样量1 μL。载气为氦气,流速1 mL/min。升温程序为:70 ℃保留2 min,以10 ℃/min升至160 ℃,再以5 ℃/min升至305 ℃,保留15 min。
1.4目标化合物回收率的计算
所有样品中均加入回收率指示物以控制样品处理流程中的损失;目标化合物的回收率通过比较实验组样品(真实沉积物/污泥中加入一定量的目标化合物)和对照组(真实样品)浓度差值计算而得,计算公式为:目标化合物回收率=(CS-CR)/C0×100%,其中,CS为加标样品实测浓度,CR为真实样品实测浓度,C0为加标浓度。
2结果与讨论
2.1仪器检出限、精密度与重复性
在最佳分析条件下[16],对各目标化合物进行全扫描以确定各组分的保留时间和特征离子,然后以选择离子扫描模式(SIM)进行定量分析,各化合物的定量离子和参考离子如表2所示。

表2 各目标化合物的定量离子、参考离子及仪器检出限
*the linearity of target compounds inn-hexane(正己烷中目标化合物的线性关系);**the linearity of target compounds in matrix(基质中目标化合物的线性关系)
采用外标法建立工作曲线,各目标化合物在0.025~5 μg/mL 范围内呈良好的线性关系,相关系数(r2) 为0.998 1~0.999 9(表2)。配制浓度接近空白的标样,连续进样7次,相对标准偏差(RSD) 为1.0%~5.0%,说明仪器具有良好的稳定性;根据化合物的信噪比(S/N)[21]计算得仪器的检出限(IDL)为0.06~3.13 ng/mL。
2.2超声萃取溶剂的筛选
考虑到OPs化合物的理化性质差异显著(logKow范围0.8~5.93),前期研究中发现乙腈-水(1∶3)对疏水性化合物的提取效率较差[17]。本研究借鉴文献报道结果[17,22-23],考察了丙酮、乙酸乙酯、乙腈-水(1∶3) 3种溶剂对沉积物中13种目标化合物的提取效果,其中沉积物样品(n=3)通过加入10 μL浓度为10 μg/mL的目标化合物制成加标样品,沉积物加标样品和实际沉积物样品(n=3)中均加入10 μg/mL 的5种回收率指示物10 μL。
各目标化合物的回收率结果如图1所示,用丙酮、乙酸乙酯、乙腈-水作提取溶剂时,5种回收率指示物的平均回收率±相对标准偏差(简称回收率)分别为(35%±4%)~(112%±13%)、(2%±1%)~(85%±9%)以及(9%±53%)~(82%±28%)。由于OPs类化合物的理化性质差异明显,不同萃取溶剂条件下其回收率差异显著。其中,TEP由于易挥发,回收率较差(<40%),尤其是乙酸乙酯作为萃取溶剂时,TEP回收率仅为(3%±1%);此外,水溶性较强的TCEP(9%±26%)和TCPP(20%±17%)的回收率也显著偏低;而以乙腈-水为溶剂时,TCEP和TCPP的回收率较为理想(分别为(82%±14%)和(70%±4%)),但疏水性的TTP回收率偏低(50%±31%);丙酮对TCEP的回收率(46%±5%)不如乙腈-水但强于乙酸乙酯,但对TTP(70%±14%)、TPHP(90%±2%)和TDCPP(91%±12%)的回收率优于乙腈-水,而对TBEP和TTP的提取效率又次于乙酸乙酯。对合成麝香而言,3种溶剂的回收率均偏低,其中丙酮(47%±43%~73%±6%)和乙酸乙酯(44%±6%~57%±13%)的回收率高于乙腈-水。
综上所述,由于本研究中目标化合物的种类较多,理化性质差异较大,单一的提取溶剂无法满足实验要求。因此,采用不同溶剂组合开展进一步实验。A组:丙酮+乙腈-水;B组:丙酮+丙酮+乙腈-水;C组:丙酮+丙酮。同时,挥发性较强的化合物回收率较低且重现性差,可能与置换溶剂过程中旋转蒸发至近干和氮吹至干两个过程的损失相关。因此在下一步的实验中,先将纯溶剂型的提取液置换为5 mL甲醇,与乙腈-水组分混合后再用水稀释至1%甲醇(乙腈)溶液。
实验结果如图2所示。为了直观对比不同萃取溶剂的提取效率,将丙酮萃取结果也列入图中。结果表明,丙酮+乙腈-水组合条件下,5种回收率指示物的回收率为(15%±9%)~(90%±1%),目标化合物回收率为(19%±12%)~(92%±1%);而丙酮+丙酮+乙腈-水组合对5种回收率指示物的回收率为(13%±5%)~(92%±4%),所有目标化合物的回收率为(17%±12%)~(95%±8%)。结果表明,采用组合溶剂萃取并改善了溶剂置换操作后,萃取效果均有明显改善。其中,以丙酮+乙腈-水为萃取溶剂时,亲水性TCEP的回收率以及合成麝香的回收率有不同程度提高;而以丙酮+丙酮+乙腈-水组合则更为理想,除TEP以外的12种目标化合物均可取得较为理想的提取效果。
2.3老化效应对提取效率的影响
Alexander等[24]研究发现,有机分子与土壤等环境介质长时间接触,会进入介质的细微空隙,被隔离或包裹而难以释放出,即会发生老化效应,因此本研究考察了老化效应对目标化合物提取效率的影响。实验组(n=3)中加入目标化合物和回收率指示物,室温避光静置24 h;次日,向对照组(n=3)中加入目标化合物和回收率指示物,两组样品同时进行萃取、富集和分析。
实验组和对照组中,5种回收率指示物的回收率为(25%±6%)~(90%±2%);实验组中目标化合物的回收率(31%±10%~97%±2%)与对照组(30%±10%~92%±1%)无显著差异。表明老化效应对提取效率的影响甚少,在实际研究中可以不考虑老化效应。考虑到实验操作的简便可行并节省时间,采用加标后立即进行前处理。
2.4基质效应对提取效率的影响
为考察基质改变对目标化合物提取效率的影响,在选定的实验条件下,对沉积物/处理后的沉积物(沉积物基质)进行加标回收实验,各组分加标浓度为20 ng/g。同时,设置污泥/抽提后的污泥(污泥基质)作为对照,加标浓度为40 ng/g。结果表明,沉积物与沉积物基质中回收率指示物的回收率为(25%±6%)~(95%±4%),污泥与污泥基质中回收率指示物的回收率为(35%±10%)~(81%±7%)。沉积物实际样品中的目标化合物回收率(30%±8%~92%±1%)与基质加标样品中的目标化合物回收率(27%±15%~93%±3%)之间无显著差异(图3);而实际污泥样品加标与污泥基质加标回收率也均在允许范围。污泥样品中TEP的回收率明显升高,这可能是污泥基质的存在减少了TEP的挥发;此外,AHMI与HHCB的回收率偏高,可能与污泥来源相关。该污泥样品本身含有较高水平的合成麝香。综上所述,在缺乏合适基质的情况下,借用提取后的沉积物和污泥样品作为质量控制和质量保证措施中的基质加标分析是可行的。
在选定的提取条件下,考察了基质中目标化合物的线性关系。由于无法获得不含目标化合物的沉积物样品,实验采用提取后的沉积物(Pre-extracted)为基质,制备出与样品介质对应的沉积物基质进行加标测定。结果表明,基质中13种目标化合物在0.025~5 μg/mL质量浓度范围内均呈良好的线性关系,相关系数(r2)为0.997 0~0.999 4(表2)。
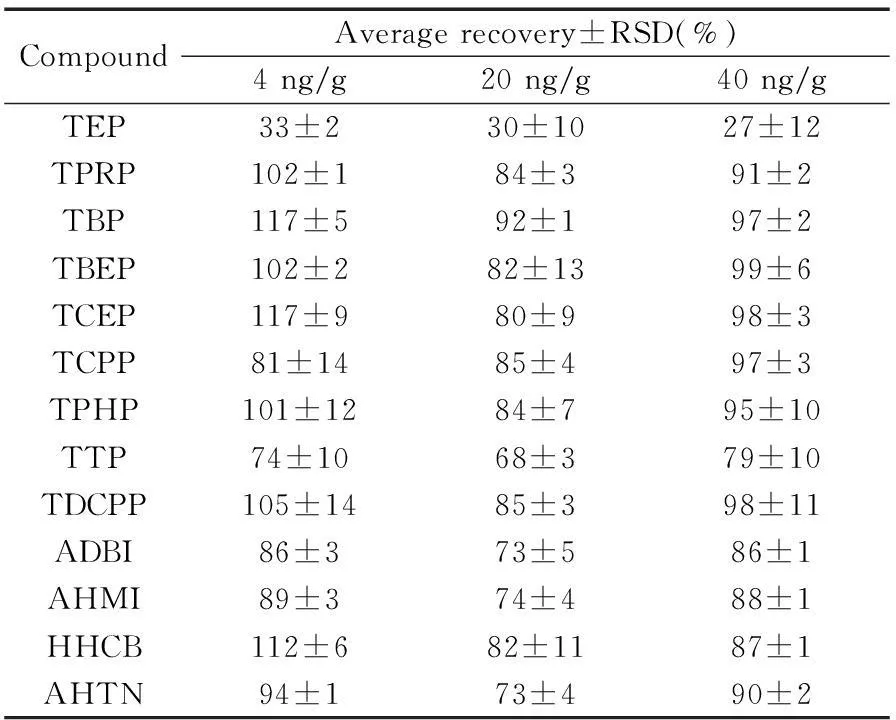
表3 不同加标水平下目标化合物的回收率(n=3)
2.5回收率与重现性
准确称量5 g沉积物,在优化条件下进行提取和测定,分别进行低浓度(4 ng/g)、中浓度(20 ng/g)和高浓度(40 ng/g)的加标实验,结果如表3所示。
5种回收率指示物的回收率为(24%±10%)~(105%±2%),9种OPs的回收率为(27%±12%)~(117%±9%),即使疏水性较强的TTP回收率也达到(68%±3%)~(79%±10%),4种合成麝香的回收率为(73%±5%)~(112%±6%)。表明本方法对沉积物中的OPs与合成麝香具有良好的回收率和重现性。
2.6方法验证
采用本方法测定了8个实际环境样品中有机磷酸酯与合成麝香的分布与含量水平,其中6个沉积物分别取自太湖(沉积物1~2)、珠江干流(沉积物3~4)和大伙房水库(沉积物5~6),2个污泥样品为广州两个市政污水处理厂的外排污泥。由实际样品分析得到回收率指示物的回收率为(13%±6%)~(103%±7%)。
由表4可以看出,太湖沉积物中均检出13种目标化合物,其中OPs含量为0.10~1.79 ng/g,合成麝香为0.04~2.79 ng/g,主要OPs污染物为TBP,TCPP和TBEP,这与课题组前期研究结果一致[18]。珠江干流沉积物中检出13种目标化合物,其中OPs含量为1.45~70.53 ng/g,合成麝香为0.10~546.80 ng/g。这两个沉积物样品中化合物的分布规律不同,沉积物4中TBEP含量(70.53 ng/g)显著高于其余样品,而沉积物3中TPHP含量(56.37 ng/g)显著高于其余样品,表现出较为显著的点源排放特征。大伙房水库沉积物中均未检出TEP,TPRP和TTP,其余5种OPs含量为LOD~3.18 ng/g,4种合成麝香为LOD~0.86 ng/g(检出限见表2)。

表4 沉积物与污泥样品中有机磷酸酯与合成麝香的含量(ng/g)
-:no detected;LOD:limit of quantification
广州污泥中检出13种目标化合物,其中OPs含量为2.97~49.99 ng/g,合成麝香为43.57~2 875.89 ng/g,可能与这些污水处理厂的污水来源为生活污水与工业废水混合来源有关。
3结论
本文建立了一种快速联合检测固体介质中9种有机磷酸酯与4种合成麝香的方法。通过丙酮+乙腈-水组合溶剂提取,Oasis HLB小柱固相萃取和富集净化,再用乙酸乙酯回收目标化合物。方法表现出良好的回收率和重现性,在不同浓度基质加标实验中显示出良好的适用性。
参考文献:
[1]Van der Veen I,de Boer J.Chemosphere,2012,88(10):1119-1153.
[2]Abdallah M A,Covaci A.Environ.Sci.Technol.,2014,48(9):4782-4789.
[3]Stapleton H M,Klosterhaus S,Eagle S,Fuh J,Meeker J D,Blum A,Webster T F.Environ.Sci.Technol.,2009,43(19):7490-7495.
[4]Shoeib M,Ahrens L,Jantunen L,Harner T.Atmos.Environ.,2014,99:140-147.
[5]Ali N,Mehdi T,Malik R N,Eqani S A,Kamal A,Dirtu A C,Neels H.Environ.Pollut.,2014,193:269-276.
[6]Rodil R,Quintana J B,Concha-Graa E,López-Mahía P,Muniategui-Lorenzo S,Prada-Rodríguez D.Chemosphere,2012,86(10):1040-1049.
[7]Celano R,Rodriguez I,Cela R,Rastrelli L,Piccinelli A L.Talanta,2014,118:312-320.
[8]Harino H,Yatsuzuka E,Yamao C,Ueno M,Ohji M.J.Mar.Biol.Assoc.UK,2014,94(1):43-49.
[9]Chen D,Letcher R J,Chu S.J.Chromatogr.A,2012,1220(0):169-174.
[10]Wang X W,Liu J F,Yin Y G.Prog.Chem.(王晓伟,刘景富,阴永光.化学进展),2010,22(10):1983-1992.
[11]Zeng X Y,Sheng G Y,Gui H Y,Chen D H,Shao W L,Fu J M.Chemosphere,2007,69:1305-1311.
[12]Luo Q,Sun L N,Zhang Y H.J.Instrum.Anal.(罗庆,孙丽娜,张耀华.分析测试学报),2011,30(7):745-749.
[13]Parolini M,Magni S,Traversi I,Villa S,Finizio A,Binelli A.J.Hazard.Mater.,2015,285:1-10.
[14]Ramskov T,Selck H,Salvitod D,Forbes V E.Environ.Toxicol.Chem.,2009,28(12):2695-2705.
[15]Luckenbach T,Epel D.Environ.HealthPerspect.,2005,113(1):17-24.
[16]He L X,Cao S X,Zeng X Y,Yu Z Q,Sheng G Y,Fu J M.J.Instrum.Anal.(何丽雄,曹曙霞,曾祥英,于志强,盛国英,傅家谟.分析测试学报),2013,32(4):437-441.
[17]Zeng X Y,He L X,Cao S X,Yu Z Q,Sheng G Y,Fu J M.Environ.Toxicol.Chem.,2014,33(8):1720-1725.
[18]Cao S X,Zeng X Y,Song H,Li H R,Yu Z Q,Sheng G Y,Fu J M.Environ.Toxicol.Chem.,2012,31(7):1478-1484.
[19]Cao S X.PreliminaryStudyontheLevelsandDistributionofOrganophosphateFlameRetardantsandPlasticizersinTypicalEnvironments.Beijing:University of Chinese Academy of Sciences(曹曙霞.典型环境中有机磷酸酯阻燃剂和增塑剂的污染现状初步研究.北京:中国科学院大学),2012.
[20]The US Environmental Protection Agency’s Office of Pollution Prevention,Toxics and Syracuse Research Corporation(SRC).Estimation Programs Interface(EPI).[2015-04-01].http://www.srcinc.com/what-we-do/environmental/scientific-databases.html.
[21]Wang D G,Alaee M,Sverko E,Li Y F,Reiner E J,Shen L.J.Environ.Monit.,2011,13(11):3104-3110.
[22]Martínez-Carballo E,González-Barreiro C,Sitka A,Scharf S,Gans O.Sci.TotalEnviron.,2007,388(1/3):290-299.
[23]Zheng J,Gao Z,Yuan W,He H,Yang S,Sun C.J.Sep.Sci.,2014,37(17):2424-2430.
[24]Alexander M.Environ.Sci.Technol.,1995,29(11):2713-2717.
Determination of Synthetic Musks and Organophosphate Flame Retardants/Plasticizers in Solid Phase by Ultrasound-assisted Extraction Coupled with Solid Phase ExtractionLIU Jing1,2,ZENG Xiang-ying1*,YU Zhi-qiang1,SHENG Guo-ying1,FU Jia-mo1
(1.State Key Laboratory of Organic Geochemistry,Guangdong Provincial Key Laboratory of Utilization and Protection
of Environmental Resources,Guangzhou Institute of Geochemistry Chinese Academy of Sciences,Guangzhou510640,
China;2.University of Chinese Academy of Sciences,Beijing100049,China)
Abstract:A rapid method was developed for the simultaneous determination of synthetic musks and organophosphate esters(OPs) in sediment/sludge,based on ultrasonic-assisted extraction,solid phase extraction(SPE) and the subsequent analysis by gas chromatography-mass spectrometry(GC-MS).In this study,different solvents were investigated and optimized,and thus acetone and acetonitrile-water(1∶3) were chosen for the extraction of analytes.Two potential factors(the matrix effect and aging effect) influencing recoveries of the target compounds of the analgtes were also studied.Under the optimized conditions,13 analytes including 9 widely used OPs and 4 synthetic musks were extracted and analyzed,and the results indicated that acceptable recoveries of the analytes were achieved in the range of (27%±12%)-(117%±9%),from sediment,sludge and pre-extracted sediment at different spiked concentrations.
Key words:organophosphate esters;synthetic musks;ultrasonic-assisted extraction;solid phase extraction;gas chromatography-mass spectrometry(GC-MS)
中图分类号:O657.63;TQ047.9
文献标识码:A
文章编号:1004-4957(2016)01-0061-07
doi:10.3969/j.issn.1004-4957.2016.01.010
通讯作者:*曾祥英,博士,副研究员,研究方向:环境毒害污染物及其风险评估,Tel:020-85292033,E-mail:zengxy@gig.an.cn
基金项目:国家自然科学基金资助项目(41373107)
收稿日期:2015-05-25;修回日期:2015-07-26
