煅烧温度对化学沉淀法制备纳米氧化钌结构与电化学性能的影响
2016-02-18冷娴杨洪志邹俭鹏熊翔何捍卫
冷娴,杨洪志,邹俭鹏,熊翔,何捍卫
煅烧温度对化学沉淀法制备纳米氧化钌结构与电化学性能的影响
冷娴,杨洪志,邹俭鹏,熊翔,何捍卫
(中南大学粉末冶金国家重点实验室,长沙 410083)
在RuCl3·nH2O水溶液中加入NaOH作为沉淀剂,采用化学沉淀法制备氧化钌粉体材料,分析与研究氧化钌的形貌、物相结构及电化学特性,以及煅烧温度的影响。结果表明:随煅烧温度从160 ℃升高到200 ℃,煅烧后获得的水合氧化钌的结晶水含量逐渐减少;热分析结果表明水合氧化钌在150~390 ℃范围内脱去结构水,由无定型转变为金红石型纳米晶体。随煅烧温度从160 ℃升高到200 ℃,氧化钌电极在0.1 A/g电流密度下的比电容由862 F/g下降至592 F/g, 但在5 A/g大电流密度下的容量保持率由34.82%提高到75.57%,在1 A/g电流密度下充放电200次后比容量保持率由88%提高到97%,即在较高温度下煅烧获得的氧化钌具有更好的电容特性和功率特性,更适合高功率下应用。
氧化钌;赝电容;化学沉淀法;纳米材料;煅烧温度
相对原电池和二次电池等化学电源,电化学电容器具有功率大、周期短、寿命长和可靠性高等优点。提高电容器的能量密度和功率密度的核心之一是改进电极材料。电化学电容器的电极材料主要包括提供界面双电层电容的碳材料和通过表面或体相氧化还原反应提供赝电容的金属氧化物和导电聚合物。金属氧化物RuO2具有极高的理论质量比容量(1 036 F/g)、优异的热稳定性和充放电循环稳定性,是最具潜力的电极材料之一。RuO2活性材料的结晶状态、微观形貌、电极膜层的厚度及均匀性等都显著影响RuO2电极性能的发挥[1]。实验制备的RuO2电化学活性材料通常为薄膜或粉末,RuO2粉末的制备方法主要有溶胶−凝胶 法[2]、化学沉淀法[3]和水热法[4]等。王晓峰等[5]用氯化钌和碳酸氢氨为原料,采用胶体法制备超级电容器电极用氧化钌材料,在250 ℃下制备的材料具有最大电化学比容量570 F/g、最低的等效串联阻抗和良好的功率特性,碳纳米管的掺入能显著提高该材料的功率特性。武彩霞等[6]研究了杂质离子对非晶态水合氧化钌电化学超电容性能的影响,结果表明Na+和Cl−杂质不仅降低氧化钌的比电容,而且降低氧化钌的功率性能。刘泓等[7]以RuCl3·3H2O异丙醇溶液为前驱体,采用原位分解法制备超级电容器用羧基氧化钌薄膜,随温度升高,RuCl3·3H2O异丙醇溶液经历先复合再分解的过程之后生成羧基氧化钌薄膜,薄膜经300 ℃保温2 h后比电容达728 F/g。陈经坤等[8]以自制的喷雾装置和十二烷基磺酸钠(SDS)分别作为反应辅助技术和表面分散剂,在175 ℃下获得比表面积为223 m2/g的蓬松状、深黑色无定形水合氧化钌材料,该材料具有较好的比电容(在扫描速度为1 mV/s时为988 F/g)和倍率性能,以及较低的等效串联内阻(约30 mΩ)和频率响应特性。RuO2的实际比电容通常比理论值低得多,主要是因为其比电容与比表面积、结晶度、结合水等实际状况紧密相关。高比表面积的RuO2能提供参加氧化还原反应的更多活性位点,从而获得高比电容。无定形态RuO2由于其氧化还原反应能在体相和表面同时进行,有利于质子和电子的扩散与传输,故表现出优异的电化学性能。RuO2的结晶水由于提供可离解的质子,在电子传输和质子传输达到平衡后,可显著提高比电容。RuO2的比表面积、结晶度、结合水均受煅烧温度的影响,但到目前为止未见关于RuO2煅烧温度的系统研究的报道。为制备综合性能优异的超级电容器用氧化钌电极材料,本文作者以RuCl3·nH2O水溶液为原料,用NaOH为沉淀剂,采用化学沉淀法制备RuO2活性粉末,系统研究煅烧温度对材料结构和电化学性能的影响,以便为制备综合电化学性能优异的钌基复合材料提供参考。
1 实验
1.1 原料
RuCl3·nH2O (优级纯,上海国药集团化学试剂有限公司);NaOH(分析纯,天津市大茂化学试剂厂);丙酮(分析纯,天津市大茂化学试剂厂);无水乙醇(分析纯,天津市大茂化学试剂厂);N-甲基吡咯烷酮(分析纯,天津市大茂化学试剂厂);乙炔黑(电池级,太原市迎泽区力之源电池销售部);聚偏二氟乙烯(电池级,太原市迎泽区力之源电池销售部);钽片(纯度99.95%,陕西宝鸡科辉钛业有限公司);去离子水(自制,电阻率为18.25 mΩ∙cm)。
1.2 氧化钌粉末的制备
配制浓度为1 mol/L的 RuCl3·nH2O水溶液,在磁力搅拌条件下缓慢滴入1 mol/L NaOH水溶液至pH=7,溶液由棕红色逐渐转变为黑色(含钌的配合物和氢氧化物)。用蒸馏水离心洗涤沉淀物数次以清除Na+和Cl−等离子,继而用极性和表面张力相对较低的有机溶剂(如无水乙醇)洗涤沉淀物数次,以减弱颗粒之间的氢键作用,从而减少团聚,然后置于真空、100 ℃下干燥,最后在空气环境下于不同温度(160,170,180,190和200 ℃)煅烧2 h,得到水合氧化钌粉末。
1.3 氧化钌电极的制备
首先对集流体钽片进行预处理,即用金相砂纸打磨,再依次在浓度为0.5 mol/L 的NaOH溶液、乙醇和丙酮中超声清洗以去除表面污染物,烘干待用。将水合氧化钌粉末、乙炔黑导电剂和聚偏二氟乙烯胶黏剂按质量比85:5:10混合,加入少量N-甲基吡咯烷酮,在玛瑙研钵中研磨使其混合均匀,然后滴涂于预处理后的钽片,再置于100 ℃烘箱中真空干燥10 h。
1.4 性能测试
采用NOVATM Nano SEM230扫描电镜和JEOL 2010 II透射电镜观察水合氧化钌粉末的表面形貌,拍摄选区电子衍射(selected area electron diffraction, SAED)谱。将氧化钌粉末于乙醇中超声处理后,滴于超薄碳支持膜上,干燥后进行TEM观察。
采用D/MAX2550+18 kW型X线衍射仪和NETZSCH STA 449C差热分析仪对氧化钌粉末的结晶状态和结晶水含量进行表征和分析。XRD分析采用Cu Kα为辐射源,=0.154 nm, 管电压为40 kV,管电流为40 mA,扫描范围(2)为8°~78°。热分析采用氩气气氛,加热速率为10 ℃/min。
采用CHI 660B电化学工作站测试氧化钌电极的电化学性能。将工作电极、铂片辅助电极和饱和甘汞参比电极(232型)浸于1 mol/L H2SO4电解质中,测试循环伏安曲线、恒流充放电曲线和交流阻抗。
分别于不同扫描速率(1,5,10,20,50和100 mV/s)下对工作电极进行循环伏安实验,根据下式计算氧化钌电极的电容量:
1=/∆(1)
式中:1为电极的电容量;为对伏安曲线积分而得的反应电荷量;∆为扫描电压。
在不同电流密度(0.1,0.5,1,2,3,4和5 A/g)下对工作电极进行恒流充放电实验,用下式计算质量比电容:
2=/∆=∙∆/∆(2)
式中:2为质量比容量,F/g;为放电电流密度,A/g;∆和∆分别为某段放电曲线对应的时间差和电位差,单位分别为s和V。
交流阻抗测试条件:交流信号幅度为5 mV;频率扫描范围为l00 kHz~l0 mHz。
2 结果与讨论
2.1 表面形貌
图1所示为160 ℃和200 ℃下煅烧获得的RuO2粉末的SEM形貌。文献[10]报道空气气氛下160~ 200 ℃煅烧2 h,煅烧温度的变化对显微形貌影响不显著[10],由图1(a)和(c)可知在160 和200 ℃下煅烧的RuO2粉末均为微米级颗粒。由图1(b)和(d)可见:大颗粒由细小颗粒团聚而成,于160 ℃煅烧的RuO2粉末呈更疏松的层状结构,在一定程度上利于电解质对其表面的润湿,能促进产生氧化还原赝电容的质子交换过程。
图2所示为不同煅烧温度下制备的RuO2粉末的TEM形貌和SAED谱。由图2(a)和(c)可知:RuO2团聚体由不规则的纳米级颗粒组成,于200 ℃下煅烧的粉末颗粒边缘发生更多烧结,团聚体较紧实。于160 ℃下煅烧的粉末,其SAED谱呈典型的无定形态弥散环特征,隐约出现衍射环,但很不明显,源于RuO2颗粒的纳米尺寸效应和高含水量[11];当煅烧温度升高到200 ℃时,衍射环数量增多,衍射轨迹较明显,电子衍射花样显示其局部结构为多晶的金红石型RuO2纳米晶体,表明微区域内发生了羟基缩聚及结晶化[12]。

图1 不同煅烧温度下制备的RuO2粉末的SEM形貌

图2 不同煅烧温度下制备的RuO2粉末TEM照片和SAED谱
2.2 物相组成
图3所示为不同煅烧温度下制备的RuO2粉末的XRD谱。由图3可知RuO2材料无尖锐的衍射峰,说明其为长程无序结构的无定型态水合RuO2,由类金红石纳米晶/团簇(电子的传递路径)和晶粒表面物理/化学吸附的结构水(质子的传递路径)组成[13]。从图3可知200 ℃煅烧后得到的水合氧化钌为非晶态,这是因为金红石相氧化钌的晶化温度为300 ℃,200 ℃煅烧未达到其晶化温度。但图2(d)所示TEM分析结果反映了材料内部微区域的结构形态,因此,有可能展现其由非晶态向晶态转变的过程,从而表现出一定的结晶特征。
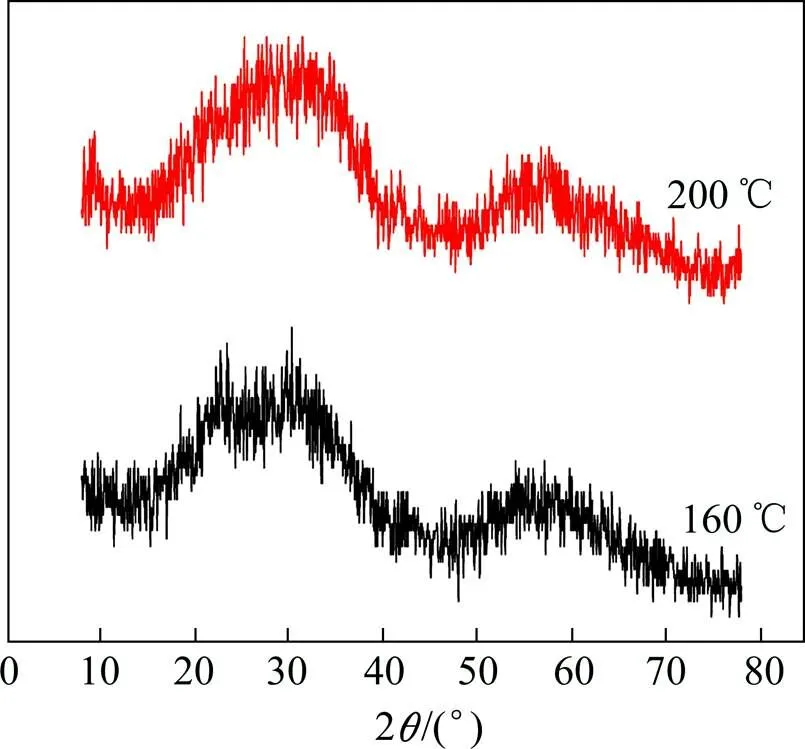
图3 不同煅烧温度下制备的RuO2粉末的XRD谱
2.3 热分析
图4所示为160~200 ℃温度下煅烧获得的RuO2粉末的热分析结果。从图4可见:随温度升高,RuO2的质量减少,即含水氧化钌先脱去物理吸附水(~100 ℃),再脱去结构水(150~390 ℃)[14−16],完成由无定型向特定晶型的转变。根据TGA曲线可计算出在160,170,180,190和 200 ℃下煅烧的样品在室温到450 ℃温度范围内的质量损失率分别为7.59%,7.13%,5.8%,5.05%和4.67%,含水氧化钌可分别表示为RuO2∙ 0.61H2O,RuO2·0.57H2O,RuO2·0.46H2O,RuO2·0.39H2O和RuO2·0.36H2O。
2.4 电化学性能
图5所示为RuO2材料的循环伏安曲线。由图5(a)可知:在160~200 ℃下煅烧后获得的RuO2在低和内扫描速率(5 mV/s)下的循环伏安曲线均呈现矩形特征,说明电极反应的可逆性高,具有较小的时间常数阻。其中,煅烧温度为160~180 ℃的RuO2材料具有较大的质量比电容,原因是结晶水含量高,有充足的质子参与赝电容反应伴随的质子/电子双注入/脱出过程。由图5(b)可知:在较高扫速(50 mV/s)下,于190 ℃和200 ℃煅烧的RuO2材料都仍然保持电容器的典型特征,即循环伏安曲线类似矩形,适合高功率下应用。而160~180 ℃下煅烧的RuO2材料的循环伏安曲线严重偏离矩形,原因是RuO2材料内部结晶水和晶格缺陷阻碍了电子的有效传递,导致内阻增加,不适合高功率下应用。

图4 不同煅烧温度下获得的RuO2粉末的热重分析

图5 不同煅烧温度下制备的RuO2材料的循环伏安曲线
图6所示为RuO2电极的充放电曲线。由图6可知:煅烧温度对RuO2的电容量和等效串联电阻影响显著。在0.5 A/g恒流条件下,160~200 ℃煅烧的氧化钌的充放电曲线的对称性都较好,基本为等腰三角形,质量比容量在758~523 F/g之间,与循环伏安沉积法制备的纳米氧化钌比容量相当[17]。在不同工艺条件下制备的RuO2材料微观组织结构不同,导致其热力学和晶体学性能不同,比容量最大的样品的结构水含量=0.5~0.75[10, 18]。本研究的结果表明:160 ℃煅烧的RuO2比容量最大,结构水含量多=0.61,与文献报道的结果相吻合;在2 A/g恒流条件下充放电,于160 ℃和170 ℃煅烧的RuO2在放电曲线的起始位置有明显电压突降,源于相对较大的等效串联电阻;于190℃和200 ℃煅烧的氧化钌的充放电曲线仍都保持良好的对称性,说明内阻较小,容量保持率较高。结合XRD结果可知:通过改变煅烧温度可控制晶粒尺寸及材料的微结构,从而提高材料的电学及电化学性能[19]。

图6 不同煅烧温度下制备的RuO2材料充放电曲线
图7所示为RuO2材料的交流阻抗曲线(其中,′和″分别为阻抗实部和虚部)。高频区阻抗圆弧与横坐标轴的截距为电解液的电阻s(反应电容器的内阻),在0.69~1.14 Ω之间。高频区压缩半圆直径代表电解质/氧化钌电极界面的电荷传输反应所引起的电荷转移电阻(ct),主要来自赝电容材料的法拉第氧化还原反应。于160~200 ℃煅烧的RuO2的ct分别为10.81,5.06,3.94,0.58和0.24 Ω。可见在190 ℃和200 ℃煅烧的RuO2的ct明显减小,倍率性能得到有效提升。低频区的直线反映超级电容器的电容特性,直线的斜率越大,说明具有更理想的电容行为,可见随煅烧温度提高,RuO2越接近理想电容行为[20−21]。

图7 不同煅烧温度下制备的RuO2材料的阻抗曲线
图8所示为RuO2电极材料的功率特性。从图8(a)与(b)可以看出:随煅烧温度升高,材料的功率特性显著提高。由图8(a)可见,于160~200 ℃下煅烧的RuO2材料在1 mV/s的扫描速率下质量比电容分别为616,572,450,461和477 F/g,100 mV/s扫描速率下的 容量保持率分别为11.84%(72.93 F/g),13.67%(78.19 F/g),28.26%(127.17 F/g),55.34%(255.12 F/g)和53.28%(254.15 F/g)。质量比电容明显高于已报道的晶体氧化钌薄膜(380 F/g)。由于较低温度下煅烧的氧化钌为无定型氧化钌,含有结构水,质子易于扩散到活性材料内部,有利于氧化还原反应的进行,而在较高煅烧温度下得到的结晶氧化钌刚性大,难膨胀,质子反应限制在近表面,限制了比电容的增大。由图8(b)可见,随煅烧温度从160 ℃升高到200 ℃,质量比容量随扫描速率增大而减小的幅度变小。低电流密度下(如0.1~2 A/g),160 ℃和170 ℃煅烧的RuO2材料质量比电容更大,0.1 A/g电流密度下分别达862 和735 F/g,因为其结晶水含量高,提高了氧化还原活性位点的利用率,使更多位于体相内部的氧化钌亦能提供赝电容。然而过多的质子通道会影响电子导通,对倍率性能不利,如160 ℃和170 ℃煅烧的氧化钌材料在大电流密度(5 A/g)下的质量比容量分别下降至300 和439 F/g,容量保持率仅为低电流密度(0.1 A/g)下的34.81%和59.73%,溶胶凝胶法制备的氧化钌同样具有随电流密度增加,比容量显著下降的特征[22]。随煅烧温度升高,有效的导电网络逐渐形成,于190 ℃和200 ℃煅烧的RuO2材料的电容保持率分别提高至70.02%和75.57%。

图8 不同温度煅烧的RuO2材料的比容量随扫描速率和恒流放电电流密度的变化
图9所示为不同温度下煅烧的RuO2材料的比容量保持率与循环次数的关系曲线。从图可见:随煅烧温度提高,比容量的保持率增加,于160,170,180,190和200 ℃热处理的RuO2材料在200次充放电循环后比容量保持率分别为88%,91%,94%,96%和97%。可见提高煅烧温度可改善RuO2材料的循环稳定性,原因是RuO2活性材料的结构水含量减少,增加了内部电子导通及导电性。
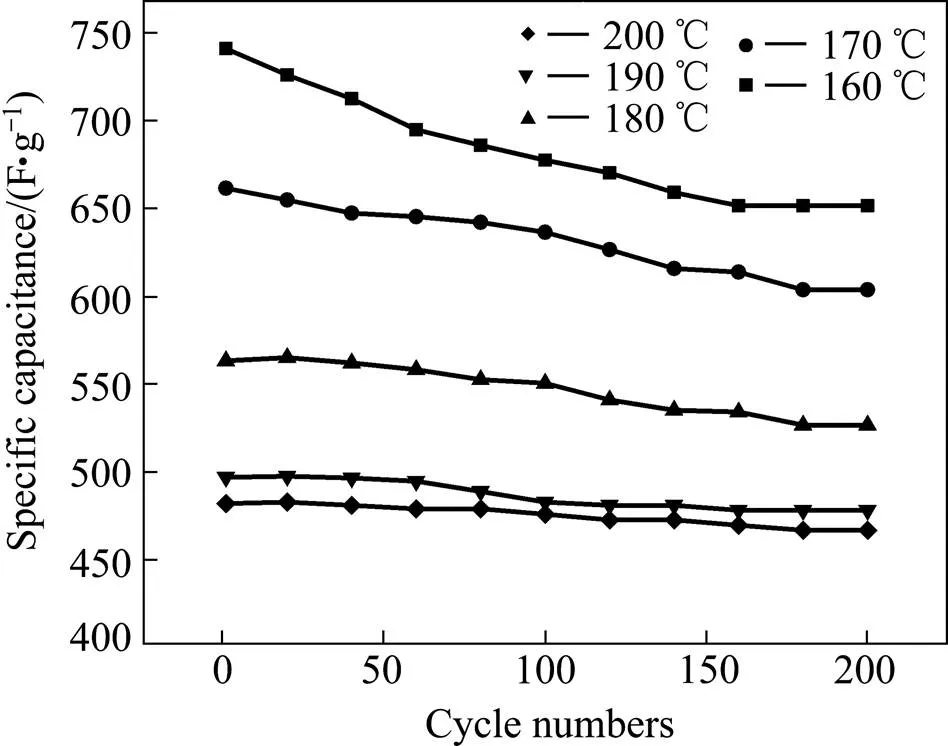
图9 不同温度下煅烧的RuO2材料的比容量与循环次数的关系曲线
3 结论
1) 采用化学沉淀法制备具有电容活性的RuO2·H2O材料,在160~200 ℃下煅烧,煅烧温度对表面形貌影响较小,但物相由无定型转变为纳米颗粒局部结晶化,结构水含量逐渐减少,=0.36~0.61。
2) 低扫描速率(5 mV/s)下,RuO2的循环伏安曲线近似矩形,在扫描速率为50 mV/s时,仅190 ℃和200 ℃煅烧的样品表现出良好的电容响应。在电流密度为0.1 A/g时,随煅烧温度升高,比容量由862 F/g下降至592 F/g,在200 ℃时煅烧获得的氧化钌具有最低的电荷转移电阻(0.24 Ω),以及优良的高功率放电特性和循环稳定性。
REFERENCES
[1] DELMER O, BALAYA P, KIENLE L, et al. Enhanced potential of amorphous electrode materials: Case study of RuO2[J]. Advanced Materials, 2008, 20(3): 501−505.
[2] CHANG K, HU C, CHOU C. Textural and pseudocapacitive characteristics of sol–gel derived RuO2·xH2O: Hydrothermal annealing vs. annealing in air[J]. Electrochimica Acta, 2009, 54(3): 978−983.
[3] CHANG K, HU C. Oxidative synthesis of RuOx·nH2O with Ideal capacitive characteristics for supercapacitors[J]. Journal of the Electrochemical Society, 2004, 151(7): A958−A964.
[4] CHANG K, HU C. Hydrothermal synthesis of hydrous crystalline RuO2nanoparticles for supercapacitors[J]. Electrochemical and Solid-State Letters, 2004, 7(12): A466−A469.
[5] 王晓峰, 王大志, 梁吉. 超细氧化钌超电容器电极材料的制备[J]. 无机化学学报, 2003, 19(4): 371−376. WANG Xiaofeng, WANG Dazhi, LIANG Ji. Preparation of ultra-fine ruthenium oxide as an electrode material for electrochemical capacitors[J]. Chinese Journal of Inorganic Chemistry, 2003, 19(4): 371−376.
[6] 武彩霞, 刘罡, 方海涛, 等. 杂质离子对非晶态水合氧化钌电化学超电容性能的影响[J]. 材料研究学报, 2009, 23(6): 628−634. WU Caixia, LIU Gang, FANG Haitao, et al. Effect of impurity ions on electrochemical super-capacitive properties of amorphous hydrated ruthenium oxide[J]. Chinese Journal of Materials Research, 2009, 23(6): 628−634.
[7] 刘泓, 甘卫平, 郑峰, 等. 羧基氧化钌薄膜的热分解机理及其伏安性能[J]. 材料热处理学报, 2010, 31(12): 1−7. LIU Hong, GAN Weiping, ZHENG Feng, et al. Thermal decomposition mechanism and electrochemical properties of carboxyl ruthenium oxide film[J]. Transactions of Materials and Heat Treatment, 2010, 31(12): 1−7.
[8] 陈经坤, 张熙贵, 陈安松, 等. 超级电容器用无定形水合二氧化钌材料及Nafion作粘接剂的电极制备研究[J]. 化学通报, 2014, 77(1): 50−57. CHEN Jingkun, Zhang Xigui, CHEN Ansong, et al. Preparation of amorphous ruthenium oxide and its electrode using Nafion as binder for supercapacitors[J]. Chemistry, 2014, 77(1): 50−57.
[9] LIU X, PICKUP P G. Ru oxide supercapacitors with high loadings and high power and energy densities[J]. Journal of Power Sources, 2008, 176(1): 410−416.
[10] KIM I H, KIM K B. Ruthenium oxide thin film electrodes for supercapacitors[J]. Electrochemical and Solid-State Letters, 2001, 4(5): A62−A64.
[11] CHANG K, HU C, CHOU C. Textural and capacitive characteristics of hydrothermally derived RuO2·xH2O nanocrystallites: Independent control of crystal size and water content[J]. Chemistry of Materials, 2007, 19(8): 2112−2119.
[12] CHANG K, HU C. Coalescence inhibition of hydrous RuO2crystallites prepared by a hydrothermal method[J]. Applied Physics Letters, 2006, 88(19): 193102−193103.
[13] DMOWSKI W, EGAMI T, SWIDER-LYONS K E, et al. Local atomic structure and conduction mechanism of nanocrystalline hydrous RuO2from X-ray scattering[J]. The Journal of Physical Chemistry B, 2002, 106(49): 12677−12683.
[14] ZHENG J, CYGAN P, JOW T. Hydrous ruthenium oxide as an electrode material for electrochemical capacitors[J]. Journal of the Electrochemical Society, 1995, 142(8): 2699−2703.
[15] LUXTON T P, EICK M J, SCHECKEL K G. Characterization and dissolution properties of ruthenium oxides[J]. Journal of Colloid and Interface Science, 2011, 359(1): 30−39.
[16] KIM I H, KIM K B. Electrochemical characterization of hydrous ruthenium oxide thin-film electrodes for electrochemical capacitor applications[J]. Journal of the Electrochemical Society, 2006, 153(2): A383−A389.
[17] 王杰, 徐友龙, 马建华, 等. 循环伏安沉积纳米氧化钌基超级电容器电极材料[J]. 稀有金属材料与工程, 2012, 41(8): 1467− 1471. WANG Jie, XU Youlong, MA Jianhua, et al. Supercapacitor electrode materials of nanostructured hydrous ruthenium oxide deposited by cyclic voltammetry method[J]. Rare Metal Materials and Engineering, 2012, 41(8): 1467−1471.
[18] ZHENG J P. A new charge storage mechanism for electrochemical capacitors[J]. Journal of the Electrochemical Society, 1995, 142(1): L6.
[19] LYTLE J C, RHODES C P, LONG J W, et al. The importance of combining disorder with order for Li-ion insertion into cryogenically prepared nanoscopic ruthenia[J]. Journal of Materials Chemistry, 2007, 13(13): 1292−1299.
[20] SUGIMOTO W, IWATA H, YOKOSHIMA K, et al. Proton and electron conductivity in hydrous ruthenium oxides evaluated by electrochemical impedance spectroscopy: The origin of large capacitance[J]. The Journal of Physical Chemistry B, 2005, 109(15): 7330−7338.
[21] ZHANG S, XU K, JOW T. Electrochemical impedance study on the low temperature of Li-ion batteries[J]. Electrochimica Acta, 2004, 49(7): 1057−1061.
[22] ZHENG J P. Ruthenium oxide-carbon composite electrodes for electrochemical capacitors[J]. Electrochemical and Solid-State Letters, 1999, 2(8): 359−361.
(编辑 汤金芝)
Effect of calcination temperature on the microstructure and electrochemistry property of nano ruthenium oxides fabricted by chemical precipitation method
LENG Xian, YANG Hongzhi, ZOU Jianpeng, XIONG Xiang, HE Hanwei
(State Key Laboratory of Powder Metallurgy, Central South University, Changsha 410083, China)
Hydrous ruthenium oxide powder materials were prepared via a chemical precipilation method using RuCl3∙nH2O solution as precursor and NaOH solution as precipitant. The effect of calcination temperature on of morphology, phase structure and electrochemistry performance was investigated. The results indicate that the water content in hydrous ruthenium oxides decreases with the increase of the calcination temperature from 160 ℃ to 200 ℃, and ruthenium oxides transform from amorphous state to rutile nanocrystalline with gradual loss of structural water at 150−390 ℃. With the increase of calcination temperature from 160 ℃ to 200 ℃, the corresponding specific capacitance decreases from 862 F/g the to 592 F/g at the current density of 0.1 A/g, however, the capacitance retention ratio increases from 34.82% to 75.57% at the current density of 5 A/g (compared with the specific capacitance obtained at 0.1 A/g), and capacitance retention ratio increases from 88% to 97% after 200 charging-discharging cycles at 1 A/g. This means that samples annealed at higher temperature have better capacitive properties and rate performance, which would be a more suited choice applying in high power supply.
ruthenium oxides; pseudo capacitance; chemical precipitation method; nanomaterial; annealing temperature
TM53
A
1673-0224(2016)01−166−08
国家自然科学基金资助项目(51274248);国家国际科技合作专项项目(2013DFA31440)
2015−03−12;
2015−06−08
邹俭鹏,教授,博士。电话:0731-88830376;E-mail: zoujp@csu.edu.cn
