磷掺杂石墨烯的合成及其电催化氧还原性能研究
2016-02-13沈娟霞
沈娟霞,姚 真
(温州大学化学与材料工程学院碳材料技术研究重点实验室,浙江 温州 325027)
磷掺杂石墨烯的合成及其电催化氧还原性能研究
沈娟霞,姚 真
(温州大学化学与材料工程学院碳材料技术研究重点实验室,浙江 温州 325027)
以石墨烯和三苯基磷为原料,采用高温热退火法制备磷掺杂石墨烯。SEM、TEM和XPS测试证明磷成功掺杂到了石墨烯中。CV和LSV测试证实,制备的磷掺杂石墨烯氧还原电催化活性较掺杂前有明显提高。稳定性测试表明,磷掺杂石墨烯比商化的铂催化剂稳定性更好。
石墨烯;三苯基膦;氧还原;电催化
随着工业生产规模化的加大,能源匮乏和环境污染的问题也越来越严重,寻求一些绿色的能源替代传统的石油、化石燃料已经迫在眉睫。燃料电池作为一种将化学能直接转化为电能的装置,具有对环境无污染、能量转换率高、不受卡诺循环的限制等优点,成为解决目前的能源和环境问题的一种理想的替代能源。
目前,成本高和寿命短是制约燃料电池发展的两大突出问题,而导致这两大问题的关键因素之一在于电催化剂。众所周知,Pt催化剂因其在燃料电池阴极电催化中表现出极好的催化性能,被广泛应用于燃料电池阴极催化剂中。但Pt价格比较昂贵,资源稀缺,稳定性比较差,因此寻找一种具有高活性和高稳定性的非贵金属催化剂来取代铂基催化剂,成为近年来研究的热点。据文献报道,杂原子掺杂的碳纳米材料表现出杰出的氧还原性能,并且价格相对于铂来说要廉价得多[1-5]。硼掺杂的碳纳米管材料也表现出明显的催化活性[6],随后又有研究揭示硫或碘掺杂能提高石墨烯的电催化性能[7-8]。大量的实验结果表明,通过掺杂改变石墨或者碳纳米管的表面电子结构,对提高材料的氧还原电催化性能可能是一个切实可行的办法[9-11]。
最近的研究证实,氮掺杂碳材料,如碳纳米管、石墨烯,有望取代铂基催化剂作为燃料电池的催化剂,因为它们在碱性介质中不仅表现出较高的催化活性、长期稳定性和优良的耐甲醇性能,而且还具有成本低、对环境友好等优点。磷与氮元素同族,有相同的价电子数,与氮的化学性质相似,也可以作为给电子基团掺杂到碳框架结构中。磷掺杂碳材料如磷掺杂碳纳米管[12]已经有报道。Liu等用高温裂解甲苯和三苯基磷的方法制备了磷掺杂石墨片,并研究了催化剂的电化学性能,发现其在碱性介质中可以表现出良好的催化活性、长期稳定性和较高的耐甲醇抗毒性。
石墨烯因其良好的电子传导性、巨大的比表面积和电化学稳定性,在电化学传感[13-16]、电池[17-18]、催化剂等多方面都有广阔的应用前景。目前,关于磷掺杂石墨烯的报道还很少。本文我们介绍一种简单、易操作的方法来制备磷掺杂的石墨烯。SEM、TEM和XPS测试证明,磷成功掺杂到石墨烯中。相应的电化学测试表明,与商业化的铂催化剂相比,磷掺杂石墨烯表现出更好的催化活性和长期的稳定性。
1 实验部分
1.1 磷掺杂石墨烯的制备
分别称取相同质量的石墨烯和三苯基磷,加入4mL的无水乙醇,放在超声波清洗仪中超声直至完全溶解。之后将所得的溶液取出放在烘箱中烘干待用。
将烘干后所得的产物收集转移至石英舟中,然后放在石英管内,通氩气保护。随后在管式炉中设定所需的温度,盖上管式炉的盖子,升温,保持30min;最后打开管式炉的盖子,常温冷却,在整个过程中始终保持管内的惰性气体氩气保护气氛。
1.2 磷掺杂石墨烯的结构表征
1.2.1 扫描电镜( SEM)
将粉末样品涂于碳导电胶后,在JSM-6700F电场发射扫描电镜(电压15kV,电子数3.0)下观察样品的表面形貌。
1.2.2 透射电镜(TEM)
采用JEOL-3010透射电子显微镜和高分辨透射电子显微镜,将适量的粉末材料溶于乙醇中,超声分散后,将其滴于铜网上,干燥后用透射电镜(加速电压为200 kV)观察其样品内部结构。
1.2.3 X射线光电子能谱( XPS)
X射线光电子能谱采用了超高真空装置,配有单色铝钾Kα的X射线源和一个高分辨率的Gammadata-Scienta SES 2002分析仪,对实验样品的元素组分结构进行分析。
1.3 磷掺杂石墨烯的电化学性能测试
1.3.1 工作电极的制备
首先将玻碳电极分别用1.0μm和0.05μm的氧化铝超细粉研磨抛光,然后在无水乙醇和超纯水中分别超声,洗净后的玻碳电极再在氮气下吹干,备用。之后称取2mg样品加入无水乙醇溶液,超声直至完全溶解,取等量的溶液滴于玻碳电极上,室温下晾干,使之形成厚薄均匀的催化剂薄层。再移取少量萘酚溶液涂于玻碳电极表面,室温下晾干,即为工作电极。
1.3.2 电化学性能测试
使用CHI760D型电化学工作站和ATA-1B型旋转圆盘电极系统,对所得实验样品采用循环伏安(CV)、计时电流法(IT)和旋转圆盘(RDE)电极进行测试。测试使用的三电极体系中,玻碳电极为工作电极、铂丝电极为对电极、Ag/AgCl电极为参比电极。测试体系中的电解液为0.1mol·L-1KOH溶液,每次测试前通高纯氧,使电解液处于氧饱和状态。
2 实验结果与讨论
2.1 磷掺杂石墨烯的电镜表征
图1(a)、(b)分别是磷掺杂石墨烯的扫描电镜图和透射电镜图。由图1可以看出,得到的样品是透明的薄层结构,这是典型的石墨烯结构,说明磷掺杂后并没有破坏石墨烯的结构。

图1 磷掺杂石墨烯的扫描电镜图(a),透射电镜图(b)
2.2 X射线光电子能谱测试(XPS)
X射线光电子能谱测试可用于测定我们制备的磷掺杂石墨烯材料中的元素构成,判断磷是否成功引入到石墨烯中。
图2给出了1000℃处理的纯石墨烯和磷掺杂石墨烯的X射线光电子能谱图。通过对比我们发现,1000℃处理的纯石墨烯的全谱图中只存在C1s和O1s的峰,而1000℃处理的磷掺杂石墨烯的全谱中除了有C1s和O1s的峰,还出现了新的P2p峰,这恰恰证明了磷元素的存在,表明磷成功引入到石墨烯中,也初步证实我们制备的是磷掺杂石墨烯。
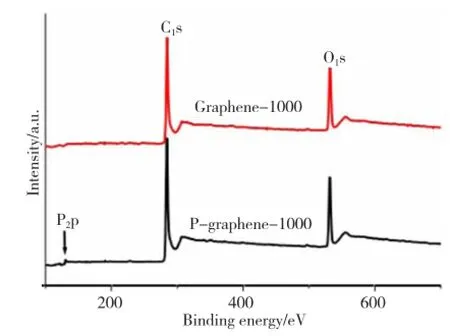
图2 1000℃处理后的纯石墨烯和磷掺杂石墨烯的XPS全谱图
2.3 循环伏安测试
循环伏安测试是一种常用的电化学测量技术,能迅速观察到所研究体系在广泛电势范围内的氧化还原行为,也能提供电子转移动力学和热力学的大量信息。曲线上的峰电位和峰电流能够反映催化剂样品的氧还原催化活性。通常来说,峰电流越大,峰电位越正,催化剂的氧还原电催化活性越高。
磷掺杂石墨烯和纯石墨烯都是在通氩气、1000℃退火后得到的。如图3所示,对比通氮和通氧条件下的曲线,可以看到,在通氧条件下有个明显的氧还原峰;对比图3(a)和图3(b)可知,1000℃处理的磷掺杂石墨烯对氧气的催化峰电流(231μA)大于1000℃处理的纯石墨烯的峰电流(113μA),峰电位(-0.28V)较纯石墨烯的峰电位(-0.34V)向正方向移动,这表明我们制备的磷掺杂石墨烯与纯石墨烯相比,具有更好的氧还原电催化活性。对比图3(a)和图3(c)可知,磷掺杂石墨烯比商业化的铂催化剂的氧还原电催化性能更好。
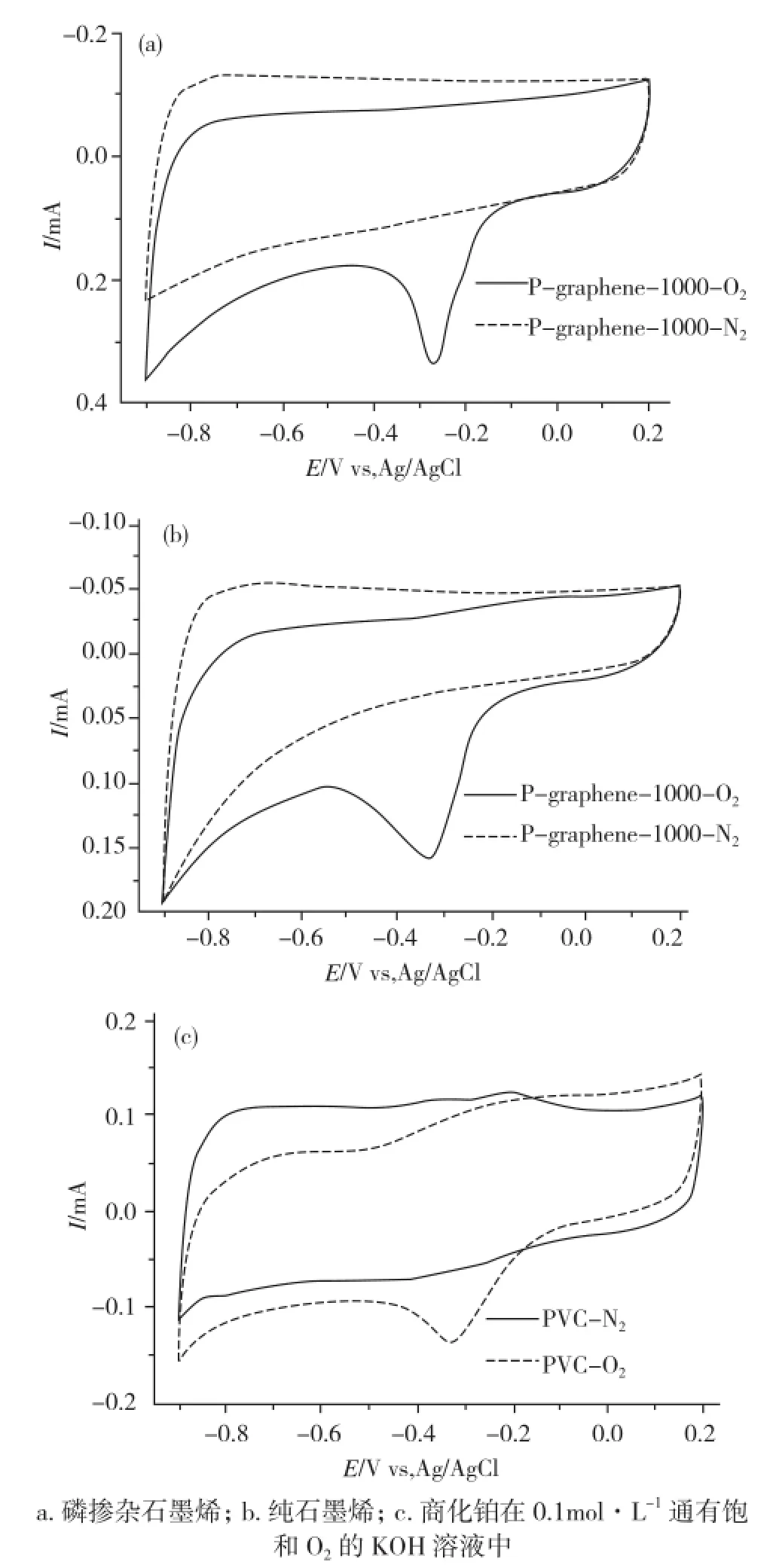
图3 循环伏安曲线
2.4 热处理温度对催化剂电化学活性的影响
图4给出了相同处理条件下,不同温度处理的磷掺杂石墨烯的循环伏安曲线。我们通过比较氧还原峰电位(电流最大的位置)的正负和峰电流的大小来描述催化剂性能的优劣。由图4可知,随着退火温度的升高,峰电流变大,峰电位越正。1000℃处理的磷掺杂石墨烯对氧气的催化峰电流最高,峰电位最正,氧还原电催化性能最高。因此,热处理退火温度明显影响磷掺杂石墨烯的电催化活性。磷掺杂石墨烯的氧还原电催化活性提高可能是因为石墨烯在高温条件下的自我修复使得其导电性更好。
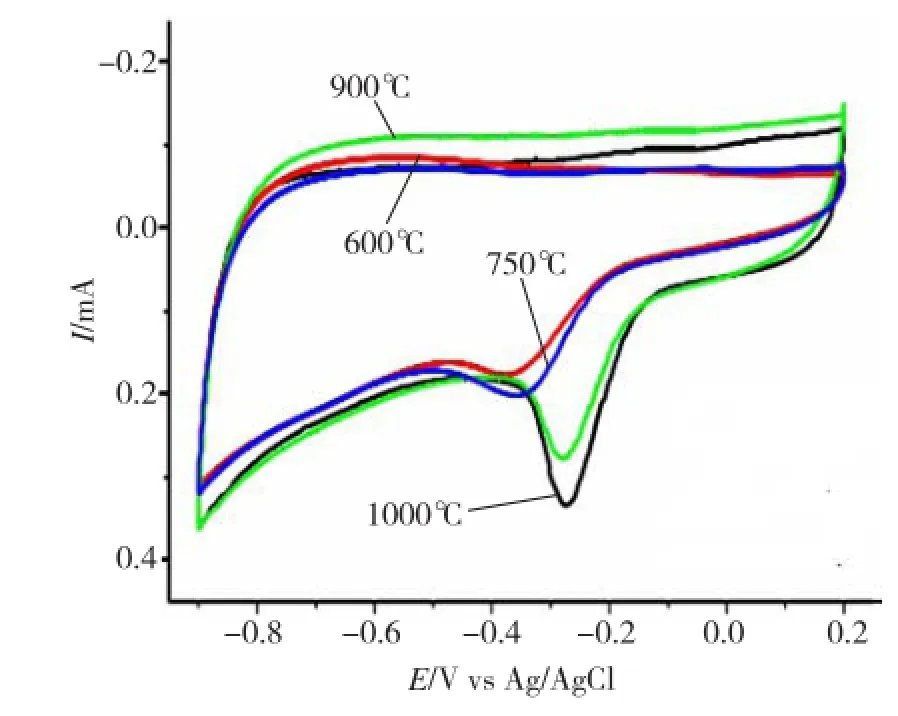
图4 相同处理条件下,不同退火温度得到的磷掺杂石墨烯在0.1mol·L-1通有饱和氧气的KOH溶液中的循环伏安曲线
2.5 线性扫描伏安测试
在实际的燃料电池应用中,充分且快速的氧传质是必要的,而在循环伏安测试中工作电极是静态的,氧气的扩散是缓慢的,而且氧气的扩散对氧还原反应有很大的影响。线性扫描伏安测试(LSV)提供了一种有效的方法来研究氧还原过程,因为工作电极高速旋转,氧气的扩散是充分的。利用线性扫描伏安测试对制备的磷掺杂石墨烯的催化机理作进一步研究,可得到不同转速下磷掺杂石墨烯的极化曲线。为此,我们对1000℃处理的磷掺杂石墨烯进行线性扫描伏安测试,研究它在不同转速下的线性扫描伏安曲线。
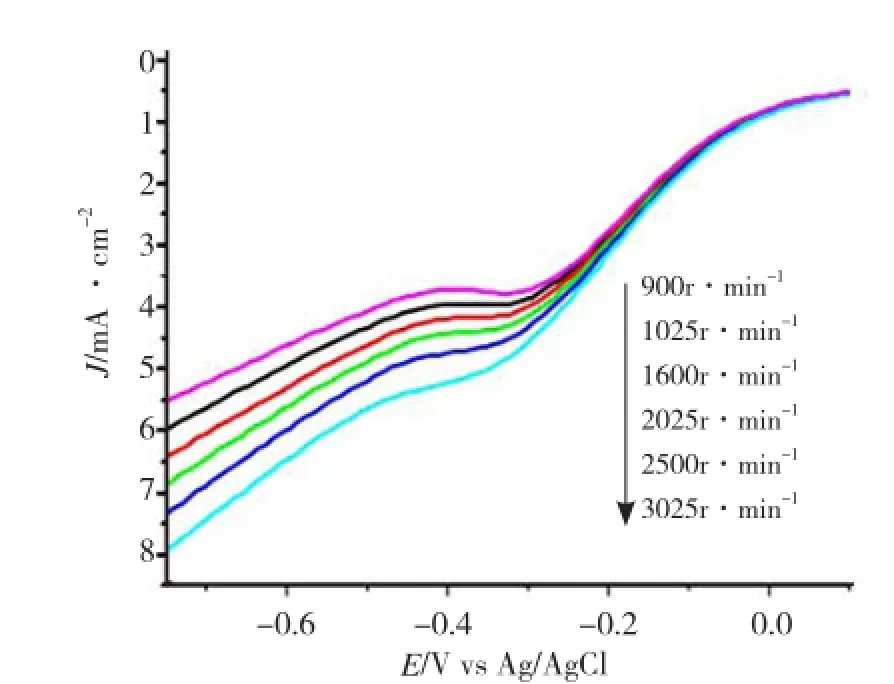
图5 1000℃处理的磷掺杂石墨烯在0.1mol·L-1KOH溶液中的线性扫描伏安曲线
由图5可以看出,随着圆盘电极的转速提高,盘上的还原电流增大,这是由于旋转提高了盘电极获得氧的能力。当电极转速较低时,随着电极电位的负移,伏安曲线呈现极限电流的特征,说明在此条件下氧还原过程受溶液中反应物扩散的控制;当电极转速较大时,伏安曲线的极限电流特征变化不明显,表明此过程受动力学控制。
2.6 磷掺杂石墨烯的稳定性测试
为了研究制备的石墨烯的催化活性的稳定性,我们采用计时电流法对其稳定性进行测试。图7为1000℃处理的磷掺杂石墨烯在0.1mol·L-1KOH溶液中的时间-电流曲线,定电位-0.45 V。从图7可以看出,在最初接通电流的时期内,催化剂出现了电流下降的现象,但是其在长时间(10000s)稳定放电时,电流基本保持不变,表明此催化剂具有较强的稳定性。
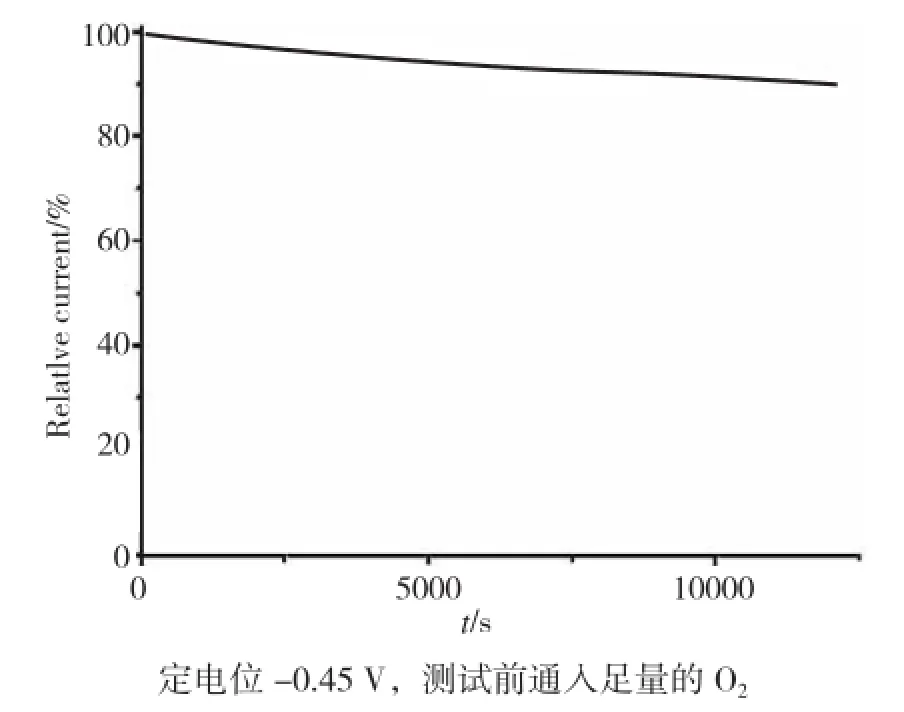
图7 1000℃处理的磷掺杂石墨烯在在0.1mol·L-1的KOH溶液中的计时-电流曲线
3 结论
采用高温热退火氧化石墨烯和三苯基磷的方法制备了磷掺杂石墨烯。SEM、TEM和 XPS 等测试证明,磷成功地掺杂到了石墨烯中。氧还原电化学性能测试证实,制备的磷掺杂石墨烯比掺杂前有明显的提高,且比商化铂催化剂更加优异。通过优化反应条件,1000℃退火温度下得到的磷掺杂石墨烯具有最高的氧还原电化学活性,氧还原峰电流达到231μA。稳定性测试表明,磷掺杂石墨烯比商化的铂催化剂稳定性更好。本实验的结果为获得理想的非金属催化剂开辟一条新的有效途径,对于燃料电池的应用研究具有重要的实际意义和研究价值。
[1] Gong K., Du F., Xia Z., Durstock M., Dai L. Nitrogen-doped carbon nanotube arrays with high electrocatalytic activity for oxygen reduction[J]. Science, 2009, 323(5915): 760-764.
[2] Qu L., Liu Y., Baek J., Dai L. Nitrogen-doped graphene as efficient metal-free electrocatalyst for oxygen reduction in fuel cells[J]. ACS Nano., 2010(3): 1321-1326.
[3] Liu R., Wu D., Feng X., Müllen K. Nitrogen-doped ordered mesoporous graphitic arrays with high electrocatalytic activity for oxygen reduction[J]. Angewandte Chemie International Edition, 2010, 122(14): 2619-2623.
[4] Sun Y., Li C., Xu Y., Bai H., Yao Z., Shi G. Chemically converted graphene as substrate for immobilizing and enhancing the activity of a polymeric catalyst[J]. Chemical Communications, 2010, 46(26): 4740-4742.
[5] Sun Y., Li C., Shi G. Nanoporous nitrogen doped carbon modified graphene as electrocatalyst for oxygen reduction reaction[J]. Journal of Materials Chemistry, 2012, 22(25): 12810-12816.
[6] Yang L., Jiang S., Zhao Y., Zhu L., Chen S., Wang X.,et al. Boron-doped carbon nanotubes as metal-free electrocatalysts for the oxygen reduction reaction[J]. Angewandte Chemie International Edition, 2011, 123(31): 7270-7273.
[7] Yang Z., Yao Z., Li G., Fang G., Nie H., Liu Z., et al. Sulfurdoped graphene as an efficient metal-free cathode catalyst for oxygen reduction[J]. ACS Nano, 2011, 6(1): 205-211.
[8] Yao Z., Nie H., Yang Z., Zhou X., Liu Z., Huang S. Catalystfree synthesis of iodine-doped graphene via a facile thermal annealing process and its use for electrocatalytic oxygen reduction in an alkaline medium[J]. Chemical Communications, 2012, 48(7): 1027-1029.
[9] Liu H., Liu Y., Zhu D. Chemical doping of graphene[J]. Journal of Materials Chemistry, 2011, 21(10): 3335-3345.
[10] Ni S., Li Z., Yang J. Oxygen molecule dissociation on carbon nanostructures with different types of nitrogen doping[J]. Nanoscale, 2012(4): 1184-1189.
[11] Boukhvalov D. W., Son Y. W. Oxygen reduction reactions on pure and nitrogen-doped graphene: a first-principles modeling[J]. Nanoscale, 2012(2): 417-420.
[12] Liu Z.W., Peng F., Wang H. J., Yu H., Zhu L. L. Novel phosphorus-doped multiwalled nanotubes with high electrocatalytic activity for O2reduction in alkalinemedium[J]. Catalysis Communications, 2011, 16(1): 35-38.
[13] Matter P. H., Zhang L., Ozkan U. S. The role of nanostructure in nitrogen-containing carbon catalysts for the oxygen reduction reaction[J]. Journal of Catalysis, 2006,239(1): 83-96.
[14] Matter P. H., Wang E., Arias M., Biddinger E. J., Ozkan U. S. Oxygen reduction reaction catalysts prepared from acetonitrile pyrolysis over alumina-supported metal particles[J]. Journal of Physical Chemistry B, 2006,110(37): 18374-18384.
[15] Patil A. J., Vickery J. L., Scott T. B., Mann S. Aqueous stabilization and self-assembly of graphene sheets into layered bio-nanocomposites using DNA[J]. Advance Materials 2009, 21(31): 3159-3164.
[16] Lu C. H., Yang H. H., Zhu C. L., Chen X., Chen G. N. A graphene platform for sensing biomolecules[J]. Angewandte Chemie International Edition, 2009, 48(26): 4785-4787.
[17] Wu Z. S., Ren W. C., Xu L., Li F., Cheng H. M. Doped graphene sheets as anode materials with superhigh rate and large capacity for lithium ion batteries[J]. ACS Nano, 2011,5(7): 5463-5471.
[18] Paek S. M., Yoo E. J., Honma I. Enhanced cyclic performance and lithium storage capacity of SnO2/graphene nanoporous electrodes with three-dimensionally delaminated flexible structure[J]. Nano Letters, 2009, 9(1): 72-75.
Catalyst-free Synthesis of Phosphorus-doped Graphene and its Use for Electrocatalytic Oxygen Reduction
SHEN Juan-xia, YAO Zhen
(Institute of Chemical and Materials Engineering, Nanomaterials & Chemistry Key Laboratory, Wenzhou University, Wenzhou 325027, China. )
Phosphorus-doped graphene was successfully fabricated through a facile thermal annealing process. The structure of the phosphorus-graphene was characterized by SEM, TEM and XPS. The electro-catalytic performances showed that the phosphorusgraphene could exhibit better catalytic activity than a commercial Pt/C catalyst. In addition, the new metal-free catalyst could exhibit long-term stability for the oxygen reduction reaction.
grapheme; phosphorustriphenyl; oxygen reduction reaction; electrocatalysis
O 643.3
A
1671-9905(2016)05-0005-05
2016-03-10
