含靶向性双膦酸基团的乙二胺衍生物的合成及细胞毒活性
2016-02-10孙艳艳吴希雯
孙艳艳,吴希雯,陈 蕾,严 生
(苏州科技大学化学生物与材料工程学院,江苏苏州 215009)
含靶向性双膦酸基团的乙二胺衍生物的合成及细胞毒活性
孙艳艳*,吴希雯,陈 蕾,严 生
(苏州科技大学化学生物与材料工程学院,江苏苏州 215009)
设计并合成一类含靶向性双膦酸基团的N,N’-二乙基乙二胺衍生物,通过元素分析、核磁氢谱、碳谱、磷谱、高分辨质谱对所有化合物进行结构表征,并利用CCK-8试剂盒检测化合物对卵巢癌SKOV3及骨肉瘤MG-63细胞系72h的体外抑制活性,并通过SPSS软件计算IC50值,寻找潜在抗肿瘤先导化合物。
双膦酸;乙二胺;合成;细胞毒活性
双磷酸盐(Bisphosphonates,BPs)是一种人工合成的焦磷酸类似物,BPs结构中的P—C—P键代替焦磷酸中的P—O—P,在生物体内有一定的稳定性,能抑制生物体内焦磷酸酯酶的降解作用,且与骨组织羟基磷灰石表现特殊亲合力,具有骨靶向性[1]。双磷酸盐在抑制骨吸收方面效果显著,用于治疗许多骨相关疾病,包括高血钙症、骨髓瘤、变形性骨炎和骨质疏松等[2]。此外,据报道BPs还有直接或间接的抗肿瘤活性,对乳腺癌、肺癌和骨肉瘤等有较高的抑制活性[3]。双膦酸类药物迄今已经历三代的发展,包括第一代的氯屈膦酸和依替膦酸(不含氮),第二代的帕米膦酸和阿仑膦酸(含氨烷基),和第三代的唑来膦酸和米诺膦酸(含氮杂环),其中唑来膦酸是治疗效果最好的双膦酸类药物,具有高度的骨亲合力及抑制骨吸收活性[4-5]。国内外研究者对双膦酸类药物的结构修饰和筛选取得很大进展,尤其是针对含氨基双膦酸类药物的研究[6-7]。本文设计并合成一类含靶向性双膦酸取代基的N,N’-二乙基乙二胺衍生物,通过核磁、元素分析及高分辨质谱等对化合物进行结构确证,并研究其对卵巢癌及骨肉瘤细胞系的细胞毒活性,这种N,N’-二双膦酸取代的衍生物目前尚未见报道。
1 实验部分
1.1 材料与仪器
实验用化学试剂均为分析纯,购于国药集团。细胞株培养基均用RPMI-1640。CCK-8试剂盒购于碧云天。核磁共振仪(Bruker Avance III HD 400 MHz),元素分析仪Vario EL(Elementar),液质联用仪(Agilent 6230 Accurate-Mass TOF LC/ MS)。
1.2 化合物的制备
化合物的合成路线如图1所示。M1的制备参考文献报道[8]。0.25mol的M1溶解在1.5mol的85%亚磷酸和120mL氯苯中,加热至100℃,逐滴滴加1mol三氯化磷,搅拌40min,反应剧烈并产生大量黄色固体,继续反应3h,弃掉上清液氯苯,残留液减压蒸馏蒸去溶剂,再加入250mL水,加热回流20 min,再加入少量活性炭回流搅拌15min,过滤,滤液减压浓缩,冷却析出得到粗产物,过滤干燥,用水-丙酮重结晶得到浅黄色固体,即化合物1。化合物2-3的合成路线参考化合物1。数据如下:
化合物1:浅黄色固体(产率35%)。1H NMR(d6-DMSO):δ 0.90~0.98(t,6H,CH3),1.44~1.52(m,4H,CH2),2.60~2.84(m,6H,NCH and NCH2),6.10~6.18(m,2H,NH),6.60(s,2H,COH),11.90(s,8H,POH)×10-6;13C NMR(d6-DMSO):δ(10.3,22.8,37.5,54.2,99.5)×10-6;31P NMR(d6-DMSO):17.20×10-6;HRMS:m/z[M-H]-calcd.for C10H27N2O14P4:523.041 27,found:523.041 78;Anal.calcd for C10H28N2O14P4:C 22.91,H 5.38,N 5.34,found:C 22.96,H 5.32,N 5.38。
化合物2:浅黄色固体(产率42%)。1H NMR(d6-DMSO):δ 0.92~1.01(t,6H,CH3),1.48~1.60(m,8H,CH2),2.58~2.85(m,6H,NCH and NCH2),6.15~6.24(m,2H,NH),6.55(s,2H,COH),11.85(s,8H,POH)×10-6;13C NMR(d6-DMSO):δ(10.5,14.0,23.8,40.2,56.6,98.5)×10-6;31P NMR(d6-DMSO):17.22×10-6;HRMS:m/z[M-H]-calcd.for C12H31N2O14P4:551.072 57,found:551.072 79;Anal.calcd for C12H32N2O14P4:C 26.10,H 5.84,N 5.07,found:C 26.05,H 5.88,N 5.01。
化合物3:浅黄色固体(产率45%)。1H NMR(d6-DMSO):δ 0.95~1.04(t,6H,CH3),1.41~1.53(m,12H,CH2),2.53~2.80(m,6H,NCH and NCH2),6.12~6.20(m,2H,NH),6.58(s,2H,COH),11.92(s,8H,POH)×10-6;13C NMR(d6-DMSO):δ(9.2,10.8,23.0,25.7,42.0,57.5,97.9)×10-6;31P NMR(d6-DMSO):17.24 ppm;HRMS:m/z[M-H]-calcd.for C14H35N2O14P4:579.103 87,found:579.103 25;Anal.calcd for C14H36N2O14P4:C 28.97,H 6.25,N 4.83,found:C 28.93,H 6.29,N 4.80。
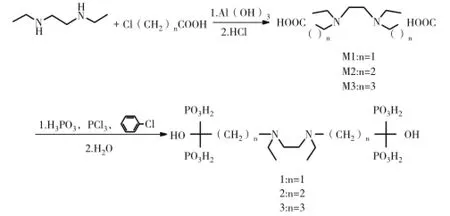
图1 化合物1-3的合成
1.3 生物活性测试
以唑来膦酸为阳性对照,利用CCK-8法检测化合物对卵巢癌和骨肉瘤细胞系的细胞毒活性,实验步骤参考文献[9],取对数生长期的肿瘤细胞计数,培养基稀释后接种于96孔培养板内,每孔100μL细胞液,浓度约为3×104个/mL。过夜培养(5%CO2,37℃),待细胞贴壁后进行给药,分别设给药组,阳性对照组和阴性对照组。待测化合物用超纯水溶解,临用前用细胞培养基稀释成7个浓度梯度。加药后培养72h,加10 μL的CCK-8溶液(5 mg/mL),37℃孵育4h。用酶标仪在450nm波长下测定每孔OD值,并计算抑制率,通过SPSS软件计算IC50值(半数抑制浓度)。
2 结果与讨论
以N,N’-二乙基乙二胺与氯乙酸为原料,氢氧化铝为缚酸剂制备中间体M1,再与亚磷酸和三氯化磷进行磷酸化反应得到化合物1,其他化合物的制备参考化合物1的制备方法,如图1所示。所有化合物均通过核磁共振氢谱、碳谱、磷谱、元素分析及高分辨质谱进行表征,结构与谱图数据一致。
通过CCK-8细胞毒活性测试试剂盒,检测化合物1-3与阳性对照唑来膦酸对卵巢癌SKOV3及骨肉瘤MG-63细胞株的体外细胞毒活性,结果如表1所示。从表1数据可知,化合物1-3对SKOV3的IC50值大于100μM,唑来膦酸的IC50值为28.3μM,表明化合物1-3对SKOV3的细胞毒活性低于阳性对照唑来膦酸;化合物1和2对MG-63的IC50值分别为48.7 μM和53.5μM,唑来膦酸的IC50值为17.5μM,说明1和2对MG-63的细胞毒活性高于化合物3,但低于阳性对照唑来膦酸。整体而言,化合物1和2对MG-63的细胞毒活性比SKOV3较高,但均低于阳性对照。
3 结论
本文设计并合成了一类含双膦酸基团的N,N’-二乙基乙二胺衍生物,并研究其对卵巢癌及骨肉瘤细胞系的体外抑制活性。通过实验结果可知,化合物1-2对骨肉瘤MG-63的细胞毒活性比卵巢癌SKOV3较高,但低于阳性对照唑来膦酸。实验结果为后续双膦酸化合物的结构改造提供依据。
Synthesis and Cytotoxicity of Ethylenediamine Derivatives with Bone-targeting Bisphosphonate Groups
Sun Yan-yan,Wu Xi-wen,Chen Lei,Yan Sheng
A novel series of N,N’-diethylethylenediamine derivatives containing N,N’-dibisphosphonate substituents have been synthesized and characterized by elemental analysis,1H NMR,13C NMR,31P NMR and HRMS spectra.The in vitro cytotoxicities of all compounds were tested with CCK-8 by WST-8 assay against SKOV3 and MG-63 cell lines after 72 h incubation and the IC50 values were obtained by SPSS software.
bisphosphonate;ethylenediamine;synthesis;cytotoxicity
R914
B
1003–6490(2016)10–0101–02
2016–09–15
国家自然科学基金青年项目(21401137),苏州市“高等院校、科研院所紧缺高层次人才”引进资助项目,江苏省大学生创新创业训练计划项目(201510332057X)。
孙艳艳(1985—),女,河南武陟人,讲师,主要研究方向为药物化学。
