HPLC法测定肝龙胶囊中肌苷的含量
2016-02-08李宇驰杨永寿肖培云
李宇驰,徐 妍,杨永寿,肖培云*
(1.大理大学药学与化学学院,云南大理 671000;2.云南省昆虫医药研发重点实验室,云南大理 671000)
HPLC法测定肝龙胶囊中肌苷的含量
李宇驰1,徐 妍1,杨永寿2,肖培云1*
(1.大理大学药学与化学学院,云南大理 671000;2.云南省昆虫医药研发重点实验室,云南大理 671000)
目的:建立肝龙胶囊中肌苷的含量测定方法,为肝龙胶囊的质量控制提供依据。方法:采用Gemini 5u C18110A(250 mm× 4.6 mm)色谱柱,流动相水(含0.05%TFA):乙腈(含0.05%TFA),采用梯度洗脱方式,流速0.8 mL∕min,柱温30℃,DAD检测器,检测波长为214 nm,进样量10 μL。结果:肌苷在0.202~2.020 μg范围之间峰面积值与进样量(μg)线性关系良好,平均回收率(n=9)为96.9%,RSD为2.18%。结论:建立的肝龙胶囊中肌苷含量测定方法科学、简便、结果准确,可作为提高肝龙胶囊质量标准的检测项目。
肝龙胶囊;肌苷;含量测定
肝龙胶囊是由药用昆虫美洲大蠊(Periplaneta americana)的干燥虫体经提取得到的活性部位研制而成,是治疗病毒性乙型肝炎和肝纤维化作用的中药二类新药,标准编号为YBZ04142005-2011Z,具有疏肝理脾,活血解毒的功效,并具有抗肝损伤作用〔1〕。该药具有疗效好,价格低,给药方便等优点。研究表明,肝龙胶囊不仅对防治乙肝病毒有较好的疗效,还具有抗病毒、抗氧化、防治慢性酒精性肝损伤,提高机体免疫功能等作用〔2-8〕。由于肝龙胶囊的质量控制方面的研究较少,目前质量标准中的含量测定项以总氨基酸为测定指标,缺乏专属性。研究表明,肌苷是肝龙胶囊活性部位中的已知成分〔9〕,为进一步提高肝龙胶囊质量标准的可控性,本文采用高效液相法对肝龙胶囊中肌苷的含量测定方法进行研究。
1 仪器与材料
1.1仪器1100型高效液相色谱仪(包括G1311A四元泵、G1313A自动进样器、G1316A柱温箱、G1315B DAD检测器,美国安捷伦公司);超声波清洗器(SK3200LH型,上海科导超声仪器有限公司);分析天平(AL240-IC型,梅特勒-托利多仪器有限公司)。
1.2材料肝龙胶囊(昆明赛诺制药公司,批号:15122002、15101201、15091701、15082002、15062401、 15042202);肌苷(中国食品药品检定研究院,批号:140669-201305,Mr=268);乙腈为色谱纯,水为超纯水,其余试剂均为分析纯。
2 实验方法与结果
2.1色谱条件以及肌苷峰的确定采用Gemini 5u C18110A(250 mm×4.6 mm)色谱柱,流动相水(含0.05%三氟乙酸,以下简称含0.05%TFA):乙腈(含0.05%TFA),采用梯度洗脱方式,流速0.8 mL∕min,柱温30℃,DAD检测器,检测波长为214 nm,进样量10 μL,按表1中的梯度洗脱程序进行洗脱,色谱图见图1,可知供试品的S峰与肌苷保留时间一致,并利用DAD检测器对其图谱进行二维检测,光谱图见图2,结果显示,供试品的S峰与肌苷峰的紫外吸收图谱相同,进一步确定S峰即为肌苷峰。
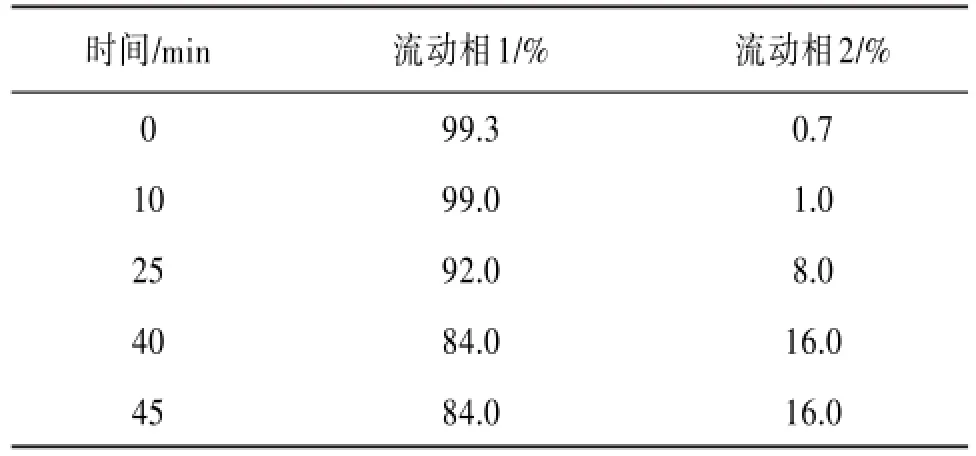
表1 梯度洗脱条件

图1 肌苷色谱图

图2 对照品与供试品中肌苷峰扫描图
2.2溶液的制备
2.2.1 对照品溶液制备 精密称取肌苷对照品适量,加蒸馏水制成每1 mL含0.202 mg的溶液,混匀,即得。
2.2.2 供试品溶液制备 取同一批次的胶囊20粒,倾出内容物,计算平均粒重,充分研细,混匀。精密称取研细后的内容物约70 mg于10 mL量瓶中,加适量蒸馏水超声15 min溶解,定容至刻度,混匀,过滤。取续滤液适量,用0.22 μm微孔滤膜过滤,备用。
2.3线性关系精密吸取对照品溶液1、2、4、6、8、10 μL注入色谱仪,按“2.1”色谱条件测定。以进样量(μg)为横坐标,峰面积为纵坐标,绘制标准曲线。得线性方程为Y=2 050.7X-298.63,r=0.999 5,结果表明肌苷在0.202~2.020 μg范围内峰面积值与进样量(μg)呈良好的线性关系。
2.4精密度实验取“15062401”批次的肝龙胶囊按“2.2.2”项制备供试品溶液,精密吸取10 μL注入高效液相色谱仪,连续进样6次,以肌苷峰面积进行计算,RSD为0.24%,结果表明仪器的精密度良好。
2.5重复性实验取“15062401”批次的肝龙胶囊,按“2.2.2”项制备6份供试液,精密吸取各供试液10 μL注入高效液相色谱仪进行测定,以肌苷峰面积计算,RSD为0.56%,经计算得样品含量为14.07 mg∕g,结果表明方法重复性良好。
2.6稳定性实验取“15062401”批次的肝龙胶囊制备的供试品溶液,分别于0、2、4、6、8、10、12 h进样10 μL,肌苷峰面积的RSD值为0.89%,表明供试品溶液中肌苷在室温下放置12 h稳定。
2.7加样回收率实验精密称取“15062401”批次样品适量于5 mL量瓶中,平行称取9份,根据样品中所含肌苷的平均含量(14.07 mg∕g),按含量的高、中、低加入对照品,依“2.2.2”项制备供试液,按“2.1”项色谱条件进样测定。见表2。

表2 加样回收率试验(n=9)
2.8样品含量测定取不同批次的样品,按“2.2.1”项制备供试液,按“2.1”项色谱条件进样测定。见表3。
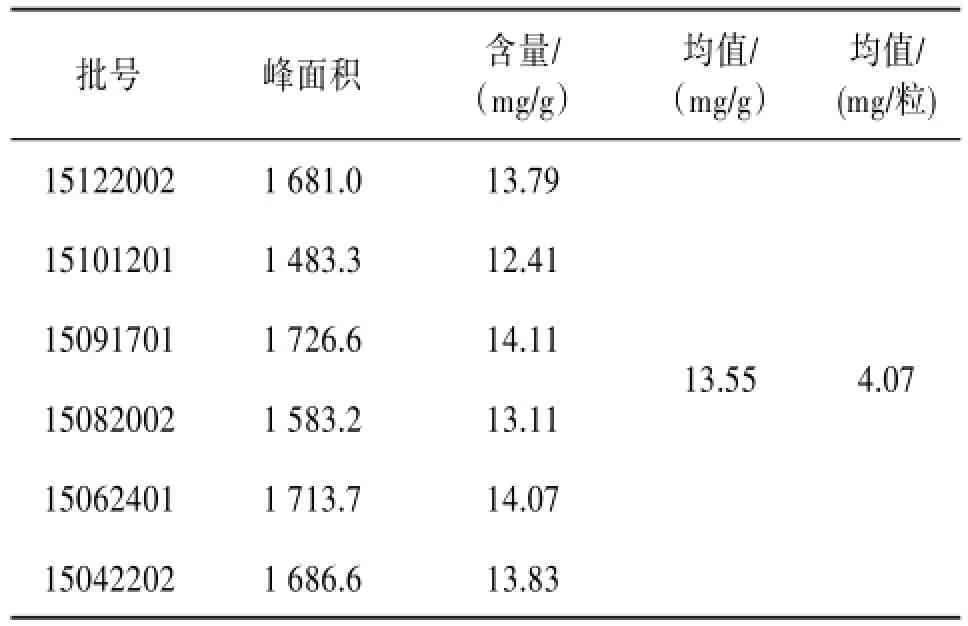
表3 样品含量测定结果(n=3)
3 讨论
实验考察了phenomenex Gemini 5u C18110A(4.60mm×250mm)、AglientZORBAXSB-C18(4.60mm× 250 mm,5 μm)及Waters Symmetry ShieldTMRP18(4.60 mm×250 mm,5 μm)的C18色谱柱,结果表明,采用phenomenex Gemini 5u C18110A(4.60 mm×250 mm)色谱柱时,色谱峰分离效果最好,且基线平稳。在流动相选择时,分别考察了乙腈(0.05%TFA)-水(0.05%TFA)、乙腈-水(0.05%TFA)、乙腈-水3种洗脱体系对样品分离的影响,结果表明,采用乙腈(0.05%TFA)-水(0.05%TFA)为流动相时,色谱峰分离度和对称性良好。实验采用DAD检测器对检测波长进行筛选,发现在214 nm波长下色谱图的基线平稳,且相邻色谱峰无干扰,故选择214 nm作为检测波长。同时,在确定上述条件的基础上,分别对流速(0.7、0.8、0.9 mL∕min)和温度(25、30、35℃)进行了考察。结果表明,样品在柱温为30℃、流速在0.8 mL∕min时分离效果最好,且基线漂移较小。
本研究建立了肝龙胶囊中肌苷含量的测定方法,并测定了6批肝龙胶囊中肌苷含量,该方法回收率高、精密性良好、方便快捷。可为完善肝龙胶囊质量标准检查提供参考。
〔1〕夏盟恺,曾菁,牛春丽,等.肝龙胶囊和美洲大蠊脱脂膏对正常大鼠胆汁分泌的影响〔J〕.大理学院学报,2015,14(2):4-7.
〔2〕杜一民,李树楠,陈鸿珊,等.新药肝龙胶囊对雏鸭体内鸭乙型肝炎病毒的抑制效果〔J〕.大理学院学报,2006,5(4):6-8.
〔3〕张旭强,吴红兵,彭丽,等.肝龙胶囊对大鼠慢性酒精性肝损伤的防治作用研究〔J〕.中国中药杂志,2013,38(13):2197-2201.
〔4〕杜一民,陈鸿珊,李树楠,等.治疗乙型肝炎新药肝龙胶囊的药效学初步研究〔J〕.时珍国医国药,2006,17(8):1369-1371.
〔5〕杨永荣,缪新权,梅光涛,等.肝龙胶囊治疗HBeAg阳性慢性乙型肝炎的疗效观察〔J〕.云南医药,2008,29(2):182-183.
〔6〕张成桂,焦春香,何正春,等.肝龙不同有效部位体外抗氧化活性的分析〔J〕.时珍国医国药,2011,22(1):69-71.
〔7〕桂罗兰,单华,史彩艳,等.肝龙胶囊对小鼠血糖浓度的影响〔J〕.大理学院学报,2013,12(9):11-13.
〔8〕肖笛,陈盛阳,马坤,等.肝龙胶囊对离体在体肠肌收缩活动的影响〔J〕.云南中医中药杂志,2013,34(1):64-66.
〔9〕那凯歌,满红霞,谭巧云,等.肝龙胶囊中总肽含量及其分子量分布的研究〔J〕.中国生化药物杂志,2015,36(3):159-161.
HPLC Method for Determination of the Inosine Content in Ganlong Capsule
Li Yuchi1,Xu Yan1,Yang Yongshou2,Xiao Peiyun1*
(1.College of Pharmacy and Chemistry,Dali University,Dali,Yunnan 671000,China;2.Key Laboratory of Pharmaceutical R&D of Insects in Yunnan Province,Dali,Yunnan 671000,China)
Objective:To establish a determination method of the content of inosine in Ganlong capsule for providing the basis for Ganlong capsule quality control.Methods:Gemini 5u C18110A(250 mm×4.6 mm)chromatographic column,mobile phase water(0.05%TFA):acetonitrile(0.05%TFA),gradient elution,0.8 mL∕min flow,30℃column temperature,DAD detector,214 nm detection wavelength,10 μL sample quantity were used in the study.Results:Peak area of inosine between 0.202-2.020 μg range and injection volume(μg)showed a linear relationship.The average recoveries(n=9)was 96.9%,RSD=2.18%.Conclusion:The established method of determination Ganlong capsules is scientific,simple and accurate,which can be used to improve Ganlong capsule quality standard test project.
Ganlong capsule;inosine;determination
R917
A
2096-2266(2016)12-0040-03
10.3969∕j.issn.2096-2266.2016.12.009
(责任编辑 李 杨)
国家自然科学基金资助项目(81360634;81560634);云南省科技厅应用基础研究基金资助项目(2015FA025)
2016-08-26
2016-09-08
李宇驰,硕士研究生,主要从事美洲大蠊活性提取物研究. *通信作者:肖培云,教授.
