光致变色分子和AIE单元共掺杂纳米胶束:光控、可逆荧光调变
2016-02-05陈尚军朱为宏
陈尚军, 朱为宏
(1.上海师范大学 生命与环境科学学院,上海 200234;2.华东理工大学 结构可控先进功能材料及其制备教育部重点实验室,上海 200237)
光致变色分子和AIE单元共掺杂纳米胶束:光控、可逆荧光调变
陈尚军1, 朱为宏2
(1.上海师范大学 生命与环境科学学院,上海 200234;2.华东理工大学 结构可控先进功能材料及其制备教育部重点实验室,上海 200237)
利用嵌段共聚物聚苯乙烯-b-聚丙烯酸(PS-b-PAA)封装二噻吩乙烯光致变色分子(BTO)和染料分子(ED)制备了纳米胶束BTO@Nm、ED@Nm和BTO-ED@Nm,胶束尺寸分布窄(63~201 nm),在水溶液中具有高度的稳定性和分散性.封装作用诱导ED产生明显的聚集诱导荧光增强效应(AIE),可使ED@Nm和BTO-ED@Nm在500~700 nm范围呈现出明显的荧光.与单体BTO类似,纳米胶束BTO@Nm和BTO-ED@Nm仍然保持从无色(λmax=308 nm)到深蓝色(λmax=595 nm)可逆光致变色性能,且至少可逆转变5次以上抗疲劳性能.利用BTO及其变环体(c-BTO)与ED之间的能量转移作用,在紫外光和可见光的交替照射下,实现对BTO-ED@Nm荧光(565 nm)定量可逆调控,且至少可调控5次以上.
聚集诱导荧光增强; 光致变色; 荧光调控; 纳米胶束
0 前 言
荧光光谱技术因其易于检测、响应速度快、灵敏度高等优点被广泛应用于荧光化学传感器、细胞成像、生物标记与识别等领域,具有高荧光量子效率、高稳定性、长波长(如近红外发射波长)的有机染料分子2016年以来被大量开发[1-5].通过化学修饰调变染料分子的π共轭体系结构,是构建具有不同荧光性能有机分子常用方法之一.大部分荧光材料在溶液中具有较强的荧光信号,然而在高浓度溶液状态或者固态时,大部分分子会发生荧光减弱甚至产生荧光猝灭.导致荧光猝灭的主要原因是大多数荧光分子都含有共平面的芳环结构,在聚集体或固体时容易发生π-π堆积,从而引起聚集荧光猝灭[6-7].在上述分子结构中引入空间位阻较大的基团或长碳链,或者掺杂表面活性剂、聚合物等可在一定程度上消除聚集引起的荧光猝灭效应,但上述方法容易导致化合物合成繁杂、电子传输差、稳定性降低等新问题.2001年,香港科技大学唐本忠等[8-9]报道了一类特殊的具有聚集诱导荧光(AIE)增强效应特征的染料分子.该类化合物在稀溶液状态时基本没有监测不到荧光信号的情况,仅在聚集态或固态下才辐射出强荧光.这一发现为设计具有高荧光效率的有机染料分子提供了全新的研究思路.最近几年,本课题组运用分子工程方法,用N-乙基取代基简单修饰吡喃腈衍生物,成功地发展了一类聚集诱导荧光增强类化合物,其荧光量子产率达到5.2%,最大荧光波超过600 nm,从本质上解决了吡喃腈衍生物的固态荧光猝灭问题.单晶结构表明,N-乙基的修饰作用导致分子产生了扭曲的超分子自组装现象,形成J-型聚集体,呈现出明显的聚集荧光增强现象[10-11].
通过光照刺激作用调控荧光信号技术在超分辨成像、光信息存储等领域具有重要应用价值[12].光诱导下可在两种不同异构体之间可逆转化的光致变色分子是调控荧光信号的重要分子之一.在众多的光致变色分子中,二噻吩乙烯光致变色分子因其良好的抗疲劳性和热稳定性成为可逆调控荧光的理想分子[13-18].在单分子层面通过光致变色单元和荧光团之间电子或者能量转移实现荧光的可逆调控已有很多报道,但是这类方法存在分子合成复杂,难以实现生物应用等局限[19-20].另一种方法是将光致变色组分和荧光团组分混合在一起,通过调节两者的比例和距离,利用分子间能量转移的方式实现荧光调控.为了达到荧光调节并实现生物应用的目的,将光致变色分子和荧光团封装在聚合物内部,制备成纳米颗粒是可行的途径之一.目前将双稳定性二噻吩乙烯光致变色分子和AIE分子掺杂制备成纳米颗粒的报道较少[21-22].
基于上述思考,利用两亲性嵌段聚合物聚苯乙烯-b-聚丙烯酸(PS-b-PAA)自组装过程,将具有良好抗疲劳性和热稳定性的光致变色分子BTO和具有长荧光波长(>600 nm)AIE分子ED封装在聚合物胶束内部,制备成纳米胶束(图1).利用聚合物的包裹作用实现了ED分子聚集诱导荧光增强效应.同时,通过光照前后BTO的共轭体系改变,以及调变BTO和ED之间配比,利用分子间能量转移实现纳米胶束的可逆荧光调控,并初步研究了纳米胶束在细胞成像中的应用.
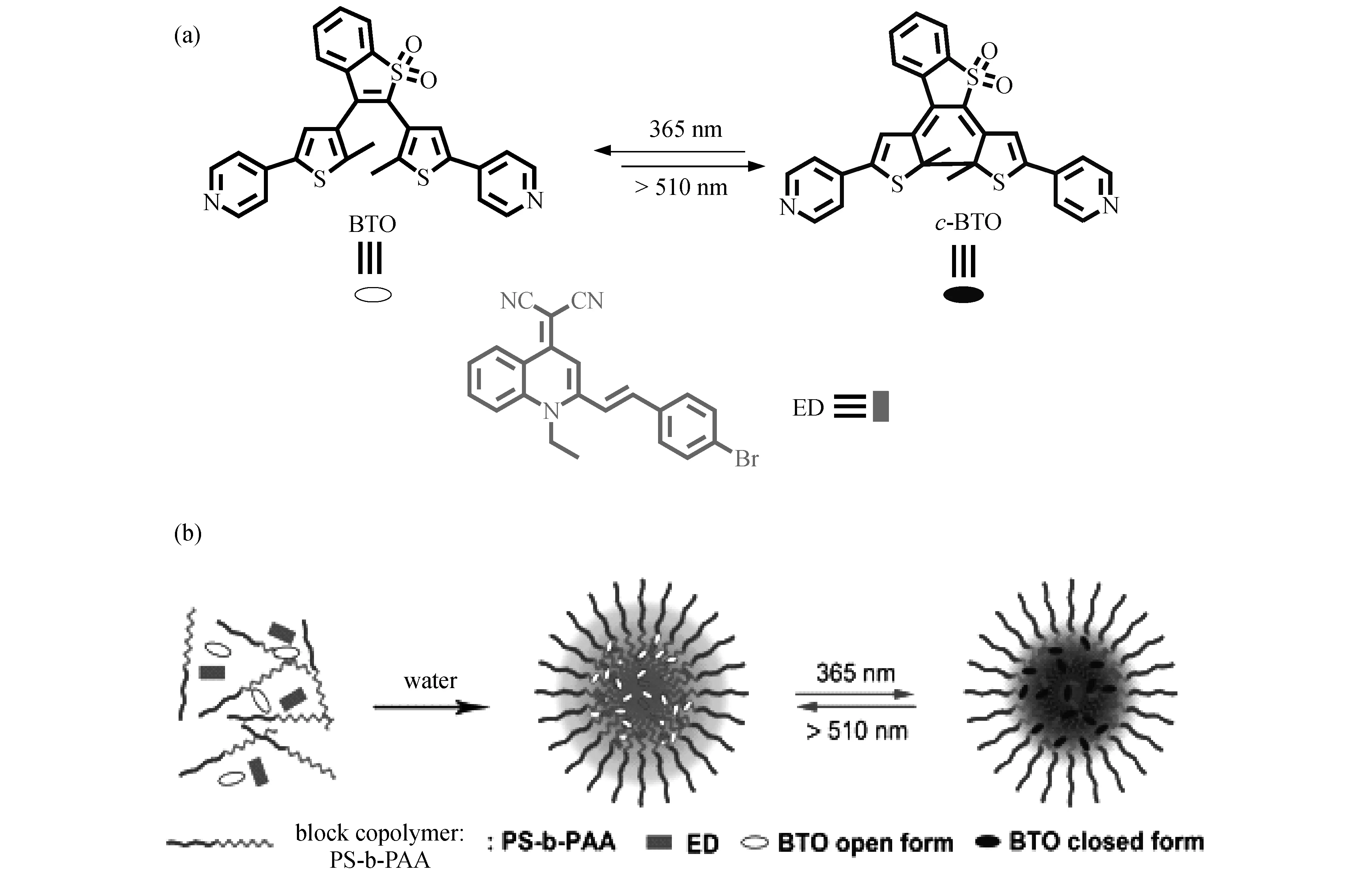
图1 (a)化合物BTO、ED的化学结构和BTO光致变色反应过程; (b)纳米颗粒BTO-ED@Nm合成及其荧光调控示意图
1 实验部分
1.1 试剂及仪器
化合物BTO、AIE分子ED、聚合物PS-b-PAA参照文献[10,23-24]报道方法合成,通过核磁氢谱(1HNMR)、碳谱(13C NMR)和高分辨率质谱(HRMS)表征分子结构.实验中使用的其他试剂和药品购自上海国药试剂集团,均为市售分析纯或化学纯.除特殊说明外,均直接使用,未作进一步提纯.
核磁共振氢谱和碳谱采用Brucker超导傅里叶变换核磁共振波谱仪(400 MHz),室温下以四甲基硅烷(TMS)为内标测定;高分辨质谱测试仪器为Waters LCT Premier XE spectrometer,测试溶剂为氘代甲醇和乙腈;紫外-可见光吸收光谱采用Varian Cary 100紫外-可见分光光度计,室温下测定;荧光发射光谱采用Varian Cary Eclipse荧光光谱仪室温下测定;光致变色反应所需光源为Hamamatsu,LC6 Lightningcure,300 W汞氙灯.吸收光谱由海洋光学CCD 跟踪检测.实验中测得的耦合常数、转化率以及量子产率等相关数据误差均小于5%.
1.2 纳米颗粒的制备
为了分析比较封装不同分子后纳米颗粒性质,分别制备了包含BTO、ED单组分以及BTO和ED两组分混合的纳米颗粒.典型的制备过程如下:将15 mg PS-b-PAA粉末溶解在有机溶剂四氢呋喃(THF)中,待固体完全溶解后,分别向上述溶液中加入1 mL含有单独BTO、单独ED或者BTO和ED混合在一起的混合物的四氢呋喃(THF)溶液(1 mg/mL),常温下搅拌2 h后,将40 mL超纯水以一定的速度加入到上述有机相中,继续搅拌30 min.然后将上述油/水混合体系转移到截留分子量为14000的透析袋中进行透析分离,除去THF溶液,即分别得到胶束颗粒BTO@Nm、ED@Nm和BTO-ED@Nm水溶液[25].
1.3 细胞毒性实验
采用甲基噻唑基四唑(MTT法)测定(BTO-ED@Nm胶束)对人乳腺癌细胞株MCF-7的体外细胞毒性.具体实验步骤如下:首先,在含有质量分数10%胎牛血清的Hyclon改良细胞培养基(DMEM)中对MCF-7细胞株进行培养,然后以每孔9 000~10 000个细胞数接种于96孔板,继续培养24 h后,将分散于含有10%胎牛血清细胞培养基中的含有不同样品质量浓度(0~500 μg/mL)的纳米胶束加入到上述孔板中,继续培养24 h.采用MTT法评估细胞毒性,再将MTT的磷酸盐缓冲液溶液(PBS)加入到每个孔板中.37 ℃孵育4 h后,弃去上清液,每孔板中加入100 μL二甲基亚砜溶液,最后测定材料在490 nm处的吸光度[25].
2 结果与讨论
2.1 荧光调控机理
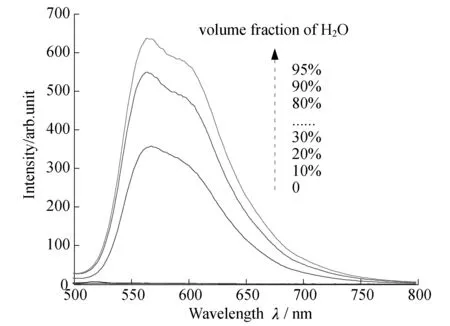
图2 ED (物质的量浓度为1×10-5mol/L)在水/THF混合溶剂中荧光光谱(λex=450 nm)
荧光染料分子ED具有典型的AIE效应.如图2所示,随着THF和水混合溶剂中水体积分数的增加,ED的荧光辐射信号逐渐增强.在水体积分数低于70%之前,荧光信号强度较弱,此时聚集体初步形成.当水的体积分数增加到80%时,荧光强度明显增加,达到95%时,无定形聚集体的形成,在500~750 nm范围内ED呈现出最强的荧光信号[26].
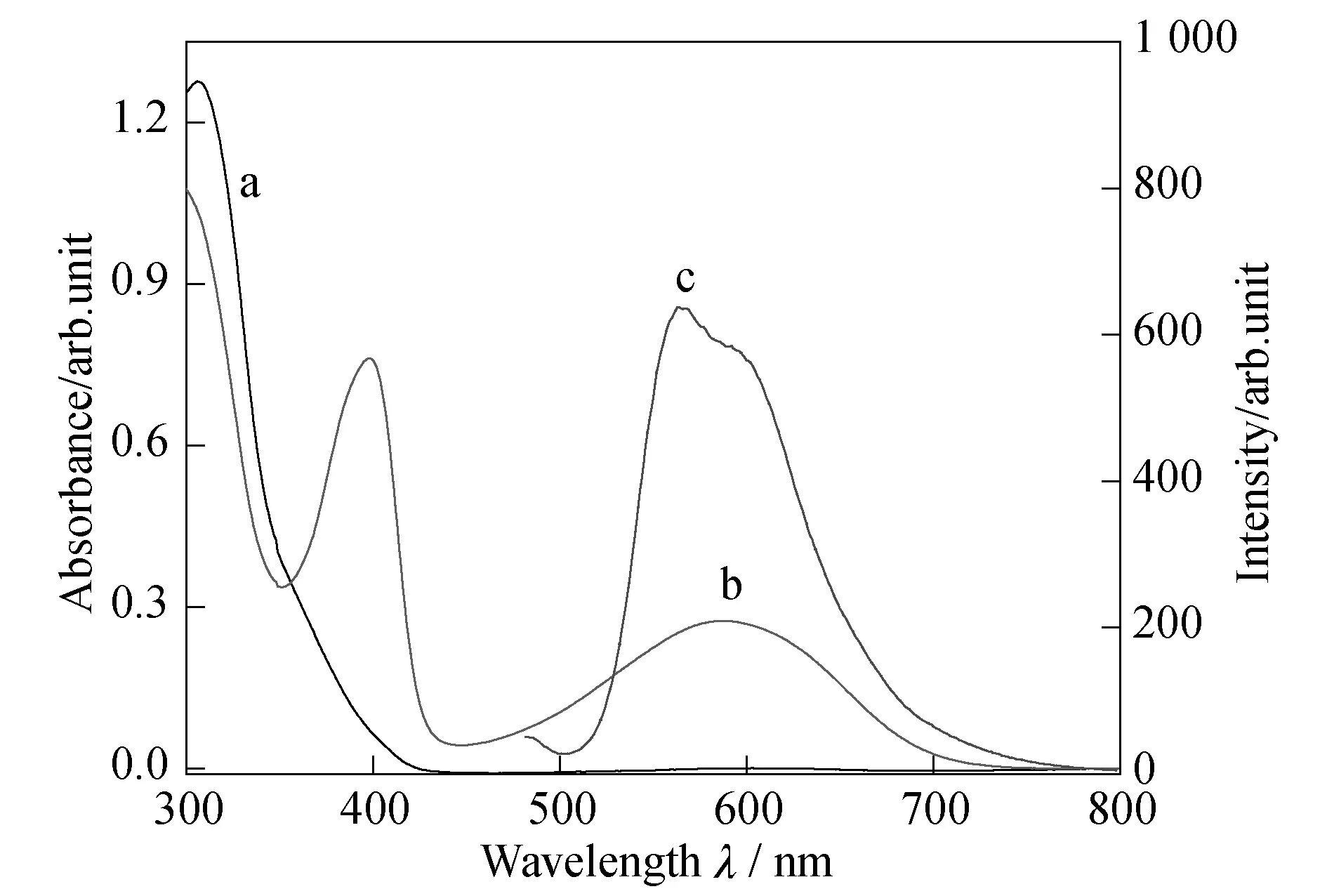
图3 BTO(a),c-BTO吸收光谱(365 nm)(b)以及ED(c)在水体积分数为95%的水/THF混合溶液中的荧光光谱(λex=450 nm)
另一方面,比较BTO、c-BTO吸收光谱以及ED聚集诱导下的荧光光谱,c-BTO吸收光谱和ED聚集诱导下荧光光谱存在很大程度叠合(图3),而BTO在可见光区域没有吸收,即与聚集态的荧光光谱几乎没有任何重叠.因此,利用分子间能量转移机理,通过光控诱导BTO发生光致变色反应,有望可逆调控ED聚集诱导荧光.
2.2 聚合物封装作用
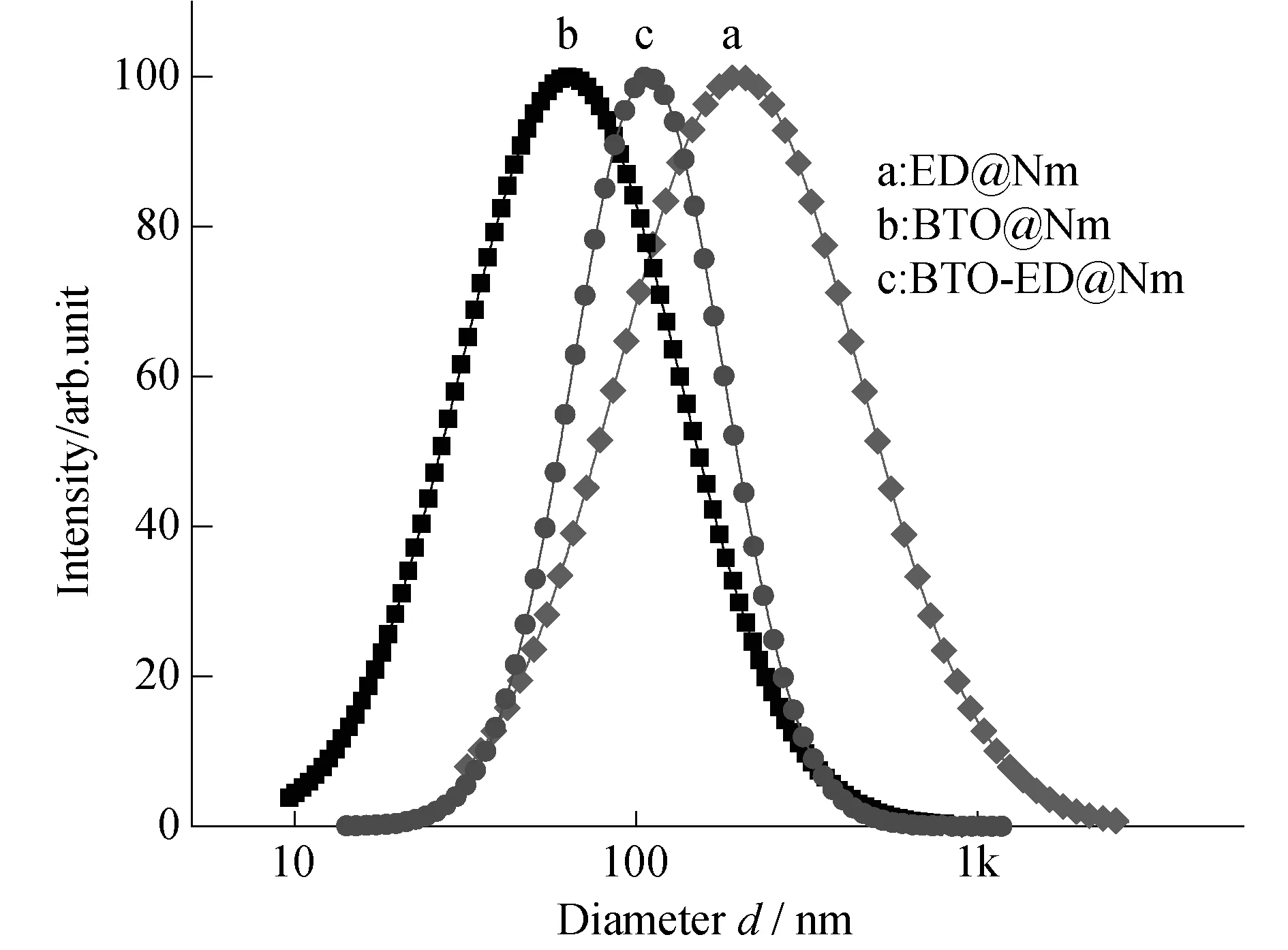
图4 ED@Nm、BTO@Nm和BTO-ED@Nm纳米胶束在水溶液中动态光散射粒径分布曲线图
制备纳米胶束所采用的方法直接影响纳米胶束的结构.制备纳米胶束有以下两种方法.1) 直接加入溶解法,即直接将双亲性嵌段共聚物溶于选择性溶剂中制备胶束,该过程中一般需通过搅拌、加热或者超声的作用促进其溶解.这种方法仅适合于小分子量或者憎水性嵌段较短的嵌段共聚物.2) 是选择性溶剂分步加入法,这种方法是指先将嵌段共聚物溶解在某种有机溶剂的非选择性溶剂中,使其以单分子链的形式存在,然后再加入一定量的难溶性选择性溶剂,通常情况下为水,使其形成核壳结构的胶束,最后采用透析或者蒸发的方式将非选择性的有机溶剂除去,即可得到结构稳定的胶束水溶液.相比于第一种方法,这种方法不仅能防止生成尺寸较大的团聚体而且还适于大分子量或者憎水性嵌段较长嵌段共聚物[27].鉴于BTO和ED疏水性都很强,在这里选择方法二制备所有的纳米胶束,嵌段共聚物选择为两亲性聚苯乙烯-b-聚丙烯酸,利用疏水的聚苯乙烯核包裹BTO和ED,最终形成稳定的纳米胶束.通过动态光散射技术(DLS),对胶束颗粒的粒径分布进行表征.图4为不同胶束样品的粒径分布图,单独封装的胶束样品BTO@Nm和ED@Nm的粒径分布为63和201 nm,而混合封装BTO-ED@Nm的纳米胶束动力学直径为108 nm.这些尺寸与文献报道中的自缩聚胶束尺寸范围一致(20~100 nm),且粒径分布较窄.
2.3 纳米颗粒的聚集诱导荧光以及光控荧光调控
在研究BTO和ED混合掺杂的纳米颗粒之前,先考察单组分纳米颗粒性质.图5为ED@Nm在水溶液中的紫外吸收光谱和荧光光谱.ED@Nm在450 nm存在一明显吸收峰,这表明嵌段聚合物PS-b-PAA 形成胶束的过程中,对ED进行了包裹,并有效促使了其无定形聚集体的形成.其荧光光谱和ED在THF/水混合溶剂中类似,呈现出与95% 含水量(体积分数)的水/THF混合溶液中荧光辐射峰.进一步证明了ED在胶束颗粒中形成了明显的聚集诱导荧光增强效应.
采用加水法同样制备了封装光致变色单组分BTO的纳米颗粒BTO@Nm.图6为其在水溶液当中紫外吸收光谱和荧光辐射光谱.如图6(a)所示,BTO@Nm在水溶液中为无色透明溶液,其吸收光谱在308 nm左右出现一个明显紫外吸收峰,而在可见光区域未见其他吸收峰,吸收波长来自于光致变色分子开环体BTO.在365 nm紫外光照射后,在可见光区域400 nm以及590 nm处逐渐产生两个显著的吸收峰.这是由于BTO发生了典型的光致变色关环反应,生成了平面结构更好、π离域体系更大的闭环体结构c-BTO,在可见光区域产生新的吸收带,同时溶液颜色变化为深蓝色[28].在等吸收点355 nm激发下,BTO@Nm水溶液在400~650 nm范围内产生明显的荧光辐射,这一荧光峰与BTO在THF溶液中荧光信号非常类似.同时随着365 nm紫外光的照射加强,纳米颗粒发生了明显的荧光猝灭现象,在180 s后荧光基本完全消失.荧光猝灭是由于BTO转化为没有荧光的闭环体c-BTO所致(图5,6)[29].此外,在紫外光(365 nm)和可见光(>510 nm)交替照射下,紫外吸收光谱以及荧光光谱都可以多次在开环态与闭环态之间可逆转化(图5,6).上述结果表明,在封装以后,BTO@Nm保持了光致变色单体BTO的光致变色性能,具有良好的抗疲劳性和稳定性.

图6 BTO@Nm在水溶液中365 nm紫外光照射后(a)紫外吸收光谱,(b)荧光光谱(λex=355 nm),(c)在紫外光(365 nm)和可见光(>510 nm)交替照射下的紫外吸收光谱
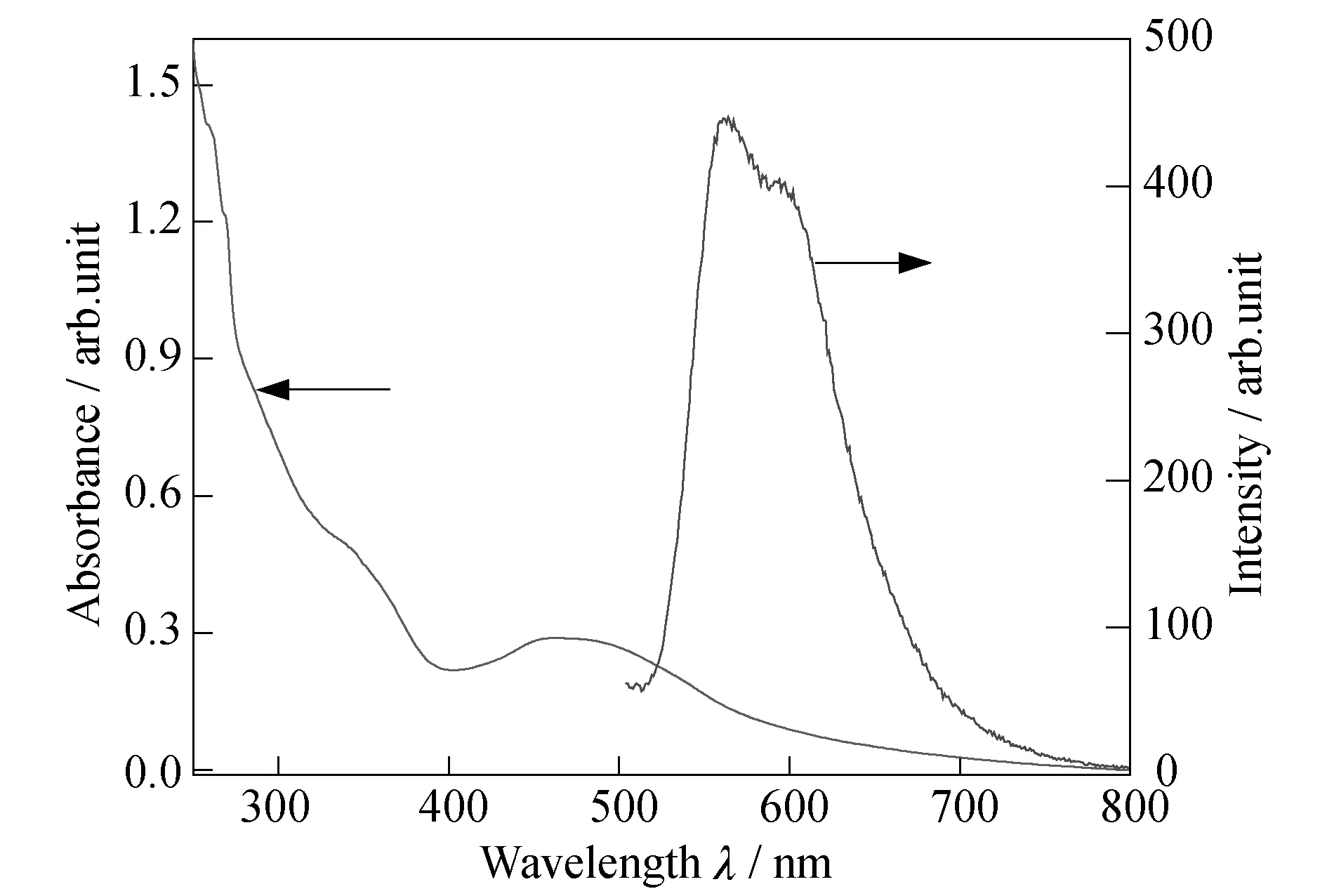
图5 ED@Nm在水溶液中紫外吸收光谱和荧光光谱(λex=450 nm)
以上研究表明通过聚合物包裹作用不仅实现了ED的聚集诱导荧光增强效应,且BTO在纳米颗粒中能保持原有的良好光致变色性能.这为混合组分纳米颗粒BTO-ED@Nm光控调节荧光奠定了基础.通过分子间能量转移实现荧光猝灭,一方面要求两个分子之间(光致变色单元和AIE分子)的距离足够近,另一方面要求两组分必须达到一定比例.采用混合封装方法制备的纳米颗粒BTO-ED@Nm,BTO和ED随机分布在同一纳米颗粒内部,有足够近的距离,需要调控两者比例.一般而言,纳米颗粒中BTO分子的含量越多越容易产生能量转移而引起荧光猝灭.因此制备了不同BTO和ED摩尔比例的BTO-ED@Nm纳米胶束.图7是BTO和ED比例为1∶1的BTO-ED@Nm在水溶液中的紫外吸收光谱和荧光光谱.如图7(a)所示,BTO-ED@Nm水溶液为无色透明溶液,其吸收光谱在308 nm处出现一个很强吸收峰,而在405 nm左右存在中等程度吸收峰,在可见光区域没有吸收峰.这两个特征吸收峰分别和光致变色分子BTO和AIE分子ED吸附峰匹配,且其吸收强度也和两者加入前的摩尔比例匹配(图2,3).经365 nm紫外光照射后,其吸收光谱在可见光区域400 nm以及590 nm左右产生2个明显的吸收峰,这和BTO@Nm经紫外光照射后产生的吸收峰完全一致.这说明ED的存在并不影响BTO@Nm的光致变色性能.与此同时,无色的水溶液逐渐变成深蓝色.图7(b)对应的是BTO-ED@Nm在365 nm照射下的荧光光谱.BTO-ED@Nm在450 nm光激发下,在500~700 nm范围内观察到一宽的荧光峰,此峰主要来自ED的聚集诱导荧光.随着紫外光照射加长,发生了明显的荧光减弱现象,在光照110 s后达到稳定态.经紫外光辐射后,BTO转化为c-BTO,BTO自身荧光部分猝灭;同时,聚集态ED与c-BTO由于能量转移作用导致聚集态的荧光也发生明显减弱.上述实验结果说明,通过光照诱导BTO发生光致变色反应,利用ED与c-BTO分子间能量转移作用可以实现荧光调控[30-31].在当前比例下,ED聚集态荧光并不能完全猝灭,仅降低为初始态的45%左右.为了实现对聚集态荧光从有到无的调控,在控制ED比例不变条件下,进一步增加BTO比例,分别制备了BTO和ED摩尔比为2∶1和10∶1的纳米颗粒,测试结果表明随着BTO含量增多,BTO@Nm的荧光猝灭效率逐渐提高(图8).当BTO∶ED比例为10∶1时,由于BTO比例增加,其荧光变得不可忽略,此时荧光光谱由BTO和ED共同贡献.BTO-ED@Nm在450 nm光激发下,在500~750 nm范围内呈现出一个较宽的荧光峰.经365 nm紫外光照射后,此荧光在大约10 s左右就可以大部分被猝灭,达到光稳态时,其荧光几乎被完全猝灭,即通过调节BTO和ED比例实现了荧光从有到无的调控作用.BTO-ED@Nm还具有良好的抗疲劳性能.如图9所示,在紫外光(365 nm)和可见光(>510 nm)交替照射下,其紫外吸收光谱和荧光光谱可多次在开环态与闭环态之间可逆转化,经5次循环后其强度仅有稍许降低.

图7 BTO-ED@Nm(BTO∶ED=1∶1)水溶液中经365 nm紫外光照射后(a)紫外吸收光谱和(b)荧光光谱(λex=450 nm)
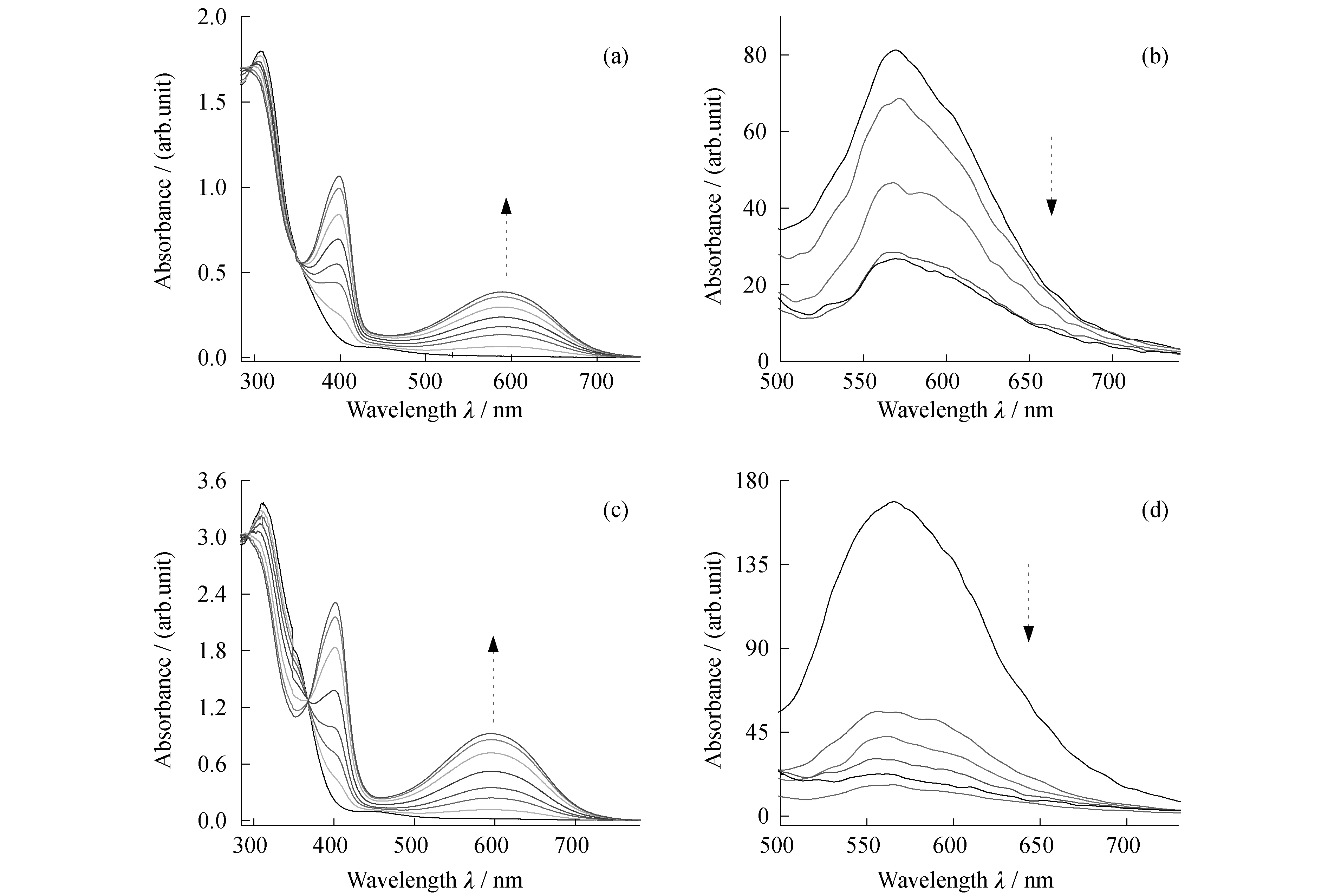
图8 不同BTO,ED比例下BTO-ED@Nm在水溶液中经365 nm紫外光照射后(nBTO∶nED=2∶1(摩尔比),λex=450 nm)吸收光谱(a),(c)和(nBTO∶nED=10∶1(摩尔比),λex=450 nm)荧光光谱(b),(d)
进一步研究了纳米胶束对于人乳腺癌细胞株MCF-7的体外细胞毒性.如图10所示,不同样品质量浓度(0~500 μg/mL)的纳米胶束BTO-ED@Nm(nBTO∶nED=10∶1)对于MCF-7的连续培养24 h后,490 nm处的吸光度变化很小.证明材料对人乳腺癌细胞株MCF-7的毒害很小,适合于细胞成像.
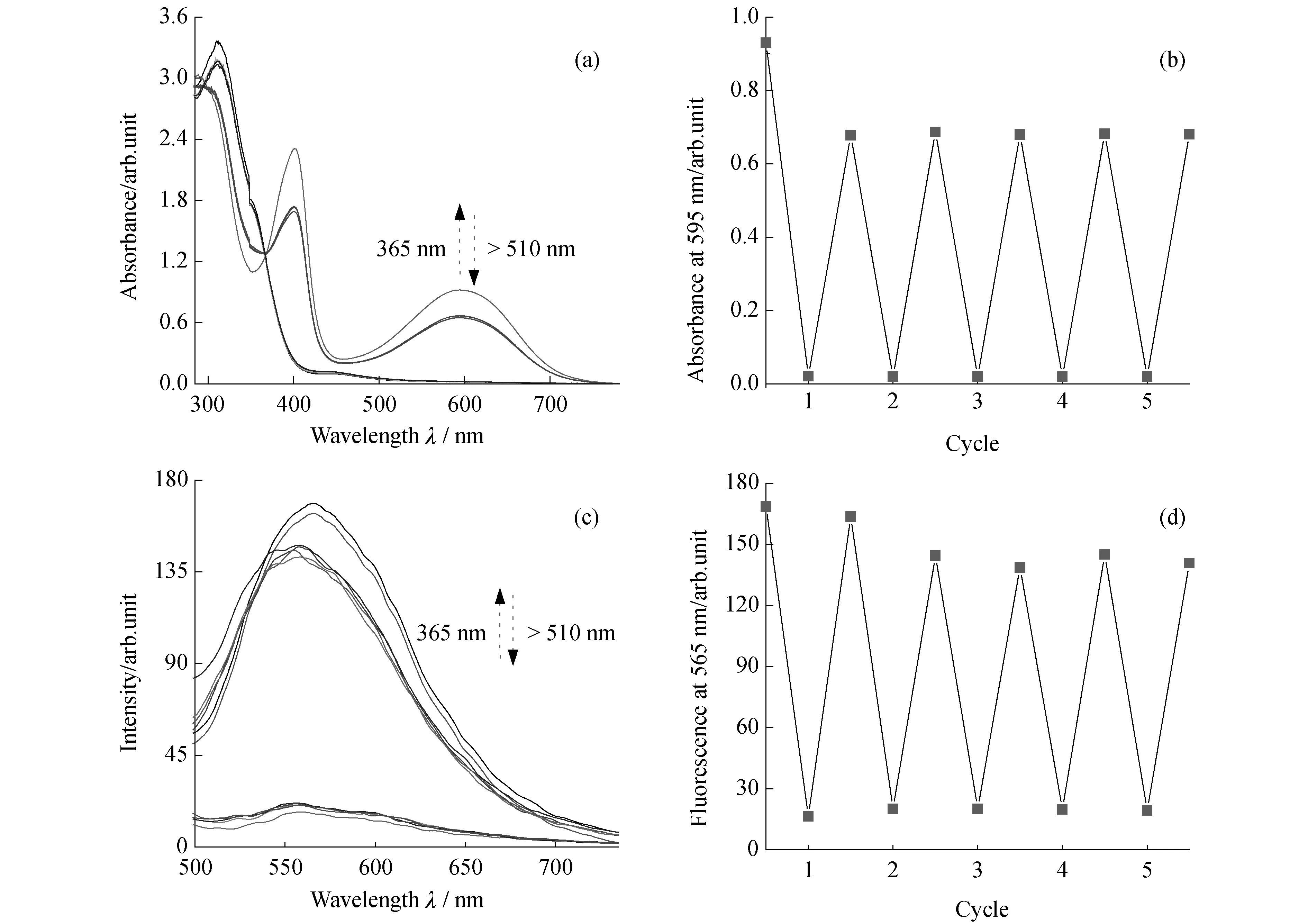
图9 BTO-ED@Nm(nBTO∶nED=10∶1)水溶液经紫外光(365 nm)和可见光(>510 nm)交替照射下吸收光谱(a),(b)和荧光光谱(c),(d),(其中(b)、(d)分别为595 nm处吸光度值和565 nm荧光值)

图10 不同质量浓度的BTO-ED@Nm(nBTO∶nED=10∶1)MCF-7细胞孵育24 h后的细胞存活率结果
3 结 论
利用加水法制备了嵌段共聚物PS-b-PAA封装的纳米胶束ED@Nm、BTO@Nm和BTO-ED@Nm,胶束的尺寸分布窄(63~210 nm),在水溶液中具有较好的稳定性和分散性.纳米胶束封装作用可诱导AIE分子(ED)产生聚集诱导荧光增长效应,ED@Nm和BTO-ED@Nm在500~700 nm范围内呈现出明显的荧光性质.同时,纳米胶束微环境对包裹光致变色分子性能无限制作用,BTO@Nm和BTO-ED@Nm仍保持与BTO类似的可变色性能和抗疲劳性.通过胶束封装将BTO与ED掺杂在一起,利用分子间能量转移作用,调控BTO与ED比例(1∶1,5∶1,10∶1),经紫外光和可见光的交替照射,实现对BTO-ED@Nm荧光从有到无的光控可逆调节.
[1] Borisov S M,Wolfbeis O S.Optical biosensors [J].Chemical Reviews,2008,108(2):423-461.
[2] Pansare V J,Hejazi S,Faenza W J,et al.Review of long-wavelength optical and NIR imaging materials:Contrast agents,fluorophores,and multifunctional nano carriers [J].Chemistry of Materials,2012,24(5):812-827.
[3] Zhu C,Liu L,Yang Q,et al.Water-soluble conjugated polymers for imaging,diagnosis,and therapy [J].Chemical Reviews,2012,112(8):4687-4735.
[4] Zhao W W,Xu J J,Chen H Y.Photoelectrochemical DNA biosensors [J].Chemical Reviews,2014,114(15):7421-7441.
[5] Lee J S,Feijen J.Polymersomes for drug delivery:Design,formation and characterization [J].Journal of Controlled Release,2012,161(2):473-483.
[6] Chen C T.Evolution of red organic light-emitting diodes:Materials and devices [J].Chemistry of Materials,2004,16(23):4389-4400.
[7] Guo Z,Zhu W,Tian H.Dicyanomethylene-4H-pyran chromophores for OLED emitters,logic gates and optical chemosensors [J].Chemical Communications,2012,48(49):6073-6084.
[8] Hong Y,Lam J W Y,Tang B Z.Aggregation-induced emission [J].Chemical Society Reviews,2011,40(11):5361-5388.
[9] Luo J,Xie Z,Lam J W Y,et al.,Aggregation-induced emission of 1-methyl-1,2,3,4,5-pentaphenylsilole [J].Chemical Communications,2001(18):1740-1741.
[10] Shi C,Guo Z,Yan Y,et al.Self-assembly solid-state enhanced red emission of quinolinemalononitrile:Optical waveguides and stimuli response [J].Acs Applied Materials & Interfaces,2013,5(1):192-198.
[11] Shao A,Xie Y,Zhu S,et al.Far-red and near-IR AIE-active fluorescent organic nanoprobes with enhanced tumor-targeting efficacy:Shape-specific effects [J].Angewandte Chemie International Edition,2015,54(25):7275-7280.
[12] Swaminathan S,Garcia-Amoros J,Fraix A,et al.Photoresponsive polymer nanocarriers with multifunctional cargo [J].Chemical Society Reviews,2014,43(12):4167-4178.
[13] Zhang J,Zou Q,Tian H.Photochromic materials:More than meets the eye [J].Advanced Materials,2013,25(3):378-399.
[14] Irie M,Fulcaminato T,Matsuda K,et al.Photochromism of diarylethene molecules and crystals:Memories,switches,and actuators [J].Chemical Reviews,2014,114(24):12174-12277.
[15] Szymanski W,Beierle J M,Kistemaker H A V,et al.Reversible photocontrol of biological systems by the incorporation of molecular photoswitches [J].Chemical Reviews,2013,113(8):6114-6178.
[16] Su J,Fukaminato T,Placial J P,et al.Giant amplification of photoswitching by a few photons in fluorescent photochromic organic nanoparticles [J].Angewandte Chemie International Edition,2016,55(11):3662-3666.
[17] Fredrich S,Gostl R,Herder M,et al.Switching diarylethenes reliably in both directions with visible light [J].Angewandte Chemie-International Edition,2016,55(3):1208-1212.
[18] Chen S,Chen L J,Yang H B,et al.Light-triggered reversible supramolecular transformations of multi-bisthienylethene hexagons [J].Journal of the American Chemical Society,2012,134(33):13596-13599.
[19] Deniz E,Kandoth N,Fraix A,et al.Photoinduced fluorescence activation and nitric oxide release with biocompatible polymer nanoparticles [J].Chemistry—A European Journal,2012,18(49):15782-15787.
[20] Liu G,Liu M,Pu S,et al.Synthesis and photochromic properties of novel pyridine:Containing diarylethenes [J].Dyes and Pigments,2012,95(3):553-562.
[21] Cusido J,Battal M,Deniz E,et al.Fast fluorescence switching within hydrophilic supramolecular assemblies [J].Chemistry-A European Journal,2012,18(33):10399-10407.
[22] Kim S,Yoon S J,Park S Y.Highly fluorescent chameleon nanoparticles and polymer films:Multicomponent organic systems that combine FRET and photochromic switching [J].Journal of the American Chemical Society,2012,134(29):12091-12097.
[23] Chen S,Yang Y,Wu Y,et al.Multi-addressable photochromic terarylene containing benzo B thiophene-1,1-dioxide unit as ethene bridge:Multifunctional molecular logic gates on unimolecular platform [J].Journal of Materials Chemistry,2012,22(12):5486-5494.
[24] Chen Y,Xu P,Chen H,et al.Colloidal HPMO nanoparticles:Silica-etching chemistry tailoring,topological transformation,and nano-biomedical applications [J].Advanced Materials,2013,25(22):3100-3105.
[25] Wu X,Chang S,Sun X,et al.Constructing NIR silica-cyanine hybrid nanocomposite for bioimaging in vivo:A breakthrough in photo-stability and bright fluorescence with large stokes shift [J].Chemical Science,2013,4(3):1221-1228.
[26] Li Y,Shao A,Wang Y,et al.Tumor bioimaging:Morphology-tailoring of a red AIEgen from microsized rods to nanospheres for tumor-targeted bioimaging [J].Advanced Materials,2016,28(16):3224-3224.
[27] Wu X,Sun X,Guo Z,et al.In vivo and in situ tracking cancer chemotherapy by highly photostable NIR fluorescent theranostic prodrug [J].Journal of the American Chemical Society,2014,136(9):3579-3588.
[28] Sumi T,Kaburagi T,Morimoto M,et al.Fluorescent photochromic diarylethene that turns on with visible light [J].Organic Letters,2015,17(19):4802-4805.
[29] Cai Y,Gao Y,Luo Q,et al.Ferrocene-grafted photochromic triads based on a sterically hindered ethene bridge:Redox-switchable fluorescence and gated photochromism [J].Advanced Optical Materials,2016,4:1410-1416.
[30] Truong K,Ikura M.The Use of FRET Imaging microscopy to detect protein-protein interactions and protein conformational changes in Vivo [J].Current Opinion in Structural Biology,2001,11(5):573-578.
[31] Clegg R M.Fluorescence resonance energy transfer [J].Current Opinion in Biotechnology,1995,6(1):103-110.
(责任编辑:包震宇,郁 慧)
Nano-micelles encapsulated photochromic molecules and AIE units:light controlled reversible fluorescence modulation
CHEN Shangjun1, ZHU Weihong2
(1.College of Life and Environmental Sciences,Shanghai Normal University,Shanghai 200234,China;2.Key Laboratory for Advanced Materials,East China University of Science and Technology,Shanghai 200237,China)
Nano-micelles containing photochromic diarylethene molecules(BTO) and/or aggregation-induced emission (AIE) characteristic chromophores (ED),BTO@Nm,ED@Nm,and BTO-ED@Nm,were prepared via self-assembly of an amphiphilic block copolymer polystryene-b-polyacrylic acid (PS-b-PAA).The as-prepared nano-micelles havenarrow size distribution (61-210 nm),excellent dispersity,and stabilityin aqueous solutions.Typical AIE properties and obvious fluorescence in the range from 500 to 700 nm were observed both in ED@Nm and BTO-ED@Nmdue to the aggregation of ED by the encapsulation of the nano-micelles.Similar to BTO,BTO@Nm and BTO-ED@Nm exhibited reversilbe photochromic reacition between colorless solution (λmax=308 nm) and deep blue (λmax=595 nm) and nice fatigure resistance,in which the cycle between colorless and colored solution can be repeated over 5 times.Moreover,the fluorescence of BTO-ED@Nm (565 nm) can be quantitatively and reversibly modulated via alternative irradiation of Uv (365 nm) and visible light as a result of the fluorescence resonance energy transfer (FRET) among BTO,the closed isomerc-BTO,and ED.The reversibly fluorescencemodulated process can be perfermed more than 5 times.
aggregation-induced emission (AIE); photochromism; fluorescence modulation; nano-micelle
2016-09-22
国家自然科学基金青年基金(21503136);上海市科学技术委员会“扬帆计划”(14YF1409200)
陈尚军,中国上海市徐汇区桂林路100号,上海师范大学生命与环境科学学院,邮编:200234,E-mail:jshchen@shnu.edu.cn
O 69
A
1000-5137(2016)06-0641-09
