恶性肿瘤患者术后芬太尼镇痛干预时的拟合血药浓度观察
2016-01-20邓玲燕邓喆黎阳黄冰覃韬黄英明彭丹晖广西医科大学附属肿瘤医院南宁530021
邓玲燕,邓喆,黎阳,黄冰,覃韬,黄英明,彭丹晖(广西医科大学附属肿瘤医院,南宁530021)
恶性肿瘤患者术后芬太尼镇痛干预时的拟合血药浓度观察
邓玲燕,邓喆,黎阳,黄冰,覃韬,黄英明,彭丹晖
(广西医科大学附属肿瘤医院,南宁530021)
摘要:目的观察恶性肿瘤患者术后芬太尼镇痛干预时的血药浓度,指导临床合理用药。方法90例恶性肿瘤根治术患者根据手术部位不同分为胸部( A组)、上腹部( B组)、下腹部( C组)各30例。患者术中采用芬太尼静脉注射全身麻醉,根据患者临床资料使用药代动力学模拟软件拟合围麻醉期芬太尼的药代动力学过程,测算术后需镇痛时的芬太尼血浆药物浓度。结果需要镇痛时A、B、C三组芬太尼的拟合血药浓度值分别为( 0.97± 0.20)、( 0.86±0.21)、( 0.75±0.19) ng/mL,95%可信区间分别为0.90~1.04、0.78~0.94、0.68~0.82 ng/mL。血药浓度C组<B组<A组,P均<0.05。结论恶性肿瘤患者术后芬太尼镇痛时血药浓度存在差异,应个体化、按需进行术后镇痛。
关键词:芬太尼;靶控输注;术后镇痛;血药浓度;肿瘤患者
芬太尼是临床最常用的麻醉性阿片类镇痛药,反复注射或大剂量注射时,停药后可出现延迟性呼吸抑制[1]。靶控输注( TCI)是以药动学和药效学为原理,以血浆药物浓度为指标,由计算机控制给药输注速率的变化,达到麻醉、镇静的目的[2]。近年来临床常用术后静脉自控镇痛( PCIA),但存在镇痛不全或镇痛过度的情况[3]。2010年11月~2011年3月,我们采用药代动力学模拟软件( Tivatrainer)对90例恶性肿瘤根治术后患者血浆芬太尼浓度变化进行拟合,计算术后疼痛时芬太尼的血药浓度,为PCIA的介入时点、芬太尼剂量的选择提供临床参考依据。现报告如下。
1 资料与方法
1.1临床资料我院同期收治的90例行恶性肿瘤根治性手术患者,其中男45例、女45例,年龄( 55± 10)岁; BMI 20~24,ASA≤Ⅲ级;肺癌30例,肝癌18例,胃癌12例,肾癌4例,宫颈癌10例,子宫内膜癌6例;均无心、肺、肝、肾等功能异常,且无酗酒及镇痛、镇静类药物依赖史,排除存在外科手术史者。90例患者根据手术部位的不同分为胸部( A组)、上腹部( B组)、下腹部( C组)各30例,根据文献[4]选择Shafer模型21例为对照。本研究经广西医科大学附属肿瘤医院伦理委员会批准,患者术前均签署麻醉和PCIA同意书。三组性别、年龄、体质量和Shafer模型均无统计学差异; A、B、C三组身高无统计学差异。见表1。
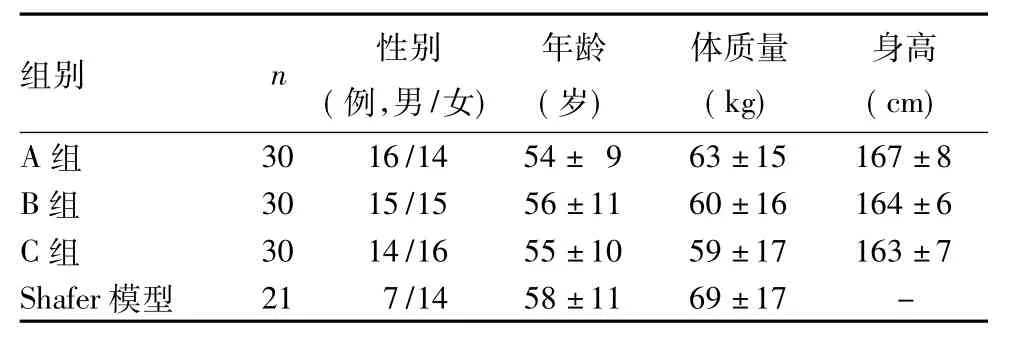
表1 四组基本情况比较
1.2麻醉方法三组择日行恶性肿瘤根治性切除术,术前5 min静注枸橼酸芬太尼注射液6 μg/kg,静脉持续泵注盐酸雷米芬太尼0.1 μg/( kg·min)、丙泊酚100 μg/( kg·min)、维库溴铵0.06 mg/( kg· min)维持术中麻醉。术后静注咪唑安定0.05 mg/kg、丙泊酚1 mg/kg、芬太尼4 μg/kg、维库溴铵0.1 mg/kg辅助气管插管,经口气管插管后机械控制呼吸。术后三组均行麻醉后复苏及监护,术后拔出气管导管。拔管标准:神志清醒;口腔、咽下腔内干净;咽喉反射恢复;肌力恢复Ⅴ级;潮气量>6 mL/kg;自主呼吸峰压>20 cmH2O;血气分析无低氧血症及CO2蓄积。
1.3芬太尼拟合浓度值的确定使用计算机软件Tivatrainer挂载的芬太尼药代动力学方程Shafer模型[4],输入患者年龄、性别、体质量、身高、ASA,麻醉过程中芬太尼剂量和给药时点等参数,拟合出围麻醉期患者芬太尼血药浓度曲线变化。患者拔除气管导管后,进行镇静评分( RSS)和疼痛评分( PHS)[5]。RSS 2~3分、PHS 3分时需要进行镇痛,观察芬太尼血药浓度曲线上对应的拟合浓度值。
1.4统计学方法采用SPSS13.0统计软件。计量资料以珋x±s表示,组间比较用单因素方差分析。P <0.05为差异有统计学意义。
2 结果
需要镇痛时,A、B、C组芬太尼的拟合血药浓度值分别为( 0.97±0.20)、( 0.86±0.21)、( 0.75± 0.19) ng/mL,95%可信区间分别为0.90~1.04、0.78~0.94、0.68~0.82 ng/mL。血药浓度C组<B组<A组,P均<0.05。
3 讨论
Shafer模型可精确拟合芬太尼在人体内的代谢过程,是目前靶控输注泵常用的芬太尼药代动力学方程[6]。Tivatrainer是一款药代动力学模拟软件,内置多种麻醉药物的药代动力学参数,可模拟药物在患者体内整个代谢过程,并拟合麻醉药物的靶浓度变化,为全身麻醉复苏和术后镇痛提供临床指导[7]。药代动力学参数源于抽样的人群,由于群体和个体间的差异,药代动力学方程拟合结果与实际血药浓度存在一定偏差,但其计算值和实际值相关。因药代动力学参数的差异比药效学的差异小,当药代动力学参数偏离度小于15%,精确度误差小于20%~30%,该方程即可指导临床药效学方面的应用[8]。由于人群的性别、年龄、体质量和Shafer模型无统计学差异,因此本研究人群的芬太尼血药浓度拟合可选择该模型。
Dolin等[9]研究发现,使用阿片类药物镇痛的患者中,35.8%的患者因药量不足仍感到中度疼痛,2.6%的患者因药量过大出现过度镇静。呼吸抑制是阿片类药物最严重的不良反应,阿片剂量滴定、严密的生命体征监护可减少过度镇静所导致的呼吸抑制[10];通过RSS调整阿片类药物剂量可以减少嗜睡、镇静过度的发生率[11]。理想的镇痛状态为患者安静状态无疼痛感觉,神志清醒并能按指令配合诊疗。患者在RSS 2~3分、PHS<3分时符合理想的镇痛、镇静状态;通过对此时芬太尼血药浓度的拟合,可计算出理想芬太尼镇痛治疗的靶浓度。
Tivatrainer软件拟合理想芬太尼镇痛治疗血药靶浓度分别为:胸部( 0.97±0.20) ng/mL、上腹部( 0.86±0.21) ng/mL、下腹部( 0.75±0.19) ng/mL;三组数据皆成正态分布,相对应的95%可信区间分别为0.90~1.04、0.78~0.94、0.68~0.82 ng/mL。不同的手术种类、部位,术后镇痛治疗的不同时间段,最佳的芬太尼镇痛靶浓度应该是不一样的。Woodhouse等[12]研究发现,静吸复合全身麻醉下行腹部手术,患者在复苏室对外界刺激有反应时,芬太尼效应室浓度为( 1.59±0.63) ng/mL;当效应室浓度达到( 1.2±0.6) ng/mL,患者不会出现难以忍受的疼痛。有报道称,患者行矫形手术后自控镇痛治疗,24 h芬太尼的最小有效血药浓度为0.23~0.99 ng/mL。本研究中,相同水平镇静、镇痛的状态下,患者的芬太尼血药浓度胸部>上腹部>下腹部,提示临床应根据所得芬太尼血药浓度精细化、个体化、按需给药,优化术后镇痛。
参考文献:
[1]Zhang L,Bao Y,Shi D.Comparing the pain of propofol via different combinations of fentanyl,sufentanil or remifentanil in gastrointestinal endoscopy[J].Acta Cir Bras,2014,29( 10) : 675-680.
[2]Jeleazcov C,Saari TI,Ihmsen H,et al.Changes in total and unbound concentrations of sufentanil during target controlled infusion for cardiac surgery with cardiopulmonary bypass[J].Br J Anaesth,2012,109( 5) : 698-706.
[3]Pruefer C,Bewlay A.Respiratory arrest with remifentanil patientcontrolled analgesia another case[J].Anaesthesia,2012,67( 9) : 1044-1045.
[4]Shafer SL,Varvel JR,Aziz N,et al.Pharmacokinetics of fentanyl administered by computer-controlled infusion pump[J].Anesthesiology,1990,73( 6) : 1091-1102.
[5]喻红辉,罗爱林,田玉科.芬太尼病人自控静脉镇痛效果的影响因素分析[J].临床麻醉学杂志,2004,20( 5) : 268-270.
[6]Kodaka M,Tsukakoshi M,Miyao H,et al.The fentanyl concentration required for immobility under propofol anesthesia is reduced by pre-treatment with flurbiprofen axetil[J].Can J Anaesth,2013,60( 12) : 1204-1211.
[7]Kamizato K,Noguchi N,Fuchigami T,et al.Utility of target controlled infusion technique for deciding the fentanyl infusion rate for post-cholecystectomy pain management in a patient on anticoagulant therapy[J].Masui,2012,61( 12) : 1362-1365.
[8]张加强,邢玉英,盂凡民.靶控输注系统的性能评价[J].国外医学:麻醉学与复苏分册,2005,5( 26) : 301-304.
[9]Dolin SJ,Cashman JN,Bland JM.Effectiveness of acute postoperative pain management: I.Evidence from published data[J].Br J Anaesth,2002,89( 3) : 409-423.
[10]Yang KS,Habib AS,Lu M,et al.A prospective evaluation of the incidence of adverse events in nurse-administered moderate sedation guided by sedation scores or Bispectral Index[J].Anesth Analg,2014,119( 1) : 43-48.
[11]Syroid ND,Johnson KB,Pace NL,et al.Response surface model predictions of emergence and response to pain in the recovery room: An evaluation of patients emerging from an isoflurane and fentanyl anesthetic[J].Anesth Analg,2010,111( 2) : 380-386.
[12]Woodhouse A,Mather LE.The minimum effective concentration of opioids: a revisitation with patient controlled analgesia fentanyl [J].Reg Anesth Pain Med,2000,25( 3) : 259-267.
收稿日期:( 2015-04-08)
文章编号:1002-266X( 2015) 30-0037-02
文献标志码:B
中图分类号:R614
doi:10.3969/j.issn.1002-266X.2015.30.014
