水体中25℃时Fe-H2O体系溶解组分优势区域图和Pourbaix图
2016-01-19黄旺银,桑世华,饶胡敏
E-mail:yyhxhwy@163.com
*通讯联系人,女,教授,博士研究生导师.主要研究方向为矿产资源与应用地球化学.E-mail:sangsh@cdut.edu.cn
水体中25 ℃时Fe-H2O体系溶解组分优势区域图和Pourbaix图
黄旺银1,2,桑世华1*,饶胡敏2
(1.成都理工大学材料与化学化工学院,四川成都610059;
2.四川省地质工程勘察院,四川成都610081)
摘要:对25 ℃不同总铁浓度时Fe-H2O体系可能存在的组分进行了热力学分析,计算了各溶解组分的浓度,运用浓度比较法为判据,确定液相和液相、液相和固相以及各固相之间的分界线,绘制了水体中不同浓度时Fe-H2O体系溶解组分优势区域图和Pourbaix图.对比不同浓度优势区域图时发现,在一定温度和压力下,总铁浓度的大小对Fe3+,Fe(OH)2+,HFeO2和的优势区域影响不大,但对,Fe(OH)+的优势区域影响明显.随着总铁浓度的减小和碱化程度的逐步加强,Fe(OH)2和Fe3O4会发生一系列复杂的质子化和聚合作用.总铁浓度越高,多核组分Fe(s),Fe3O4(s),Fe(OH)2(s)和FeOOH(s)的稳定区域越大,性质越稳定.
关键词:Fe-H2O体系;优势区域图;Pourbaix图;浓度比较法
收稿日期:2015-05-01;修改稿收到日期:2015-07-18
基金项目:国家自然科学基金资助项目(41373062);四川省科技支撑计划资助项目(2014GZ0189);四川省高校科研创新团队资助项目(15TD0009)
作者简介:黄旺银(1983—),男,甘肃天水人,博士研究生.主要研究方向为环境水体中重金属污染与防治.
中图分类号:O 646.6文献标志码:A
Predominance diagram of dissolved species and
Pourbaix diagram of Fe-H2O system in water at 25 ℃
HUANG Wang-yin1,2,SANG Shi-hua1*,RAO Hu-min2
(1.College of Materials and Chemistry & Chemical Engineering,Chengdu University of Technology,
Chengdu 610059,Sichuan,China;
2.Sichuan Institute of Geological Engineering Investigation,Chengdu 610081,Sichuan,China)
Abstract:The predominance diagram of dissolved species and a Pourbaix diagram of the Fe-H2O system in water are studied at 25 ℃ by a concentration comparison method.The concentration of dissolved species,borderlines for liquid phases or solid phases and borderlines between the solid and solid phase are calculated on the basis of thermodynamic analysis and electrochemical analysis with a total Fe concentration of CT(Fe)=1.0×10-4 mol·L-1 and CT(Fe)=1.0×10-7 mol·L-1.The predominance diagram of dissolved species and the Pourbaix diagram of the Fe-H2O system are then plotted..and Fe(OH)+.A series of hydroxylation and polymerization reactions may occur with Fe(OH)2 and Fe3O4 resulting in change the total concentration of iron and acidity.A higher total concentration of iron results in a more big area and stable for the species Fe(s),Fe3O4(s),Fe(OH)2(s)and FeOOH(s).
Key words:Fe-H2O system;predominance diagram;Pourbaix diagram;concentration comparison method
铁在自然界分布较广,是地壳含量第二高的金属元素,目前几乎在世界的每个角落都在进行铁矿的发现、冶炼、机械制造、钢铁生产、腐蚀等现象[1].环境中铁的主要来源有矿山开采、金属冶炼、工业废水、管道腐蚀等.人类的生产活动以及自然作用,使铁不断地由岩石圈向土壤、水、大气、生物转移,从而对人体的健康和环境构成潜在威胁[2-6].然而,铁在水溶液中以多种形态存在,相互间有一系列动态平衡,溶液pH值、电位的不同,铁的主要存在形态也不同.在一定温度下,水溶液中铁的浸出和沉淀分离过程主要是通过控制溶液的pH值来实现.明确给定条件下各形态铁在溶液中的优势分布区域和沉淀区,是制定铁污染控制及处理工艺的基础和前提.电势-pH图在电化学中有着很重要的意义,主要应用于分析化学、矿物地质学、生物学、核电技术、金属的腐蚀与防腐等领域[7-13],有很强的实用性.它相当于研究相平衡时的相图,是一种电化学的平衡图.可直观地反应体系中各形态物种间反应进行的可能性、生成物的稳定性、反应限度及某种组分的优势区域等重要性息.对于多价态元素铁,其在水溶液中的聚集状态及区域分布与总铁浓度和氧化还原性能息息相关.工业生产中研究高温磁黄铁矿、含铁闪锌矿及热液矿床体系的较多[14-16],25 ℃不同浓度的铁水体系电势-pH图相关文献报道较少.本文在对Fe-H2O体系可能存在的组分进行热力学分析和电化学分析的基础上,运用“浓度比较法”[17-19],计算绘制了25 ℃总铁浓度为CT(Fe)=1.0×10-4mol·L-1和1.0×10-7mol·L-1时溶解态物种优势区域图和Pourbaix图.
1Fe-H2O体系溶解组分的优势区域图
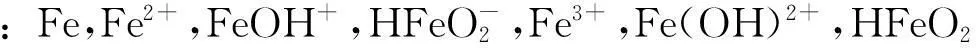

表1 Fe-H 2O体系溶解态物种间的反应
1.1独立反应的确定
Fe-H2O体系中可能存在8种含铁的溶解态物种,其对应可能的化学反应方程式有14个.各化学反应的化学计量系数可以表示为一个14×8的矩阵,称为化学计量系数矩阵,记为B:

1.2相率分析
根据相律,铁水体系自由度F的计算公式可以表示为

在Fe-H2O体系中,含有铁(Fe)元素的物种数为8,独立反应数为7,加上e-,H+,OH-和H2O,则总物质数S=12;独立的反应数R=7+1(水电离)=8;限制条件R′=1(即设定溶液的总铁浓度CT(Fe)=1.0×10-4mol·L-1或者CT(Fe)=1.0×10-7mol·L-1);相数P=1.固定温度和压力,此时“2(T,P)”项为零,则体系的自由度F=(12-8-1)-1+0=2.由此可见,一旦确定了溶液的电位值E和pH值,就能够计算出各溶解态物种的浓度.
1.3计算过程
通过矩阵转置及一系列的初等变化后得到最简矩阵,其中与线性无关的独立反应方程为表1中反应(1)~(5)式和(8)式.溶液中总铁浓度的表达式为
其中,[CFei]为第i种铁物种的浓度;ki为铁物种Fei中含有铁原子的个数.建立一个有唯一解的非线性方程组:
代入E,pH值,计算一个组分的浓度,同时根据平衡原理,得到其他组分的浓度.根据浓度比较法可确定(E,pH)所对应的优势点物种,进而可绘制各组分优势区域图.
1.4优势区域的判定
采用浓度比较法构建优势区域图,遵循的原则是:优势区中组分Fei所含有活性元素的总浓度大于其他任一组分Fej所含有活性元素的总浓度.即
其中,ki,kj为组分Fei,Fej含有铁原子的个数;CFei,CFej为浓度.即在组分Fei的优势区域内,Fei的浓度大于其他组分的浓度.当组分Fei的浓度等于组分Fej的浓度时,处于两物种优势区域的边界线上.
1.5计算结果
由浓度比较法,经编程求解,绘制得E为-2.0~2.0 V,pH为0~14范围内Fe-H2O体系在298 K,CT(Fe)=1.0×10-4mol·L-1和1.0×10-7mol·L-1时的优势区域图(图1),图中关键点数据列于表2.



图1 不同总铁浓度Fe-H 2O体系的优势区域图

序号pHE/V序号pHE/V12.17 0.770129.96-0.47222.172.000130.000.77033.230.707140.002.00043.232.000150.00-2.00059.31-0.640160.00-0.64069.31-0.3721714.00-0.71079.572.0001814.00-2.00089.57-0.4031914.002.00099.96-0.6592014.00-1.018100.00-0.728219.96-0.747119.31-0.7282214.00-1.106
2Fe-H2O体系的Pourbaix图
在25 ℃时,不考虑体系可能存在的气相组分,总铁浓度为CT(Fe)=1.0×10-4mol·L-1和1.0×10-7mol·L-1Fe-H2O体系中存在的固相有Fe(s),FeO(s),Fe2O3(s),Fe3O4(s),Fe(OH)2(s),Fe(OH)3(s)和FeOOH(s)[20-22].体系的固-液、固-固平衡方程式列于表3.

表3 Fe-H 2O体系固相平衡反应方程
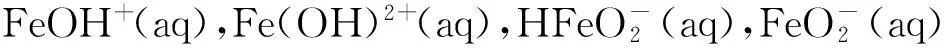

图2 1.0×10 -4mol·L -1时Fe-H 2O
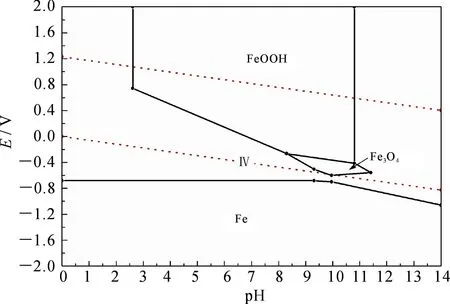
图3 1.0×10 -7mol·L -1时Fe-H 2O
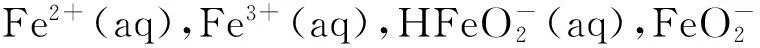
对比不同浓度Fe-H2O体系的Pourbaix图可见,体系中的固相组分以单核和多核形式存在.随着体系中总铁浓度的减小,固相组分Fe(s),Fe3O4(s)和FeOOH(s)的稳定区域明显减小,Fe(OH)2(s)稳定区域减小直至消失,而相应的溶液区域面积有所增大.由于固相Fe(s)的稳定区域横跨整个pH范围,所以当溶液中总铁浓度发生改变时,固相Fe(s)的区域基本保持不变,说明溶液中总铁浓度的变化对固相Fe(s)的影响不大.
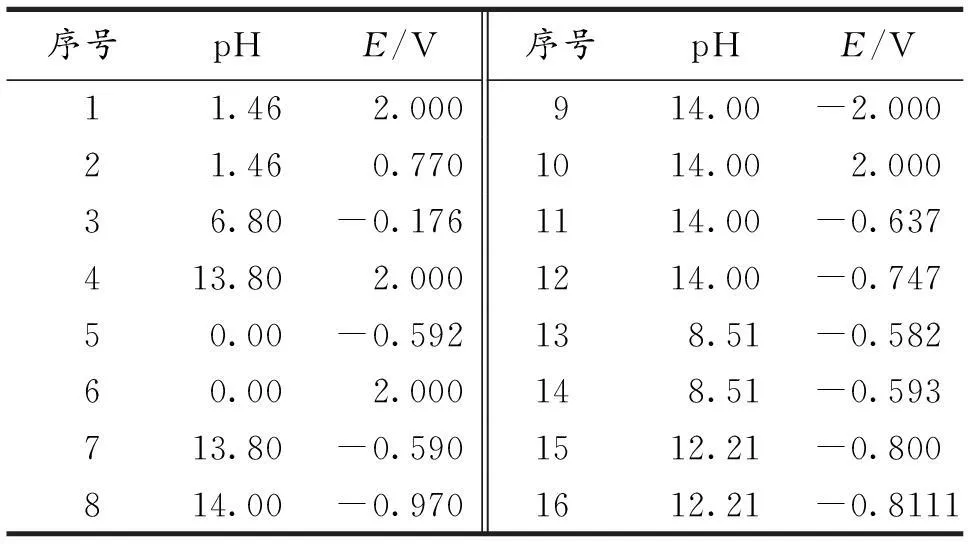
表4 C T(Fe)=1.0×10 -4 mol·L -1,Fe-H 2O体系
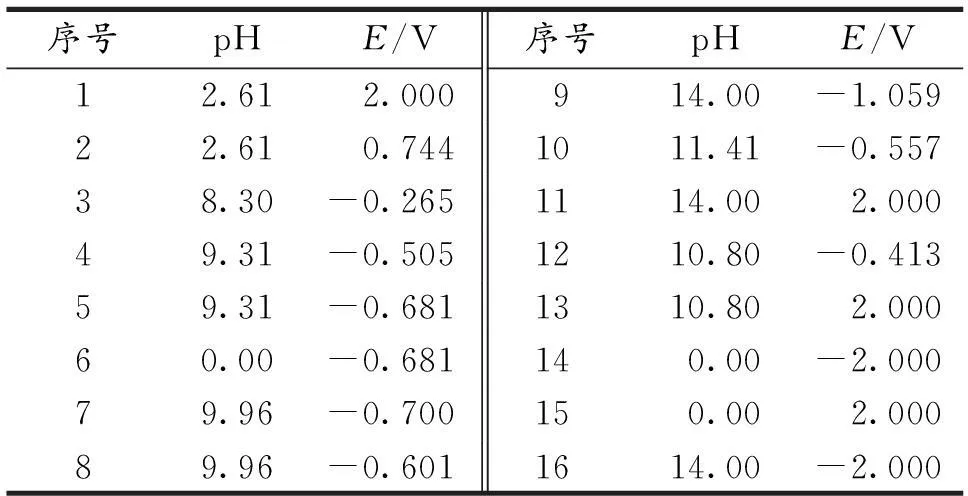
表5 在 C T(Fe)=1.0×10 -7 mol·L -1时Fe-H 2O体系
3结论

参考文献:
[1]吴吉春,张景飞,王晓蓉.水环境化学[M].北京:中国水利水电出版社,1998.
[2]黄昌勇,谢正苗,陈一定,等.皇天畈试验场地下水的砷、铁污染及自净作用[J].环境科学学报,1989,9(1):55.
[3]宋冠宇,赵杰,程从前,等.核电用奥氏体不锈钢表面铁素体污染的影响及对策[J].腐蚀与防护,2011,32(10):813.
[4]李茂东.工业锅炉铁杂质污染与控制[J].腐蚀与防护,2002,23(9):414.
[5]许胜先.天然锰砂去除工业冷却水中的锰、铁污染[J].环境工程,1999,17(1):20.
[6]曾英,马旻锐.高浓度V-H2O体系的溶解组分优势区域图和Pourbaix图[J].物理化学学报,2009,25(5):953.
[7]丁明刚,曾英,孙世林.电位-pH图及其研究进展[J].世界科技研究与发展,2005,27(3):20.
[8]马旻锐.V-Cl-H2O体系优势区域图和Pourbaix图研究[D].成都:成都理工大学,2009.
[9]梁成浩,黄乃宝,扈显琦.铜在55%LiBr溶液中的电势-pH图[J].腐蚀科学与防护技术,2006,18(3):157.
[10]吴进明.V-H2O体系的溶解组分优势区域图和电势-pH图[D].成都:成都理工大学,2007.
[11]冯其明,马运柱,王毓华,等.Eh-pH图形数据库开发与应用的现状及趋势[J].矿产保护与利用,1998(5):30.
[12]张索林,李军锁,张光宁.M-H2O体系亚稳定态物质的φ-pH图[J].中国有色金属学报,1997,7(2):50.
[13]吴玉林,徐志峰,郝士涛.炼铜烟灰碱浸脱砷的热力学及动力学[J].有色金属:冶炼部分,2013(4):3.
[14]周雍茂,刘铭.基于同时平衡原理的Fe-H2O电势-pH图[J].长沙理工大学学报(自然科学版),2004,1(2):89.
[15]WALTER J H,WU Yung-chi.Osmotic coefficients and mean activity coefficients of uniunivalent electrolytes in water at 25 ℃[J].JournalofThePhysicalChemistryReferenceData,1972,1(4):1047.
[16]何清鉴.Cu-Fe-S-O-H、Fe-S-O-H等体系Eh-pH图(150 ℃)及其在热液矿床中的应用[J].中国矿冶学院学报,1984,39(1):54.
[17]吴进明,曾英.V-H2O体系的溶解组分优势区域图和电势-pH图[J].物理化学学报,2007,23(9):1411.
[18]易清风,赵红钢,刘小平,等.Cu-S-H2O系和Zn-S-H2O系E-pH图[J].湘潭矿业学院学报,2002,17(1):51.
[19]YI Qing-feng.Withthebalanceprincipaldrawpotential-pHdiagram[M].Beijing:Chemical Industry Presss,2003.
[20]迪安J A.兰氏化学手册[M].尚文方,操时杰,辛无名,等,译.北京:科学出版社,1991.
[21]LIDE D R.CRChandbookofchemistryandphysics[M].Florida:CRC Press,2004.
[22]MILAZZO G,CAROLI S.TalbesofStandardElectrodePotentials[M].Trans.WU W C,FENG Hong-qing,WU Kai-zhi.Beijing:Science Presss,1991.
(责任编辑陆泉芳)
