氧化石墨烯对水溶液中中性红的吸附行为
2016-01-11白海鑫,刘小花,王瑾等
氧化石墨烯对水溶液中中性红的吸附行为
白海鑫1,刘小花1,王瑾2,金秋1
(1.河南农业大学 理学院,河南 郑州450002;2.河南教育学院 化学与环境学院,河南 郑州450002)
摘要:研究了氧化石墨烯(GO)对水溶液中染料中性红的吸附性能.考察了GO浓度、吸附时间等因素对吸附效果的影响,探究了动力学及热力学吸附规律.结果表明,GO对中性红具有显著、快速的去除能力,最大饱和吸附量可达到约900 mg/g,该吸附过程可用准二级吸附速率方程进行描述.不同温度下的热力学参数研究表明GO对中性红的吸附过程符合Langmuir等温吸附方程式,是一个自发、放热、熵增的过程.
关键词:氧化石墨烯;中性红;吸附动力学;吸附热力学
DOI:10.3969/j.issn.1000-1565.2015.05.006
中图分类号:O647.31文献标志码:A
收稿日期:2015-01-29
基金项目:河南省教育厅科学技术研究重点项目(13A150481);河南省高等学校青年骨干教师资助计划项目(2012GGJS-044).
Adsorption of neutral red from
aqueous solution using graphene oxide
BAI Haixin1, LIU Xiaohua1, WANG Jin2, JIN Qiu1
(1.College of Sciences, Henan Agricultural University,Zhengzhou 450002,China;
2. Department of Chemistry and Environment, Henan Institute of Education, Zhengzhou 450002,China)
Abstract:Graphene oxide (GO) was employed to be as adsorbent to remove neutral red in aqueous solution in this research. The affecting factors on the adsorption of neutral red had been investigated, including concentration of GO and adsorption time. The laws of adsorption kinetics and thermodynamics were also investigated. The results indicate that the graphene oxide has significant ability to remove neutral red quickly. The maximum adsorption capacity was 900 mg/g. The kinetic studies showed that the adsorption data could be represented by a pseudo second-order kinetic model. The adsorption isotherms measured at different temperatures show that Langmuir models could suitably describe the adsorption process with spontaneous, exothermic, entropy increase.
Key words:graphene oxide; neutral red; adsorption kinetics; adsorption thermodynamics
第一作者:白海鑫(1973-),男,河南中牟人,河南农业大学副教授,博士,主要从事材料化学研究.
E-mail:haixin_bai@aliyun.com
随着中国染料工业迅速发展,染料应用领域大大拓宽,不仅用于装点服饰、美化生活和环境,也已经成为化学工业的一个重要分支.染料大多是以化工产品合成的芳香类化合物,年产量很大,其中10%~15%被排放到废水中;染料化学性质稳定,难以降解,具有潜在的毒性及致癌作用,对人类及生态环境造成了严重的威胁.因此,工业染料废水的处理及环境水中染料污染的去除受到人们的广泛关注.多种方法[1-2]如吸附法、膜分离法、磁分离法、化学氧化法、生物法等已应用于废水中染料的去除,其中吸附法[3-5]效果较好,应用广泛.传统的吸附剂存在吸附容量低、难分离等缺点,因此,新型吸附剂材料的开发与研制成为近年来的研究热点[6].氧化石墨烯(GO)是一种新型二维碳纳米材料,具有超大的比表面积,表面有大量的含氧官能团(包括羟基、环氧基、羧基等),可以有效地吸附废水中的染料[7-11],已成为一种性能优异的新型吸附剂.
本文以中性红为模拟染料,研究了GO对中性红的吸附性能,考察了GO的用量、吸附时间等各因素对吸附的影响,对吸附等温线和吸附动力学曲线进行了分析,为GO处理印染废水提供了科学依据.
1实验部分
1.1 仪器和试剂
TU-1901紫外分光光度计(北京普析通用仪器有限责任公司);数显恒温水浴震荡器(上海巨纳科技有限公司);电热恒温水/油浴锅(常州诺基仪器有限公司);802台式离心机(金坛市恒丰仪器制造有限公司);超声波清洗仪(昆山市超声仪器有限公司).
中性红、石墨粉均购自阿拉丁试剂上海有限公司;其余试剂均为分析纯,未经纯化直接使用;实验所用水为去离子水.
1.2 GO的制备
GO的合成采用改进的Hummers法[12].称取2.0 g石墨粉和1.0 g硝酸钠加入到46 mL质量分数为98%的硫酸中,冰水浴,使温度冷却到0 ℃,强力搅拌20 min后加入10.0 g高锰酸钾.严格控制加入速度,使混合液温度不超过20 ℃,继续强力搅拌1 h.撤去冰水浴,将混合液移入35 ℃恒温水浴锅中继续搅拌1 h后停止水浴,在搅拌的条件下向反应物中加入92 mL蒸馏水,控制温度在92 ℃反应30 min.将混合液中加入280 mL蒸馏水,此时溶液的颜色为土黄色,滴入质量分数为30%双氧水后溶液变为亮黄色悬浮液.静置后,取下层沉淀,离心分离并用蒸馏水洗至中性.取离心管底部沉淀平铺于表面皿中,放入60 ℃干燥箱中烘至恒重,即得GO.
1.3 氧化石墨烯的表征
红外光谱分析(FTIR)采用Nicolet iS10傅里叶变换红外光谱仪(赛默飞世尔科技分子光谱部),扫描为400~4 000 cm-1,KBr压片法制样.X线衍射分析(XRD)采用D8 Advance X线衍射仪(德国).Cu靶(λ=0.154 18 nm),管电压40 kV,管电流40 mA.
1.4 吸附实验及分析方法
1.4.1吸附实验
准确移取20 mL一定质量浓度的中性红溶液于100 mL的锥形瓶中,加入20 mL一定质量浓度的GO分散液作为吸附剂,密封置于水浴振荡器恒温振荡吸附一定时间后,离心,取上清液,用分光光度法于530 nm波长处测定吸光度值,计算去除率.
1.4.2吸附量分析方法
采用标准曲线法将实验所测得的吸光度值换算成溶液浓度,并根据吸附前后溶液中的中性红浓度计算溶液中中性红的去除率η(%)和吸附剂GO的吸附量q(mg/g).
溶液中中性红的去除率η(%)和吸附剂的吸附量q(mg/g)可分别按式(1)和式(2)计算:
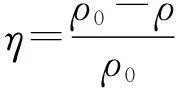
(1)
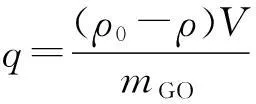
(2)
式中ρ0和ρ分别为GO与中性红混合液中中性红的初始质量浓度(mg/mL)和吸附结束时的质量浓度(mg/mL),V(mL)为混合液的总体积,mGO为GO的质量(g).
1.5 计算模型
1.5.1动力学模型
将准一级、准二级和Elovich模型[13-14]分别用于研究GO对中性红的吸附.3种动力学模型的方程表达式如下:
1)准一级动力学方程
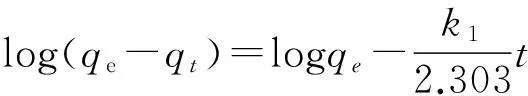
(3)
其中,k1为吸附速率常数(min-1),qt(mg/g)为t时刻的吸附量,qe为平衡吸附量(mg/g).
2)准二级动力学方程
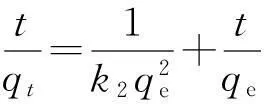
(4)
k2为准二级吸附常数g/(mg·min)
3)Elovich模型
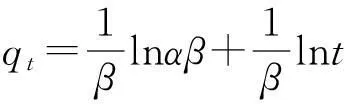
(5)
其中α是初始吸附速率mg/(g·min),β是脱附常数(g/mg).
1.5.2热力学模型
液固吸附过程采用Langmuir方程(6)和Freundlich方程(7)进行描述[15-16].

(6)
式中ρe为中性红的平衡质量浓度(mg/L),qm为饱和吸附量(mg/g);kL为经验常数,与吸附剂和吸附质之间的亲和度有关;
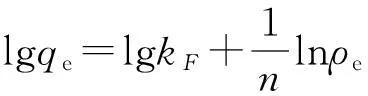
(7)
式中kF以及n为经验常数,n表示吸附发生的难易程度,kF(L/g)表示吸附剂的吸附能力.
2结果与讨论
2.1 GO的表征
图1为石墨和GO的红外光谱图.由图1可知,石墨无明显的红外吸收峰(曲线1).石墨经过氧化后,表面会出现-OH,C-O-C,C=O,COOH等多种含氧基团.因此,GO的红外光谱图(曲线2)上出现许多新的红外吸收峰.其中3 414,3 132,1 718,1 618,1 400和1 137 cm-1处的红外吸收峰分别为水分子伸缩振动、结构羟基OH伸缩振动、边缘羧基或羰基C=O伸缩振动、水分子弯曲振动、结构层羟基OH弯曲振动和片层中C-O-C伸缩振动[17].
X线衍射图(图2)中显示了GO在2θ=11.6o处的特征衍射峰[18],由Bragg方程可以计算出其晶面间距为0.76 nm,较大的晶面间距缘于氧化石墨烯上含氧官能团的存在.由于-OH和-COOH基团具有较强的亲水性,因此所合成的GO在水中具有较好的分散性及稳定性.
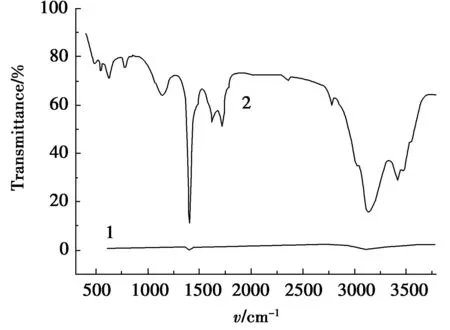
图1 石墨与GO的红处谱 Fig.1 FTIR spectra of graphite and GO
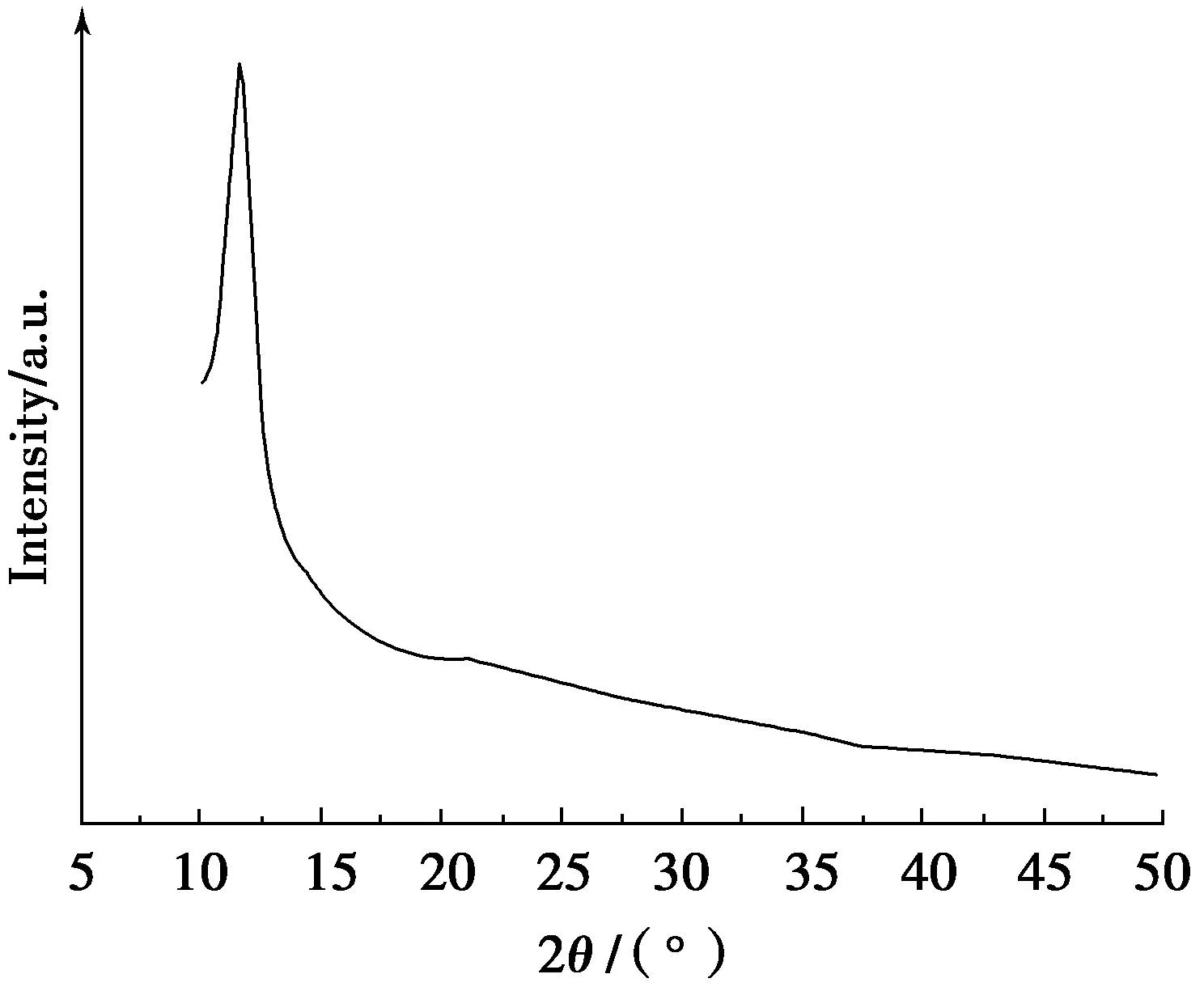
图2 GO的XRD Fig.2 RD pattern of GO
2.2 GO质量浓度对GO吸附能力的影响
研究了GO质量浓度对中性红去除率的影响,结果如表1.由表可知,当GO的质量浓度由0.2 mg/mL增大到1.0 mg/mL时,溶液中中性红的去除率也随之明显上升;随着GO的质量浓度进一步增加,去除率的上升趋于平缓并逐渐不变.因此,以下实验选择GO的质量浓度为1.0 mg/mL.

表1 GO质量浓度对中性红去除率的影响
吸附条件:0.50 mg/mL中性红,1 mg/mL GO分散液,25 ℃,震荡24 h
2.3 吸附动力学
图3为1.0 mg/mLGO吸附剂对0.5 mg/mL中性红染料的吸附动力学曲线.由图3可知GO对中性红的吸附速度非常快,吸附量在5 min内增加迅速,为快吸附阶段.吸附时间超过5 min后,吸附量缓慢增加,为慢吸附阶段.超过30 min后,吸附量基本不再变化,吸附达到平衡.如此快的吸附速度不仅取决于GO超大的比表面积,更是由于GO是均匀分散在水中的,吸附时可以与中性红充分接触,因此吸附速率非常快.这一现象在文献中也有报道[20],更有利于GO作为吸附剂在实际中的应用.

图3 吸附速率曲线 Fig.3 Adsorption kinetic curve
采用了准一级动力学方程(log(qe-qt)对t作图)、准二级动力学方程(t/qt对t作图)和Elorich模型(qt对lnt作图)进行了吸附动力学的分析,结果如图4所示.三者的线性相关系数分别为0.909 8,0.999 9和0.853 7,说明GO对水溶液中中性红的吸附符合准二级动力学吸附模型.由回归方程(t/qt=3.09×10-4+0.002 04t)的斜率以及截距可以求得qe为490.2 mg/g,与图2中的实验数据一致;k为0.012 g/(mg·min),数值较大,证明GO对中性红的吸附速率较大.

图4 GO吸附中性红的动力学拟合(a)准一级(b)准二级(c)Elovich
2.4 等温吸附研究及热力学研究
吸附等温线是指在一定温度下溶质分子在两相界面上进行的吸附过程达到平衡时它们在两相间的浓度关系曲线[21].依次在一系列20 mL不同初始质量浓度的中性红溶液中加入等体积的 1.0 mg/mL GO分散液,震荡24 h,考察了不同温度下中性红在GO上的吸附等温曲线,结果如图5.
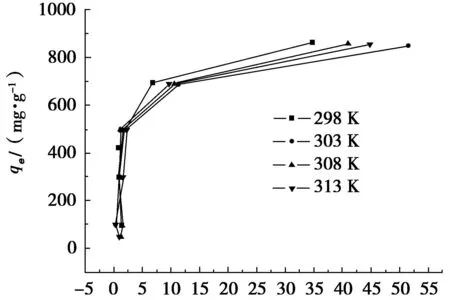
ρ e/(mg·L -1)
根据Langmuir和Freundlich模型,采用方程(6)和(7)分析了中性红在GO上的吸附等温线,结果如表2所示.Freundich线性拟合(lgqe对lgρe作图)的相关系数r明显低于Langmuir线性拟合(ρe/qe对ρe作图)的相关系数,表明GO对中性红的吸附符合Langmuir吸附方程,该吸附过程为单分子层吸附,以物理吸附为主,最大饱和吸附量约为900 mg/g.由表2可以看出,Langmuir常数b(b=kLqm)随着温度的升高而下降,由此推测中性红在GO上的吸附过程为放热过程.
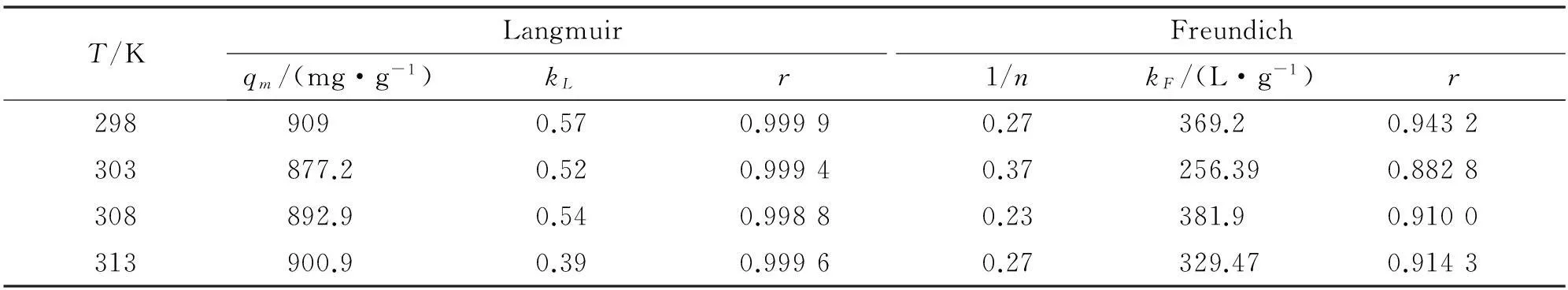
表2 Langmuir和Freundlich吸附等温线拟合结果
为判断GO对中性红的吸附过程在热力学上的可逆性,采用Langmuir常数b计算该过程的热力学参数,如ΔGθ,ΔHθ和ΔSθ,并由此评价温度对该吸附过程的影响[21].ΔGθ可以采用下述方程来计算:
ΔGθ=-RTlnb,
(8)
其中R表示理想气体常数,T表示温度(K),b(b=KLqm)为Langmuir常数.
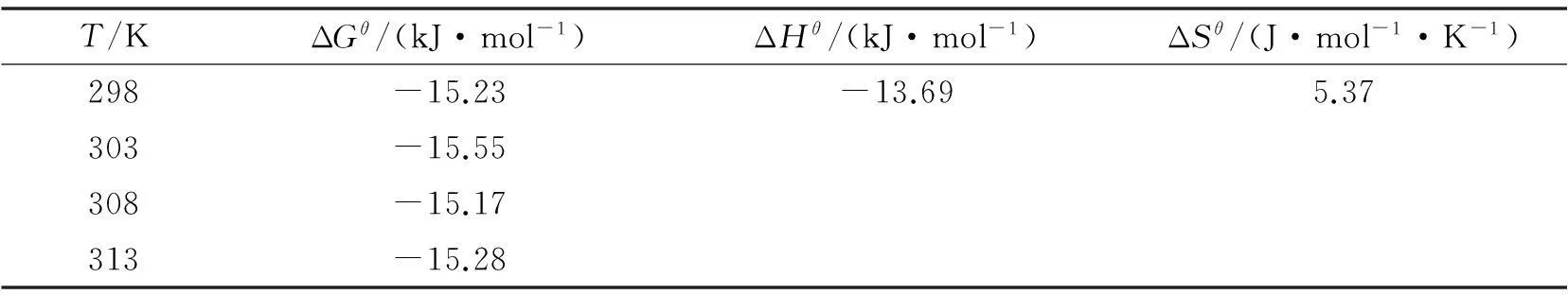
表3 热力学参数
由表3可知,GO对中性红吸附过程的ΔGθ约为-15 kJ/mol,表明此吸附过程是一个自发过程.该过程的焓变ΔHθ为-13.69 kJ/mol,证明中性红在GO上的吸附是一个放热过程,而较小的焓变说明此吸附过程为物理吸附.熵变ΔSθ为5.37 J/(mol·K),说明该过程混乱度变大.这可能是因为当中性红吸附到GO上时,水分子就会从GO上解吸下来,而水分子解析引起的熵增大于中性红吸附造成的熵减,因此总体上熵是增加的.
3结论
1)GO对中性红具有显著、快速的去除能力.实验结果表明在室温条件下,GO质量浓度为1.0 mg/mL,中性红初始质量浓度为0.5 mg/mL,吸附时间为5 min的条件下,中性红的去除率可以达到97%以上.
2)可以采用准二级吸附速率方程对GO吸附中性红进行描述,动力学参数证明GO对中性红具有较快的吸附速率.
3)Langmuir吸附等温式可较好地描述GO吸附中性红的过程,最大饱和吸附量可达到900 mg/g,为单分子层物理吸附.利用Langmuir常数进行了热力学分析,证明该吸附过程是一个自发、放热、熵增的过程.
参考文献:
[1]任南琪,周显娇,郭婉茜,等.染料废水处理技术研究进展[J].化工学报,2013,64(1):84-94.
REN Nanqi,ZHOU Xianjiao,GUO Wanqian,et al, A review on treatment methods of dye wastewater [J]. CIESC Journal, 2013, 64 (1): 84-94.
[2]FORGACS E, CSERHATI T, OROS G. Removal of synthetic dyes from wastewaters: a review [J]. Environ Int, 2004, 30: 953-971.
[3]RAFATULLAHA M, SULAIMANA O, HASHIMA, et al. Adsorption of methylene blue on low-cost adsorbents: a review [J]. J Hazard Mater, 2010, 177: 70-80.
[4]高程,黄涛,彭道平.吸附法处理印染废水的研究进展[J].能源环境保护,2014,28(1):30-34.
GAO Cheng, HUANG Tao, PENG Daoping. The research progress of adsorption method for dyeing wastewater treatment [J]. Energy Environmental Protection, 2014,28(1):30-34.
[5]陆朝阳,沈莉莉,张全兴.吸附法处理染料废水的工艺及其机理研究进展[J].工业水处理,2004,24(3):12-16.
LU Zhaoyang, SHENG Lili, ZHANG Quanxing. Research development of technics and mechanism of dye wastewater treatment by adsorption [J]. Industrial Water Treatment, 2004,24(3):12-16.
[6]赵庆松,王艳旗,代 彦,等.新型微纳米材料在染料污染吸附去除上的应用[J].天津工业大学学报,2013,32(5):33-37.
ZHAO Qingsong, WANG Yanqi, DAI Yan, et al. Utilization of new micro/nano materials as potential adsorbents for removal of dye pollutants [J]. Journal of Tianjin Polytechnic University, 2013,32(5):33-37.
[7]LI Yanhui, DU Qiuju, LIU Tonghao, et al. Comparative study of methylene blue dye adsorption onto activated carbon, graphene oxide, and carbon nanotubes [J]. Chem Eng Res Des, 2013, 91: 361-368.
[8]吕莎莎,危晶,江峰,等.羧基化石墨烯对4种离子型染料的吸附脱色[J].应用化学,2013,30(10):1215-1221.
LV Shasha,WEI Jing,JIANG Feng, et al. Adsorption-decolorization of four ionic dyes by carboxylated graphene [J]. Chinese Journal of Applied Chemistry, 2013,30(10):1215-1221.
[9]李丽霞,弓晓娟,宋金萍,等.氧化石墨及石墨烯对阳离子染料的吸附行为研究[J].分析科学学报,2014,30(3):323-326.
LI Lixia, GONG Xiaojuan, SONG Jinping, et al. Investigation of adsorption of cationic dyes on graphene oxide and graphene [J]. Journal of Analytical Science, 2014,30(3):323-326.
[10]KIM H, KANG S O, PARK S Y, et al. Adsorption isotherms and kinetics of cationic and anionic dyes on three-dimensional reduced graphene oxide macrostructure [J]. J Ind Eng Chem, 2015, 21: 1191-1196.
[11]BRADDER P, LING KINGSIE, WANG Shaobin, et a1. Dye adsorption on layered graphite oxide [J]. J Chem Eng Data, 2011, 56: 138-141.
[12]WILLIAM S, HUMMERS JR, RICHARD E O. Preparation of graphitic oxide [J]. J Am Chem Soc, 1958, 80 (6): 1339-1339.
[13]BENGUELLA B, BENAISSA H. Cadmium removal from aqueous solutions by chitin: kinetic and equilibrium studies [J]. Water Res, 2002, 36: 2463-2474.
[14]SHIEN S H, CLAYTON W R. Application of Elovich equation to the kinetics of phosphate release and sorption in soils [J]. Soil Sci Soc Am J, 1980, 44: 260-264.
[15]LANGMUIR I. The constitution and fundamental properties of solids and liquids [J]. J Am Chem Soc, 1916, 38: 2221-2295.
[16]FREUNDLICH H M F. Over the adsorption in solution [J]. J Phys Chem, 1906, 57: 385-470.
[17]万臣,彭同江,孙红娟,等.不同氧化程度氧化石墨烯的制备及湿敏性能研究[J].无机化学学报,2012,28(5):915-921.
WAN Chen, PENG Tongjiang, SUN Hongjuan, et al. Preparation and humidity-sensitive properties of graphene oxide in different oxidation degree [J]. Chinese Journal of Inorganic Chemistry, 2012,28(5):915-921.
[18]WANG Ying, XIA Guangmei, WU Cong, et al. Porous chitosan doped with graphene oxide as highly effective adsorbent for methyl orange and amido black 10B [J]. Carbohyd Polym, 2015, 115: 686-693.
[19]司文会. 核糖核酸与中性红作用机理及含量测定的研究[J]. 光谱学与光谱分析,2007,27(6):1181-1184.
SI Wenhui. Studies on the interaction between RNA with neutral red and determination of RNA by spectrophotometry [J]. Spectroscopy and Spectral Analysis, 2007, 27(6):1181-1184.
[20]YAN Han, TAO Xue, YANG Zhen, et al. Effects of the oxidation degree of graphene oxide on the adsorption of methylene blue [J]. J Hazard Mater, 2014, 268:191-198.
[21]薛继龙,钱萍萍,倪哲明.阴离子型有机化合物在LDHs上的动力学和热力学研究[J].无机化学学报,2014,30(5):1009-1016.
XUE Jilong, QIAN Pingping, NI Zheming. Kinetics and thermodynamics for znionic dye adsorption on calcined layered double hydroxides [J]. Chinese Journal of Inorganic Chemistry, 2014,30(5):1009-1016.
(责任编辑:梁俊红)
