疼痛恐惧的形成及其对疼痛知觉的影响*
2016-01-10ToddJackson黄承志
苏 琳 杨 周,Todd Jackson 陈 红 黄承志
(1西南大学认知与人格教育部重点实验室;2西南大学心理学院,重庆 400715)(3西南大学化学化工学院,重庆 400715)
1 引言
疼痛恐惧对于慢性疼痛的形成、维持与发展有重要的作用(Vlaeyen&Linton,2012)。疼痛恐惧是指个体在预期或体验组织损伤时产生的恐惧和紧张的情绪反应,伴随着疼痛即是伤害的灾难化信念或是对疼痛的负性解释(Turk&Wilson,2010;吕振勇,纪晓蕾,黄丽,Jackson,陈红,2013)。疼痛恐惧程度能够预测患者知觉到的疼痛强度(Riva,Williams,&Gallucci,2014),并能够部分调节疼痛强度对患者功能损伤的影响(Gay,Horn,Bishop,Robinson,&Bialosky,2015)。疼痛恐惧通过增强患者的疼痛敏感性和疼痛体验,引起患者回避可能诱发疼痛的活动,提高患者的抑郁和焦虑情绪水平,最终导致其滥用止痛药,丧失日常功能(Trost,France,&Thomas,2011)。
疼痛恐惧对疼痛知觉的影响得到大量临床和实证研究的支持。临床研究表明疼痛恐惧提高了患者的疼痛感受性(Crombez,Viane,Eccleston,Devulder,&Goubert,2013)。Roelofs,Peters,van der Zijden和Vlaeyen(2004)采用电子日记测量方法,考察慢性腰背痛患者的疼痛恐惧、疼痛注意以及疼痛强度之间的关系,研究发现疼痛恐惧程度与疼痛患者报告的疼痛强度呈显著正相关。对于健康群体的研究发现同样的结果 (Parr et al.,2012),Kirwilliam和Derbyshire(2008)采用疼痛线索图片启动疼痛恐惧,结果发现具有高水平疼痛恐惧的健康个体更倾向于把常温温度报告为热或疼痛。
文章首先回顾了疼痛恐惧的形成及其神经机制,再结合现今主要使用的研究范式(经典条件范式和启动范式),系统回顾了疼痛恐惧影响个体(健康个体和慢性疼痛患者)的疼痛知觉及其神经基础,以及矫正疼痛恐惧相关的认知对慢性疼痛患者的疼痛体验和功能损伤程度的影响。最后分析和总结了现有研究的主要发现以及存在的不足,并为未来研究提出方向。明晰疼痛恐惧的形成、疼痛恐惧对疼痛知觉的影响及其神经基础,对于深化当前对疼痛恐惧影响慢性疼痛的内在认知神经机制的理解具有重要理论意义。干预疼痛恐惧认知则对降低患者的疼痛感受性、改善情绪问题以及提升日常生活功能具有重要的临床实践意义。
2 疼痛恐惧的形成
2.1 疼痛恐惧的形成模型
Vlaeyen和Linton(2012)提出了疼痛恐惧的形成模型(见图1),该模型阐释了通过经典条件反射形成疼痛恐惧的过程和途径。疼痛属于非条件刺激(unconditioned stimulus,UCS),警示个体存在正在接近或真实的威胁(如身体损伤),使个体产生恐惧情绪、激活防御系统,表现出适应性行为,如相应的面部表情、生理唤醒、高度警觉等,并产生逃离或回避行为。在适应性行为发展过程中,个体通过中性线索即条件刺激(conditioned stimulus,CS)与UCS的连接,建立起CS与UCS一致性关系的认知,从而学会对CS做出条件性反应(conditioned response,CR)。疼痛恐惧情绪引起的保护性行为可以使个体免受伤害。但对于慢性疼痛患者,疼痛恐惧情绪引起的持续性的保护性行为反而会加强CS与UCS的连接,导致个体的疼痛恐惧水平提升,形成疼痛恐惧-回避的恶性循环,最终引起患者滥用止痛药、丧失日常功能等严重后果。在疼痛恐惧的形成过程中,CS形态主要包括外部型(如颜色信号)、内部型(如心悸、胃肠感觉、轻微疼痛以及关节僵硬等)(Gramsch et al.,2014;Icenhour et al.,2015)和本体型(如因运动产生的骨骼肌肉痛)(Meulders,Vansteenwegen,&Vlaeyen,2011)。疼痛恐惧的形成途径包括直接经验、观察学习和替代学习(吕振勇等,2013)。该模型也阐释了疼痛恐惧的消退途径。通过只给予个体CS且不施加UCS的方法,可以降低个体对CS与UCS一致性关系的认知,逐渐减少或消除个体对CS做出条件性反应。
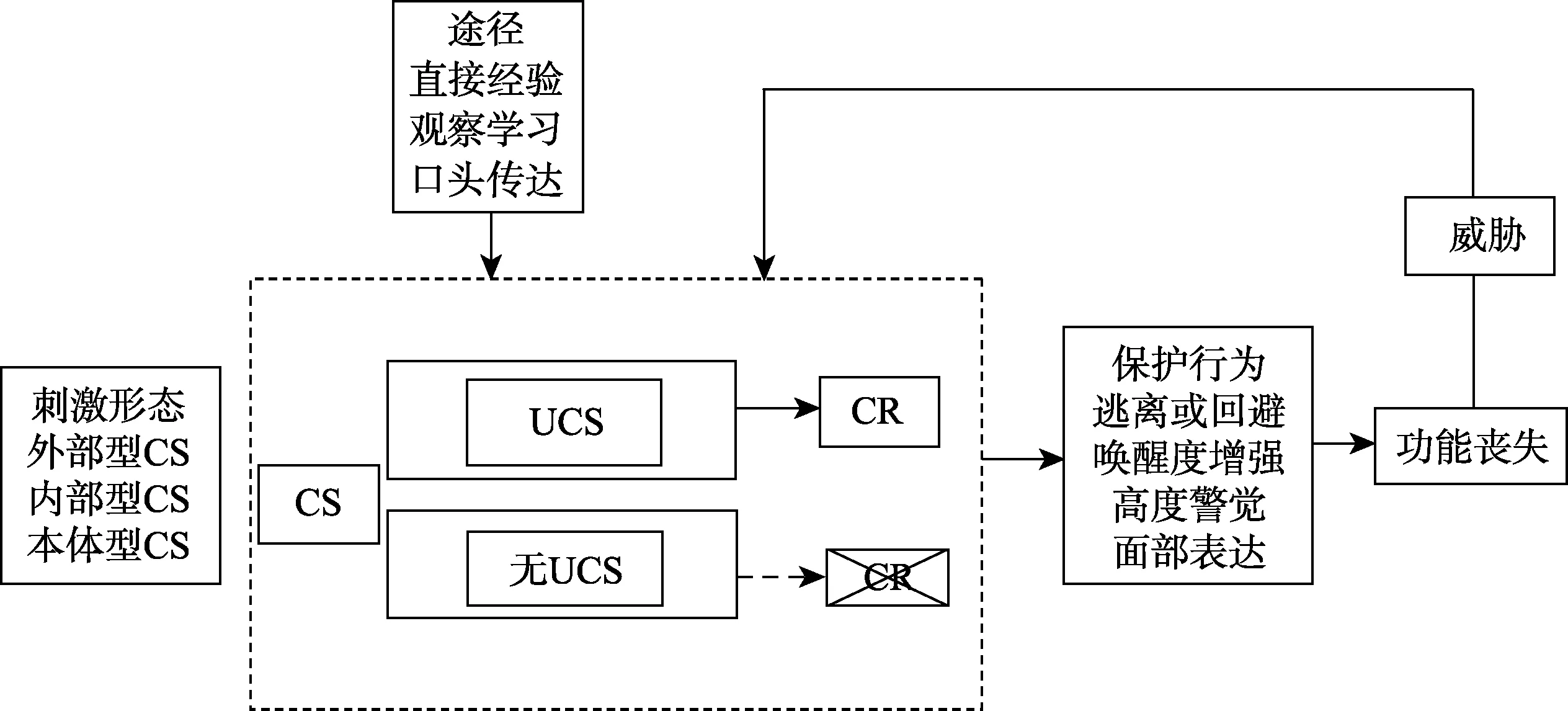
图1 疼痛恐惧的形成与消退模型,包括刺激形态、保护行为和形成路径注:CS:条件性刺激;UCS:无条件刺激;CR:条件性反应(资料来源:Vlaeyen&Linton,2012)
2.2 疼痛恐惧形成的神经基础
研究者们常采用经典条件反射任务探究个体有意识形成疼痛恐惧的神经基础。该任务通过事先告知个体CS和UCS之间存在一致性关系,使个体有意识地学会对CS做出条件性反应,从而形成疼痛恐惧。通过测量个体在此过程中大脑的活动情况,探究个体有意识形成疼痛恐惧的神经基础。Funayama,Grillon,Davis和Phelps(2001)通过指导语让被试学会对CS产生恐惧反应,发现在此过程中左半球杏仁核起着重要的调节作用。在疼痛恐惧形成的研究中,通过实时追踪记录被试在评定电击期望水平时的大脑激活情况,发现被试对CS-UCS的一致性认识与双侧前额叶皮层中部和海马旁回的激活相关,而更强的皮肤电反应与杏仁核的激活有关(Carter,O'Doherty,Seymour,Koch,&Dolan,2006)。有意识地疼痛恐惧形成还与中部腹背侧前额叶的激活存在稳定相关(Mechias,Etkin,&Kalisch,2010)。Gramsch 等人(2014)的研究进一步证实,在疼痛恐惧形成过程中伴随着前额叶皮层、杏仁核和脑岛的激活。因此,有意识形成疼痛恐惧的神经基础主要在于前额叶皮层、杏仁核及脑岛。前额皮层调控注意,在个体准备接受疼痛刺激时,主要负责整合对疼痛刺激的预期和提高对刺激的认知评价,杏仁核参与了疼痛恐惧相关情绪的唤醒和对威胁性刺激的选择性注意(Icenhour et al.,2015),而前脑岛的激活使个体能够自动对即将到来的厌恶刺激进行准备 (Knight,Waters,&Bandettini,2009)。
研究者们同样使用经典条件反射任务探究个体无意识形成疼痛恐惧的神经基础。该任务通过工作记忆等认知干扰活动,让个体意识不到CS与UCS之间的一致性关系。个体无意间建立起CS与UCS的一致性连接,对CS也做出条件反应,因此在无意识情况下形成疼痛恐惧。通过测量此过程中个体的大脑活动情况,探究个体无意识形成疼痛恐惧的神经基础。无意识和有意识疼痛恐惧形成的神经基础存在着异同。差异性方面,Klucken等人(2009)在无意识地条件恐惧形成研究中发现,与没有获得一致性认识组相比,意外获得一致性认识组具有更强烈的伏隔核激活。Knight等(2009)在疼痛恐惧习得研究中,通过阈上和阈下呈现条件刺激操作被试习得恐惧时的意识卷入程度。结果发现,仅在阈上呈现条件下,被试对电击期望的评定与海马、海马旁回以及后扣带回的激活有关。相似性方面,Tabbert,Stark,Kirsch和Vaitl(2006)比较了有意识习得疼痛恐惧组与无意识习得组,发现前者的激活脑区包括中部腹背侧前额叶、颞叶以及顶叶,但是激活水平并不显著高于无意识组。与有意识形成疼痛恐惧相关的脑区,如杏仁核、眶额叶皮层、左侧脑岛和丘脑等,也与无意识形成疼痛恐惧有关(Knight et al.,2009;Tabbert et al.,2006)。来自动物学模型的研究也为疼痛恐惧形成的神经机制提供了证据。研究者使用足底电击诱导条件性位置回避(shock- induced conditioned place avoidance,S-CPA)模型,发现仅在注射微量兴奋性毒素损毁大鼠的杏仁核后,S-CPA的程度降低,结果显示杏仁核参与疼痛相关的恐惧和厌恶情绪的产生(高永静,2004)。无意识和有意识疼痛恐惧形成过程中,共同且稳定激活的脑区主要在于脑岛和杏仁核。因此,脑岛和杏仁核是疼痛恐惧形成的重要神经网络中心。
3 疼痛恐惧影响疼痛知觉
近年来,研究者们主要采用经典条件反射范式和启动范式研究疼痛恐惧对疼痛知觉的影响。经典条件反射范式通过CS与UCS的配对训练,测量疼痛恐惧对个体疼痛知觉的影响(Klinger et al.,2010;Williams&Rhudy,2007)。启动范式采用声音、图片和指导语等方式启动疼痛恐惧,考察疼痛恐惧对个体疼痛感受性的影响(Jackson et al.,2005;Kirwilliam&Derbyshire,2008)。在疼痛恐惧影响疼痛知觉的研究中,研究者们常采用的疼痛刺激类型包括冷压痛、温度刺激、辐射热和电刺激等。
3.1 对健康个体的研究
有研究表明疼痛恐惧程度与疼痛强度呈显著正相关,即疼痛恐惧程度显著预测了个体的疼痛感受和报告的疼痛强度(George,Dannecker,&Robinson,2006;Hirsh,George, Bialosky,&Robinson,2008;张西磊,Jackson,陈红,杨周,2014),增强了个体对疼痛刺激的敏感性和疼痛体验(Parr et al.,2012)。Roelofs等(2004)发现焦虑、疼痛警惕和疼痛灾难化作为疼痛恐惧的重要指标,也与疼痛强度呈正相关。Ploner,Lee,Wiech,Bingel和Tracey(2010)发现被试在状态-特质焦虑(State-Trait Anxiety Inventory,STAI)与疼痛警惕和觉知(Pain Vigilance and Awareness Questionnaire,PVAQ)上的得分与其疼痛阈限值呈显著负相关,即特质焦虑水平和疼痛警惕程度越高的个体,越倾向于将低强度的热刺激判断为疼痛。一项基于疼痛诱导模型的心理结构时间评估研究,为疼痛恐惧与疼痛知觉的正相关关系提供了新的证据。这项研究通过锻炼诱发伤害模型,发现受伤前的疼痛恐惧得分预测了从基线到96小时的疼痛强度(Parr et al.,2012)。
实验研究为状态性疼痛恐惧促进个体疼痛知觉提供了证据。Williams和Rhudy(2007)采用经典条件反射范式,以恐惧和快乐面部表情图片作为CS,厌恶性电刺激作为UCS,在CS与UCS的配对训练后,研究发现被试在恐惧表情面孔条件下的疼痛阈限更低,即被试受到电刺激后手指回缩的时间更短,表现出痛觉过敏(hyperalgesia)反应。Wiech等人(2010)通过口头指导语启动恐惧情绪,即事先告知被试深灰色圆圈代表威胁位置,在相应位置施加辐射热刺激可能导致皮肤损伤,浅灰色圆圈代表安全位置,在相应位置施加辐射热刺激已经过充分测定,非常安全。研究结果表明被试将更多的威胁位置的近阈限刺激评定为疼痛,对疼痛强度的评分更高,体验到的焦虑水平也更高。
但是,也有研究发现疼痛恐惧降低了个体对疼痛刺激的感受性。Rhudy和Meagher(2000)通过给予被试重复电刺激启动被试强烈的疼痛恐惧情绪,之后再测量被试的热辐射痛阈限(radiant heat pain threshold),即被试从接受热刺激到感觉到疼痛(手指回缩)的时间。结果发现实验组被试的手指回缩反射时间比控制组的长,表明恐惧情绪降低了个体对疼痛刺激的感受性。也有研究表明疼痛恐惧不影响个体的疼痛知觉。de Wied和Verbaten(2001)采用带有疼痛信息的负性情绪图片启动疼痛恐惧情绪,测量疼痛恐惧对被试感知冷压痛的影响。研究发现与疼痛图片启动条件下忍耐疼痛的时间相比,非疼痛图片启动下个体忍耐疼痛的时间更长,但是在个体报告的疼痛强度上没有显著差异。Jackson等人(2005)通过给予被试关于冷压痛(cold pressor task,CPT)的冻伤信息和安全信息,启动被试对冷压痛的威胁性认知(即恐惧认知)和安全性认知,控制组则阅读疼痛知识。研究表明疼痛恐惧减少了个体忍耐疼痛的时间,但对个体报告所感受到的疼痛强度没有影响。Boston和Sharpe(2005)采用口头告知的方法启动被试对冷压任务的威胁性和安全性认知,测量威胁认知对冷压痛阈限(即刚感觉到疼痛所需要的时间)和忍耐疼痛时间的影响。研究发现威胁性疼痛认知减少了个体忍耐疼痛的时间,但对疼痛阈限和疼痛强度没有影响。
综上所述,疼痛恐惧对疼痛知觉的影响在健康群体中的研究结果不一。原因可能在于这些研究使用了图片、口头叙述、电击等不同的疼痛恐惧启动方法,诱发出的疼痛恐惧水平可能不同。有研究者认为,适中的疼痛恐惧水平会增强疼痛知觉,而高疼痛恐惧会降低个体对疼痛的知觉(吕振勇等,2013)。观察到疼痛恐惧促进了疼痛知觉的研究,可能是因为图片、口头叙述等方式诱发出的是适中的疼痛恐惧水平。观察到疼痛恐惧降低疼痛知觉的研究,则可能是因为重复电刺激诱导出的是高水平的疼痛恐惧(Rhudy&Meagher,2000)。有研究者指出疼痛恐惧对疼痛知觉的影响取决于疼痛刺激的类型以及刺激的持续时间(Jackson,Chen,Iezzi,Yee,&Chen,2014)。因此,研究中使用的不同疼痛刺激类型是导致研究结果不一的重要因素。上述研究中,使用电刺激和辐射热刺激的研究表明疼痛恐惧对个体的疼痛感受性有影响,而使用冷压痛刺激的研究,均发现疼痛恐惧不影响个体的疼痛感受性,但对个体的疼痛忍耐力具有显著影响。
3.2 对慢性疼痛患者的研究
疼痛恐惧影响疼痛知觉的研究结果在慢性疼痛患者中较为一致,表现为疼痛恐惧促进个体疼痛知觉。临床研究表明,慢性疼痛患者中的高疼痛恐惧者表现出对疼痛刺激更高的敏感性,报告更高的疼痛强度、消极情绪和功能丧失程度(Crombez et al.,2013;Peters,Vlaeyen,&van Drunen,2000;Roelofs et al.,2004)。疼痛恐惧增加了患者肌肉紧张和生理唤醒,从而加剧和维持了患者的疼痛感受(Gatchel,Peng,Peters,Fuchs,&Turk,2007;Kirmani,Jehan,& Sanam,2015;Lindstroem,Graven-Nielsen,&Falla,2012)。疼痛恐惧显著预测了纤维肌肉痛患者感受到的疼痛强度(Sánchez,Martínez,Miró,&Medina,2011)。实验研究中,采用问卷测量的特质性疼痛恐惧水平越高的肩痛患者,在冷压任务中对疼痛敏感性越强,疼痛恐惧程度与被试报告的冷压痛强度呈正相关,与被试忍耐疼痛的时间和疼痛阈限呈负相关(George& Hirsh,2009)。Kirwilliam 和Derbyshire(2008)的研究让被试需完成以疼痛图片和中性图片为材料的点探测任务,即在疼痛和中性图片对呈现后,在疼痛或中性图片的位置上出现探测点,被试需对探测点出现的位置进行又快又准地按键反应,以此启动患者的状态性疼痛恐惧情绪,结合热刺激探测任务,考察疼痛恐惧对慢性疼痛患者疼痛知觉的影响。结果表明疼痛恐惧显著促进了患者对不同温度下的热和疼痛刺激的知觉。
对慢性疼痛患者的研究表明疼痛恐惧促进了慢性疼痛患者的疼痛感受性。研究结果较一致的原因可能在于,上述第一项实验研究考察的是特质性疼痛恐惧对慢性疼痛患者疼痛感受性的影响。较之实验室条件下启动的健康个体的状态性疼痛恐惧水平,具有更好的稳定性。上述第二项启动疼痛恐惧情绪的研究也发现疼痛恐惧对慢性疼痛患者疼痛感受性的促进,这可能与样本特征密切相关。研究者们指出,较之健康个体,慢性疼痛患者对疼痛或疼痛线索具有更高的敏感性(Crombez et al.,2013;Kirwilliam&Derbyshire,2008)。另外,目前考察疼痛恐惧影响慢性疼痛患者的疼痛知觉的实验研究较少。因此,对于慢性疼痛患者而言,疼痛恐惧对个体在其它疼痛刺激类型情况下的感受性是否也有影响尚未可知。
4 疼痛恐惧影响疼痛知觉的神经基础
近几年,研究者们采用事件相关电位(eventrelated potential,ERP)和功能磁共振成像(functional Magnetic Resonance Imaging,fMRI)技术,考察了疼痛恐惧影响疼痛知觉的神经基础。ERP研究方面,Lyby,Aslaksen和Flaten(2011)发现疼痛恐惧与P2成分有关。N2/P2成分反映了疼痛强度以及个体对疼痛的感觉,该成分峰值出现在疼痛刺激施加后的250~350毫秒,与前扣带回的激活有关,而前扣带回是加工疼痛情感成分的重要脑区(Garcia-Larrea,Frot,&Valeriani,2003),也是疼痛过程中调节恐惧回避的特殊区域(Vogt,2005)。fMRI研究表明,情绪或认知影响疼痛感受的过程与前额叶和扣带回区域的结构或功能变化有关(Elsenbruch,2011),其中疼痛恐惧对疼痛知觉的影响与前扣带回、内侧前额皮层和杏仁核有关(Lumley et al.,2011)。Ochsner等人(2006)发现, 疼痛恐惧在个体体验疼痛过程中预测了扣带回前部和后部区域的激活,当疼痛恐惧提高疼痛知觉时伴随着前扣带回、眶额叶皮层、脑岛和海马区域的激活(Seifert&Maihöfner,2009)。故疼痛恐惧影响疼痛知觉的神经基础主要在于前扣带回,及其与前额叶、脑岛等区域的功能连接。扣带回中部和前脑岛的功能连接反映了个体对疼痛的威胁性认知,而前额叶区域的作用可能在于促进痛觉信号的传输 (Wiech et al.,2010)。另一方面,杏仁核通过改变感觉皮层的输入信号(Zaman,Vlaeyen,van Oudenhove,Wiech,&van Diest,2015),以及通过眶额叶皮层等脑区间接调节个体的疼痛知觉(Pourtois,Schettino,&Vuilleumier,2013),导致个体出现更强的疼痛知觉。因此,疼痛恐惧影响疼痛知觉的神经基础主要在于杏仁核、脑岛、前额皮层和前扣带回。其中,杏仁核和脑岛也是疼痛恐惧形成的关键脑区。
5 认知干预疼痛恐惧对疼痛知觉的影响
降低疼痛恐惧水平能有效改善患者的疼痛体验和功能损伤。临床慢性疼痛治疗中,也将疼痛恐惧作为了治疗目标(Zale&Ditre,2015)。当前较为流行的方法是通过认知干预降低对疼痛的过度恐惧(Linton&Shaw,2011)。最为常用的是认知行为疗法(cognitive behavioral therapy,CBT),该方法通过改变患者不合理的恐惧-回避信念,降低患者过度的疼痛恐惧和疼痛体验,改善患者的日常功能(Zale&Ditre,2015)。在实验研究中,Vowles和Gross(2003)的研究发现,接受CBT的慢性疼痛患者,其疼痛恐惧情绪和疼痛水平较之治疗前均有显著降低,参与日常工作的能力也得到显著提高。一项纵向研究表明,经过治疗后,患者报告的疼痛恐惧、疼痛强度、疼痛警觉和功能损伤水平有显著降低,而身体活动水平显著提高(Vlaeyen,de Jong,Onghena,Kerckhoffs-Hanssen,&Kole-Snijders,2002)。认知再评价可以降低被试对疼痛信息的过度恐惧,从而改变对疼痛的感受性。有研究者进一步探究了认知再评价过程中伴随着的脑活动情况。Ochsner,Bunge,Gross和Gabrieli(2002)发现当被试对引发疼痛恐惧的信息进行认知再评价时,内外侧前额皮层激活,而杏仁核和内侧眶额叶皮层活动受到抑制。
另外,降低疼痛恐惧的方法还包括暴露疗法、条件反射的消退以及正念导向的恢复增强疗法等。逐步暴露疗法是通过给疼痛相关刺激建立强度等级,让患者依等级逐步暴露在不同刺激情境中,使之产生耐受性,从而逐渐降低患者对疼痛的过度恐惧。近年来也有研究从疼痛恐惧形成的角度入手,通过条件反射消退个体对疼痛信号的恐惧,即以新的联系替代原有的联系,通过在给予中性条件刺激后不伴随疼痛的非条件刺激,从而降低和消退被试对疼痛信号的恐惧(Meulders et al.,2011;Meulders,Vansteenwegen,&Vlaeyen,2012)。以往对恐惧消退的研究中发现,杏仁核是恐惧习得和消退的关键脑区(Greco&Liberzon,2016)。在疼痛相关恐惧消退的研究中,发现除了杏仁核,腹内侧前额皮层也有显著激活。杏仁核被认为在早期习得CS与无UCS连接过程中起作用,而腹内侧前额皮层的作用在于维持疼痛恐惧的消退效果(Phelps,Delgado,Nearing,&LeDoux,2004)。另外,最近发展出的正念导向的恢复增强疗法(Mindfulness-Oriented Recovery Enhancement)被认为能够降低慢性疼痛患者对疼痛的过度恐惧,引发患者的积极情绪,治疗患者的药物依赖(Garland,2014)。在临床实践中,多种疗法相结合能够起到更优化的效果,有研究者将CBT,放松训练和生物反馈三者结合起来。CBT可以通过自我教育降低疼痛恐惧,放松训练和生物反馈可以帮助患者减少肌肉紧张,控制压力从而降低患者的疼痛感受(Kirmani et al.,2015)。
6 小结与展望
疼痛恐惧影响疼痛知觉因被试类型、疼痛恐惧的启动方法以及疼痛刺激类型而异。疼痛恐惧对健康群体的疼痛知觉的影响结果不一,主要原因与疼痛恐惧的启动方法有关。重复电击诱发出的高水平疼痛恐惧降低了疼痛感受性,图片、口头叙述等方法诱发出的适度疼痛恐惧水平促进了疼痛感受性。在慢性疼痛患者中取得的结果较为一致,疼痛恐惧促进了慢性疼痛患者的疼痛感受性。这与疼痛恐惧的特质性和状态性,以及慢性疼痛患者的高疼痛敏感性有关。关于疼痛恐惧影响疼痛知觉的研究存在着不足,未来研究需进一步考察的内容主要集中在以下几个方面。
首先,在未来研究中应同时考虑疼痛恐惧的特质性和状态性。疼痛恐惧的研究有两类测量方法。一类是特质性疼痛恐惧,即把疼痛恐惧作为一种人格特质,测量时使用疼痛恐惧问卷(the Fear ofPain Questionnaire-III,FPQ-III)(McNeil&Rainwater,1998;杨周,孟景,Jackson,陈红,2013)。有研究发现具有高焦虑特质的个体更容易维持疼痛体验,并对慢性疼痛具有易感性(Tracey,2011)。但也有研究者提出仅是个体的焦虑敏感性而非焦虑特质与其疼痛耐受性存在相关(Thibodeau,Welch,Katz,&Asmundson,2013)。另一类是状态性疼痛恐惧,即在特定情境下的疼痛恐惧情绪,通过个体的皮肤电反应、眨眼惊吓肌电和心率等生理指标加以测量(Meulders et al.,2012),在实验室和临床研究中,两者可能共同影响个体对于疼痛刺激的知觉。未来研究应同时考虑特质性与状态性疼痛恐惧,以及二者之间的相互作用是如何影响个体加工疼痛信息时的感受性。
其次,对疼痛恐惧的评估应更加准确。在目前的研究中,多采用量表和生理指标测量个体的疼痛恐惧唤醒程度,量表多是根据慢性疼痛病人的特点编制的(Suhr&Spickard,2012),对于一般群体的研究并不能够完全适应,并且有研究者认为,当前使用的测量疼痛恐惧的量表,其因素结构还存在争议,并且个体对恐惧程度的报告会受到主观因素影响使效度降低(Lumley et al.,2011)。在生理指标上,当前也没有具体标准表示疼痛恐惧的唤醒水平。未来需要拓展对疼痛恐惧的测量方法,以使研究获得更高的效度。
最后,在研究疼痛恐惧影响疼痛知觉的神经机制上,fMRI技术的发展促进了疼痛恐惧影响知觉偏向的研究,脑岛、杏仁核、前额皮层和前扣带回是疼痛恐惧影响疼痛知觉的重要神经基础。但目前对此仍存在争议,因为在疼痛恐惧影响疼痛知觉的过程中,会产生注意、记忆等认知过程和焦虑等消极情绪并激活相应脑区(孟景,沈林,Jackson,陈红,2011),所以关于疼痛恐惧影响疼痛知觉偏向的神经生理机制还不明晰。此外,当前对疼痛恐惧影响慢性疼痛患者知觉偏向相关的神经机制研究几乎没有,有研究发现慢性疼痛患者与健康人群在神经结构和功能上存在一定差异,慢性背痛患者表现出前额叶和前脑岛灰质的减少,这可能会影响患者对痛觉的感受性(Fritz et al.,2016)。未来研究应进一步揭示疼痛恐惧影响慢性疼痛病人的疼痛知觉的神经基础。
高永静.(2004).大鼠前扣带皮层参与痛厌恶情绪的神经机制研究(博士学位论文).复旦大学,上海.
吕振勇,纪晓蕾,黄丽,Jackson,T.,陈红.(2013).疼痛恐惧对疼痛的影响及其认知机制.心理科学进展,21(5),817-826.
孟景,沈林,Jackson,T.,陈红.(2011).疼痛对心理的影响及其机制.心理科学进展,19(10),1493-1501.
杨周,孟景,Jackson,T.,陈红.(2013).中文版疼痛恐惧问卷-Ⅲ的信效度.中国临床心理学杂志,21(5),768-770.
张西磊,Jackson,T.,陈红,杨周.(2014).恐惧的代价:疼痛恐惧,心理忧虑和躯体化对疼痛感知预测作用的比较.心理科学,37,53-59.
Boston,A.,& Sharpe,L.(2005).The role ofthreatexpectancy in acute pain:Effects on attentional bias,coping strategy effectiveness and response to pain.Pain,119(1-3),168-175.
Carter,R.M.,O'Doherty,J.P.,Seymour,B.,Koch,C.,&Dolan,R.J.(2006).Contingency awareness in human aversive conditioning involves the middle frontal gyrus.Neuroimage,29(3),1007-1012.
Crombez,G.,Viane,I.,Eccleston,C.,Devulder,J.,&Goubert,L.(2013).Attention to pain and fear of pain in patients with chronic pain.Journal of Behavioral Medicine,36(4),371-378.
de Wied,M.,&Verbaten,M.N.(2001).Affective pictures processing, attention, and pain tolerance.Pain,90(1),163-172.
Elsenbruch,S.(2011).Abdominal pain in Irritable Bowel Syndrome:A review of putative psychological,neural and neuro-immune mechanisms.Brain,Behavior,and Immunity,25(3),386-394.
Fritz,H.C.,McAuley,J.H.,Wittfeld,K.,Hegenscheid,K.,Schmidt,C.O.,Langner,S.,&Lotze,M.(2016).Chronic back pain is associated with decreased prefrontal and anterior insular gray matter:Results from a populationbased cohort study.The Journal of Pain,17,111-118.
Funayama,E.S.,Grillon,C.,Davis,M.,&Phelps,E.A.(2001).A double dissociation in the affective modulation of startle in humans:Effects of unilateral temporal lobectomy.Journal of Cognitive Neuroscience,13(6),721-729.
Garcia-Larrea,L.,Frot,M.,&Valeriani,M.(2003).Brain generatorsof laser-evoked potentials:From dipoles to functional significance.Neurophysiologie Clinique/Clinical Neurophysiology,33(6),279-292.
Garland,E.L.(2014).Treating chronic pain:The need for non-opioid options.Expert Review of Clinical Pharmacology,7(5),545-550.
Gatchel,R.J.,Peng,Y.B.,Peters,M.L.,Fuchs,P.N.,&Turk,D.C.(2007).The biopsychosocial approach to chronic pain:Scientific advances and future directions.Psychological Bulletin,133(4),581-624.
Gay,C.W.,Horn,M.E.,Bishop,M.D.,Robinson,M.E.,&Bialosky, J. E. (2015). Investigating dynamic pain sensitivity in the context of the fear-avoidance model.European Journal of Pain,19(1),48-58.
George,S.Z.,Dannecker,E.A.,&Robinson,M.E.(2006).Fear of pain,not pain catastrophizing,predicts acute pain intensity,but neither factor predicts tolerance or blood pressure reactivity:An experimental investigation in painfree individuals.European Journal of Pain,10(5),457.
George,S.Z.,&Hirsh,A.T.(2009).Psychologic influence on experimental pain sensitivity and clinical pain intensity for patients with shoulder pain.The Journal of Pain,10(3),293-299.
Gramsch,C.,Kattoor,J.,Icenhour,A.,Forsting, M.,Schedlowski,M.,Gizewski,E.R.,& Elsenbruch,S.(2014).Learning pain-related fear:Neural mechanisms mediating rapid differential conditioning,extinction and reinstatement processes in human visceral pain.Neurobiology of Learning and Memory,116,36-45.
Greco,J.A.,& Liberzon,I.(2016).Neuroimaging of fear-associated learning.Neuropsychopharmacology,41(1),320-334.
Hirsh,A.T.,George,S.Z.,Bialosky,J.E.,&Robinson,M.E.(2008).Fear of pain,pain catastrophizing,and acute pain perception: Relative prediction and timing of assessment.The Journal of Pain,9(9),806-812.
Icenhour,A.,Langhorst,J.,Benson,S.,Schlamann,M.,Hampel,S.,Engler,H.,...Elsenbruch,S.(2015).Neural circuitry ofabdominalpain-related fearlearning and reinstatement in irritable bowel syndrome.Neurogastroenterology&Motility,27(1),114-127.
Jackson,T.,Chen,H.,Iezzi,T.,Yee,M.,&Chen,F.G.(2014).Prevalence and correlates of chronic pain in a random population study of adults in Chongqing,China.The Clinical Journal of Pain,30(4),346-352.
Jackson,T.,Pope,L.,Nagasaka,T.,Fritch,A.,Iezzi,T.,&Chen,H.(2005).The impact of threatening information about pain on coping and pain tolerance.British Journal of Health Psychology,10(3),441-451.
Kirmani, M. N., Jehan, F., & Sanam, R. (2015).Psychological interventions in pain management.The Internatioal Jounal of Indian Psychology,2(3),159-174.
Kirwilliam,S.S.,&Derbyshire,S.W.G.(2008).Increased bias to report heat or pain following emotional priming of pain-related fear.PAIN®,137(1),60-65.
Klinger,R.,Matter,N.,Kothe,R.,Dahme,B.,Hofmann,U.G.,&Krug,F.(2010).Unconditioned and conditioned muscular responses in patients with chronic back pain and chronic tension-type headaches and in healthy controls.Pain,150(1),66-74.
Klucken,T.,Kagerer,S.,Schweckendiek,J.,Tabbert,K.,Vaitl,D.,&Stark,R.(2009).Neural,electrodermal and behavioral response patterns in contingency aware and unaware subjects during a picture-picture conditioning paradigm.Neuroscience,158(2),721-731.
Knight,D.C.,Waters,N.S.,&Bandettini,P.A.(2009).Neural substrates of explicit and implicit fear memory.Neuroimage,45(1),208-214.
Lindstroem,R.,Graven-Nielsen,T.,& Falla,D.(2012).Currentpain and fearofpain contribute to reduced maximum voluntary contraction of neck muscles in patients with chronic neck pain.Archives of Physical Medicine and Rehabilitation,93(11),2042-2048.
Linton,S.J.,&Shaw,W.S.(2011).Impact of psychological factors in the experience of pain.Physical Therapy,91(5),700-711.
Lumley,M.A.,Cohen,J.L.,Borszcz,G.S.,Cano,A.,Radcliffe,A.M.,Porter,L.S.,...Keefe,F.J.(2011).Pain and emotion:A biopsychosocial review of recent research.Journal of Clinical Psychology,67(9),942-968.
Lyby,P.S.,Aslaksen,P.M.,& Flaten,M.A.(2011).Variability in placebo analgesia and the role of fear of pain—an ERP study.PAIN®,152(10),2405-2412.
McNeil,D.W.,&Rainwater,A.J.(1998).Development of the fear of pain questionnaire-III.Journal of Behavioral Medicine,21(4),389-410.
Mechias,M.L.,Etkin,A.,& Kalisch,R.(2010).A meta-analysis of instructed fear studies:Implications for conscious appraisal of threat.Neuroimage,49(2),1760-1768.
Meulders,A.,Vansteenwegen,D.,& Vlaeyen,J.W.S.(2011).The acquisition of fear of movement-related pain and associative learning:A novel pain-relevant human fear conditioning paradigm.Pain,152(11),2460-2469.
Meulders,A.,Vansteenwegen,D.,&Vlaeyen,J.W.S.(2012).Women,but not men,report increasingly more pain during repeated (un) predictable painful electrocutaneous stimulation:Evidence formediation by fearofpain.PAIN®,153(5),1030-1041.
Ochsner,K.N.,Bunge,S.A.,Gross,J.J.,&Gabrieli,J.D.E.(2002).Rethinking feelings:An fMRIstudy ofthe cognitive regulation of emotion.Journal of Cognitive Neuroscience,14(8),1215-1229.
Ochsner,K.N.,Ludlow,D.H.,Knierim,K.,Hanelin,J.,Ramachandran,T.,Glover,G.C.,&Mackey,S.C.(2006).Neural correlates of individual differences in pain-related fear and anxiety.Pain,120,69-77.
Parr,J.J.,Borsa,P.A.,Fillingim,R.B.,Tillman,M.D.,Manini,T.M.,Gregory,C.M.,&George,S.Z.(2012).Pain-related fear and catastrophizing predict pain intensity and disability independently using an induced muscle injury model.The Journal of Pain,13(4),370-378.
Peters,M.L.,Vlaeyen,J.W.S.,&van Drunen,C.(2000).Do fibromyalgia patients display hypervigilance for innocuous somatosensory stimuli?Application of a body scanning reaction time paradigm.Pain,86(3),283-292.
Phelps,E.A.,Delgado,M.R.,Nearing,K.I.,&LeDoux,J.E.(2004).Extinction learning in humans:Role of the amygdala and vmPFC.Neuron,43(6),897-905.
Ploner,M.,Lee,M.C.,Wiech,K.,Bingel,U.,&Tracey,I.(2010).Prestimulus functional connectivity determines pain perception in humans.Proceedings of the National Academy of Sciences of the United States of America,107(1),355-360.
Pourtois,G.,Schettino,A.,&Vuilleumier,P.(2013).Brain mechanisms for emotional influences on perception and attention:Whatis magic and what is not.Biological Psychology,92(3),492-512.
Rhudy,J.L.,&Meagher,M.W.(2000).Fear and anxiety:Divergent effects on human pain thresholds.Pain,84(1),65-75.
Riva,P.,Williams,K.D.,& Gallucci,M.(2014).The relationship between fear of social and physical threat and its effect on social distress and physical pain perception.PAIN®,155(3),485-493.
Roelofs,J.,Peters,M.L.,van der Zijden,M.,&Vlaeyen,J.W.S.(2004).Does fear of pain moderate the effects of sensory focusing and distraction on cold pressor pain in pain-free individuals?The Journal of Pain,5(5),250-256.
Sánchez,A.I.,Martínez,M.P.,Miró,E.,&Medina,A.(2011).Predictors of the pain perception and self-efficacy for pain control in patients with fibromyalgia.The Spanish Journal of Psychology,14(1),366-373.
Seifert,F.,&Maihöfner,C.(2009).Central mechanisms of experimental and chronic neuropathic pain:Findings from functional imaging studies.Cellular and Molecular Life Sciences,66(3),375-390.
Suhr,J.,& Spickard,B.(2012).Pain-related fear is associated with cognitive task avoidance:Exploration of the cogniphobia construct in a recurrent headache sample.The Clinical Neuropsychologist,26(7),1128-1141.
Tabbert,K.,Stark,R.,Kirsch,P.,& Vaitl,D.(2006).Dissociation of neural responses and skin conductance reactions during fear conditioning with and without awareness of stimulus contingencies.Neuroimage,32(2),761-770.
Thibodeau,M.A.,Welch,P.G.,Katz,J.,&Asmundson,G.J.G.(2013).Pain-related anxiety influences pain perception differently in men and women:A quantitative sensory test across thermal pain modalities.PAIN®,154(3),419-426.
Tracey,I.(2011).Can neuroimaging studies identify pain endophenotypes in humans?Nature Reviews Neurology,7(3),173-181.
Trost,Z.,France,C.R.,&Thomas,J.S.(2011).Pain-related fear and avoidance of physical exertion following delayed-onset muscle soreness.PAIN®,152(7),1540-1547.
Turk,D.C.,&Wilson,H.D.(2010).Fear of pain as a prognostic factor in chronic pain:Conceptual models,assessment,and treatment implications.Current Pain and Headache Reports,14(2),88-95.
Vlaeyen,J.W.S.,De Jong,J.R.,Onghena,P.,Kerckhoffs-Hanssen,M.,& Kole-Snijders,A.M.J.(2002).Can pain-related fear be reduced?The application of cognitivebehavioural exposure in vivo.Pain Research&Management,7(3),144-153.
Vlaeyen,J.W.S.,&Linton,S.J.(2012).Fear-avoidance model of chronic musculoskeletal pain:12 years on.Pain,153(6),1144-1147.
Vogt,B.A.(2005).Pain and emotion interactions in subregions of the cingulate gyrus.Nature Reviews Neuroscience,6(7),533-544.
Vowles,K.E.,&Gross,R.T.(2003).Work-related beliefs about injury and physical capability for work in individuals with chronic pain.Pain,101(3),291-298.
Wiech,K.,Lin,C.S.,Brodersen,K.H.,Bingel,U.,Ploner,M.,& Tracey,I.(2010).Anterior insula integrates information about salience into perceptual decisions about pain.The Journal of Neuroscience,30(48),16324-16331.
Williams,A.E.,&Rhudy,J.L.(2007).The influence of conditioned fear on human pain thresholds: Does preparedness play a role?The Journal of Pain,8(7),598-606.
Zale,E.L.,& Ditre,J.W.(2015).Pain-related fear,disability,and the fear-avoidance model of chronic pain.Current Opinion in Psychology,5,24-30.
Zaman,J.,Vlaeyen,J.W.S.,van Oudenhove,L.,Wiech,K.,& van Diest,I.(2015).Associative fear learning and perceptual discrimination:A perceptual pathway in the development of chronic pain.Neuroscience &Biobehavioral Reviews,51,118-125.
