N-(2-吡啶甲基)取代的阿伐那非类似物的合成条件优化
2016-01-06田红潮杨亮茹屈凌波
田红潮,毛 璞,杨亮茹,屈凌波
(河南工业大学 生物工程学院,河南 郑州 450000)
N-(2-吡啶甲基)取代的阿伐那非类似物的合成条件优化
田红潮,毛璞,杨亮茹,屈凌波*
(河南工业大学 生物工程学院,河南 郑州 450000)
摘要:以4-(3-氯-4-甲氧基苄基氨基)-2-[(2S)-2-羟甲基-1-吡咯烷基]-5-嘧啶羧酸乙酯为原料,合成了4-(3-氯-4-甲氧基苄基氨基)-2-[(2S)-2-羟甲基-1-吡咯烷基]-N-(2-吡啶甲基)-5-嘧啶甲酰胺,研究了此种阿伐那非类似物的合成条件优化,考察了投料比、反应温度、反应时间等因素对产率的影响.获得较高产率的反应条件为n(C6H8N2)∶n(C18H21ClN4O4)∶n(EDCI)∶n(HOBt)∶n(Et3N)=1.2∶1∶1.2∶1.2∶2,在搅拌下,60 ℃反应6 h,经过后处理,柱层析纯化,得到类白色固体产物,产率为84.3%.所合成的产物经FT-IR、1H NMR、13C NMR、ESI-MS得到验证.
关键词:阿伐那非类似物; 酰胺缩合; 条件优化
勃起功能障碍(ED)是一种常见的男性疾病并且患病率随着年龄的增长而增加.美国马萨诸塞州男性衰老研究(MMAS)表明[1],男性在40~70岁的ED患病率为52%,而70岁以上的为70%.随着老年人口的比例不断增加,预计到2025年受到ED影响的男性会有3.2亿,他们中的大多数预计将寻求医学治疗来治愈这种疾病[2].阿伐那非(avanafil,StendraTM)是一种于2012年4月获US-FDA批准用于治疗ED的口服速效高选择性磷酸二酯酶5抑制剂(PDE5i)[3].与其他PDE5i相比,阿伐那非选择性更高,起效更快,副作用更少[4],预计将会有非常大的市场前景.
本文作者基于阿伐那非的结构(图1),合成了阿伐那非的类似物(A-1).得到了一种YAMADA等人[5]专利文献报道的阿伐那非类似物4-(3-氯-4-甲氧基苄基氨基)-2-[(2S)-2-羟甲基-1-吡咯烷基]-N-(2-吡啶甲基)-5-嘧啶甲酰胺(A-1),并对其最后一步酰胺缩合反应进行了条件优化.酰胺缩合的方法有很多种,文献报道[6-9]常用的酰胺缩合试剂有EDCI/HOBt/TEA、EDCI/DMAP/TEA、HATU/TEA、TBTU/TEA和HOBt/DCC等.本研究以4-(3-氯-4-甲氧基苄基氨基)-2-[(2S)-2-羟甲基-1-吡咯烷基]-5-嘧啶羧酸乙酯(1)为原料,先进行酯的水解,再与2-氨甲基吡啶(3)进行酰胺缩合反应,合成了阿伐那非类似物A-1(图2).通过改变投料比、反应温度等条件,进一步提高了产物的产率.

图1 阿伐那非的结构式Fig.1 The Structural formula of avanafil
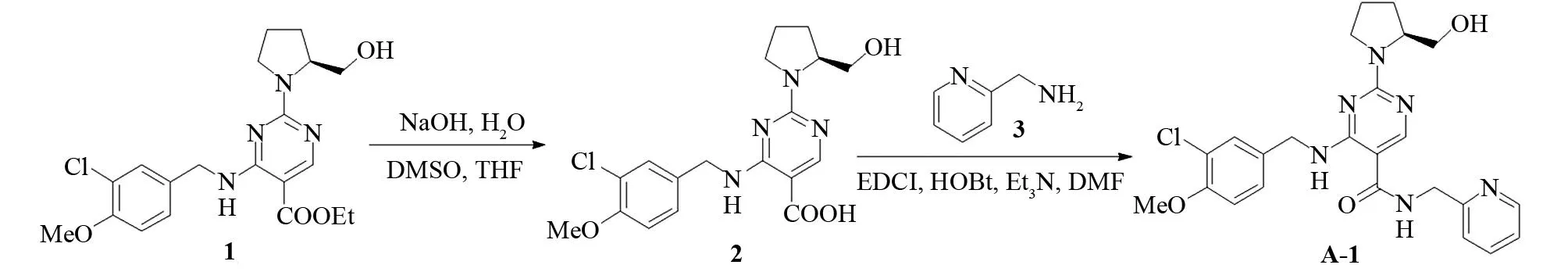
图2 阿伐那非类似物A-1的合成路线Fig.2 The synthetic route of avanafil analogue A-1
1实验部分
1.1 仪器与试剂
Bruker Avance 400型超导核磁共振仪,瑞士Bruker公司;ICPMS7700型电感耦合等离子体质谱仪,深圳华普通用科技有限公司;WQF-510型傅立叶变换红外光谱仪,北京北分瑞利分析仪器厂;X-4型数字显微熔点测定仪,北京福凯科仪科技有限公司;DF-101D型集热式恒温加热磁力搅拌器、旋转蒸发器RE-2000B、SHD-D(Ⅲ)型循环水式真空泵均为巩义市予华仪器有限责任公司产品;DZF-6020型真空干燥箱,上海申贤恒温设备厂.
4-(3-氯-4-甲氧基苄基氨基)-2-[(2S)-2-羟甲基-1-吡咯烷基]-5-嘧啶羧酸乙酯(1,实验室自制);2-氨甲基吡啶、1-乙基-3-(3-二甲基氨基丙基)碳化二亚胺盐酸盐(EDCI)和1-羟基苯并三唑水合物(HOBt)均购自阿拉丁试剂有限公司;二甲基亚砜(DMSO)、四氢呋喃(THF)、三乙胺(Et3N)等均为市售分析纯试剂.
1.2 化合物的合成
1.2.14-(3-氯-4-甲氧基苄基氨基)-2-[(2S)-2-羟甲基-1-吡咯烷基]-5-嘧啶羧酸(2)的合成
在50 mL圆底烧瓶中加入2.5 mmol 4-(3-氯-4-甲氧基苄基氨基)-2-[(2S)-2-羟甲基-1-吡咯烷基]-5-嘧啶羧酸乙酯(1),用体积比为V(DMSO)∶V(THF)=1∶1的混合溶剂溶解,再加入8 mL 10%的NaOH水溶液,室温下搅拌,反应结束后向混合物中加入25 mL 10%的柠檬酸水溶液,35 ℃下减压蒸馏除去THF,析出白色固体,抽滤,滤饼用蒸馏水洗涤,真空干燥6 h,得到化合物2,白色粉末状固体,性状与文献[10]相符.产物纯度较高,无需提纯,直接进行下一步反应.
化合物1(实验室自制):mp:86~88 ℃(文献[5]值:mp:88~90 ℃);1H NMR (400 MHz,DMSO-d6)δ:8.53 (q,J=6.4 Hz,1H,NH),8.48 (d,J=6 Hz,1H,Pyrimidine-H),7.42 (dd,J=2 Hz,J=4.4 Hz,1H,Ph-H),7.29 (d,J=8.4 Hz,1H,Ph-H),7.08 (d,J=8.4 Hz,1H,Ph-H),4.81 (m,1H,OH),4.55 (t,J=7.6 Hz,2H,Ph-CH2),4.21 (q,J=6.8 Hz,2H,OCH2CH3),4.13~4.08 (m,1H,Pyrrolidine-H),3.82 (d,J=1.6 Hz,3H,OCH3),3.63~3.58 (m,1H,Pyrrolidine-H),3.51~3.45 (m,2H,Pyrrolidine-H),3.35~3.31 (m,1H,Pyrrolidine-H),2.02~1.83 (m,4H,Pyrrolidine-H),1.26 (t,J=7.2 Hz,3H,OCH2CH3);1H NMR (400 MHz,DMSO-d6,D2O)δ:8.47 (q,J=5.6 Hz,1H,NH),8.42 (d,J=2.4 Hz,1H,Pyrimidine-H),7.35 (t,J=1.5 Hz,1H,Ph-H),7.25 (d,J=8.4 Hz,1H,Ph-H) 7.03 (dd,J=2.5,8.4 Hz,1H,Ph-H),4.51 (d,J=6.5 Hz,2H,Ph-CH2),4.17 (q,J=7.1 Hz,2H,OCH2CH3),4.07 (s,1H,Pyrrolidine-H),3.77 (d,J=1.1 Hz,3H,OCH3),3.60~3.52 (m,1H,Pyrrolidine-H),3.48~3.40 (m,2H,Pyrrolidine-H),3.30 (dd,J=7.5,10.3 Hz,1H,Pyrrolidine-H),1.95~1.81 (m,4H,Pyrrolidine-H),1.22 (t,J=7.1 Hz,3H,OCH2CH3); IR (KBr,cm-1)σ:3 340,1 674,1 525,1 257,804; ESI-MS (m/z):421.25 [M+H]+.
化合物2:产率95.1%,mp:202~204 ℃(文献[5]值:mp:205~208 ℃);1H NMR (400 MHz,DMSO-d6,D2O)δ:8.37 (s,1H,Pyrimidine-H),7.35 (d,J=8.2 Hz,1H,Ph-H),7.24 (s,1H,Ph-H),7.04 (d,J=8.2 Hz,1H,Ph-H) 4.52 (s,2H,Ph-CH2),4.06 (s,1H,Pyrrolidine-H),3.78 (s,3H,OCH3),3.57 (d,J=10.4 Hz,1H,Pyrrolidine-H),3.45 (s,2H,Pyrrolidine-H),3.32 (t,J=9.0 Hz,1H,Pyrrolidine-H),1.91 (s,2H,Pyrrolidine-H),1.82 (s,2H,Pyrrolidine-H); ESI-MS (m/z):393.25 [M+H]+.
1.2.24-(3-氯-4-甲氧基苄基氨基)-2-[(2S)-2-羟甲基-1-吡咯烷基]-N-(2-吡啶甲基)-5-嘧啶甲酰胺(A-1)的合成
在50 mL圆底烧瓶中加入0.5 mmol化合物2,用DMF溶解,依次加入0.6 mmol 2-氨甲基吡啶(3),0.6 mmol 1-乙基-3-(3-二甲基氨基丙基)碳二亚胺盐酸盐(EDCI)、0.6 mmol 1-羟基苯并三唑水合物(HOBt)和1.0 mmol三乙胺(Et3N),磁力搅拌下反应,反应结束后把反应液倒入18 mL饱和NaHCO3溶液中,乙酸乙酯萃取,有机层用饱和食盐水洗涤,通过无水硫酸钠干燥,在减压旋蒸下除去溶剂,残留物通过硅胶柱色谱[洗脱剂为乙酸乙酯/甲醇(体积比为15∶1)]纯化,得到阿伐那非类似物A-1,类白色固体.
化合物A-1 产率84.3%,mp:100~102 ℃(文献[5]值:mp:101~103 ℃);1H NMR (400 MHz,DMSO-d6)δ:9.19 (t,J=8 Hz,1H,C(O)NH),8.82 (t,J=5.9 Hz,1H,Ph-CH2NH),8.52 (s,1H,Pyridine-H),8.50 (d,J=4 Hz,1H,Pyrimidine-H),7.76~7.72 (m,1H,Pyridine-H),7.40 (s,1H,Ph-H),7.30~7.23 (m,3H,Ph-H,Pyridine-H),7.08 (d,J=8.4 Hz,1H,Ph-H),4.87 (m,1H,OH),4.51 (s,4H,Ph-CH2,Pyridine-CH2),4.10 (s,1H,Pyrrolidine-H),3.81 (s,3H,OCH3),3.63 (s,1H,Pyrrolidine-H),3.51~3.45 (m,2H,Pyrrolidine-H),3.33 (d,J=8.2 Hz,1H,Pyrrolidine-H),1.96~1.85 (m,4H,Pyrrolidine-H);13C NMR (100MHz,DMSO-d6)δ:167.7,161.3,160.3,159.5,156.8,153.8,149.2,137.1,133.7,129.8,128.1,122.4,121.3,121.0,113.1,98.6,62.3,59.4,56.5,47.8,44.6,42.6,28.1,23.0; IR (KBr,cm-1),σ:3 278,1 635,1 522,1 250,802; ESI-MS (m/z):483.13 [M+H]+.
2结果与讨论
2.1 投料比对酰胺缩合反应产率的影响
首先考察了反应物4-(3-氯-4-甲氧基苄基氨基)-2-[(2S)-2-羟甲基-1-吡咯烷基]-5-嘧啶羧酸(2)与2-氨甲基吡啶(3)的投料比对产物的影响,结果如图3所示.随着投料比n(C6H8N2)∶n(C18H21ClN4O4)从0.9∶1增加到1.3∶1,产物的产率先增加后趋于不变,当n(C6H8N2)∶n(C18H21ClN4O4)=1.2∶1时,产率达到最大,为69.4%,再增加化合物3的量对产率没有明显影响.因此n(C6H8N2)∶n(C18H21ClN4O4)=1.2∶1是最佳值.化合物3需要过量可能是在反应过程中氨基被部分氧化,只有在过量时产率才能达到最大.

图3 投料比对产率的影响Fig.3 Effect of feed ratio on the yield of product
2.2 缩合试剂用量对产率的影响
酰胺缩合的方法有很多种,常用的酰胺缩合试剂[11]有EDCI/HOBt/TEA、EDCI/DMAP/TEA、HATU/TEA、TBTU/TEA和HOBt/DCC等,本文作者利用缩合试剂EDCI、HOBt和Et3N研究了缩合试剂用量对产率的影响,结果如表1所示,在保持n(C6H8N2)∶n(C18H21ClN4O4)=1.2∶1,n(EDCI)∶n(HOBt)∶n(Et3N) =1∶1∶2不变时,随着缩合试剂用量从1∶1增加到1.4∶1,产物的产率先增加后趋于不变,当n(C6H8N2)∶n(C18H21ClN4O4)∶n(EDCI)∶n(HOBt)∶n(Et3N)=1.2∶1∶1.2∶1.2∶2时,产率最高,为70.2%.酰胺缩合试剂EDCI和HOBt的用量必须相等,因为EDCI过多时会使产物消旋而使产率降低,而HOBt可以抑制消旋产物的产生.

表1 缩合试剂用量对产率的影响Table 1 Effect of condensation reagents amounton the yield of product
2.3 反应温度对酰胺缩合反应产率的影响
反应温度对反应产率的影响如图4所示,随着反应温度从20 ℃升高到70 ℃,产物产率先增加后趋于平缓,在60 ℃时达到最大,为81.3%.从图4可以看出温度对产物的产率影响明显,温度较低时,产物的产率比60 ℃时要低.因此,反应温度选为60 ℃最为合适.本文参考文献[5]和文献[11]的反应温度,在室温反应过夜,结果显示原料并未完全反应,即使延长反应时间也不能反应完全.

图4 反应温度对产率的影响Fig.4 Effect of reaction temperature on the yield of product
2.4 反应时间对酰胺缩合反应产率的影响
考察反应时间对产率的影响,结果如表2所示.随着反应时间从2 h延长到10 h,产物的产率先逐渐增大后趋于平缓.当反应时间在6 h时,产物产率达到最大,为84.3%;超过6 h以后,再延长反应时间对产物产率影响不大.反应时间太短,反应物未进行充分的反应,之后再延长反应时间对产率影响不明显,反应6 h以后原料基本消耗完全.因此,最佳反应时间为6 h.保持在60 ℃时,反应时间比文献所用时间明显缩短,产物产率也有较大提高.
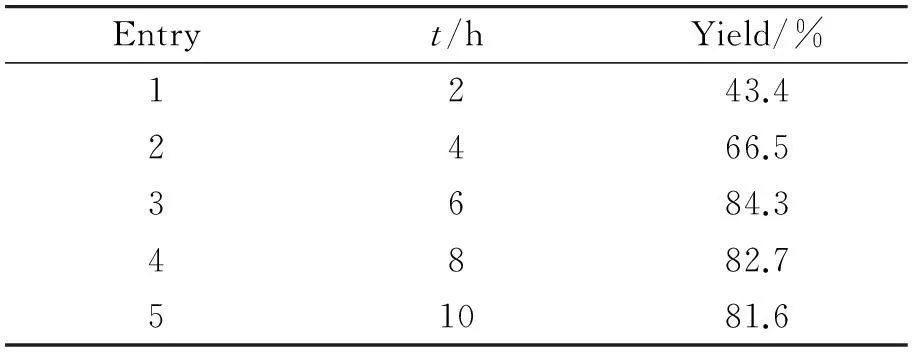
表2 反应时间对产率的影响Table 2 Effect of reaction time on the yield of product
3结论
以4-(3-氯-4-甲氧基苄基氨基)-2-[(2S)-2-羟甲基-1-吡咯烷基]-5-嘧啶羧酸乙酯为原料,经过酯水解和酰胺缩合反应,合成了阿伐那非类似物4-(3-氯-4-甲氧基苄基氨基)-2-[(2S)-2-羟甲基-1-吡咯烷基]-N-(2-吡啶甲基)-5-嘧啶甲酰胺.n(C6H8N2)∶n(C18H21ClN4O4)∶n(EDCI)∶n(HOBt)∶n(Et3N)=1.2∶1∶1.2∶1.2∶2,60 ℃下反应6 h,经过后处理,柱层析纯化,得到类白色固体产物,产率为84.3%.反应时间比文献明显缩短,产率有较大提高.该工艺路线操作简便、反应条件温和、原料价格低廉,对阿伐那非及其类似物的工业化生产具有一定的应用价值.
参考文献:
[1] GRAHAM J,RAYMOND C,ROBERT A,et al.The second princeton consensus on sexual dysfunction and cardiac risk:New guidelines for sexual medicine [J].J Sex Med,2006,3:28-36.
[2] GEORGE T,STEFAN Ü,FARHANG A,et al.Avanafil for the treatment of erectile dysfunction:initial data and clinical key properties [J].Ther Adv Urol,2013,5(1):35-41.
[3] 徐慧兰.阿伐那非(avanafil)[J].中国药物化学杂志,2012,22(5):458.
[4] 范鸣.勃起功能障碍治疗药avanafil [J].药学进展,2012,36(3):135-136.
[5] YAMADA K,MATSUKI K,OMORI K,et al.Aromatic nitrogen-containing 6-membered cyclic compounds:US,20030229095 A1 [P].2003-12-11.
[6] IVANKA S,KIRIL C,STOYAN S,et al.Synthesis,antioxidative and antiviral activity of hydroxycinnamic acid amides of thiazole containing amino acid [J].Amino Acids,2009,37:383-388.
[7] XU Z R,ZHANG F Y,ZHANG L H,et al.Total synthesis of (-)-indolactam v [J].Org Biomol Chem,2011,9:2512-2517.
[8] ZHANG W,SONG N,LI Z Z,et al.Synthesis of obyanamide,a marine cytotoxic cyclic depsipeptide [J].Chin Chem Lett,2006,17:285-288.
[9] ALI A I,AL-MASOUDI I A,SAEED B,et al.Amino acid derivatives,part 2:synthesis,antiviral,and antitumor activity of simple protected amino acids functionalized at N-terminus with naphthalene side chain [J].Heteroat Chem,2005,16:148-155.
[10] 童瑶,李金玲,姜申德.阿伐那非的合成方法:中国,104003981 A [P].2014-08-27.
[11] 蒋慧敏.阿伐那非类似物N-(2-嘧啶甲基)-2-氨基-4-(3-氯-4-甲氧基苄氨基)-5-嘧啶甲酰胺的合成研究[D].上海:复旦大学化学系,2012:19-33.
[责任编辑:任铁钢]
The optimized synthesis conditions of the avanafil analogue
replaced by N-(2-pyridinyl-methyl)
TIAN Hongchao,MAO Pu,YANG Liangru,QU Lingbo*
(CollegeofBiologicalEngineering,HenanUniversityofTechnology,Zhengzhou450000,Henan,China)
Abstract:4-[(3-chloro-4-methoxybenzyl)amino]-2-[(2S)-2-hydroxymethyl-1-pyrrolidinyl]-N-(2-pyridinyl-methyl)-5-pyrimidinecar-boxamide was synthesized from 4-[(3-chloro-4-methoxybenzyl)amino]-2-[(2S)-2-hydroxymethyl-1-pyrrolidinyl]-5-pyrimidineethyl-formate.The conditions of feed ratio,reaction temperature,reaction time and other factors were optimized to prepare the yield.The reaction mixture was stirred at 60 ℃ temperature for 6h with n(C6H8N2)∶n(C18H21ClN4O4)∶n(EDCI):n(HOBt)∶n(Et3N) = 1.2∶1∶1.2∶1.2∶2.After column chromatography purification,the product was obtained as white solid,with the yield of 84.3%.Its structure was characterized by FT-IR,1H NMR,13C NMR and ESI-MS.
Keywords:avanafil analogue; amide condensation; conditions optimization
作者简介:田红潮(1988-),男,硕士生,研究方向为药物有机合成.*通讯联系人,E-mail:mxyy9510@126.com.
基金项目:国家自然科学基金(21172055).
收稿日期:2014-12-08.
中图分类号:O625.6
文献标志码:A
文章编号:1008-1011(2015)02-0148-05
