PEG为碳源碳热法合成LiFePO4/C的改性研究
2015-12-31米增财
米增财
(太原工业学院材料工程系,山西 太原 030008)
随着信息通信产业、环保节能技术的不断发展进步,可充二次锂离子电池逐渐向大型动力电动领域深入。大型动力电源不仅要求材料具有较高的体积比容量,而且对材料的价格、安全及环保性能提出更高要求。世界发达国家都把合成电化学性能优越与安全性能良好的锂离子二次电池用正极材料作为研究开发的重点,而研制高性能的锂离子二次电池的关键是要得到高性能的正极材料[1-2]。具有橄榄石型结构的LiFePO4理论比容量值为170mAh/g,并具有非常稳定的充放电电压平台以及很好的热稳定性和安全性。与其他正极材料相比,磷酸铁锂具有价格低廉、对环境友好、循环性能优良、安全性能突出等优点,成为最具开发和应用潜力的新一代锂离子正极材料[3-5]。
但是,正极材料LiFePO4主要存在的问题,一是电导率低及由此而生的可逆容量的瓶颈;二是材料的Li+化学扩散系数低,导致了材料的理论容量不能得到最大限度的释放以及大电流放电性能不佳。解决LiFePO4正极材料存在的低电导率以及由此产生的可逆容量瓶颈有效的方法是,通过在LiFePO4的合成过程中引入碳添加剂[6-7]。
本实验采用碳热还原法合成LiFePO4,以Fe-PO4和Li2CO3为主要原料,采用单因素法进行研究,主要研究碳源PEG(聚乙二醇6000)的用量及锂源用量对产物结构与性能的影响,以期找到最佳的合成条件,制备合成出性能稳定的LiFePO4正极材料。
1 实验部分
1.1 试剂及仪器
工业级磷酸铁,分析纯碳酸锂,乙炔黑,聚四氟乙烯(PTFE),无水乙醇,锂片,电解液,Celgard2400隔膜,去离子水。
LU-900M管式电炉,电子天平,电热真空干燥箱,真空手套箱,TD-3000型X射线衍射仪,KYKYEM3800扫描电子显微镜,CT2001A电池测试系统。
1.2 实验方法
1)LiFePO4的制备:本实验采用碳热还原法制备LiFePO4。按化学计量比称量FePO4、Li2CO3和PEG,研磨混合(加乙醇),放入管式炉中,氮气气氛保护下,一定温度焙烧一定时间,自然冷却,冷却后过筛。采用PEG作为碳源进行实验,一方面,PEG的分解温度与LiFePO4的生成温度基本一致;另一方面,PEG能够溶于乙醇,用乙醇作为助磨剂形成流变态,从而达到均匀混料的目的。
2)PEG不同用量的影响:在实验中按生成每摩尔 LiFePO4为基准分别加入[n(FePO4)∶n(Li2CO3)∶n(C)]=2.00∶1.02∶x,x为PEG掺碳量],掺入量x=0.50、0.75、1.00、1.25,制备LiFePO4/C材料,对样品进行性能测试。
3)锂源不同用量的影响:由于锂源在实验过程中存在各种损失,因此,一般在实验原料中要用多于理论值量的锂源。对LiFePO4的研究目的是找到锂源合适的用量,使所制得的LiFePO4/C达到更好的性能。
1.3 样品电化学性能测试
采用CT2001A电池测试系统在室温下以不同的充放电倍率 0.2C、1.0C、5.0C(其中 1.0C=150mAh/g),在2.3V~4.2V电压范围内对合成的LiFePO4/C复合正极材料的充放电比容量、循环性能和容量保持率进行测试。具体充放电制度如下:
1)恒电流充电至4.2V;
2)恒电压(4.2V)充电至电流小于0.05mA;
3)静置1min;
4)恒电流放电至2.3V;
5)循环。
2 结果与讨论
2.1 选择PEG为碳源制备LiFePO4
2.1.1 实验条件
碳源采用PEG,碳源的加入,一方面,可以使得Fe3+还原完全;另一方面,烧结过程中可以在LiFe-PO4颗粒表面包覆一部分碳,起到提高电子导电的作用[8],所以对碳源用量的研究成为必要。样品原料配比及合成制度如表1。
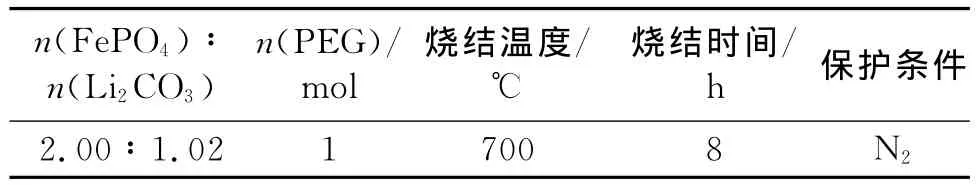
表1 样品的原料配比及合成制度
2.1.2 样品的SEM分析(见图1)
从图1可以看出,所得样品为类球形,粒度分布为400nm左右,且分布均匀,晶粒形貌较规则。这可能是由于,PEG的分解温度与LiFePO4的生成温度基本一致,其分解出来的碳可以很好地抑制LiFePO4晶粒的生长,达到减小LiFePO4粒径的目的。图中的初级颗粒存在一定的团聚现象,一次颗粒之间紧密接触,其间的联结物可能是剩余的碳,它们不仅能够提高活性物质的导电率,降低电荷转移阻抗,进而提高材料的电化学性能,而且能够降低活性物质的表面能,有利于工业生产中正极材料的涂膜,使其不易脱落。

图1 以PEG为碳源制得LiFePO4/C的SEM图谱
2.1.3 样品的XRD分析(见图2)
如图2所示,以PEG作为碳源在700℃、8h氮气保护条件下进行烧结制得LiFePO4/C材料的X射线衍射图谱与LiFePO4的标准图谱基本吻合,没有发现任何杂相峰,并且由图中可以看到其衍射峰强度较高,峰型窄而尖锐,说明该材料的结晶较完全。此外,XRD图中并没有出现碳的特征峰,这可能是碳的含量过少或以无定形形式存在的缘故。
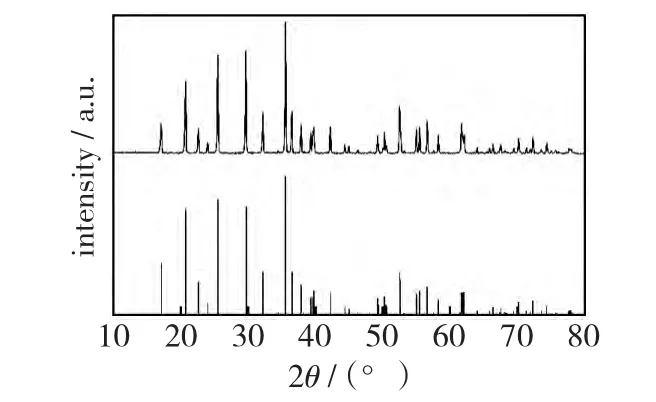
图2 以PEG为碳源制得LiFePO4/C的XRD图谱
2.1.4 电化学性能分析
添加PEG的LiFePO4/C的电化学性能用CT2001A电池测试系统测试,实验结果如第25页图3所示。由图3可见,以PEG为碳源制得的LiFePO4/C复合材料在0.2C时的首次放电比容量可达155.9mAh/g,且在高倍率5.0C下的放电容量可达107.5mAh/g,说明以PEG为碳源对LiFe-PO4高倍率放电性能的提高有利。因此,我们对PEG碳源的用量进行了系统研究。
2.2 PEG用量对LiFePO4结构和电化学性能的影响
2.2.1 实验条件(见第25页表2)
2.2.2 充放电性能分析(见第25页图4)
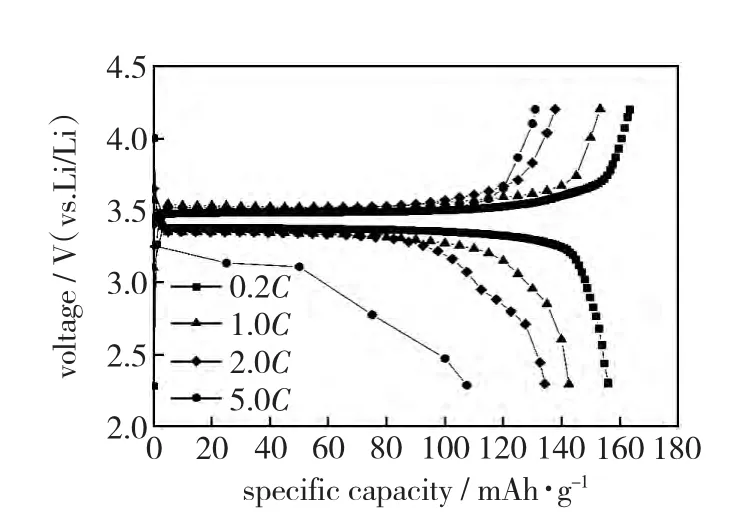
图3 以PEG为碳源制得LiFePO4/C在不同放电倍率下的充放电曲线
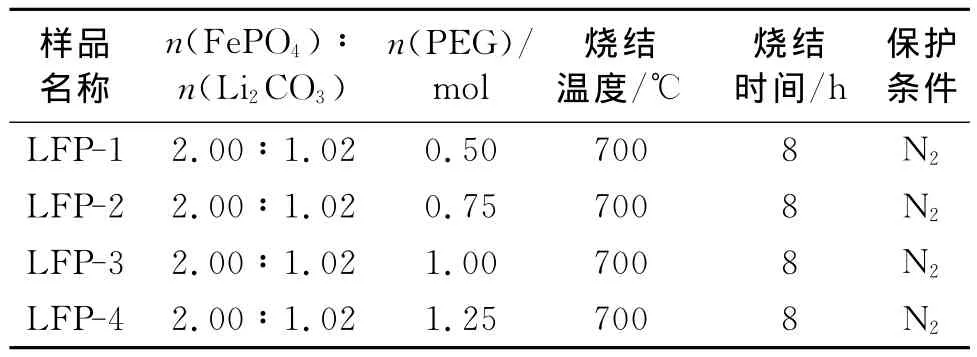
表2 PEG用量对LiFePO4结构和电化学性能影响实验条件
从图4中可以明显看出,当PEG用量为1mol时,所合成的LiFePO4在0.2C状态下首次放电比容量最高,可以达到155.9mAh/g。PEG用量小于1mol时,随着其用量的增加,其0.2C首次放电比容量增加;大于1mol时,其放电比容量急剧下降。这可能是由于,用量较小时,PEG分解得到的碳只能够满足其对Fe3+还原所需要的碳量,剩余的碳不能对LiFePO4颗粒进行均匀包覆;当用量逐渐增加,PEG分解得到的碳在Fe3+还原完全后,剩余的碳量也逐渐增加,这些碳均匀地分布在LiFePO4颗粒之间对LiFePO4晶粒的生长进行有效控制,同时还提高了活性物质本身的导电性能,进而提高了LiFePO4的充放电性能。但当继续增加PEG的用量时,由于生成的碳过多,而碳本身不具有电化学活性且密度较低,因此碳量的增加会降低材料中活性物质的含量,从而造成材料电化学性能的降低。综合上述分析可知,当PEG用量为1mol时,材料的放电性能最佳。
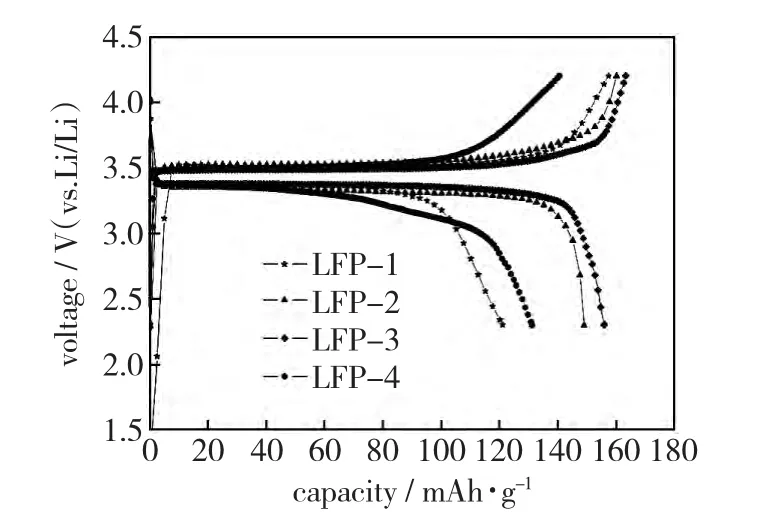
图4 不同PEG用量所合成样品0.2 C首次放电比容量
2.3 锂源用量对LiFePO4结构和电化学性能的影响
锂离子电池充放电过程中,Li不可避免地要有部分损失:1)在锂离子电池首次充放电过程中,电极材料与电解液在固液界面上发生反应,形成覆盖于电极材料表面的钝化层,即SEI膜,SEI膜的形成要消耗部分锂离子;2)锂离子电池在多次充放电过程后,其电池材料的结构会发生变化,导致Li+不能在放电时完全返回到正极,形成LiC6附着在负极表面,从而消耗部分Li+;3)固相烧结过程中部分锂源会以Li2O的形式挥发,从而也会造成部分锂的损失[9]。
由于锂源在实验过程中存在以上各种损失,因此,一般在实验原料中要用多于理论值量的锂源。本实验的研究目的是找到锂源合适的用量,使所制得的LiFePO4/C达到更好的性能。
2.3.1 实验条件
确定添加PEG的用量为1mol,设计锂源用量x=0.02、0.04、0.06、0.08、0.10,(x指 按 LiFePO4化学计量比所计算的Li2CO3用量理论值为“1”,多添加的量),混料后700℃、8h烧结,并同时进行氮气 保 护。 所 得 样 品 名 分 别 为 LFP1.02、LFP1.04、LFP1.06、LFP1.08、LFP1.10。
2.3.2 样品的SEM分析(见第26页图5)
从图5可以看出,所得样品均为类球形,其粒径分布较为均匀,并且随着x值的增加粒度有明显的减小。当x=0.10时,粒度分布为400nm左右。这可能是由于,PEG的分解温度与LiFePO4的生成温度基本一致,其分解出来的碳可以很好地抑制LiFePO4晶粒的生长,达到减小LiFePO4粒径的目的。从图5中还可以看到,初级颗粒存在一定的团聚现象,一次颗粒之间紧密接触,其间的联结物可能是剩余的碳,它们不仅能够提高活性物质的导电率,降低电荷转移阻抗,进而提高材料的电化学性能,而且能够降低活性物质的表面能,有利于工业生产中正极材料的涂膜,使其不易脱落。
2.3.3 充放电性能分析(见第26页图6)
如图6所示,各样品在0.2C下放电,其充放电比容量没有太大的差异。当x=0.04时,其放电比容量最大,可以达到156.6mAh/g;当x=0.02时,其放电比容量也可以达到153.1mAh/g;当x=0.10时,也能够达到148.5mAh/g。从图6中可以看出,0.2C放电状态下,各样品的极差均较小,基本在0.1V左右,并且有明显的充放电平台。与0.2C放电状态下的曲线相比,1.0C放电曲线在放电性能上各样品均有明显下降。其中,放电比容量减小,当x=0.04时最大,为143.5mAh/g;x=0.10时最小,为133.7mAh/g。极差电压增大,当x=0.06时,极差电压达到0.3V。其原因可能是,放电电流增大时,锂离子的扩散速率不能够满足需要,造成一定的容量损失。可见,当x=0.04时,材料的放电性能最佳。

图5 样品LFP1.02、LFP1.04、LFP1.06、LFP1.08、LFP1.10的 SEM 图
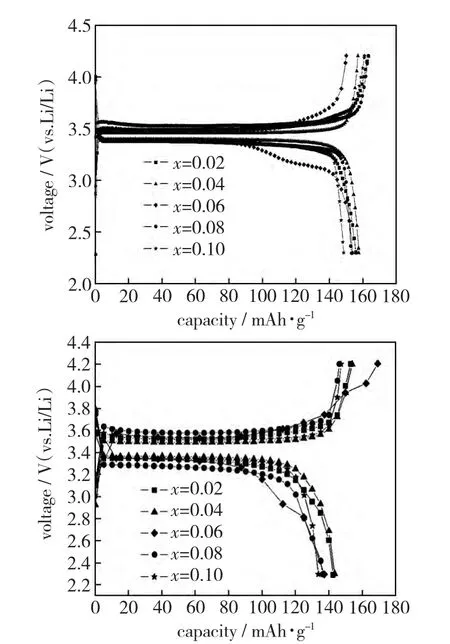
图6 样品 LFP1.02、LFP1.04、LFP1.06、LFP1.08、LFP1.10,在0.2 C、1.0C倍率下首次充放电比曲线
2.3.4 XRD分析(见图7)
如图7所示,LFP1.04样品的X射线衍射图谱与LiFePO4的标准图谱基本吻合,没有发现任何杂相峰,并且其衍射峰强度较高,峰型窄而尖锐,说明该材料的结晶较完全。此外,XRD图中并没有出现碳的特征峰,这可能是碳的含量过少或以无定形形式存在的缘故。
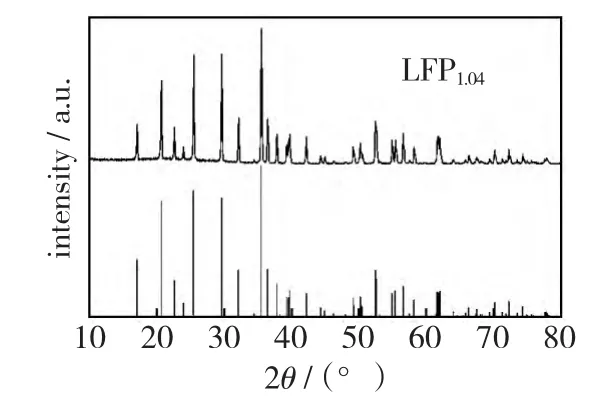
图7 样品LFP1.04的XRD谱图
2.3.5 循环性能分析(见图8)
从图8可以看出样品LFP1.04高倍率下的放电情况,1.0C下的最高比容量能够达到143.5mAh/g,5C下其可以达到110.3mAh/g。图8主要表征的是样品在2.0C下的循环性能。从图8可以看到,100次放电后样品的容量基本不损失,但是图线不够平稳,存在波动。这种波动一方面,可能是由于测试温度在循环过程中有波动,造成高倍率下放电容量的不稳定;另一方面,可能是经过多次循环后材料本身结构发生变化造成的。其电导率也有明显的提高,可达1.26×10-1S/cm,较纯LiFePO4高8个数量级。
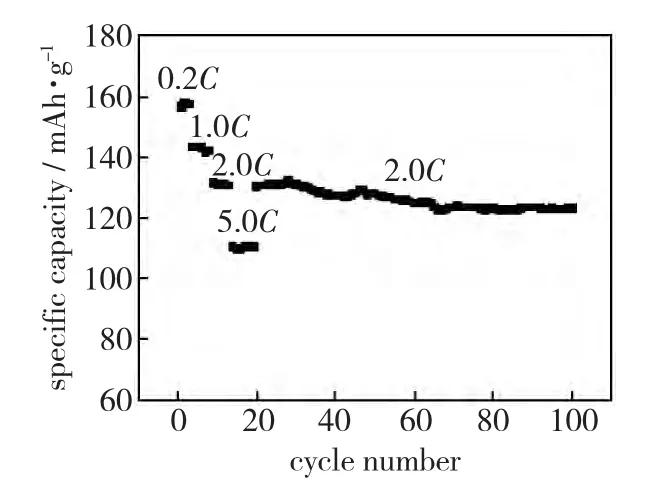
图8 样品LFP1.04不同倍率下循环性能曲线
3 结论
以FePO4为铁源,以PEG为碳源和还原剂,采用碳热还原法制备LiFePO4/C复合正极材料。采用XRD、SEM分析表征样品的结构和形貌,采用恒流充放电循环测试考察样品的电化学性能。得出结论如下:
1)研究了不同PEG掺入量对LiFePO4/C结构和电化学性能的影响。XRD结果表明,加入PEG后仍能得到结晶完好的LiFePO4晶体,PEG的加入并没有改变LiFePO4的晶体结构。电化学测试结果表明,随着PEG掺入量的增加,材料的放电容量先增大后减小,当PEG掺入量为1mol时,所合成的LiFePO4的性能最好,其0.2C时的首次放电比容量可达155.9mAh/g。
2)研究了不同锂源用量对LiFePO4/C结构和电化学性能的影响。实验结果表明,当锂源用量过量4%时,材料的放电性能最佳,其0.2C、1.0C和5.0C时的放电比容量可分别达 156.6、143.5、110.3mAh/g,且表现出良好的循环稳定性。
[1] Andersson A S,Kalska B.Lithium extraction/insertion in LiFePO4:an X-ray diffraction and mossbauer spectroscopy study[J].Solid State Ionics,2000,130(1/2):41-52.
[2] Koksbang R,Barker J,Shi H.Cathode materials for lithium rocking cjair batteries[J].Solid State Lonics,1996,84(1/2):1-21.
[3] 曹艳军,龙翔云,程云峰.锂离子电池正极材料的研究现状和展望[J].化工技术与开发,2007,36(3):16-18.
[4] 郭文彦,王恩通,任引哲.橄榄石型锂离子电池正极材料LiFePO4的研究[J].山西师范大学学报,2007,21(3):62-66.
[5] Yamada A,Chung S C,Hinokuma K.Optimized LiFe-PO4for lithium battery cathodes[J].J Electrochem Soc,2001,148:A224-A229.
[6] 米常焕,曹高劭,赵新兵.碳包覆LiFePO4的一步固相法制备及高温电化学性能[J].无机化学学报,2005,20(4):556-561.
[7] Takahashi M,Tobishima S,Takei K.Reaction behavior of LiFePO4as a cathode material for rechargeable lithium batteries[J].Solid State Lonics,2002,148:283-289.
[8] 刘素琴,龚本利,黄可龙,等.新型碳热还原法制备LiFePO4/C复合材料及其性能研究[J].无机材料学报,2007,22(2):283.
[9] Bhuvaneswari M S,Bramnik N N,Ensling H D,et al.J aegermann synthesis and characterization of carbon nanofiber/LiFePO4composites for Li-ion batteries[J].J Power Sources,2008,180(1):553.
