新型吡啶羧酸类Tb(Ⅲ)和Eu(Ⅲ)配合物与牛血清白蛋白的结合研究
2015-12-15王广彬,马捷,陈奎章
新型吡啶羧酸类Tb(Ⅲ)和Eu(Ⅲ)配合物与牛血清白蛋白的结合研究
王广彬1,马捷2,陈奎章3
(1.徐州绿健乳业有限责任公司,江苏 徐州221006;2.徐州工程学院,江苏 徐州221018;
3.徐州市环境应急与事故调查中心,江苏 徐州221002)
摘要:合成并表征1种新型配体及配合物Na2EuLCl5·4H2O和Na2TbLCl5·4H2O.研究结果表明这2种配合物有较高的热稳定性,配体L性能优良.紫外可见吸收和Stern|Volmer分析显示牛血清白蛋白荧光的猝灭机制为静态猝灭.通过Van't Hoff方程计算出键合常数和键合位点数,并表明范德华力和氢键是BSA|complex形成的主要动力.
关键词:荧光光谱;牛血清白蛋白;Eu和Tb配合物
收稿日期:2015-03-29
基金项目:国家星火计划项目(2014GA690133);徐州市科技发展计划项目(XF13C028);国家建筑材料行业科技创新计划项目(2014|M3|3)
作者简介:王广彬(1976-),男,江苏徐州人,教授级高级工程师,博士,硕士生导师,主要从事生物与食品工程研究.
中图分类号:O622文献标志码:A
近年来,稀土荧光材料以其丰富的电子能级和发光性能在电子、节能、环境、建筑生物、化学、医学等领域得到了广泛的运用.然而稀土元素弱的吸收和发射光谱以及较低的量子产率和摩尔吸收系数,使其稀土离子的发光效率不高.因此,为了提高其荧光效率,通常将稀土离子与具有优良的吸光系数和能量传递效率的有机配体配位,使有机配体作为天线生色团敏化中心稀土离子发光[1].基于此效应,人们已经研制出许多新型的配合物[2],其中含有吡啶环和咪唑环的配体是一种非常重要的有机配合物.它具有多种配位方式[3],其庞大的共轭结构可以通过高效率的分子间能量转移敏化稀土离子的发射态.以吡啶二甲酸(DPA)及其衍生物为有机配体并对其荧光性能进行的研究结果表明它们均具有较好的敏化和配位能力,是一类有潜力的稀土荧光配体[4|5].2,6|吡啶二甲酸(DPA)是一种很好的与稀土离子结合的化合物,它的羧酸基团能强烈地与稀土离子配位,并能高效率地敏化稀土离子,表现出高的荧光稳定性[6].基于以上优点,成功试制备1种新型的具有大的共轭结构的多官能团有机配体,即{4,4'|(3,3'|(2,6|二吡啶基)二[5|(4|甲氧基苯基)|1氢|1,3|二咪唑基]二亚甲基}二(吡啶|2,6|二羧酸)L和它的Eu(Ⅲ)和Tb(Ⅲ)配合物.
人血清白蛋白(HSA)是循环系统中重要的可溶性运输蛋白,可以同许多内源和外源性物质结合,如药物结合,同时也是体内的运输载体,起着存储和转运的作用.而牛血清蛋白(BSA)与人血清蛋白具有极高的相似性[7],所以探究稀土配合物与BSA的相互作用机制对药物的设计和应用具有非常重要的意义.
1 实验
1.1仪器与材料
1)实验用仪器的名称、型号、生产厂家见表1.
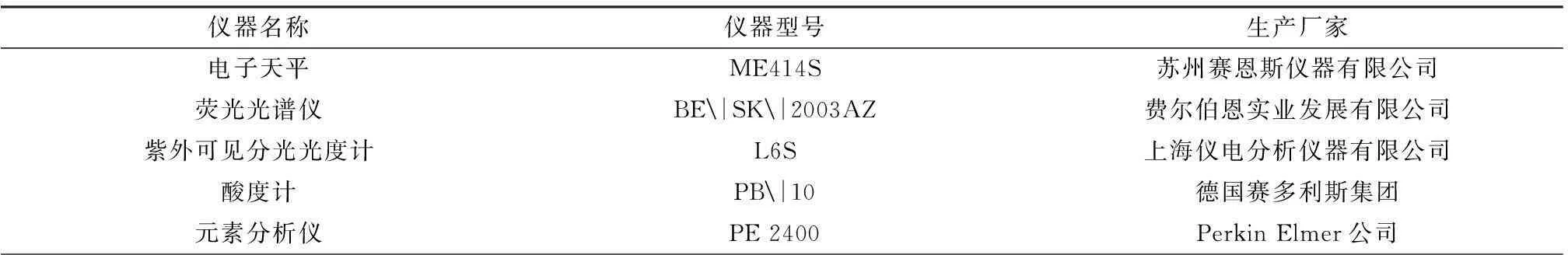
表1 实验仪器

续表1
2)实验原料.用0.1 mol/L Tris和0.1 mol/L盐酸配置pH7.4的Tris|HCl缓冲液,将此缓冲溶液配置成浓度为1.0×10-5mol/L的储备液[8];配合物Na2EuLCl5·4H2O和Na2TbLCl5·4H2O的储备液(1.0×10-3mol/L)用水配置(二次去离子水);质量分数为0.9%的NaCl溶液用于维持溶液的离子强度;吡啶|2,6|二甲酸二甲酯2和4|羟甲基|吡啶|2,6|二甲酸二甲酯3参照文献[8]、[9]中的方法制备.
1.2配体L的合成
1)取一干燥的25 mL圆底烧瓶,分别加入10 mL 无水THF,4|羟甲基|吡啶|2,6|二甲酸二甲酯3(0.5 g,2.22 mmol),搅拌溶解,将PBr3(0.9 g,3.32 mmol)缓慢滴加到上述溶液中,滴加完毕,室温搅拌12 h,反应完成后,加入NaHCO3,调节pH=7,并用CH2Cl2(3×30 mL)萃取,取有机层并加无水硫酸钠干燥,旋干有机溶剂,得淡黄色初产物.重结晶(二氯甲烷∶石油醚=1∶4),得到白色絮状固体4|甲基溴|2,6|吡啶二甲酸二甲酯4(0.5 g,78.3%).熔点:105~107 ℃;IR (KBr),νmax(cm-1):3077 (CH2),2949 (CH3),1720(C=O),1604(C-O),1443,1420,1356(skeleton of Py);1HNMR(CDCl3,10-6):δ8.73(s,2H,Py-H), 4.50(s,2H,CH2Br),4.03(s,6H,CO2CH3).
2)取新鲜钠丝 (0.92 g,40 mmol)、2,6|吡啶二甲酸二甲酯2(1.95 g,10 mmol)和20 mL干燥过的甲苯于50 mL的圆底烧瓶中,油浴100 ℃,加热回流2 h,将10 mL含对甲氧基苯乙酮(6 g,40 mmol) 的无水甲苯溶液逐滴加入上述溶液,滴加完毕,110 ℃继续搅拌24 h,反应完全后,加入20 mL石油醚搅拌5 min,抽滤,并用石油醚洗涤滤饼3次,收集固体,红外干燥,再将固体放入烧杯中,加入少量的水,用5%盐酸调pH至3~4,过滤收集滤饼,甲醇重结晶,得到淡黄色固体2,6|二|(4|甲氧基苯甲酰乙酰基)吡啶5(3.17 g,83.2%).熔点:192~195 ℃;IR(KBr),νmax(cm-1):3422(C=C-OH),3064(CH),1620(C=O),1565(C=N);1HNMR(CDCl3,10-6):δ16.5(s,2H,OH),8.04~8.32(m,3H,J=8 Hz,Py-CH=),7.25~7.75(m,10H,J=8 Hz,Ar-H),6.9(s,2H,CH),3.8(s,6H,CH3).
3)于100 mL的圆底烧瓶中,分别加入2,6|二|(4|甲氧基苯甲酰乙酰基)吡啶5(0.86 g,2 mmol)和30 mL乙酸溶液,60 ℃搅拌反应,将8 mL(85%)的水合肼逐滴加入上述溶液,滴加完毕,130 ℃回流搅拌反应24 h,反应完全后,抽滤,用蒸馏水洗涤滤饼并用乙酸乙酯重结晶,得到白色固体2,6|二|(5|(4|甲氧基苯基)|1H|3|咪唑基)|吡啶6(0.62 g,73.3%).熔点:241~243 ℃;IR (KBr),νmax(cm-1):3201 (N-H),1675,1582,1529,1466,1315(skeleton of Ph,Py and Pyraz),1280(C-N);1HNMR(DMSO-d6,10-6):δ13.57~13.62(d,2H,J=2 Hz,NH),7.94~8.05(m,3H,J=8 Hz,Py-CH=),7.41~7.92(m,10H,J=8 Hz,Ar-H),7.35~7.37(d,2H,J=8 Hz,Pyraz),3.85(s,6H,CH3).
4)于100 mL的圆底烧瓶中,加入2,6|二|(5|(4|甲氧基苯基)|1H|3|咪唑基)|吡啶6(0.44 g,1.04 mmol)和15 mL的干燥乙腈溶液,将0.3 g的K2CO3加入其中,回流搅拌24 h.抽滤,将滤液旋干,所得粗产物经柱层析分离纯化(甲醇∶二氯甲烷=1∶19),得白色固体{4,4'|(3,3'|(2,6|二吡啶基)二[5|(4|甲氧基苯基)|1氢|1,3|二咪唑基]二亚甲基}二(吡啶|2,6|二羧酸二甲酯)7(0.31 g,79.5%).熔点:>300 ℃;IR (KBr), νmax(cm-1):2951(CH3),2851(CH2),1724(C=O),1601(C-O),1675,1582,1529,1466,1315(skeleton of Ph,Py and Pyraz);1HNMR(DMSO-d6,10-6):δ8.04~8.15(s,4H,Py-CH=),7.85~7.92(m,3H,J=8 Hz,Py-H),7.22~7.83(m,10H,J=4 Hz,Ar-H),7.1(s,1H,Pyraz),5.51~6.29(s,4H,CH2),3.88~3.99(s,12H,CH3),3.85(s,6H,CH3).
5)将0.5 g 化合物7(0.63 mmol)加入30 mL的无水甲醇溶液中,再将0.3 g KOH 溶液(30%)在冰浴下加入其中,滴加完毕,回流搅拌反应24 h,用5%的盐酸调节pH值至1后,过滤收集固体,并用乙腈和水重结晶,得到淡黄色固体4,4'|((3,3'|(2,6|二吡啶基)二(5|(4|甲氧基苯基)|1氢|1,3|二咪唑基)二亚甲基)二(吡啶|2,6|二羧酸L(0.378 g,57.1%).熔点:>300 ℃;IR(KBr),νmax(cm-1):3422(O-H),1721(C=O),1454(C=N);1HNMR (DMSO-d6,10-6):δ7.88~8.03(s,4H,Py-CH=),7.90~7.92(m,3H,J=8 Hz,Py-H),7.33~7.66(s,2H,Pyraz),7.26~7.84(m,10H,J=4 Hz,Ar-H),5.68~6.43(s,4H,CH2),3.87(s,6H,CH3),3.43-3.44(s,4H,OH).配体L的合成路线如图1所示.
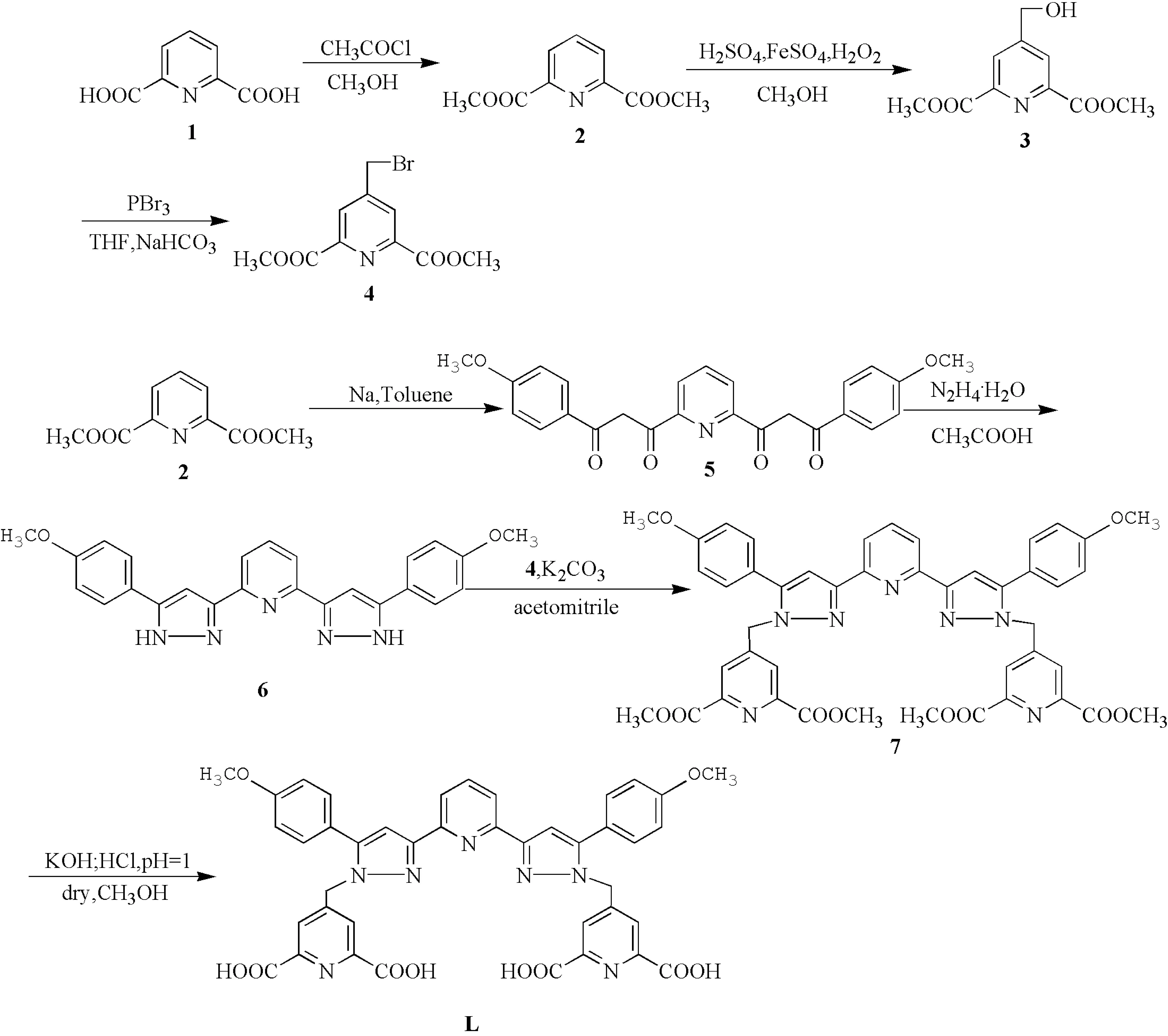
图1 配体L的合成路线
6)取0.4 mmol 配体L分别于2个50 mL的圆底烧瓶中,各加入10 mL无水甲醇,搅拌至溶解,分别将2.000 mL的0.4610 mol/L TbCl3溶液和2.000 mL的0.4401 mol/L EuCl3溶液逐滴加入其中,充分搅拌,用1.0 mol/L 的NaOH溶液调pH值至6~7,60 ℃搅拌反应24 h,溶液变浑浊,过滤,用甲醇洗涤3次,真空干燥,即得到Eu(Ⅲ)和Tb(Ⅲ)的配合物.
2 结果与讨论
2.1结构表征
2.1.1Tb(Ⅲ) 和Eu(Ⅲ)配合物的元素分析
配体L及其配合物的元素分析数据分别见表2.从表2可知,Eu(Ⅲ)和Tb(Ⅲ)这2个配合物元素分析的实验值和理论值能够较好的吻合.
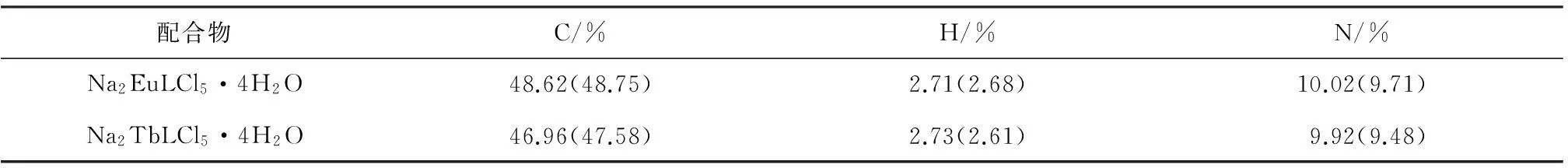
表2 配合物元素分析结果
2.1.2配体与其相应配合物的FT|IR光谱
配体L与其相应配合物的红外光谱如图2所示.
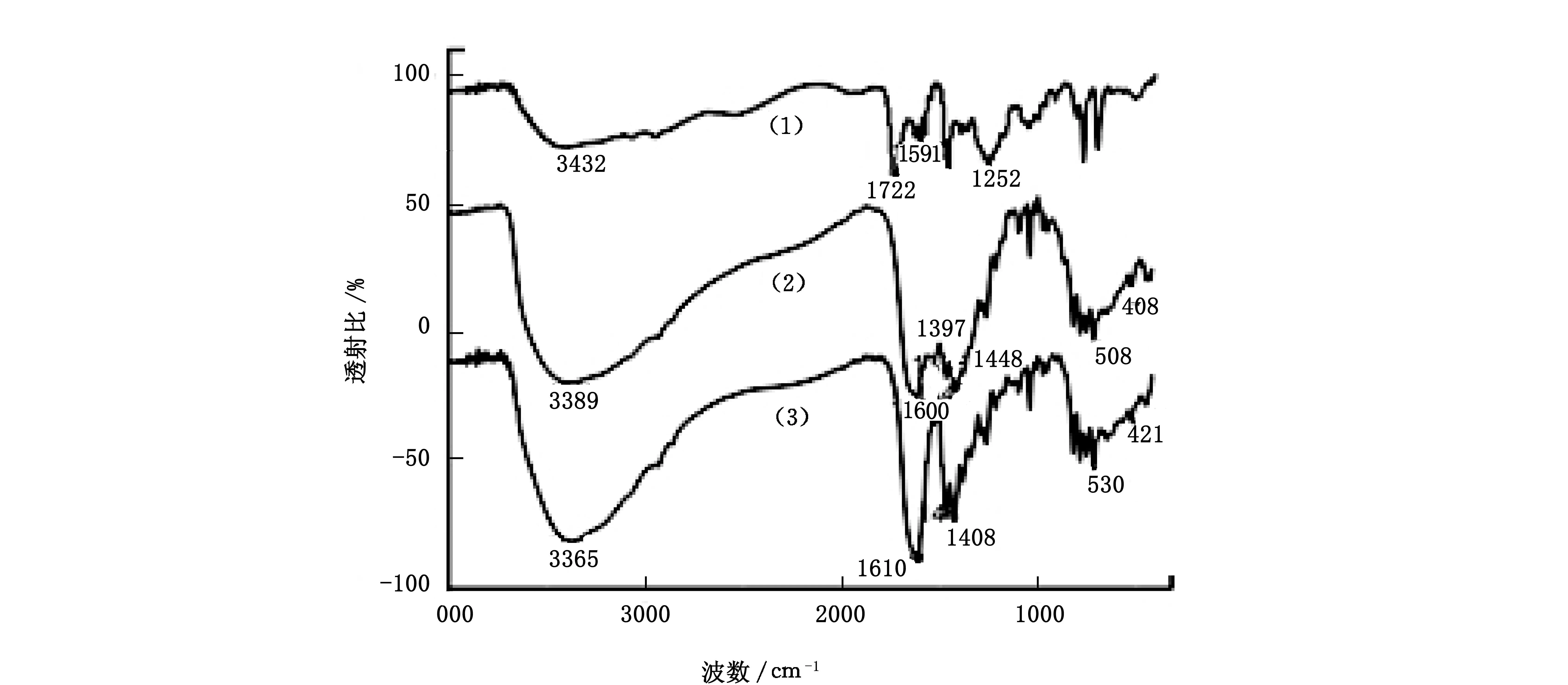
(1)配体L;(2)Na 2TbLCl 5·4H 2O;(3)Na 2EuLCl 5·4H 2O 图2 FT|IR谱图
通过分析图2中配体和配合物的红外(FT|IR)图谱可知,这2种配合物的结构相似,配体与它们的结构差别比较大.配体的ν(C=O)从1722 cm-1变为配合物中1610~1600 cm-1和1408~1397 cm-1的[νas(COO-)+νs(COO-)]峰,且在408 cm-1和421 cm-1附近的峰分别为ν(Tb-O) 和ν(Eu-O)的伸缩振动峰,表明羧基O原子参与了配位.配体的C=N伸缩振动峰从1591 cm-1分别蓝移至1440~1448 cm-1,证明配体中的吡啶环和咪唑环的N原子均与稀土离子Tb、Eu螯合,而在508 cm-1和530 cm-1附近出现了典型的ν(Re|N)吸收峰,进一步证明N原子与稀土离子发生了配位[10].配合物在3389 cm-1和3365 cm-1附近出现的峰为结晶水分子的羟基伸缩振动峰,峰型较宽.
2.1.3稀土配合物的热重分析
为探究配合物的热稳定性,在30~700 ℃范围内,对配合物Na2TbLCl5·4H2O和Na2EuLCl5·4H2O进行热分析实验(温度的上升速度为10 ℃/min).热重谱曲线如图3所示,热重分析数据见表3.它们表明配合物重量损失的实测值和理论值较匹配,由此可知配合物结构的正确性,且配合物的分解温度分别为373 ℃和385 ℃,说明配合物具有高的热稳定性.
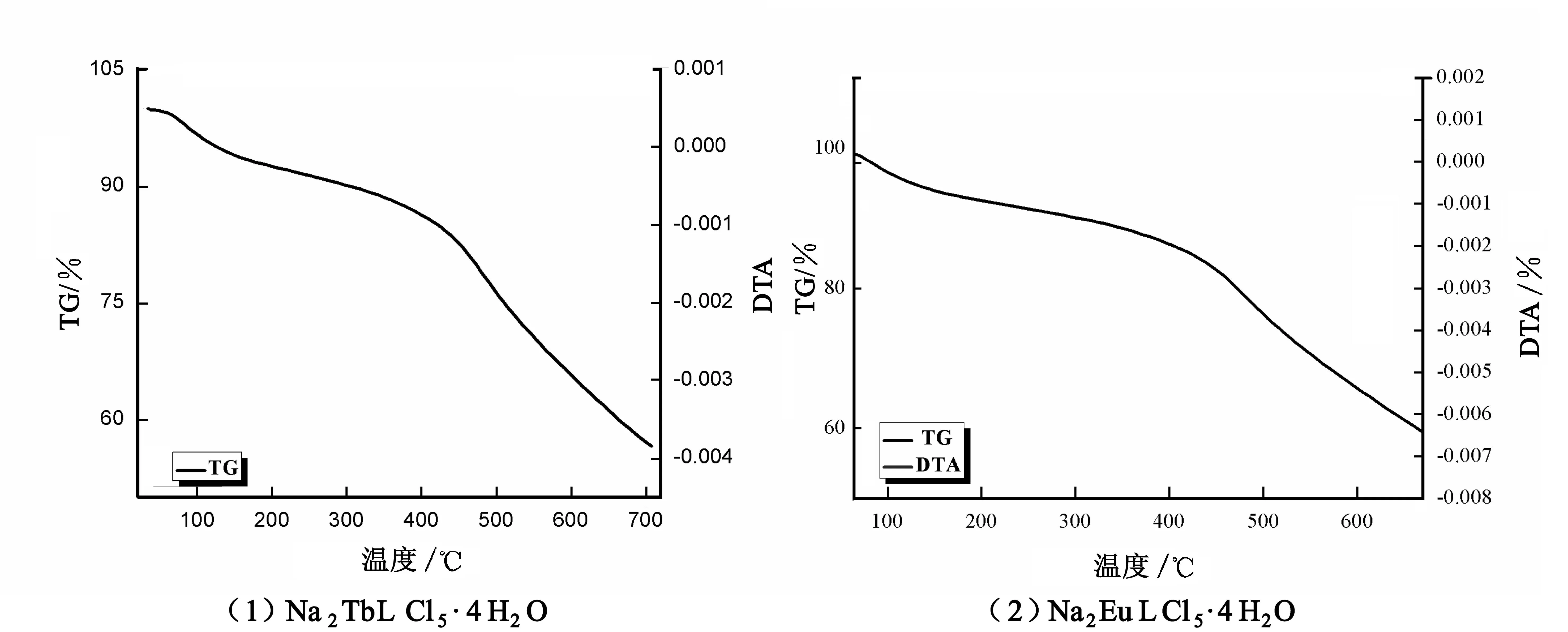
图3 配合物热重谱图

配合物阶段温度/℃质量损失/%分子损失Na2EuLCl5·4H2OⅠ30~1609.24(7.13)4H2OⅡ270~70070.34(77.66)LNa2TbLCl5·4H2OⅠ30~1808.75(6.96)4H2OⅡ280~70072.84(75.78)L
2.1.4配合物的结构
综上所述,根据元素分析(EA)、红外(FT|IR)光谱和热重分析(TG|DTA),对配合物的结构和组成进行了初步确认,结构式如图4所示.
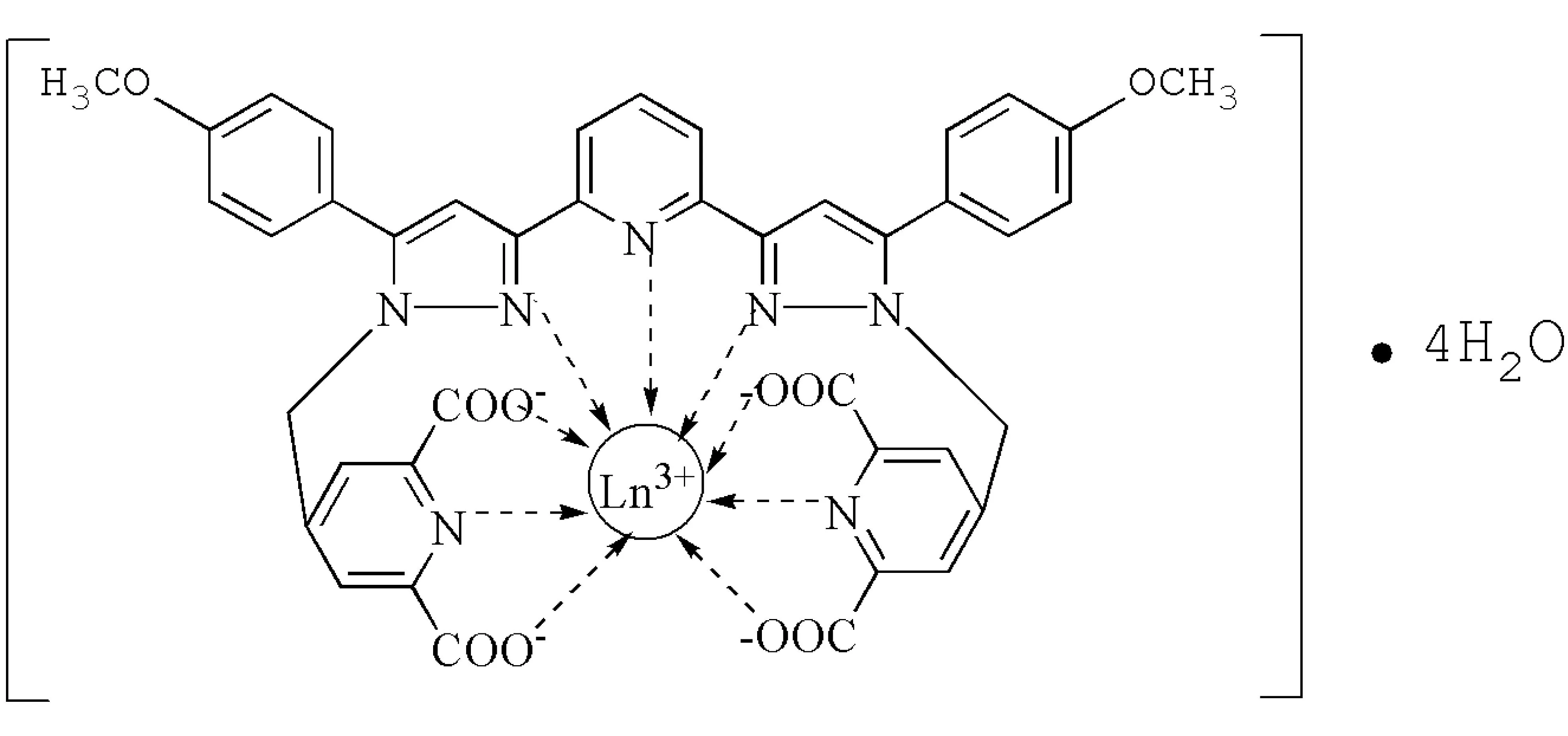
图4 配合物的结构式
2.1.5稀土配合物的荧光性能
图5是配合物Na2EuLCl5·4H2O 和Na2TbLCl5·4H2O的荧光光谱.表4分别列出了它们的激发波长、特征荧光强度和相应的电子能级跃迁.对于Eu3+配合物,从中可以观察到Eu3+离子发射峰,分别为496,550,583 ,625 nm,归属于Eu3+离子的5D0→7FJ(J=4~1) 跃迁,最强的峰为550 nm,归属于Eu3+离子的5D0→7F2跃迁.同样对于Tb3+配合物,最强的峰为472 nm,归属于Tb3+的5D4→7F7跃迁.由上述分析得知,配体L能很好地敏化稀土离子Eu3+和Tb3+[11].
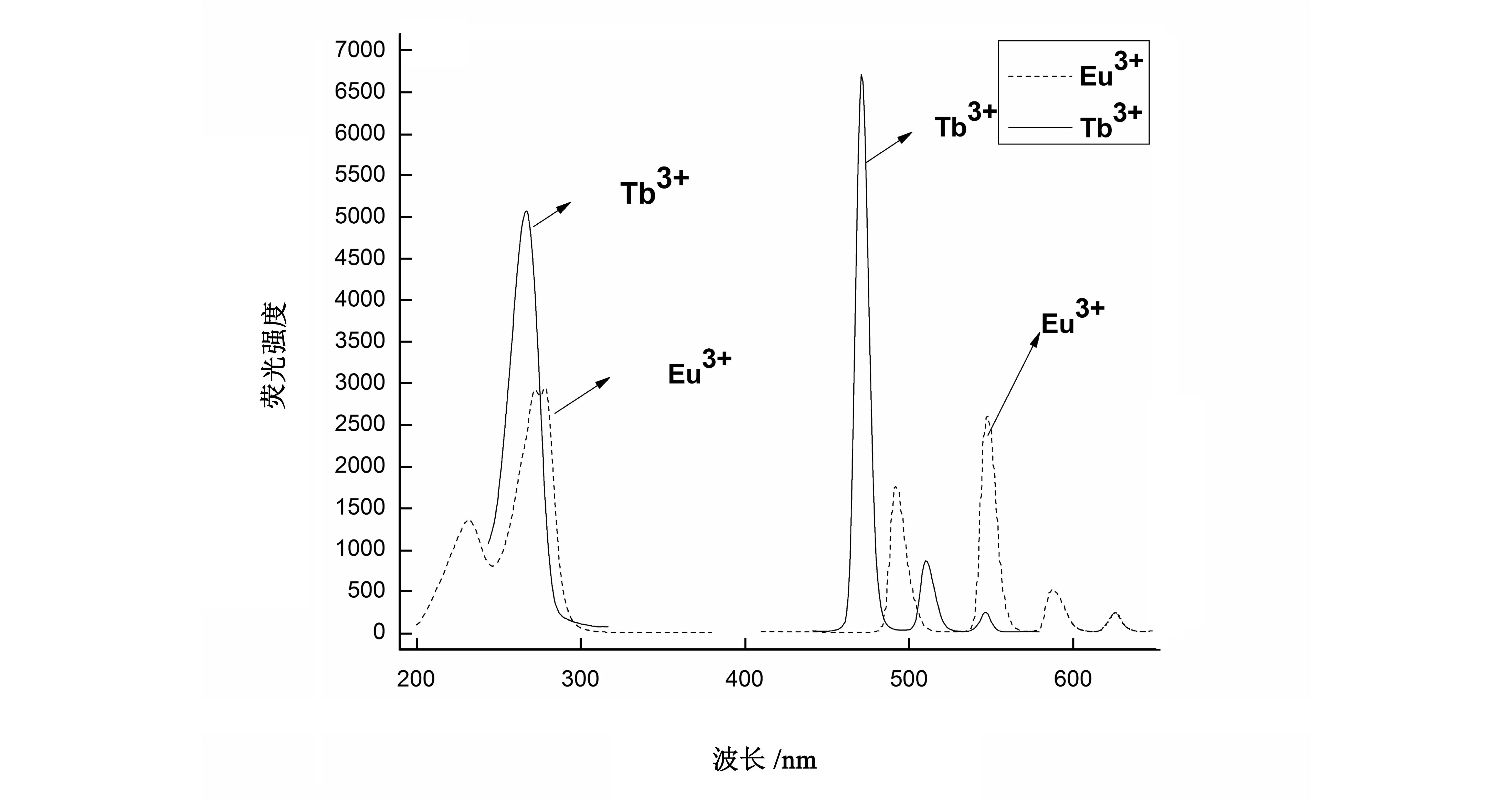
图5 Na 2EuLCl 5·4H 2O 和Na 2TbLCl 5·4H 2O的激发光谱(左)和发射光谱(右)
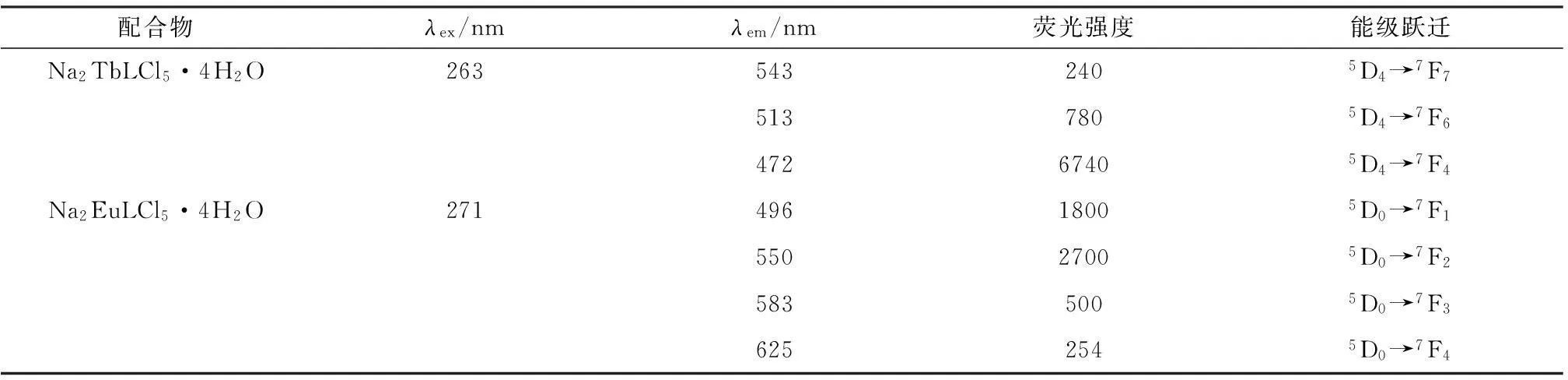
配合物λex/nmλem/nm荧光强度能级跃迁Na2TbLCl5·4H2O2635432405D4→7F75137805D4→7F647267405D4→7F4Na2EuLCl5·4H2O27149618005D0→7F155027005D0→7F25835005D0→7F36252545D0→7F4
2.2配合物与BSA的相互作用
2.2.1荧光光谱
以280 nm为激发波长,得到BSA的荧光发射峰出现在340 nm附近,且配合物在300~500 nm范围内无荧光.固定BSA浓度时,向其中不断加入配合物,随着配合物浓度的不断增加,BSA的荧光发射峰强度呈规律性递减,进而证明BSA与配合物发生了相互作用,致使荧光猝灭[12].如图6所示.
2.2.2猝灭机理
通常引起牛血清白蛋白(BSA) 内源性荧光猝灭的原因分为静态猝灭和动态猝灭2种.为研究配合物Na2TbLCl5·4H2O对蛋白质的作用机理,通过Stern|Volmer方程对荧光猝灭实验中的的数据进行分析[13]:
F0/F=1+Ksv[Q]=1+τ0kq[Q],
(1)
式中F0与F分别是加入猝灭剂前后蛋白质的荧光强度;Ksv是猝灭常数;[Q] 是猝灭剂的浓度;kq为双分子猝灭过程的速率常数,最大值为2.0×1010L·mol-1·s-1;τ0是没有加入猝灭剂时的生物大分子荧光分子的平均寿命(约为10-8s)[14].在不同温度(293,300,310 K)下,以F0/F对[Q]作图(图7),不同温度下的双分子猝灭速率常数kq和猝灭常数Ksv的值见表5.从表中可知,kq远远大于最大扩散碰撞速率常数2.0×1010L·mol-1·s-1,说明配合物Na2TbLCl5·4H2O对BSA是静态猝灭.
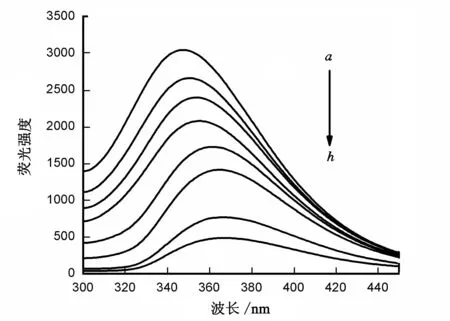
图6 Na 2TbLCl 5·4H 2O 对 BSA荧光光谱的影响
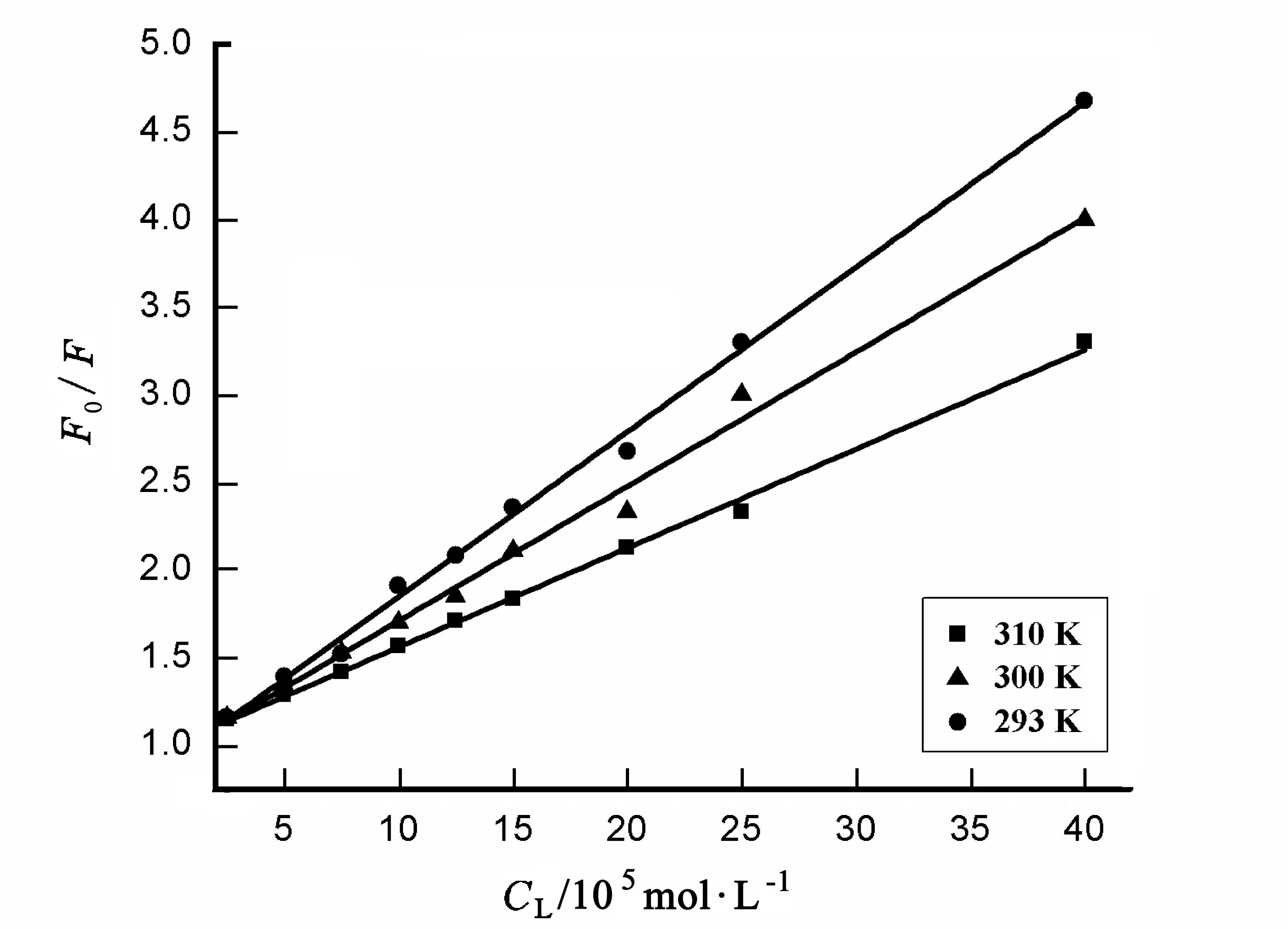
图7 Na 2TbLCl 5·4H 2O对 BSA猝灭的Stern|Volmer曲线

T/KnKsv/L·mol-1kq/L·mol-1·s-1ka/L·mol-1ΔH/kJ·mol-1ΔS/J·mol-1·K-1ΔG/kJ·mol-1R22931.109.26×1049.26×10121.89×105-53.26-96.16-28.630.996683001.037.42×1047.42×10121.02×105——-21.570.992233100.921.13×1041.13×10125.61×104——-21.430.99723
注:R2为Ksv的相关系数.
2.2.3结合常数及其结合位点数
配合物对BSA的猝灭过程为静态荧光猝灭,可通过公式(2)[15]求得结合常数和结合位点数.
log(F/(F0-F)=log1/ka+nlog1/[Q],
(2)
式中:F0与F分别是加入猝灭剂前后的荧光强度,Ka是结合常数,n是结合位点数.从表5可知,Na2TbLCl5·4H2O的n均在1左右,说明配合物与BSA只有1个结合位点.
2.2.4热力学参数
配合物与BSA之间的作用力类型可通过热力学参数(熵变ΔS和焓变ΔH)的大小来判断.根据Van't Hoff方程计算得
lnka=-ΔΗ/RT+ΔS/R ,
(3)
ΔG=ΔΗ-TΔS,
(4)
式中:Ka是猝灭剂与BSA之间的结合常数,R是理想气体常数.通过式(4)求得吉布斯自由能ΔG.热力学参数值见表5.从表5可知,配合物与BSA反应的吉布斯自由能ΔG、焓变ΔH和熵变ΔS均<0,表明配合物与BSA之间是可以自发进行的且其作用力主要为范德华力和氢键.
3 结语
合成了一种新型的化合物,4,4'|((3,3'|(2,6|二吡啶基)二(5|(4|甲氧基苯基)|1氢|1,3|二咪唑基)二亚甲基)二(吡啶|2,6|二羧酸(L)和它相应的配合物Na2EuLCl5·4H2O、Na2TbLCl5·4H2O.通过元素分析、热重差热分析以及红外光谱初步确认了该配合物的组成和结构.运用荧光光谱法和紫外光谱法分别研究了配合物Na2TbLCl5·4H2O与BSA的相互作用,证明了配合物对BSA的内源性荧光猝灭为静态猝灭过程,并且通过Van't Hoff方程计算得到ΔH、ΔS、ΔG值,从而可知该反应为自发过程,氢键和范德华力是促使配合物与BSA结合的主要作用力.这2个配合物在不同温度下的结合常数都在1.0×104L·mol-1以上,说明配合物易与BSA结合.
参考文献:
[1] 刘政,孙丽宁,施利毅,等.近红外稀土荧光在功能材料领域的研究进展[J].化学进展,2011,23(1):154|162.
[2] Bettencourt|Dias A D.Small molecule luminescent lanthanide ion complexes|photophysical characterization and recent developments[J].Curr Org Chem,2007(11):1460|1480.
[3] 王晓龙,李彦锋,张树江,等.主链含吡啶环的聚合物[J].化学通报,2005(5):329|337.
[4] Shyni R,Biju S,Reddy M L P,et al.Synthesis,crystal structures,and photophysical properties of homodinuclear lanthanide xanthene|9|carboxylates[J].Inorg Chem,2007,46:11025|11030.
[5] 刘崇波,贺谊,刘淑芳,等.Eu3+和Tb3+的2,3|吡啶二甲酸配合物的发光研究[J].南昌大学学报:理科版,2000,24(4):341|345.
[6] Wu Q R,Wang J J,Hu H M,et al.A series of lanthanide coordination polymers with 4′|(4|carboxyphenyl)|2,2′:6′,2″|terpyridine:Syntheses,crystal structures and luminescence properties[J].Inorg Chem Commun,2011,14:484|488.
[7] 陶在琴,钱鹰.一种红光发射三苯胺吡啶盐的合成及荧光探针性质[J].有机化学,2014,34:2354|2361.
[8] Schmuck C,Machon U.Amino acid binding by 2|(guanidiniocarbonyl)pyridines in aqueous solvents:a comparative binding study correlating complex stability with stereoelectronic factors[J].Chem Eur J,2005(11):1109|1118.
[9] Gu G L,Tang R R,Zheng Y H,et al.Synthesis,characterization and fluorescence properties of novel pyridine dicarboxylic acid derivatives and corresponding Tb(Ⅲ) complexes[J].Spectrochim Acta A:Mol Biomol Spectrosc,2008,71:209|214.
[10] Shi X M,Tang R R,Gu G L,et al.Synthesis and fluorescence properties of lanthanide(Ⅲ) complexes of a novel bis(pyrazolyl|carboxyl)pyridine|based ligand[J].Spectrochim Acta A: Mol Biomol Spectrosc,2009,72:198|203.
[11] 杨青,唐瑞仁.新型对称双核β|二酮及其Eu3+三元螯合物的合成及荧光性质[J].徐州工程学院学报:自然科学版,2013,28(1):56|60.
[12] 宋国庆.SDS水溶液荧光光谱研究[J].徐州工程学院学报,2006,21(9):81|84.
[13] Liu Y C,Yang Z Y.Synthesis,crystal structure,antioxidation and DNA binding properties of binuclear Ho(III) complexes of schiff|base ligands derived from 8|hydroxyquinoline|2|carboxyaldehyde and four aroylhydrazines[J].J Organomet Chem,2009,694:3091|3101.
[14] Lakowicz J R,Weber G.A probe for structural fluctuations in macromoleculest[J].Biochem,1973,12:4161|4170.
[15] Kang J,Liu Y,Xie M X,et al.Interactions of human serum albumin with chlorogenic acid and ferulic acid[J].Biochim Biophys Acta,2004(1674):205|214.
Synthesis of Luminescence Properties of Eu(Ⅲ)and
Tb(Ⅲ)Complexes with a Novel Polyamine Polycarboxylic Ligand as well as
Their Binding Characteristics with Bovine Serum Albumin
WANG Guangbin1,MA Jie2,CHEN Kuizhang3
(1.Xuzhou Lvjian Dairy Co., Ltd. ,Xuzhou 221006,China;
2.Xuzhou Institute of Technology,Xuzhou 221018,China;
3.Environmental Emergency and Accident Investigation Center of Xuzhou ,Xuzhou 221002,China)
Abstract:A novel ligand (L) and its corresponding complexes Na2EuLCl5·4H2O and Na2TbLCl5·4H2O,were prepared and characterized.The thermogravimetric analysis shows the two complexes have good thermal stabilities with decomposition temperatures 373 and 385 ℃,respectively.The luminescence spectra showed that the ligand L was an efficient sensitizer for Eu(Ⅲ)and Tb(Ⅲ)luminescence.The UV|vis absorbance and the Stern|Volmer analysis indicate that the main quenching mechanism is a static quenching procedure.The binding constants, binding site number at different temperatures were calculated by Van't Hoff equation, which confirms that the Van der Waals and hydrogen bond interactions are mainly impulse to the formation of complexes BSA|L coordination compound.
Key words:luminescence spectra; BSA; Eu(Ⅲ)and Tb(Ⅲ)complexes
(编辑徐永铭)
