吉西他滨联合顺铂与紫杉醇联合顺铂方案一线治疗晚期肺鳞癌临床比较
2015-12-15崔洪霞李玉权马丽霞吉林省肿瘤医院内一科吉林长春130012
崔洪霞 李玉权 马丽霞 程 颖 (吉林省肿瘤医院内一科,吉林 长春 130012)
吉西他滨联合顺铂与紫杉醇联合顺铂方案一线治疗晚期肺鳞癌临床比较
崔洪霞李玉权马丽霞程颖(吉林省肿瘤医院内一科,吉林长春130012)
〔摘要〕目的比较吉西他滨联合顺铂(GP)与紫杉醇联合顺铂(TP)方案治疗晚期肺鳞癌临床疗效及不良反应。方法回顾性分析我院初治的76例晚期肺鳞癌患者的临床资料,37例接受GP方案化疗,39例接受TP方案化疗,每2个周期评价疗效和不良反应。结果GP组及TP组近期疾病控制率、中位总生存期及1年生存率无明显差异; GP组的近期有效率高于TP组,低分化鳞癌有效率、中位无疾病进展生存期GP组长于TP组差异有统计学意义。不良反应: GP组血小板减少发生率高于TP组,而TP组白细胞下降、贫血及脱发发生率高于GP组。结论在晚期肺鳞癌一线治疗中,低分化鳞癌有效率高于高分化鳞癌,GP组近期有效率高于TP,中位无疾病进展生存期GP组长于TP组,两组药物不良反应均可耐受。
〔关键词〕肺鳞癌;一线化疗;临床疗效;不良反应
肺癌是对人类健康和生命威胁最大的恶性肿瘤之一,其发病率和死亡率增长均较快〔1〕。肺癌包括小细胞肺癌和非小细胞肺癌。其中非小细胞肺癌约占肺癌的85%,主要包括鳞状细胞癌和非鳞状细胞癌,其中肺鳞癌的发病比例在减少,但仍是肺癌的主要病理类型之一(约占肺癌的30%)。近年来随着分子靶向药物在晚期非小细胞肺癌中的应用,为晚期非小细胞肺癌的治疗尤其是肺腺癌的治疗提供了除了化疗以外的新的治疗策略,但肺鳞癌的治疗一直没有突破性的进展,目前临床上仍采用以顺铂或卡铂为基础的紫杉醇、多西紫杉醇、吉西他滨、长春瑞滨等二联方案为主进行治疗。本研究对吉西他滨联合顺铂(GP)与紫杉醇联合顺铂(TP)方案一线治疗晚期肺鳞癌患者,比较临床疗效。
1 资料与方法
1. 1一般资料回顾性分析2010年1月至2012年12月吉林省肿瘤医院应用GP及TP方案一线治疗的76晚期肺鳞癌患者,随访时间5~36个月,中位随访时间为10个月(截止时间2013年12月)入组患者均为经细胞学或组织学确诊的ⅢB-Ⅳ期肺鳞癌,其中39例患者接受TP方案治疗,37例接受GP方案治疗。两组患者均具有可测量或可评价的肿瘤病灶,预计生存期>3个月,以往未接受任何抗肿瘤治疗,PS评分为0~1分,无化疗禁忌证。患者临床资料见表1。
1. 2治疗方法患者均采用国产化疗药物,其中GP组: GEM 1 000 mg/m2静脉滴注d1、8,DDP 75 mg/m2静脉滴注d1~3; TP 组Taxol 135~175 mg/m2静脉滴注d1,DDP 75 mg/m2静脉滴注d1~3。TP组用药前1 d口服地塞米松8 mg/次,2次/d,连续服3 d,21 d为1个化疗周期,患者至少接受2个化疗周期,化疗后评价疗效及不良反应。如患者病情稳定或缓解的则按原方案继续化疗2~4个周期。
1. 3评价标准(1)根据实体瘤疗效评价标准(RECIST)1. 1版分为:完全缓解(CR)、部分缓解(PR)、稳定(SD)和进展(PD),客观有效率(RR)为CR + PR,疾病控制率(DCR)为CR+ PR+SD。(2)按照NCI-CTC 4. 0(2009)毒性分级标准进行不良反应评价,不良反应分0~4级。化疗前复查肝肾功能等项目,化疗期间每周复查血常规并记录各种不良反应。(3)总生存期(OS)是指从初始治疗至死亡或失访的时间。无进展生存期(PFS)是指初始治疗至客观证据表明疾病进展或患者死亡的时间。1年生存率为1年存活患者例数/校正总患者例数× 100%。
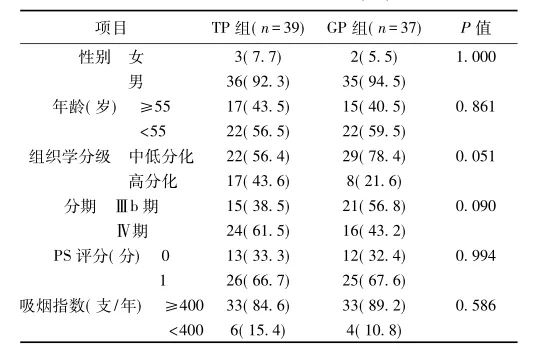
表1 两组患者临床特征〔n(%)〕
1. 4统计学分析采用SPSS13. 0软件系统进行分析,运用χ2检验比较RR、DCR,采用Kaplan-meier法计算患者生存率,logrank检验进行生存比较。
2 结果
2. 1近期疗效76例患者中有22例(28. 9%)获得缓解,GP 组RR为40. 5%,TP组RR为17. 5%,组间比较差异有统计学意义(P<0. 05)。中低分化鳞癌患者RR高于高分化鳞癌,组间差异有统计学意义(P<0. 05),ⅢB期与Ⅳ期患者的RR比较差异无统计学意义(P>0. 05)。GP组DCR为86. 5%,TP组DCR 为75. 0%,两组差异无统计学意义(P>0. 05)。高分化与中低分化鳞癌的DCR比较,差异无统计学意义(P>0. 05)。ⅢB期与Ⅳ期的DCR比较,差异无统计学意义(P>0. 05)。见表2。

表2 76例患者的近期疗效〔n(%)〕
2. 2远期疗效76例患者全部进入生存统计。截尾统计数据共27例(存活20例,失访7例),其中GP组15例(40. 5%),TP 组12例(30. 0%)。GP组患者1年生存率为32. 1%,TP组1年生存率为29. 2%,差异无统计学意义(χ2=0. 726,P>0. 05)。GP组中位生存期(mOS)为10. 0个月,TP组mOS为9. 0个月,组间生存时间差异无统计学意义(P>0. 05)。76例患者随访期内疾病无进展或失访者共11例(14. 3%),其中GP组7例(18. 9%),PFS为18. 0 w,TP组4例(10. 0%),PFS为13. 0 w,差异有统计学意义(P<0. 05)。见图1、图2。
2. 3不良反应主要的不良反应为骨髓抑制、胃肠道反应、肝肾功能异常、脱发及骨关节疼痛。两组近期毒性比较显示,两组中恶心、呕吐发生率相似。GP组血小板减少发生率高于TP组,而TP组白细胞下降、贫血及脱发发生率高于GP组。GP组发生3~4级血液学不良反应中白细胞、血小板减少者分别为8例(13. 5%)和4例(10. 8%); TP组3~4级白细胞减少及贫血分别为12例、5例,未见其他3~4级不良反应。见表3。
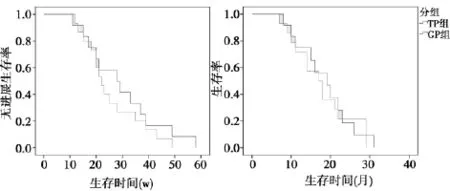
图1 两组患者PFS情况 图2 两组患者mOS情况

表3 两组不良反应比较〔n(%)〕
3 讨论
紫杉醇是紫杉醇属细胞毒类化合物,为抗微管药物,主要通过促进微管蛋白组装成微管和阻止其解聚,使微管的生理功能受到破坏,从而抑制肿瘤细胞的有丝分裂,导致肿瘤细胞死亡〔2〕。吉西他滨是细胞周期特异性抗代谢类药物,主要作用于DNA合成期的肿瘤细胞,在一定条件下,也可以阻止细胞由G1期向S期的进展,使DNA链合成停止,进而使DNA断裂导致细胞死亡。紫杉醇、吉西他滨与顺铂联合治疗具有协同和叠加作用,两药联用有效率为30%~45%〔3〕。美国东部肿瘤协作组(ECOG)进行了一项较大规模的临床随机研究,比较4种第三代联合化疗方案对晚期非小细胞肺癌的疗效,这4种化疗方案为紫杉醇+顺铂、吉西他滨+顺铂、多西紫杉醇+顺铂和紫杉醇+卡铂,研究发现这4种方案缓解率均在15%~36%,总生存期一般为8~10个月〔4~7〕,1年生存率不超过30%~40%〔8〕,仅少数试验〔9〕的中有报道GP在鳞癌中有更好的生存优势。
本研究选择鳞癌进行观察,结果显示近期疗效中GP组及TP组的DCR均无明显差别,远期疗效中mOS及1年生存率无明显差别但GP组的近期RR高于TP组,同时低分化鳞癌RR优于高分化鳞癌。远期疗效中GP组和TP组的PFS差异有统计学意义。原因考虑低分化鳞癌对化疗比高分化鳞癌敏感,而GP组中低分化比例高于TP组。对于鳞癌患者选择GP方案可能有一定优势,但需进一步行大样本前瞻性临床研究。
4参考文献
1 Yang L,Parkin DM,Ferlay J,et al.Estimates of cancer incidence in China for 2000 and projections for 2005〔J〕.Cancer Epidemiol Biomarkers Prev,2005; 14(1): 243-50.
2 Kingston DG,Samaramayake G,Lvey CA.The chemistry of taxol,a clinically useful anticancer agent〔J〕.J Nat Prod,1990; 53(1): 11.
3 Liu L,Wang XW,Li L,et al.A randomized comparative trial of There combined regimens containing cisplatin for treatment of advanced nonsmall-cell lung cancer〔J〕.Chin J Cancer,2006; 25(8): 990-4.
4 Schiller JH,Harrington D,Belani CP,et al.Comparison of four chemotherapy regimens for advanced non-small cell lung cancer〔J〕.N Engl J Med,2002; 346(2): 921.
5 Bonomi P,Kim K,Fairclough D,et al.Comparison of survival and quality of life in advanced non-small-cell lung cancer patients treated with two dose levels of paclitaxel combined with cisplatin versus etoposide with cisplatin: results of an Eastern Cooperative Oncology Group trial〔J〕.J Clin Oncol,2000; 18(3): 623-31.
6 Giaccone G,Splinter TA,Debruyne C,et al.Randomised study of paclitaxel-cisplatin versus cisplatin-eniposidein patients with advanced non-smallcell lung cancer. The European Organization for Research and Treatmentof Cancer Lung Cancer Cooperative Group〔J〕.J Clin Oncol,1998; 16(6): 2133-41.
7 Cardenal F,Lopez-Cabrerizo MP,Anton A,et al.Randomized PhaseⅢ study of gemcitabine-cisplatin versus etoposide-cisplatin in the treatment of locally advanced or metastatic non-small-cell lung cancer〔J〕.J Clin Oncol,1999; 17(1): 12-8.
8 Schiller JH,Harrington D,Belani CP,et al.Eastern Cooperative Oncology Group. Comparison of four chemotherapy regimens for advanced nonsmall-cell lung cancer〔J〕.N Engl J Med,2002; 346(2): 92-8.
9 Adams VRs,Harvey RD. Histological and genetic markers for non-smallcell lung cancer; customizing treatment based on individual tumor biology 〔J〕.Am J Health Syst Pharm,2010; 67(1): 3-9.
〔2014-11-04修回〕
(编辑滕欣航)
通讯作者:程颖(1962-),女,主任医师,博士生导师,主要从事肺癌研究。
〔文章编号〕1005-9202(2015)20-5811-03;
doi:10. 3969/j. issn. 1005-9202. 2015. 20. 061
〔文献标识码〕A
〔中图分类号〕R734. 2
第一作者:崔洪霞(1975-),女,副主任医师,硕士,主要从事肺癌研究。
