伊马替尼治疗慢性髓细胞白血病慢性期临床疗效观察
2015-12-14朱晓峰蔡晓燕
朱晓峰,蔡晓燕
(安徽医科大学附属省立医院血液内科,安徽合肥 230001)
慢性髓细胞白血病(chronic myelocytic leukemia,CML),惯称慢粒,是一种造血干细胞恶性克隆性扩增为特征的骨髓增生性疾病,起病缓慢,其主要发病基础是有标志性Ph染色体t(9;22)(q34;q11)形成BCR-ABL融合基因为其标记性改变;甲磺酸伊马替尼(IM)是BCR-ABL酪氨酸激酶的靶向抑制剂,基于IRIS(international randomized interferon ver-sus STI571)试验,在 NCCN(national comprehensive cancer network)指南中将其推荐为CML的首选治疗药物;我们回顾性分析了74例在我院参加GIPAP(glivec international patient assistance program)项目CML慢性期患者应用伊马替尼的疗效及疗效影响因素。
1 资料与方法
1.1 一般资料 从2008年6月—2014年6月在我院加入GIPAP项目的CML慢性期患者74例,其中男48例,女26例,中位年龄45(13~69)岁,所有患者均经过骨髓细胞形态学、染色体及融合基因检查确诊;嗜碱粒细胞数0.031(0~0.19),脾肋下5(0~25)cm;依据从确诊到服用IM治疗前病程的长短分为初治组(病程≤6个月,共41例)、复治组(病程>6个月,共33例),所有患者在服用IM治疗前的主要治疗药物为羟基脲、干扰素或羟基脲联合干扰素等,但均未达到主要细胞遗传学缓解;依据欧洲白血病治疗及转归研究中心(EUTOS)评分将患者分为低危组(45例)、高危组(29例),EUTOS评分是根据公式计算,即7×外周血嗜碱性粒细胞百分比+4×脾脏在肋缘下面大小(cm),评分≤87为低危组患者,>87为高危组患者;所用甲磺酸伊马替尼为瑞士诺华公司产品(商品名:格列卫),中位治疗剂量为400(200~600)mg·d-1,中位治疗时间25(6~72)月,随访截止日期为2014年12月1日,中位随访时间为20(6~72)个月。
1.2 治疗方法 IM治疗剂量为200~600 mg·d-1,慢性期患者 400 mg·d-1、1 例 13 岁慢性期患者给予300 mg·d-1,治疗初期每2周复查血常规,依据IM血液学毒性调整IM剂量;所有患者在治疗的第3、6、9、12、18、24 个月给予复查骨髓细胞形态学、染色体核型及定量检测BCR-ABL转录本表达,超过24个月者在一般情况尚可的前提下每半年复查一次染色体核型及定量检测BCR-ABL转录本表达;对IM治疗期间BCR-ABL转录本表达呈动态增高趋势患者剂量调整为600 mg·d-1;治疗过程中进展为加速期或急性变期患者剂量调整为600 mg·d-1(急性变期患者均联合化疗)。
1.3 疗效评估 参照国内2013年中国慢性髓性白血病(CML)诊疗指南,分为血液学完全缓解(CHR)、主要细胞遗传学缓解(MCyR)、完全细胞遗传学缓解(CCyR)、主要分子生物学缓解(MMR)、完全分子生物学缓解(CMR)。
1.4 疾病无进展生存率(PFS)及总生存率(OS)评估 疾病无进展生存率(PFS)为从服用IM治疗后疾病获得缓解至疾病进展或最后一次随访时间;总生存率(OS)指从患者服用IM至死亡日或行造血干细胞移植日或最后一次失访时间。
1.5 统计学处理 应用SPSS 19.0软件进行分析,数据以中位数(范围)表示,各组间率的比较用χ2检验及Fisher确切概率法,疾病无进展生存率及总生存率采用Kaplan-Meier方法进行分析,生存率采用Log-Rank法检验,以P≤0.05为差异有统计学意义。
2 结果
截止到2014年12月1日,74例患者中有1例患者在治疗1年后死亡,死于CML急性变;3例患者在治疗2年后失访,其中2例达主要细胞遗传学缓解,1例达部分细胞遗传学缓解;1例患者在治疗3个月时出现较严重消化道反应,剂量调至最低200 mg·d-1时仍然不能耐受,在治疗的第6个月更换为口服尼罗替尼;另1例患者在治疗9个月时定量检测BCR-ABL P210转录本表达呈逐渐增高趋势,且出现甲磺酸伊马替尼耐药基因(ABL1激酶PLoop区发生突变),治疗第12个月时更换为口服尼罗替尼;其余患者目前仍继续服用甲磺酸伊马替尼。
2.1 累积获得治疗反应 至随访截止日期,所有患者中除1例患者疾病进展死亡外,其余73例患者均达到血液学缓解(CHR),缓解率为98.6%,中位缓解时间1(1~3)个月;63例(85.1%)达到MCyR,中位达MCyR时间为9(5~24)个月;53例(71.6%)达CCyR,41 例(55.4%)达到MMR;6 例(8.1%)达到CMR,达到CMR患者中4例为初治组患者,2例为复治组患者,但均为EUTOS评分低危组。
2.2 不同组别间的治疗疗效观察 初治组与复治组应用IM治疗后CHR及MCyR差异无统计学意义,但CCyR及MMR差异均有统计学意义(见表1);由EUTOS评分区分的低危组与高危组应用IM治疗后CHR差异无统计学意义,但MCyR、CCyR及MMR差异均有统计学意义(见表2)。

表1 CML慢性期患者初治组与复治组疗效比较
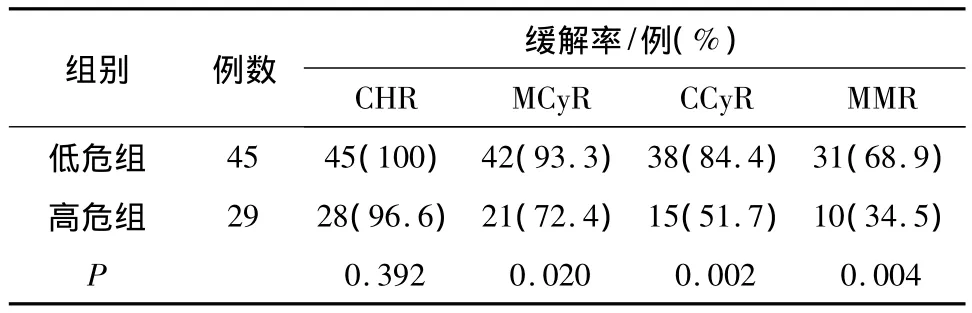
表2 CML慢性期患者EUTOS评分低危组与高危组疗效比较
2.3 不同组别间患者的OS及PFS比较 所有患者中位随访时间为20个月,其中初治组与复治组及EUTOS评分低危组与高危组OS差异无统计学意义(P>0.851),但其PFS差异均有统计学意义(P <0.021)。
2.4 不良反应与处理 应用IM治疗后,部分患者出现血液学不良反应,主要为白细胞、血红蛋白及血小板减少,分别占 14.9%、12.2%、9.5%;非血液学不良反应主要表现为水肿、恶心、骨关节与肌肉疼痛、皮疹,分别占 33.8%、27.0%、25.7%、10.8%;经过对症处理后大多均可耐受。
3 讨论
甲磺酸伊马替尼通过作用于BCR-ABL融合基因的ATP结合位点来抑制ABL激酶活性,且具有高度特异性,从而使BCR-ABL阳性细胞的增殖受到抑制甚至发生凋亡。Almeida等[1]报道,BCRABL转录本下降水平与细胞遗传学缓解率有良好的相关性,在IM治疗过程中,定期检测染色体及BCR-ABL转录本表达对发现IM耐药及疾病进展情况最为敏感和直观,能在早期阶段发现需要临床干预的患者,对提高CML整体疗效有重要指导意义。同时IRIS试验结果也证实了IM治疗CML慢性期的疗效优于之前的任何治疗手段,且患者对IM耐受性较好,目前已经成为国际公认CML慢性期一线治疗药物,Druker等[2]研究显示,应用 IM 治疗12个月时 CCyR缓解率可达69%,60个月时可达87%,与我们本次研究基本一致。
最近几年有部分学者对CML慢性期治疗提出了早慢性期与晚慢性期的概念[3-4],即从确诊开始IM作为起始治疗与从确诊开始IM治疗前时间大于6个月的患者,前者预后相对较好,且分析显示在IM治疗前时间大于6个月或用过其他治疗方案是影响CCyR和PFS预后不良因素,也就是说,初次确诊CML慢性期患者应尽早给予IM作为起始治疗方案,而不能作为其他方案后期替代治疗,甚至是其它方案治疗效果不佳时的挽救治疗,其机制可能为CML慢性早期患者在诊断时就应用IM治疗发生耐药性几率较少,而在慢性后期开始应用IM明显增高其耐药比[5];另有说法是,在疾病早期阶段可能是骨髓中Ph+细胞数相对较少,能够正常造血的干祖细胞数储备相对比较充足,导致IM在治疗过程中相对容易达到细胞遗传学缓解[6-7]。我们的观察结果也证明 IM治疗 CML慢性期患者,其CCyR和MMR疗效初治组相对复治组患者好,且PFS率初治组比复治组患者高,但OS率差异无统计学意义;然而 Breccia 等[8-9]报道,IM 对 CML 晚慢期患者同样具有较高的细胞遗传学反应及良好的的 PFS 和 OS 时间;Yilmaz等[10-11]报道,IM 治疗前是否使用干扰素等其它治疗方案对血液学及遗传学疗效均无明显影响,对于这两种不同的观点可能需要通过扩大样本量做进一步验证。
2011年欧洲白血病治疗及转归研究中心通过用IM治疗2 060例CML患者,依据获得完全细胞遗传学缓解率及其以后的疾病无进展生存率,创建EUTOS评分系统[12];该系统通过计算患者嗜碱性粒细胞百分比和脾脏大小来区分低危组及高危组患者,与Sokal评分相比较,此评分系统对疾病的疗效及预后可能具有更强大的预测力;Sokal评分提出在IM治疗时代之前,部分学者对该评分指导预后的意义提出了质疑,多个研究表明Sokal评分得出的CML低危组、中危组及高危组患者与IM疗效及疾病无进展生存率无明显相关性[13];当然不能排除Sokal积分因涉及影响因素较多,可能是导致不同研究中心结果存在差异的可能性,其价值同样有待于扩大样本量以及进行前瞻性试验后才能得出比较确切的结论。Tao等[14]研究表明EUTOS评分低危组和高危组患者CCyR缓解率为(87%vs 52.6%,P<0.000 1),且5年预期PFS和OS时间低危组患者比高危组患者高;我们本次研究低危组和高危组患者 CCyR 缓解率为(84.4%vs 51.7%,P=0.002),其PFS时间低危组也比高危组患者高,基本一致,但两组OS时间差异无统计学意义,可能与病例数不够及随访时间较短有关。
应用IM治疗过程中其主要不良反应为血细胞减少、水肿、乏力、腹泻、恶心、皮疹、骨关节与肌肉疼痛,多数患者对症处理后均可耐受,一般不需要调整剂量或停药。
[1]Almeida MH,Fogliatto L,Couto D.Importance of adherence to BCR-ABL tyrosine-kinase inhibitors in the treatment of chronic myeloid leukemia[J].Revista Brasileira de Hematologiae Hemoterapia,2014,36(1):54 -59.
[2]Druker BJ,O’Brien SG,Guilhot F,et al.Five - year follow - up of patients receiving imatinib for chronic myeloid Leukemia[J].N Engl J Med,2006,355(23):2408 -2417.
[3]Castagnetti F,Testoni N,Luatti S,et al.Deletions of the derivative chromosome 9 do not influence the response and the outcome of chronic myeloid leukemia in early chronic phase treated with imatinib mesylate:GIMEMA CML working party analysis[J].J Clin Oncol,2010,28(16):2748 -2754.
[4]陈莹莹,曾庆曙.TKI治疗慢性粒细胞白血病慢性期的新目标转换[J].安徽医药,2014,18(11):2021 -2024.
[5]Stein B,Smith BD.Treatment options for patients with chronic myeloid leukemia who are resistant to or unable to tolerate imatinib[J].Clinical Therapeutics,2010,32(5):804 -820.
[6]Hardan I,Stanevsky A,Volchek Y,et al.Treatment with Interferon alpha prior to discontinuation of Imatinib in patients with chronic myeloid leukemia[J].Cytokine,2012,57(2):290 -293.
[7]谢杏仪,黎毓光,韩泽平,等.Hsa-miR-203联合伊马替尼对慢性粒细胞白血病K562细胞的作用[J].安徽医药,2013,17(10):1764-1766.
[8]Breccia M,Alimena G.The significance of early,major and stable molecular responses in chronic myeloid leukemia in the imatinib era[J].Critical Reviews in Oncology/Hematology,2011,79(2):135-143.
[9]金美四,李淳娥,李雪梅.甲磺酸伊马替尼治疗慢性粒细胞白血病疗效观察[J].中国现代医药杂志,2014,16(4):40 -42.
[10]Yilmaz M,Kantarjian H,Jabbour E,et al.Similar Outcome of Patients With Chronic Myeloid Leukemia Treated With Imatinib in or Out of Clinical Trials[J].Clinical Lymphoma Myeloma and Leukemia,2013,13(6):693 -699.
[11]苗圣超,糜坚青.慢性粒细胞白血病对伊马替尼的耐药机制研究进展[J].中国临床医学,2014,21(6):740 -744.
[12]Joerg H,Michele B,Verena H,et al.Predicting complete cytogenetic response and subsequent progression-free survival in 2060 patients with CML on imatinib treatment:the EUTOS score[J].Blood,2011,118(3):686 -692.
[13]Stagno F,Vigneri P,Raimondo FD.Towards a need to a“biological Sokal risk”in the era of tyrosine kinase inhibitors in choosing front- line therapy in chronic myeloid leukemia[J].Leukemia Research,2012,36(7):803.
[14]Tao ZF,Liu BC,Zhao YZ,et al.EUTOSscore predicts survival and cytogenetic response in atients with chronic phase chronic myeloid leukemia treated with first- line imatinib[J].Leukemia Research,2014,38(9):1030 -1035.
