应用便携式比色计测定水中亚氯酸盐残留浓度
2015-12-03阙绍辉秦惠邓金花吴清平
阙绍辉+ 秦惠++邓金花++吴清平
[摘 要] 本文参考五步碘量法测亚氯酸盐及N,N-二乙基对苯二胺(DPD)分光光度法原理,开发了一款环凯(HK)-便携式比色计(ClO2-)。该比色计测试量程为:0~2.0mg/L,应用于水中亚氯酸盐的测试与五步碘量法对比测试结果较为一致,合成样品测试加标回收率为:95%~103%。HK-便携式比色计(ClO2-)可在现场准确、快速测得结果。本文还探讨了测定过程中的影响因素。
[关键词] 便携式比色计;五步碘量法;亚氯酸盐残留;影响因素
中图分类号:O657 文献标识码:A 文章编号:2095-5200(2015)02-072-04
DOI:10.11876/mimt201502027
随着二氧化氯消毒剂应用日益广泛,亚氯酸盐(ClO2-)作为二氧化氯消毒剂在饮用水消毒中的主要副产物对健康威胁问题也不断凸显。国际癌症研究中心已将亚氯酸盐列为致癌物[1],世界卫生组织(WHO)[2] 和我国生活饮用水卫生标准GB5749-2006[3]均规定,使用二氧化氯消毒时,亚氯酸盐的残留浓度不得超过0.7mg/L,因此准确快速检测出亚氯酸盐残留浓度十分重要。
水中亚氯酸盐检测可能受到共存的二氧化氯本身及次氯酸、次氯酸根、氯酸根、一氯胺、二氯胺等物质干扰。干扰过多使得亚氯酸盐残留浓度的检测尤为困难。目前实验室检测方法主要有电流滴定法、碘量法、色谱法[4-5]、光谱法[6-7]、电化学法[8-9]等,这些方法有的需用到大型仪器,有的需要用到高纯氮气进行样品前处理以排除二氧化氯干扰,均不方便进行现场快速检测。
本文参考国标GB26366-2010[10]中五步碘量法及国标GB5750.11- 2006中N,N-二乙基对苯二胺(DPD)分光光度法[11]原理开发了一款亚氯酸盐便携式比色计,结合特定测试程序和定量包装配套试剂,通过调节pH进行分步测试,无需赶气即可排除游离余氯、化合性余氯、二氧化氯及氯酸盐干扰,可方便实现水中亚氯酸盐残留浓度现场快速检测。
1 方法原理
在五步碘量法中,第一步和第三步反应的pH值为7.0,而DPD分光光度法中DPD最佳显色pH为6.5[11],本文选择该仪器各步骤最终反应pH为6.5。
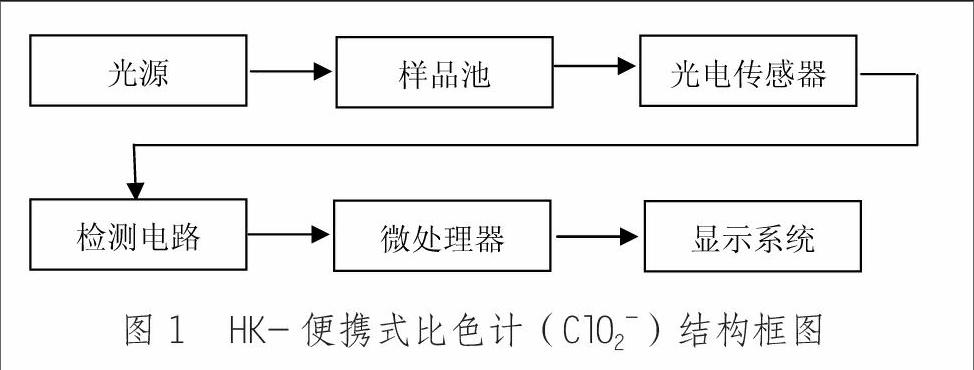
本仪器测试过程及原理如下:①样品在pH=6.5条件下,甘氨酸掩蔽游离余氯,DPD与水中20%二氧化氯发生显色反应[11],亚氯酸盐和化合性余氯不干扰测定;②重新取样,在pH=6.5及碘化钾存在条件下,部分二氧化氯、游离余氯和化和性余氯均会与碘化钾发生反应生成碘(其中二氧化氯反应方程式如(1)所述),碘与DPD显色;③继续调节0.1 2ClO2+2I-=2ClO2-+I2 (pH=6.5) (1) 2ClO2+10I-+8H+=5I2 +2Cl- +4H2O (0.1 ClO2-+4I-+4H+=2I2 +Cl-+2H2O (0.1 Cl2+2I-=2Cl-+I2 (4) 所有步骤得到吸光度值均换算成有效氯浓度,且分别记为X、Y、Z,则可推出以下结论:在步骤①中,ClO2只有1/5参与反应,则1/5ClO2产生有效氯浓度为X,根据ClO2折算成有效氯折算系数2.63(该折算系数可在标准HJ/T272-2006[12]中由公式(3)查到)可计算出ClO2质量浓度为5X/2.63;在步骤②中,游离余氯、化合性余氯以及1/5ClO2均参与反应,产生有效氯浓度为Y,在步骤③中,游离余氯、化合性余氯、亚氯酸盐、二氧化氯全部反应,产生有效氯浓度为Z,则Z-Y-4X即为亚氯酸盐有效氯浓度,根据ClO2-与Cl2电子得失数之比(2:1)(理论上1个ClO2-分子完全反应时+3价Cl转变成-1价Cl将得到4个电子(见反应式(3)),1个Cl2分子完全反应时0价Cl转变成-1价Cl将得到2个电子(见反应式(4))及分子量之比(67.5:71)可计算出亚氯酸盐质量浓度为(Z-Y-4X)/2.1。根据有效氯与DPD反应标准曲线在便携式比色计上采集原始数据,并结合上述计算公式进行编程即可方便进行亚氯酸盐测试。 2 仪器结构 本仪器结构如图1所示,主要由光源及单色器(525nm蓝光二极管),样品池(l0mL圆柱形旋盖玻璃比色管),光电传感器,检测电路,微处理器以及液晶显示系统组成。 图1 HK-便携式比色计(ClO2-)结构框图 3 仪器技术指标及使用方法 3.1 仪器技术指标 测定范围:0~2.0mg/L;检测光源:525nm;电源:9V电池;测量误差:±5%(测量温度在25℃时);使用温度:0~40℃;相对湿度:0%~90%(无冷凝);尺寸:170×70×30mm;重量:200g(含电池)。 3.2 仪器使用方法 (1)打开比色计开关,加待测水样至比色管10mL刻度线,对准“△”标志放入比色槽后盖上遮光盖,按“调零”键将仪器调零。 (2)加入4滴亚氯酸盐(Ⅰ)试剂,摇匀后加入1包亚氯酸盐(Ⅱ)试剂,摇匀溶解,对准“△”标志放入比色槽后盖上遮光盖,按“读数”键显示为二氧化氯含量(mg/L)。 (3)洗净比色瓶,重新取样至比色管10mL刻度线,加入1包亚氯酸盐(Ⅲ)试剂,对准“△”标志放入比色槽后盖上遮光盖,按“读数”键显示一中间值,该值可不记录。 (4)继续加入2滴亚氯酸盐(Ⅳ)试剂,摇匀后静置2min,再加入2滴亚氯酸盐(Ⅴ),摇匀后立即对准“△”标志放入比色槽后盖上遮光盖,按“读数”键显示亚氯酸盐浓度值(mg/L)。
4 实验部分
4.1 仪器
HK-便携式比色计(ClO2-);岛津UV-1800紫外可见分光光度;HITECH- SCIENCE TOOL实验室纯水系统。
4.2 试剂
本文所用甘氨酸、硫酸、氢氧化钠、碘化钾、DPD、碘酸钾、次氯酸钠及氯化铵均为分析纯试剂,所用水为实验室纯水系统提供超纯水。亚氯酸盐(Ⅰ)试剂:10%甘氨酸溶液;亚氯酸盐(Ⅱ)试剂:含pH6.5缓冲剂DPD试剂;亚氯酸盐(Ⅲ)试剂:含碘化钾及pH6.5缓冲剂DPD试剂;亚氯酸盐(Ⅳ)试剂:1mol/L硫酸;亚氯酸盐(Ⅴ)试剂:2mol/L氢氧化钠;亚氯酸盐标准使用液:采用标准方法(HG3250-2001)标定工业级亚氯酸钠(约80%)含量并配制成1000mg/L标准溶液(加入2mol/L氢氧化钠2mL作为稳定剂),再稀释成浓度为10.0mg/L亚氯酸盐标准使用液,该溶液在棕色瓶中保存,且现配现用;碘酸钾标准贮备液(1.006g/L):称取于120℃~140℃烘干2h碘酸钾1.006g,纯水溶解并定容至1000mL,摇匀备用。此溶液相当于1000mg/L氯(Cl2);碘酸钾标准使用溶液(10.06mg/L),吸取10.00mL贮备液,加入约1g碘化钾,纯水溶解并定容至1000mL。此标准溶液相当于10.00 mg/L氯(Cl2);二氧化氯纯溶液制备:根据GB 26366-2010中二氧化氯纯溶液制备方法制备纯ClO2 溶液,装于棕色密封试剂瓶中,于4℃冰箱中保存,临用前采用该标准中碘量法测定其浓度,并逐级稀释至试验所需浓度。
4.3 实验方法
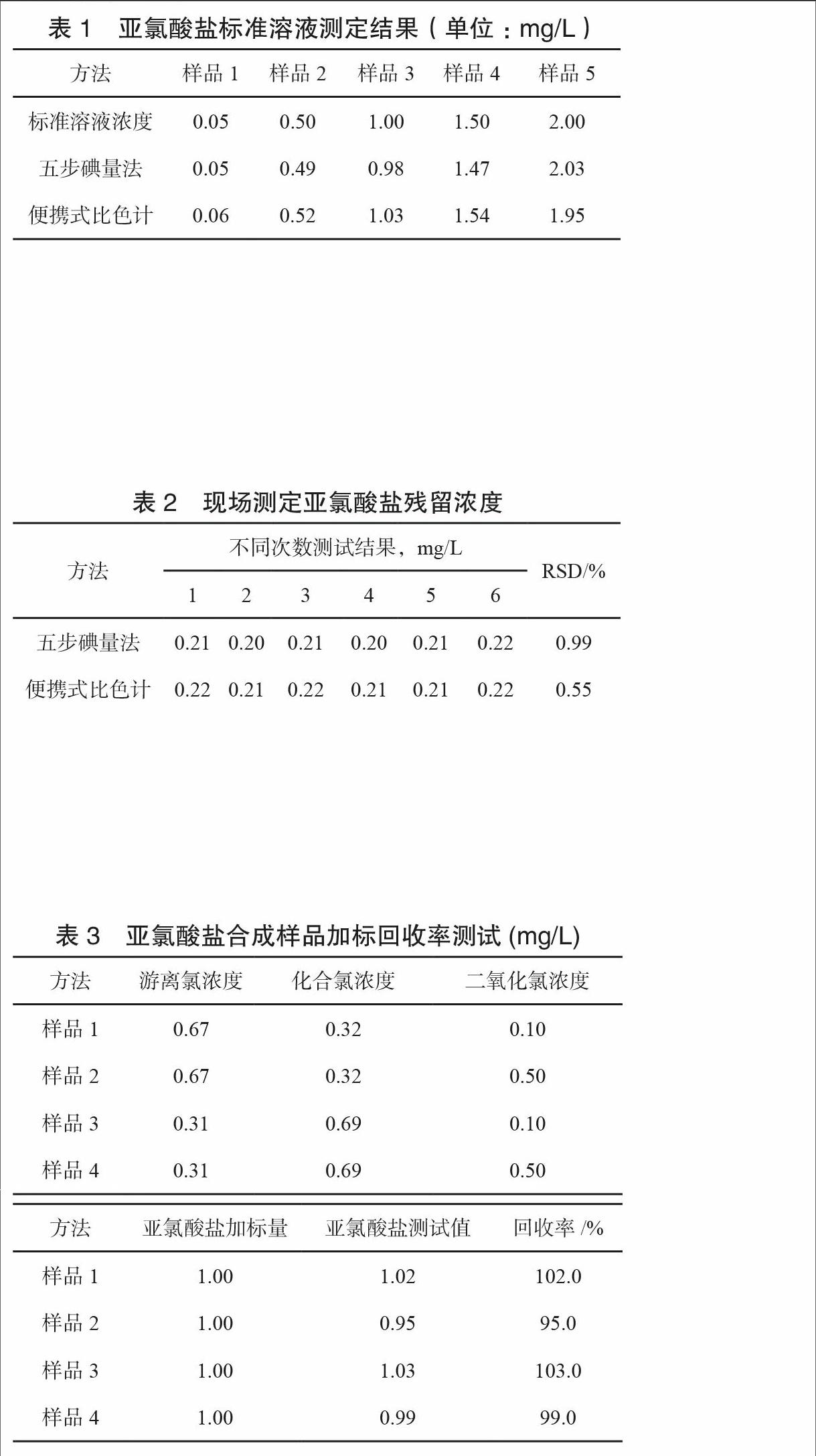
4.3.1 测定波长选择 亚氯酸盐测定最终转化为碘与DPD显色反应,直接移取10mL稀释碘酸钾标准使用溶液,加入1滴1mol/L硫酸,摇匀后加入1滴2mol/L氢氧化钠,加入1包亚氯酸盐(Ⅱ)试剂,溶解,此时溶液呈粉红色,以纯水为参比,在300~700nm范围内扫描吸收光谱。
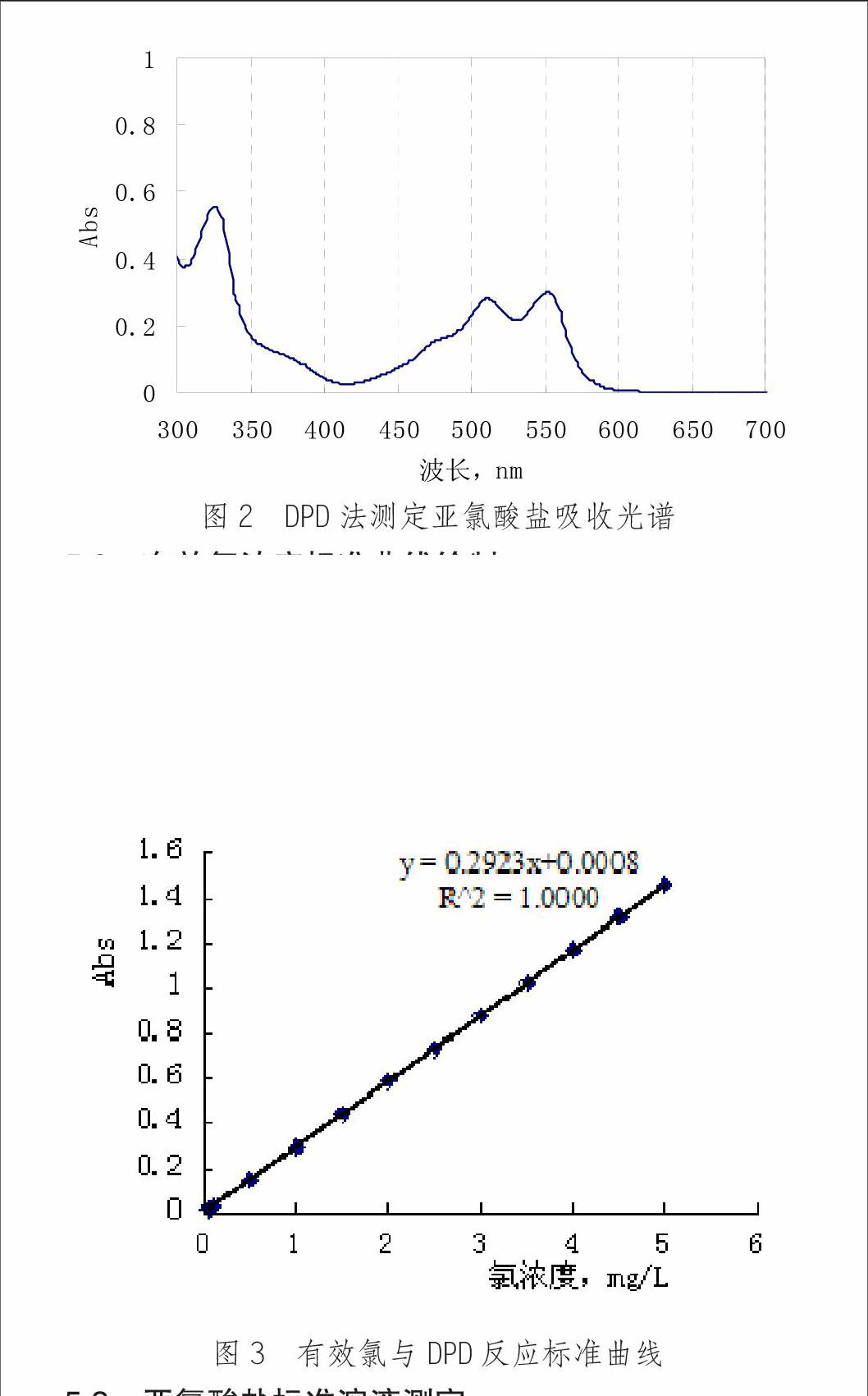
4.3.2 有效氯浓度标准曲线绘制 取11个50mL棕色容量瓶,分别加入一定量碘酸钾标准使用溶液,加纯水至约25mL,加入1mL1mol/L硫酸,2min后加入1mL2mol/L氢氧化钠,稀释至标线,摇匀,分别得到相当于氯浓度为0mg/L、0.5mg/L、1.0mg/L、1.5mg/L、2.0mg/L、2.5mg/L、3.0mg/L、3.5mg/L、4.0mg/L、4.5mg/L、5.0mg/L标准溶液。各取10mL标准液,加入1包亚氯酸盐(Ⅱ)试剂,摇匀溶解后立即以纯水为参比,采用1cm比色皿测试波长525nm处吸光度值。
4.3.3 亚氯酸盐标准溶液测定 将亚氯酸盐标准溶液稀释成一系列不同浓度亚氯酸盐溶液,分别使用五步碘量法及便携式比色计法测定其浓度,每个样品进行3次平行测定,并计算出平均值。
4.3.4 亚氯酸盐现场测定 在广州市某个采用二氧化氯消毒自来水厂采集出厂水样,分别采用五步碘量法和便携式比色计法测定亚氯酸盐残留浓度,平行测定6次,计算RSD。
4.3.5 加标回收实验 为了考察本仪器在干扰存在条件下测试结果可靠性,通过人为添加不同含量次氯酸钠、氯化铵、二氧化氯纯溶液等物质配制成含不同干扰物配比亚氯酸盐合成样品溶液。采用HK-便携式比色计(ClO2-)测定亚氯酸盐浓度,计算加标回收率。
5 结果讨论
5.1 测定波长选择
由图2可见,使用DPD法测定亚氯酸盐时在可见光区有两个吸收峰,分别是510nm与552nm,另外528nm左右也存在一个平缓波谷。DPD法测试亚氯酸盐具有较高灵敏度,为了使测试范围更宽及使测试结果更稳定,选择灵敏度相对较低且呈平台状波谷作为测试波长。在比色计设计时选择市售峰值波长接近528nm525nmLED作为光源。
5.2 有效氯浓度标准曲线绘制
结果表明(见图3),有效氯浓度在0~5.0mg/L范围内符合比尔定律,其回归方程为y=0.2923x+0.0008(x为质量浓度,mg/L)r2=1.0000。依据此回归方程进行亚氯酸盐比色计原始数据采集。
5.3 亚氯酸盐标准溶液测定
实验结果表明(见表1):便携式比色计法与五步碘量法同时测试不同浓度亚氯酸盐标准溶液,测定结果较为一致。
5.4 亚氯酸盐残留样品浓度测定
实验结果表明(见表2),便携式比色计法与五步碘量法同时现场测定亚氯酸盐残留浓度,测定结果较为一致,均具有较好测试重复性,但便携式比色计法相对而言操作更为简便,省时,更适于亚氯酸盐现场快速测定。
5.5 加标回收率实验
实验结果表明(见表3),当样品中同时存在游离余氯、化合氯、二氧化氯干扰时,便携式比色计法能在不赶气情况下便捷、准确得到测试结果,加标回收率为95%~103%。
6 影响因素探讨
6.1 测试时间影响
步骤2中加完亚氯酸盐(Ⅱ)试剂后,读数时间应控制在1min以内,否则受空气中氧或共存化合氯影响,吸光度值将逐渐升高,延长测试时间将使亚氯酸盐测试结果偏低。步骤3中加完亚氯酸盐(Ⅲ)试剂后,应在3min后读数,这样可确保所有化合性氯反应完全,若测试过快,有可能导致最终亚氯酸盐测试结果偏高。步骤4中加入2滴亚氯酸盐(Ⅳ)试剂后,需静置反应2min,否者亚氯酸盐无法与碘化钾立即反应完全,操作太快将导致亚氯酸盐测试结果偏低。步骤4中加入2滴亚氯酸盐(Ⅴ)后,应立即测试,高浓度DPD显色液本身不稳定,体系酸度或碱度超过150mg/L时也将导致DPD显色液褪色,延长测试时间将导致亚氯酸盐测试结果偏低。
6.2 测试温度影响
在10℃~40℃温度范围内进行1mg/L亚氯酸盐标准溶液测试,温度较低时会影响到粉剂溶解速度,读数前静置30s将未溶解颗粒沉降完全,未溶解物质将不干扰测定。温度高低对DPD显色反应本身无明显影响。
6.3 其它影响因素
水样总硬度值过高(超过600mg/L)也会影响粉剂溶解速度,读数前需静置30s将未溶解颗粒沉降完全;比色瓶洁净程度也是影响测试因素之一,每次测试完需立即洗净比色瓶,长时间放置后将引起有色物质在玻璃上吸附,影响测试结果准确性,建议每周用乙醇清洗一次比色管。
7 结论
(1)HK-便携式比色计(ClO2-)结合定量包装配套试剂,无需赶气即可方便实现亚氯酸盐现场快速检测,与五步碘量法比较同时测试不同浓度亚氯酸盐标准溶液和实际样品,结果较为一致;用于合成样品测试结果较为可靠,加标回收率为95%~103%。
(2)每一步测试时间控制,水样温度、酸度、碱度、总硬度,比色瓶洁净程度等因素均会影响测试结果准确性,所以测试时需按照仪器使用要求严格操作。
参 考 文 献
[1] 吴玉华.饮用水使用二氧化氯毒性及对策[J]. 环境与健康杂志, 1999, 16(1): 57-59.
[2] WHO, Guidelines for Drinking-Water Quality[S]. 3rd edi, Recommendations, Geneva , 2004: 335.
[3] 中华人民共和国卫生部, 中国国家标准化管理委员会. GB5749-2006生活饮用水卫生标准[S]. 北京:中国标准出版社.
[4] Shminke G., Seubert A., Simultaneous determination of inorganic disinfection by-products and the seven standard anions by ion chromatography[J]. Journal of Chromatography A 2000(89): 295-301.
[5] Bnghui Z., Zhixiong Z., Jing Y., Ion chromatographic determination of trace iodate, chlorite, chlorate, bromide, bromate and nitrite in drinking water using suppressed conductivity detection and visible detection[J]. Journal of Chromatography A, 2006, 1118(1): 106-111.
[6] Michael P. Doublier,Tony Roache,Sébastien Potel,et al.Short-wavelength infrared spectroscopy of chlorite can be used to determine very low metamorphic grades[J].European Journal of Mineralogy,2012,24(5):891-902.
[7] Herman M., Wieczorek M., Matuszek M., Tokarczyk J., et al. Determination of chlorite in drinking water and related aspects of environment protection[J]. Journal of Elementology, 2006, 11: 449-453.
[8] Giovanni Pezzatini,Ilaria Midili,Gabriele Toti,et al.Determination of chlorite in drinking water by differential pulse voltammetry on graphite[J].Anal Bioanal Chem,2004,380(4):650-657.
[9] John N. Myers,William H. Steinecker,Zechariah D. Sandlin,et al.Development of an automated on-line electrochemical chlorite ion sensor[J].Talanta,2012,94:227-231.
[10] 中华人民共和国卫生部, 中国国家标准化管理委员会. GB 26366-2010.二氧化氯消毒剂卫生标准[S]. 北京:中国标准出版社.
[11] 中华人民共和国卫生部, 中国国家标准化管理委员会. GB5750.11-2006生活饮用水标准检验方法消毒剂指标[S]. 北京:中国标准出版社.
[12] 国家环境保护总局. HJ/T 272-2006环境保护产品技术要求 化学法二氧化氯消毒剂发生器[S]. 北京:中国标准出版社.
