A型肉毒毒素轻链的原核表达、纯化及活性鉴定
2015-11-29罗森齐芬芳宫路路刘昊李涛王慧
罗森,齐芬芳,宫路路,刘昊,李涛,王慧
1.遵义医药高等专科学校,贵州 遵义 563002;2.军事医学科学院 微生物流行病研究所,病原微生物生物安全国家重点实验室,北京 100071
肉毒毒素(botulinum neurotoxin,BoNT)是由肉毒梭状芽孢杆菌在厌氧环境中产生的外毒素,是目前已知毒性最强的一种生物毒素,对人的致死量约为0.1 μg。根据肉毒毒素抗原性的不同,分为7 个血清型(A~G),人类的肉毒中毒主要由A、B 和E 型引起[1],其中以A 型肉毒毒素(BoNT/A)中毒更为常见,且相比其他型可引起更严重的症状和导致更高的死亡率。肉毒毒素的相对分子质量(Mr)约150×103,由N 端的一条Mr约50×103的轻链(light chain,LC)和C端的一条Mr约100×103的重链(heavy chain,HC)通过二硫键联结在一起,具有锌离子依赖的催化活性结构域位于毒素的LC 中[2-3]。肉毒毒素的致病机制是由HC 结合到后胆碱神经能细胞并易位通过细胞膜进入神经细胞释放出LC[4-6]。作为一种锌内肽酶,LC 选择性切割神经细胞内的底物SNARE蛋白,每个血清型的BoNT轻链都切割特异的底物蛋白,A 和E 型切割SNARE 蛋白中的SNAP-25[2-4],其中BoNT/A裂解SNAP-25(裂解肽键Q197-R198)。这些具有神经毒力的内肽酶通过裂解SNAP-25 从而阻断神经递质乙酰胆碱的释放,引起肌肉松弛麻痹、呼吸肌麻痹甚至导致人畜中毒死亡。在我国许多省区时有A型和B型肉毒中毒病例发生。同时,A型肉毒毒素也越来越多地被应用于美容和一些神经疾病的治疗中[10-13]。
由于肉毒毒素的稳定性差和具有剧毒性,若对其操作将面临潜在的健康危害甚至生命危险,同时,目前尚无法有效地使肉毒毒素的LC和HC分离。如能经济高效地得到有活性的稳定的肉毒毒素LC,则可避免上述问题,并可作为试剂应用于肉毒毒素酶类抑制剂高通量检测方法的研究、食品卫生、进出口检疫检验,以及对美容医疗用肉毒毒素的活性分析和检测。我们通过基因克隆技术,从A 型肉毒梭菌中调取BoNT/A LC 基因,在大肠杆菌中重组表达,通过SDS-PAGE 对重组蛋白进行鉴定,亲和纯化后,利用底物SNAP-25分析了重组蛋白的催化活性。
1 材料和方法
1.1 材料
大肠杆菌DH5α、BL21(DE3)Rosetta 感受态细胞购自北京全式金生物技术有限公司;A 型肉毒梭菌、pET-32a 表达质粒由本室保存;BoNT/A、底物SNAP-25 由本室制备保存;DNA marker、蛋白质相对分子质量标准、质粒小提试剂盒、DNA 凝胶回收试剂盒购自天根生化科技有限公司;限制性内切酶NcoⅠ和XhoⅠ购自New England Biolabs 公司;IPTG购自Promega 公司;引物合成及基因测序由生工生物工程(上海)股份有限公司完成;HisTrap FF 柱(5 mL)购自GE Healthcare公司。
1.2 引物设计与合成
根据GanBank 中A 型肉毒毒素序列(GenBank:M30196.1)中的LC 片段及载体序列,设计合成上游引 物P3(5'-CCATGGCTTATAAAGATCCTGTAAAT GGTGTT-3')和下游引物P4(5'-CTCGAGTAATCTA GTAAAATTCCTGCTGTT-3'),上、下游引物中分别引入NcoⅠ和XhoⅠ酶切位点(下划线部分)。
1.3 目的基因的克隆和原核表达载体pET-32a-BoNT/A LC的构建与鉴定
将培养的A 型肉毒梭菌菌体离心,用50 μL 0.01 mol/L 的Tris-HCl(pH7.4)重悬菌体,加入50 μL 0.5 mol/L 的KOH,96℃加热10 min,加入100 μL 0.5 mol/L 的Tris-HCl(pH6.5),12 000 r/min 离心10 min,取上清10 μL 作为模板进行PCR 扩增。PCR 扩增体系(25 μL)包括H2O 17.5 μL,Taq酶缓冲液2.5 μL,dNTP 2 μL,上、下游引物(10 μmol/L)各1 μL,Taq酶1 μL,模板1 μL。PCR 扩增条件:95℃3 min;94℃30 s,53℃40 s,72℃1.5 min,30次循环;72℃延伸10 min。用凝胶回收试剂盒回收PCR 扩增产物,连接T 载体后转化大肠杆菌DH5α,PCR 鉴定的阳性重组质粒用NcoⅠ和XhoⅠ双酶切,回收BoNT/A LC 片段,与经同样双酶切处理的pET-32a 载体用T4DNA 连接酶连接,构建成BoNT/A LC的原核表达载体pET-32a-BoNT/A LC,转化大肠杆菌DH5α,挑选阳性菌落,提取质粒,由生工生物工程(上海)股份有限公司测序鉴定。
1.4 BoNT/A LC重组蛋白的诱导表达
将鉴定正确的重组质粒转化大肠杆菌BL21(DE3)Rosetta 感受态细胞,挑选阳性菌落接种于含氨苄西林(100 mg/L)的LB 培养基中,37℃过夜培养,以1∶100 转接于LB 培养基中,37℃振荡培养至D600nm为0.6左右,加入IPTG 至1 mmol/L,20℃继续培养20 h,4℃、6000 r/min 离心20 min 收集菌体。用结合缓冲液(A 液)重悬菌体,放置冰上进行超声波破碎30 min,4℃、12 000 r/min 离心20 min,SDSPAGE分析上清和沉淀中的目的蛋白。
1.5 BoNT/A LC重组蛋白的纯化
取细菌培养液,4℃、6000 r/min 离心收集菌体,重悬于结合缓冲液(20 mmol/L 磷酸钠,500 mmol/L NaCl,40 mmol/L 咪唑,pH7.0)中,超声波破碎处理后取上清上样HisTrap FF 柱,用10 个柱床体积的结合缓冲液平衡柱子,然后用洗脱缓冲液(20 mmol/L 磷酸钠,500 mmol/L NaCl,500 mmol/L 咪 唑,pH7.4)线性梯度洗脱;收集洗脱液洗脱的样品行SDS-PAGE分析;采用Bradford法对纯化产物进行定量测定;纯化后的重组蛋白透析于缓冲液(50 mmol/L HEPES,pH7.5)中,于-20℃保存备用。
1.6 BoNT/A LC重组蛋白的活性验证
在反应 液(50 mmol/L HEPES,2.5 mmol/L DTT,10 μmol/L ZnCl2,pH7.4)中,将重组蛋白BoNT/A LC 与SNAP-25 于37℃反应30 min,同时设定一组不加BoNT/A LC 作为阴性对照。对BoNT/A LC的活性进行20% SDS-PAGE 后,考马斯亮蓝染色检测切割情况。通过BoNT/A LC(10 nmol/L)切割2~100 μmol/L 不同浓度的SNAP-25 测定动力学参数,切割反应时间为20 min,加入SDS-PAGE 上样缓冲液终止反应,将SDS-PAGE 胶用Chemi Doc XRS 成像系统(BIO-RAD)采用光密度分析法测定切割和未切割SNAP-25蛋白所占百分比。
2 结果
2.1 BoNT/A LC的基因克隆和表达质粒的构建
PCR 扩增获得BoNT/A LC 基因片段,与预期大小(1221 bp)相符(图1),测序显示与GenBank 中报道的基因序列一致性为99%。用NcoⅠ和XhoⅠ双酶切重组质粒pET-32a-BoNT/A LC,产物大小与PCR 结果一致,提示目的基因正确插入pET-32a 表达载体中(图1)。
2.2 重组蛋白BoNT/A LC 在大肠杆菌中的诱导表达与纯化
将鉴定正确的pET-32a-BoNT/A LC 质粒转化表达菌株大肠杆菌BL21(DE3)Rosetta 感受态细胞,在1 mmol/L IPTG 的诱导下进行表达。SDS-PAGE分析显示,与未诱导菌相比,诱导菌有明显表达条带,相对分子质量约为70×103,与预期相符(图2)。SDS-PAGE 分析重组蛋白经HisTrap FF 柱纯化后的产物,目的条带较为单一,纯度在90%左右,表明得到较高纯度的目的蛋白(图3)。
2.3 重组蛋白BoNT/A LC的活性检测
BoNT/A LC 可特异性识别、裂解其底物SNAP-25 蛋白的Q197-R198,将10 nmol/L 重组蛋白BoNT/A LC 与SNAP-25 在反应液(50 mmol/L HEPES,2.5 mmol/L DTT,10 μmol/L ZnCl2,pH7.5)中于37℃孵育,每2 min 检测一次,SDS-PAGE 分析结果见图4,BoNT/A LC 酶解SNAP-25 后产生了与预期相符的2条蛋白片段,说明重组蛋白BoNT/A LC 能特异性酶解底物SNAP-25。动力学参数测定表明,BoNT/A LC 酶解SNAP-25 的Km和kcat值分别为0.96±0.05 mmol/L和0.09±0.01 s-1。
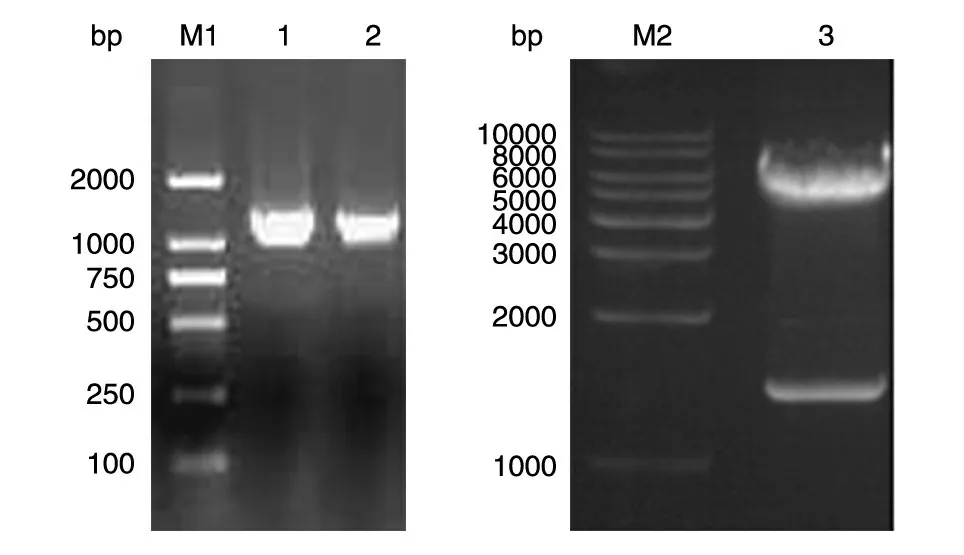
图1 BoNT/A LC基因PCR产物和
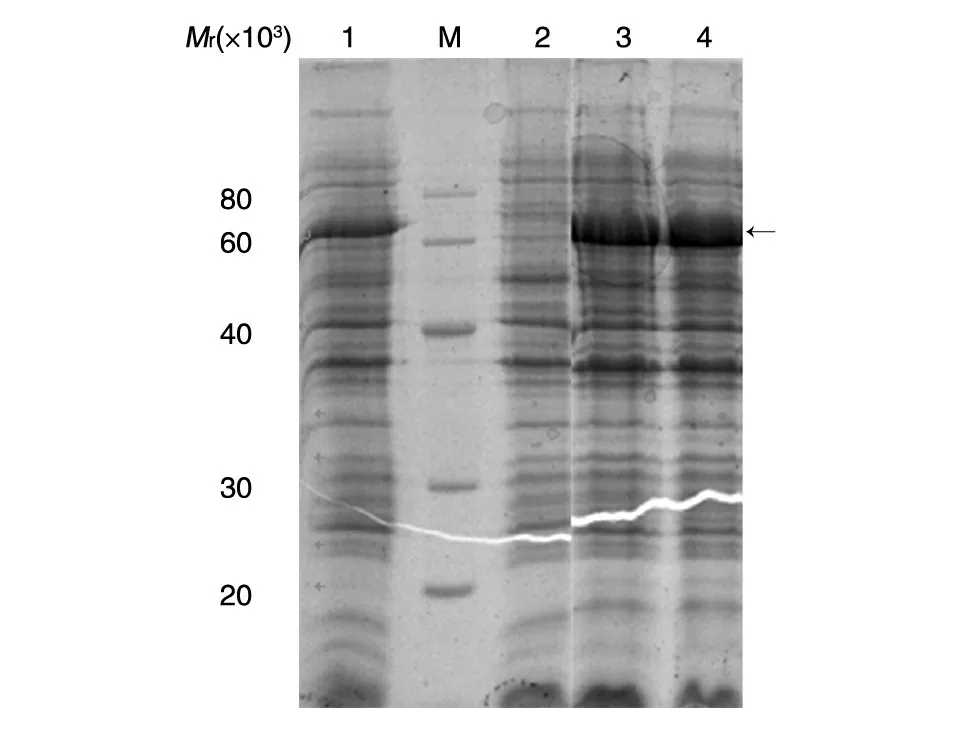
图2 重组BoNT/A LC在大肠杆菌BL21(DE3)Rosetta中的表达
3 讨论
对于肉毒中毒,迄今国内外尚未有较满意的解毒药物,仅有的马血清抗毒剂存在易产生免疫反应副作用等缺点。LC 已被证实是治疗肉毒毒素中毒的关键药靶,开发高效的BoNT LC 抑制剂是当前研究的热点领域[14-21]。在基于肉毒神经毒素活性的分析方法中,小鼠生物检测仍是目前惟一被公认的确认BoNT 的方法[22]。但小鼠生物检测本身也有缺点,如检测花费时间较长、使用小鼠的检测成本较高、对大批量的样本进行检测存在困难等。针对BoNT LC抑制剂开发的大量样本的初步筛选,建立高通量的体外检测方法能够极大地减少检测时间和工作量。本研究的目的是以BoNT LC 代替BoNT 作为试剂,应用于BoNT LC抑制剂高通量体外检测方法研究。
我们在重组BoNT/A LC 蛋白的C端加上组氨酸标签,利用HisTrap FF柱进行亲和纯化,通过一次过柱纯化得到高纯度的目的蛋白,纯化方法简单容易。为了提高目标蛋白的表达产量,我们选择携带稀有密码子的表达菌株BL21(DE3)Rosetta,发现其比BL21(DE3)的表达量更高,重组蛋白达到全菌蛋白总量的20%;采用20℃低温诱导并延长诱导时间,比37℃诱导时的表达量提高50%以上,且包涵体更少,可能是由于低温条件下更有利于该蛋白的表达和正确折叠,表达的目的蛋白绝大部分存在于超声波破碎后的上清中。酶活分析证明所制备的重组蛋白的酶活性略高于全毒素,这可能是由于全毒素中LC 的活性部位被包围在HC 的易位域带中,而单独的LC 比全毒素中的LC 可暴露更多的活性位点。曾有类似结果报道[21]。
图3 重组BoNT/A LC蛋白的纯化
图4 SDS-PAGE分析BoNT/A LC与SNAP-25的反应
综上,本研究构建的表达菌株能够高表达重组BoNT/A LC,获得的BoNT/A LC 重组蛋白具有高活性、高稳定性,容易制备且安全无毒,可用于后续研究。这为BoNT/A LC 抑制剂高通量体外检测方法的研究和BoNT/A LC抑制剂的筛选奠定了基础。
[1]Sollner T,Whiteheart S W,Brunner M,et al.SNAP receptors implicated in vesicle targeting and fusion[J].Nature,1993,362(6418):318-324.
[2]Poulain B,Mochida S,Weller U,et al.Heterologous combinations of heavy and light chains from botulinum neurotoxin A and tetanus toxin inhibit neurotransmitter release in Aplysia,[J].Biol Chem,1991,266:9580-9585.
[3]Black J D,Dolly J O.Interaction of125I-labeled botulinum neurotoxins with nerve terminals.II.Autoradiographic evidence for its uptake into motor nerves by acceptor-mediated endocytosis[J].Cell Biol,1986,103:535-544.
[4]Shone C C,Hambleton P,Melling J.A 50kDa fragment from the NH2-terminus of the heavy subunit of Clostridium botulinum type A neurotoxin forms channels in lipid vesicles[J].Eur J Biochem,1987,167:175-180.
[5]Montal M S,Blewitt R,Tomich J M,et al.Identification of an ion channel-forming motif in the primary structure of tetanus and botulinum neurotoxins[J].FEBS Lett,1992,313:12-18.
[6]Schmid M F,Robinson J P,DasGupta B R.Direct visualization of botulinum neurotoxin-induced channels in phospholipid vesicles[J].Nature,1993,364:827-830.
[7]Montecucco C,Schiavo G.Structure and function of tetanus and botulinum neurotoxins[J].Q Rev Biophys,1995,28(4):423-472.
[8]Foran P,Shone C C,Dolly J O.Differences in the proteaseactivities of tetanus and botulinum B toxins revealed by the cleavage of vesicle-associated membrane protein and various sized fragments[J].Biochemistry,1994,33(51):15365-15374.
[9]Chen S,Hall C,Barbieri J T.Substrate recognition of VAMP-2 by botulinum neurotoxin B and tetanus neurotoxin[J].J Biol Chem,2008,283(30):21153-21159.
[10]Benecke R,Dressler D.Botulinum toxin treatment of axial and cervical dystonia[J].Disabil Rehabil,2007,29:1769-1777.
[11]Sinha D,Karri K,Arunkalaivanan A S.Applications of botulinum toxin in urogynaecology[J].Eur J Obstet Gynecol Reprod Biol,2007,133:4-11.
[12]Mahajan S T,Brubaker L.Botulinum toxin:from life-threatening disease to novel medical therapy[J].Am J Obstet Gynecol,2007,196:7-15.
[13]Dmochowski R,Sand P K.Botulinum toxin A in the overactive bladder:current status and future directions[J].BJU Int,2007,99:247-262.
[14]Ruge D R,Dunning F M,Piazza T M,et al.Detection of six serotypes of botulinum neurotoxin using fluorogenic reporters[J].Anal Biochem,2011,411(2):200-209.
[15]Benagiano V,Lorusso L,Flace P,et al.VAMP-2,SNAP-25A/B and syntaxin-1 in glutamatergic and GABAergic synapses of the rat cerebellar cortex[J].BMC Neurosci,2011,12:118.
[16]Li B,Pai R,Cardinale S C,et al.Synthesis and biological evaluation of botulinum neurot oxin A protease inhibitors[J].Med Chem,2010,53:2264-2276.
[17]Cardinale S C,Butler M M,Ruthel G,et al.Novel benzimidazole inhibitors of botulinum neurotoxin/A display enzyme and cell based potency[J].Botulinum J,2011,2(1):16-29.
[18]Park J B,Simpson L L.Progress toward development of an inhalation vaccine against botulinum toxin[J].Expert Rev Vaccines,2004,3:477-487.
[19]Lindström M,Korkeala H.Laboratory diagnostics of botulism,[J].Clin Microbiol Rev,2006,19(2):298-314.
[20]Gilsdorf J,Gul N,Smith L A.Expression,purification,and characterization of Clostridium botulinum type B light chain,[J].Protein Expr Purif,2006,46(2):256-267.
[21]Ahmed S A,Byrne M P,Jensen M,et al.Enzymatic autocatalysis of botulinum A neurotoxin light chain[J].Protein Chem,2001,20:221-231.
