雷诺嗪口崩片的制备及质量评价
2015-11-20李伟伟史建俊徐静云
李伟伟,史建俊,徐静云
(黄山学院 化学化工学院,安徽 黄山245041)
在临床应用中,雷诺嗪能显著减缓慢性心绞痛的产生以及使心绞痛发作的次数减少,继而达到治疗慢性心绞痛、心肌缺血[1-3]。雷诺嗪缓释片在2006年获得FDA批准在美国上市,商品名为RanexaTM,是治疗心绞痛的首选药物。口崩片适宜应用于老年人、儿童、吞咽困难等条件特殊的患者。本研究将雷诺嗪制成口崩片,不仅可提高患者的服药顺应性,而且还可提高其生物利用度。
1 仪器与试药
1.1 仪器
TD单冲压片机(开封市宏兴科教器械厂);YD-1A片剂硬度测试仪 (天津市光学仪器厂);FA/JA系列分析天平(上海越平科学仪器有限公司);T6新世纪紫外可见分光光度计(北京普析通用仪器有限责任公司);GZX-9146数显鼓风干燥箱(上海博迅实业有限公司医疗器械厂);RC-8DS溶出度测量仪 (天津市国铭医药设备有限公司)。
1.2 药品与试剂
雷诺嗪对照品(北京海步国际医药科技发展有限公司,纯度99.3%);雷诺嗪原料药(本实验室自制);羧甲基淀粉钠(CMS-Na)(安徽省山河药用辅料有限公司);甘露醇(天津市博迪化工有限公司);乳糖,微晶纤维素(MCC),硬脂酸镁(国药集团化学试剂有限公司),阿斯巴甜(江苏维多股份公司),试验用水为二次蒸馏水,其他试剂均为分析纯。
2 雷诺嗪口崩片的制备
2.1 制备工艺
处方由雷诺嗪及填充剂、崩解剂、矫味剂、润滑剂等组成,采用等量递加法加入主药及辅料并混匀,于75℃烘箱中干燥30min,采用直接粉末压片法压制片重为220mg的雷诺嗪口崩片,每片含主药80mg。
2.2 正交试验优化处方
通过参考文献[4]和预实验得出影响雷诺嗪口崩片质量的主要因素为CMS-Na的用量(A)、MCC的用量(B)和甘露醇的用量(C),以其为考察因素,选用3因素3水平的L9(33)进行正交试验,以崩解时间为指标,兼顾其硬度筛选出最佳处方。结果见表1-3。
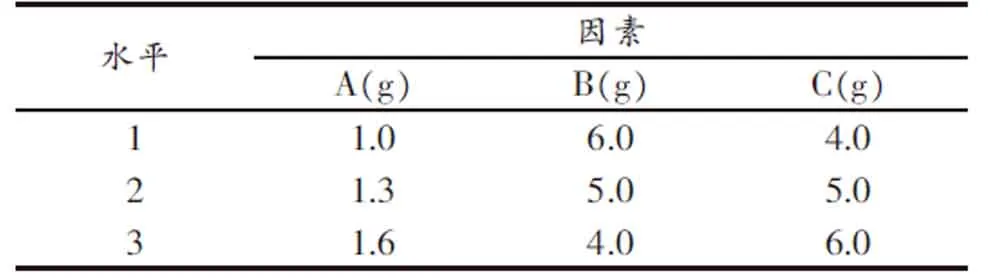
表1 正交试验因素水平表

表2 正交试验结果与分析
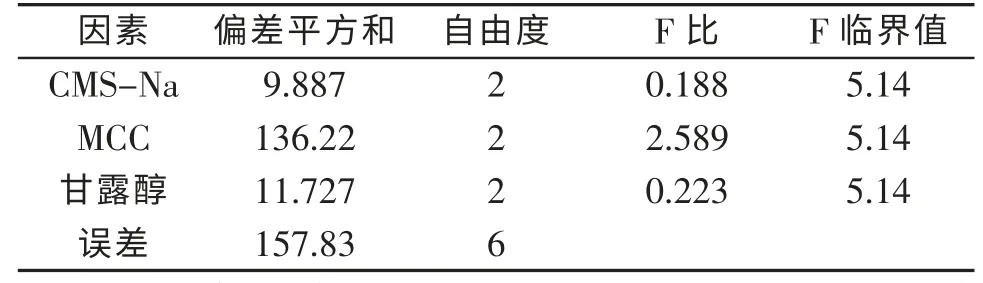
表3 方差分析表
由正交试验结果可知MCC对雷诺嗪口崩片的崩解时间影响最大,甘露醇其次,CMS-Na对其影响最小。最佳处方为A2B1C3,即CMS-Na的用量为1.3g,MCC的用量为6.0g,甘露醇的用量为6.0g。
2.3 矫味剂的选择
在口崩片的制备过程中,口感至关重要,雷诺嗪原料药有少许苦味,需不断调整矫味剂的用量及组合来改善片剂的口感,方便病人服用。
精密称取相当于雷诺嗪口崩片20片的量进行试验,然后分别按表4添加矫味剂,混合均匀后,随机挑选6名志愿者试验片剂的口感,以6名志愿者的主观感受为评价标准。

表4 不同矫味剂组合及口感效果评价
实验表明,矫味剂的比例为阿斯巴甜0.3%,NaCl 0.2%,薄荷脑0.1%,柠檬酸0.1%时,雷诺嗪口崩片的口感最佳,既无苦味,又无砂砾感。
3 雷诺嗪口崩片的含量测定
3.1 标准曲线的制备
精密称取恒重的雷诺嗪对照品0.0507g,置于100mL容量瓶中,用0.1moL/L的盐酸溶液稀释定容,摇匀,得到浓度为0.507mg/mL的标准溶液。分别精密量取对照品溶液4.0、6.0、8.0、10.0、12.0、14.0mL 于50mL容量瓶中,用0.1mol/L的HCl溶液稀释至刻度,摇匀,以不含主药的空白辅料配制参比溶液,用紫外分光光度计于272nm处测得其吸光度[5],雷诺嗪的浓度在40.56-141.96μg/mL范围内,吸光度与浓度呈很好的线性关系,回归方程为A=0.006C-0.0041,r=0.9991(n=6)。
3.2 精密度实验
精确量取3.1项下雷诺嗪对照品溶液12mL,稀释至50mL容量瓶中,用紫外分光光度计测定其吸光度,重复测定6次,相对标准偏差RSD=0.28%,精密度良好。
3.3 稳定性实验
取稀释后的对照品溶液,分别放置1、2、4、8、12小时后,测定其吸光度。结果RSD=0.47%,表明雷诺嗪样品溶液在室温12h内稳定。
3.4 回收率实验
取制得的雷诺嗪口崩片20片,用研钵研细,精密称取相当于雷诺嗪25mg的粉末置于100mL容量瓶中,加入恒重的雷诺嗪标准品25mg,用0.1mol/L的HCl溶液定容,过滤,精密量取12mL上述所配溶液于50mL容量瓶中,用0.1mol/L的HCl溶液定容,摇匀[6]。测定其吸光度,重复上述步骤6次,计算平均回收率为99.42%,RSD=0.96%。
3.5 样品测定
按照上述方法对雷诺嗪口崩片进行含量测定,结果所制备的雷诺嗪口崩片(3批)的含量分别为标示量的99.8%,99.2%,100.1%。
4 雷诺嗪口崩片的质量评价
4.1 外观性状
所制备的雷诺嗪口崩片表面光滑均匀,颜色均匀,无杂斑异物。放置10天后,外观性状保持不变。
4.2 片重差异
取雷诺嗪口崩片20片,精密称定每片重量,并称定总重量,求平均片重,比较平均片重与每片重量,计算其片重差异,结果20片口崩片的片重差异限度均低于±7.5%,符合《中国药典》2010年版规定[7]。
4.3 崩解时限的测定
体外崩解时限:任取雷诺嗪口崩片6片,分别放入装有2mL(37±1)℃蒸馏水的试管中,即刻计时,每隔5s震荡一下试管,观察其崩解情况,完全崩解时,记录崩解时限[8],结果平均崩解时间为15s。
口腔崩解时限:6名用清水清洁口腔的健康志愿者,随机取药片置于舌面之上,不用水助溶,也不咀嚼,允许舌头适当轻微运动,记录片剂在口腔中完全崩解的时间[9],结果口腔内崩解时间平均为19s,口感酸甜,有清凉感。
4.4 溶出度的检测
参照《中国药典》2010年版二部附录XC浆法操作,取雷诺嗪口崩片6片,以0.1mol/L的HCl溶液作为溶出介质,将溶出度仪温度设置为37℃,转速设置为100r/min,分别在1、2、4、6、8、10、15、20、25、30、40min时用注射器吸取5ml样品,同时补充5ml溶出介质,样品用0.8μm的微孔滤膜过滤后,用紫外分光光度计于272nm波长处测定吸光度,根据实验数据计算累积溶出率,结果见图1。

图1 雷诺嗪口崩片的溶出度曲线
5 结论与讨论
MCC既是填充剂又是崩解剂,MCC的可压性较好,但溶胀性较弱,选用联合崩解剂CMS-Na使雷诺嗪口崩片达到迅速崩解的效果。为了遮掩主药的苦味以及MCC用量多引起的砂砾感,采用甜味剂阿斯巴甜、酸味剂柠檬酸、NaCl和薄荷脑为矫味剂,使雷诺嗪口崩片的口感酸甜,既无苦味,也无砂砾感。
应用了正交试验法对处方进行优化,制备的雷诺嗪口腔崩解片表面光滑均匀,片重差异在±7.5%以内,崩解时间在20s内,累积溶出率在1min内就达到了93.95%,释放迅速,符合口崩片质量要求。
[1]Brendan C, Katrina M W, James G M.Ranolazine Increases Active Pyruvate Dehydrogenase in Perfused Normoxic Rat Hearts:Evidence for an Indirect Mechanism[J].J Mol Cell Cardiol, 1996, 28(2):341-350.
[2]王志宏,李扬,侯文静,等.雷诺嗪缓释片在中国健康受试者中的药动学研究[J].中国药学杂志,2014,49(6):496-500.
[3]陈頔,傅得兴,孙春华.抗心绞痛药雷诺嗪的研究进展[J].中国新药杂志,2008,17(21):1834-1837.
[4]代琴,郑兴,姚旭,等.口腔崩解片辅料选用研究[J].中国医药指南,2013,11(7):463-466.
[5]李伟伟,史建俊.紫外分光光度法测定雷诺嗪原料药的含量[J].黄山学院学报,2010,12(5):50-51.
[6]卫晓晓,焦海胜.卡马西平口腔速崩片的制备及质量评价[J].中国药房,2011,22(5):424-427.
[7]国家药典委员会编.中华人民共和国药典(第二部)[S].北京:中国医药科技出版社,2010,附录ⅠA片剂:附录5.
[8]巫传玲,于波涛,范开华.盐酸异丙嗪口崩片的制备[J].华西药学杂志,2013,28(2):129-131.
[9]施震,尹银嘉,张先洲.小剂量阿司匹林口腔崩解片的制备[J].中国医药工业杂志,2003,34(7):26-27.
