低品位钼精矿石灰焙烧-酸浸提取钼
2015-11-19陈许玲王海波范晓慧曾金林中南大学资源加工与生物工程学院长沙40083大冶有色金属集团控股有限公司黄石43500
陈许玲,王海波,甘 敏, ,范晓慧,张 麟,邓 琼,王 勇,曾金林(.中南大学 资源加工与生物工程学院,长沙 40083;.大冶有色金属集团控股有限公司,黄石 43500)
低品位钼精矿石灰焙烧-酸浸提取钼

陈许玲1,王海波1,甘敏1, 2,范晓慧1,张麟2,邓琼1,王勇2,曾金林1
(1.中南大学 资源加工与生物工程学院,长沙 410083;2.大冶有色金属集团控股有限公司,黄石 435100)
采用XRD和TG-DSC分析研究低品位钼精矿石灰氧化焙烧过程的反应机理,确定石灰法焙烧-酸浸提钼工艺的优化参数。热重分析表明:石灰法焙烧主要发生Ca(OH)2的分解、MoS2的氧化、MoO2的再氧化及钼酸盐的生成等反应,焙烧过程主要产生MoO2、MoO3、CaMoO4、CaSO4等物相。XRD分析表明:当温度高于600℃、反应时间大于90 min时,焙砂中低价态钼的衍射峰完全消失,此时焙砂主要物相为CaMoO4和CaSO4,辉钼矿被充分氧化;石灰焙烧适宜的条件为Ca(OH)2与钼精矿质量比1:1、焙烧温度650℃、焙烧时间90 min,焙烧过程硫的保留率可达91.49%。钼焙砂酸浸适宜的浸出温度为90℃、浸出时间为2 h、H2SO4浓度为70 g/L、液固比为5:1,此时钼浸出率可达99.12%,CaMoO4被完全溶出。
低品位钼精矿;石灰焙烧;酸浸;物相变化
钼是一种稀有金属,具有高强度、高熔点、耐研磨、耐腐蚀等优点,被广泛运用于冶金、航天航空、光电材料等领域[1]。2013年,我国钼产量8.57万t,钼消费量8.94万t,均居世界首位[2]。随着钼矿资源的不断开采,高品位钼资源日益匮乏,优质资源远不能满足市场需求,因而贫、细、杂等难选矿石逐渐成为提取钼的主要原料[3-4]。低品位钼精矿因钼含量低(仅为20%~40%),低于标准钼精矿(钼含量≥45%)的品位要求,且因SiO2、CaO、MgO、Cu和Fe等杂质含量高,在工业应用上存在诸多问题[5]。传统提钼工艺主要有火法和湿法两类。湿法工艺主要包括硝酸常压分解工艺[6-7]、氧压煮工艺[8-10]、电氧化工艺[11-14]、NaClO分解工艺[15-16]、生物浸出工艺[17-18]等,其原理均是利用溶液中强氧化剂使低价态钼转变为钼酸或钼酸盐后溶出,其金属综合回收率高,适合处理各种品位的含钼矿石,但由于浸出成本及设备问题的制约,国内目前工业化程度相对较低。氧化焙烧-氨浸工艺是目前处理钼精矿的主流工艺,具有成本低、生产效率高的优势;主要缺点是处理低品位钼精矿时,尾气中SO2浓度低,制酸不经济,易造成环境污染,且焙烧过程易生成不可氨溶的钼酸盐,钼综合回收率较低[19]。
甘敏等[20]研究了低品位钼精矿的氧化焙烧物相演变规律,焙烧过程包括MoS2氧化不充分、MoO3稳定存在和钼酸盐生成3个阶段,其中低价氧化钼和钼酸盐是导致其氨浸溶出率低的主要原因。为解决低品位钼精矿冶炼困难的现状,杨红英等[4]对钼含量为25.40%的钼精矿采用氢氟酸-盐酸法预处理,获得了钼含量(质量分数)为49.94%的标准钼精矿,可直接采用氧化焙烧-氨浸工艺进行后续提取,但预处理工艺无法克服设备腐蚀、环境污染等问题。俞娟[21]采用焙烧-氨浸-浸渣再浸出工艺处理低品位钼精矿,可使钼综合回收率达到96.80%;李飞等[22]对难溶钼酸盐的浸出热力学分析时也证实,碱法再浸出可实现钼酸盐的溶出。彭俊等[23]采用加钙氧化焙烧-低温硫酸化焙烧-水浸处理钼含量5.42%的低品位镍钼矿,钼浸出率可达97.33%,该工艺既减轻了SO2对环境的污染,又促进了后续钼的浸出。综合分析发现,上述工艺主要无法解决流程长、处理量大等问题。为进一步降低成本,减轻SO2污染和提高钼回收率,本文作者拟采用石灰焙烧-酸浸工艺提钼,通过揭示低品位钼精矿石灰法焙烧过程的氧化机理,系统研究石灰焙烧和浸出工艺过程的优化工艺技术参数,为低品位钼精矿的高效利用提供理论依据和技术支持。
1 实验
1.1实验原料
本实验中所用钼精矿来自铜矿选矿过程回收的副产品,其化学成分如表1所示。由表1可知,钼和硫的含量(质量分数)分别为39.27%和29.73%,主要杂质成分由SiO2、CaO、MgO、含铁矿物等组成。钼精矿物的XRD谱如图1所示。该钼精矿中的主要矿物有辉钼矿(MoS2)、碳酸钙(CaCO3)、滑石(Mg3(Si4O10)· (OH)2)和黄铁矿(FeS2)等。
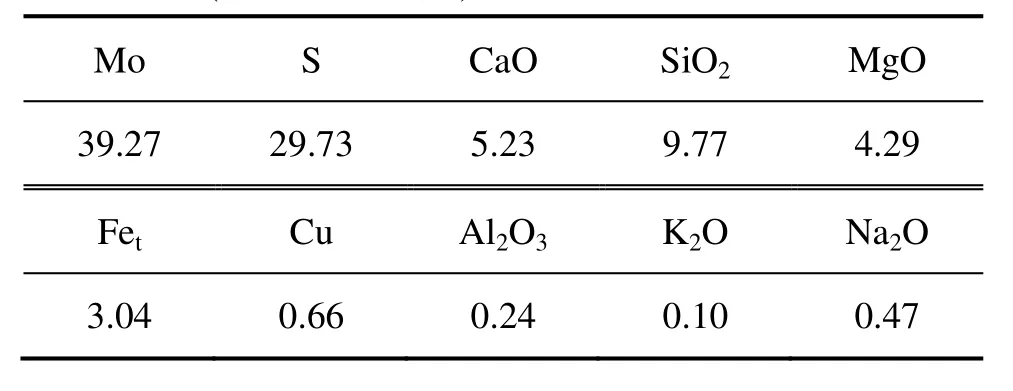
表1 钼精矿主要化学成分Table 1 Main chemical compositions of molybdenum concentrate (mass fraction,%)
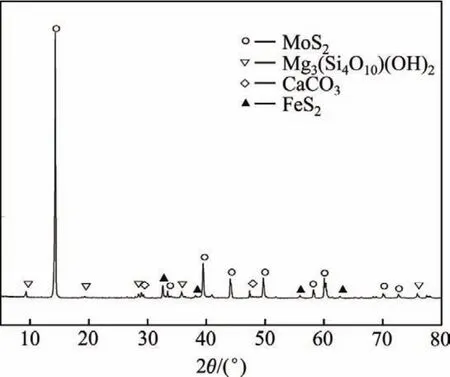
图1 钼精矿的XRD谱Fig.1 XRD pattern of molybdenite concentrate
采用光学显微镜分析精矿中主要矿物的嵌布关系,结果如图2所示。由图2可以看出,辉钼矿为精矿中的主要矿物,以单体形式产出者较多,粒径和形状不一,有鳞片状、板状、条状,更多的是不规则粒状。辉钼矿与黄铜矿、黄铁矿连生,或与黄铜矿相互包裹,或与斑铜矿连生(见图2(a));原矿中还存在单独黄铜矿、黄铁矿和斑铜矿(见图2(b))。综上分析可知,钼精矿中钼含量低于标准钼精矿中的钼品位(≥45%),并有少量辉钼矿与其他硫化矿交织共生,且杂质成分复杂,是典型的低品位钼精矿。
1.2试验方法及评价指标
将钼精矿与氢氧化钙(分析纯)按质量比配矿、混匀后,取15 g混匀矿放入耐高温坩埚中,按照设定的温度置于马弗炉中氧化焙烧,待试验达到预定焙烧时间后在惰性气氛下冷却至室温,并称量。将不同焙烧条件下获得的钼焙砂研磨至粒度小于0.074mm的为80%(质量分数)以上,取样分析硫含量;另取5 g不同焙烧条件下的钼焙砂,按设定的液固比溶于盛有稀硫酸的烧杯中,搅拌均匀后密封,置于预先设定温度的水浴锅中恒温浸出,待达到预定浸出时间后,真空过滤,干燥称量,分析钼含量。评价指标主要有钼浸出率Moα和硫保留率Sβ,其计算式如下:

图2 辉钼矿的显微结构特征Fig.2 Microstructure characteristics of molybdenite:(a)Raw ore;(b)Monomer sulfide ore

式中:m1、m2、m3分别为钼精矿、钼焙砂和浸渣的质量,g;w1、w2、w3分别为钼精矿、钼焙砂和浸渣中钼品位,%;ε1、ε2分别为钼精矿、钼焙砂中硫含量,%。
2 结果与分析
2.1石灰法焙烧工艺的研究
研究了不同焙烧工艺参数对辉钼矿氧化和固硫的影响。焙烧后对焙砂采用酸浸处理,通过钼的浸出率反映焙砂的氧化效果。焙砂酸浸条件如下:硫酸浓度70 g/L、浸出温度90℃、浸出时间2 h、液固比5:1。
2.1.1Ca(OH)2用量的影响
首先研究了钼精矿与Ca(OH)2在空气中加热的反应行为,将钼精矿与Ca(OH)2在空气气氛、升温速率10℃/min条件下进行TG-DSC分析,结果如图3所示。由图3可见,在低温阶段主要为钼精矿中水分、浮选药剂等易挥发部分的析出;在400~470℃的温度范围内,主要发生了Ca(OH)2的分解;温度为470~696℃时,存在3个明显的放热峰,温度分别为530.5、574.4和640.9℃,反应生成MoO2、MoO3和CaMoO4速度最大的温度点,反应主要由式(3)~(7)组成,最终产物为CaMoO4和CaSO4。当温度高于696℃时,部分滑石发生了分解。


图3 钼精矿与Ca(OH)2质量比为1:1时的TG-DCS曲线Fig.3 TG-DCS curves at mass ratio of Ca(OH)2to molybdenum concentrate 1:1
在考察钼精矿与Ca(OH)2在空气介质中热重分析的基础上,选择焙烧温度650℃、焙烧时间90 min的条件下,研究了Ca(OH)2用量对焙烧效果的影响,其结果如图4所示。随着Ca(OH)2与钼精矿质量比的增加,钼浸出率和硫保留率提高显著,但比例提高到一定程度时,钼浸出率和硫保留率变化不大或有所降低。当Ca(OH)2与钼精矿为理论配比(通过计算得到其质量比为0.84:1)时,钼浸出率和硫保留率分别为73.33% 和85.92%;当Ca(OH)2与钼精矿质量比达到1:1时,钼浸出率达到最大,焙砂中硫的保留率稳定在90%左右。试验发现,Ca(OH)2与钼精矿质量比超过1.1:1,硫的保留率虽有微量上升,但浸出过程中酸耗明显增加,浸出率反而降低。因此,适量的Ca(OH)2可将MoS2转变为CaSO4和易酸溶的CaMoO4,减少SO2的排放,并显著提高钼的浸出率。根据以上试验结果,确定Ca(OH)2与钼精矿适宜的质量比为1:1。
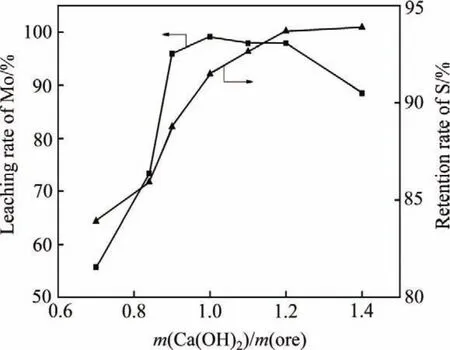
图4 Ca(OH)2用量对钼浸出率和硫保留率的影响Fig.4 Effect of Ca(OH)2addition on molybdenum leaching rate and sulfur retention rate
2.1.2焙烧温度的影响
在Ca(OH)2与精矿质量比为1:1、焙烧时间为90 min的条件下研究了焙烧温度对焙烧效果的影响,其结果如图5所示。由图5可知:当温度从550℃升高到650℃,钼浸出率和硫保留率提高明显,分别由81.03%、83.72%提高到99.12%、91.49%,这是因为一定范围内提高焙烧温度有利于加快物料中钼的氧化和硫的吸附。当焙烧温度由650℃升高至675℃时,硫保留率仍呈小幅度增加趋势,而钼浸出率降低,其原因是温度达到675℃时,反应的放热效应明显增强,该过程部分MoO3未及时与CaO反应,而与CaMoO4形成MoO3-CaMoO4共熔物,物料烧结现象明显,对未反应的MoS2颗粒形成包裹,并对O2的扩散传输产生障碍,不利于MoS2氧化反应速率的提升,并最终阻碍物料中低价态钼转变为CaMoO4,导致钼浸出率降低。综合以上分析,焙烧温度确定为650℃。

图5 焙烧温度对钼浸出率和硫保留率的影响Fig.5 Effect of roasting temperature on molybdenum leaching rate and sulfur retention rate

图6 不同焙烧温度下焙烧产物的XRD谱Fig.6 XRD patterns of roasted products at different roasting temperatures
采用X射线衍射技术研究了不同焙烧温度下钼精矿与Ca(OH)2反应的物相变化,结果如图6所示。由图6可知:在400℃左右,钼相主要由MoS2组成,当温度达到450℃时,才出现少量MoO2、MoO3和CaO的衍射峰,说明当温度达到450℃时,MoS2开始氧化,Ca(OH)2开始分解;当温度达到500℃时,MoS2和MoO3衍射峰明显减弱,同时还出现了CaMoO4和CaSO4的衍射峰,说明此时MoS2氧化生成的MoO3、SO2与CaO开始剧烈反应,由于MoO3的不可酸溶,部分MoS2仍未氧化完全,这是钼浸出率仅为60%左右的主要原因。当温度在600℃以上时,主要的衍射峰为CaMoO4和CaSO4,温度继续提高,焙砂的物相不再发生变化,钼相已基本完全转变为CaMoO4。2.1.3焙烧时间的影响
在Ca(OH)2与钼精矿质量比为1:1、焙烧温度650℃的条件下,研究了焙烧时间对焙烧效果的影响,其结果如图7所示。由图7可见:焙烧时间对钼浸出率、硫保留率的影响均较明显;当焙烧时间由30 min延长到90 min时,钼浸出率由85.89%提高到99.12%,硫保留率由94.50%降低到91.49%;但当焙烧时间超过90 min后,钼浸出率和硫保留率变化不大。这是由于焙烧前期MoS2的氧化不完全,钼酸钙的生成量较少,造成钼浸出率较低,而硫主要以未反应完全的MoS2和CaSO4保留在钼焙砂中。由于此时CaO充分过剩,生成的SO2基本能完全固定在焙烧中,因此,硫保留率高;但随着焙烧时间的延长,MoS2中钼大部分转化为钼酸钙,钼浸出得到改善,而部分逸出的SO2在焙烧过程中未被及时吸附,造成硫保留率稍有下降;焙烧完全后,钼浸出率、硫保留率均变化不大。综合分析确定焙烧时间为90 min。

图7 反应时间对钼浸出率和硫保留率的影响Fig.7 Effect of roasting time on molybdenum leaching rate and sulfur retention rate
不同焙烧时间下焙烧产物的XRD谱如图8所示。由图8可知:当焙烧时间为10 min时,MoS2衍射峰强度明显减弱且部分消失,同时出现大量的CaMoO4和CaSO4的衍射峰,并出现MoO2、CaO的衍射峰,这说明该过程中Ca(OH)2分解产生的CaO与MoS2的氧化产物MoO3、SO2迅速反应,由于环境温度急剧上升,部分SO2未被CaO有效吸附,因此,该时段为SO2最大逸出时段。当焙烧时间为30~60 min时,MoS2衍射峰强度明显减弱,CaMoO4衍射峰强度明显增强;当焙烧时间大于90 min时,MoS2基本氧化完全,焙砂的主要物相由CaSO4和CaMoO4组成。

图8 不同焙烧时间下焙烧产物的XRD谱Fig.8 XRD patterns of roasted products for different roasting time
2.2酸浸工艺参数对钼浸出的影响
在焙烧温度650℃、焙烧时间90min、Ca(OH)2与钼精矿质量比为1:1的条件下,进一步研究浸出温度、硫酸浓度、浸出时间和液固比对钼浸出率的影响,结果如图9所示。
由图9(a)可知,温度对钼的浸出率影响较大,随着温度的升高,浸出率逐渐提高。因温度升高,钼酸钙溶解速度增加,溶液黏度降低,使分子、离子的扩散速度明显加快,浸出剂进入矿物晶格和产物扩散更加迅速,钼的浸出率得到提高,90℃时浸出率可达99%以上,故选择浸出温度为90℃。由图9(b)可知,钼的浸出率随着硫酸用量的增加而提高,硫酸浓度越大,H+浓度增加,结合MoO42-的概率随之增加,更有利于破坏晶格结构,从而钼浸出率就越高,但硫酸用量增加会加大酸浸废液的处理量,综合考虑,选定硫酸浓度为70 g/L。由图9(c)可知,随着浸出时间的延长,浸出剂可充分接触矿物,提高钼浸出率,当浸出时间达到2 h,浸出率趋于稳定,因此,最佳浸出时间为2 h。由图9(d)可知,随着液固比增加,矿浆流动性增强,矿物与浸出剂的接触更加充分,浸出率随之提高,当液固比超过5:1时,浸出率变化不大,综合考虑,选择液固比为5:1。
对最佳焙烧条件下获得的焙砂及最佳浸出条件下的酸浸渣进行XRD分析,其结果如图10所示。由图10可知:焙砂中CaMoO4特征峰在酸浸后彻底消失,表明酸浸过程中钼酸钙被完全溶出;浸出渣中主要成分为CaSO4、石膏(Ca(SO4)(H2O)2)和滑石(Mg3(Si4O10)· (OH)2)。这说明钼精矿经石灰焙烧-酸浸工艺处理后,钼可以得到完全回收。

图9 不同浸出条件对钼浸出率的影响Fig.9 Effect of leaching conditions on leaching rate of molybdenum:(a)Leaching temperature;(b)Sulphuric acid consumption;(c)Leaching time;(d)Liquid-solid ratio

图10 铜焙砂酸浸前后物相的XRD谱Fig.10 XRD patterns of molybolenum calcine before and after leaching
3 结论
1)热重分析表明:石灰法焙烧过程主要发生包括Ca(OH)2分解、低价钼氧化、CaMoO4与CaSO4生成等多种反应。XRD分析表明:最终焙烧产物的主要物相为CaMoO4和CaSO4。
2)石灰焙烧过程中Ca(OH)2与钼精矿质量比宜控制在1:1左右,在保证CaMoO4充分生成的同时减少浸出耗酸量;焙烧温度不宜高于650℃,当温度过高时,易产生MoO3-CaMoO4共熔物,不利于MoS2的充分氧化。确定最优焙烧条件如下:焙烧温度650℃、焙烧时间90 min,此时硫保留率可达91.49%。
3)浸出温度和硫酸浓度对钼浸出率影响较显著,钼浸出率随浸出温度和硫酸浓度的增加而提高。最佳酸浸条件为浸出温度90℃、硫酸浓度70 g/L、浸出时间2 h、液固比5:1,此时钼的浸出率可达99.12%。
REFERENCES
[1] 黄卉, 陈福亮, 姜艳, 容会, 朵云峰, 杨志鸿.我国钼资源现状及钼的冶炼分析[J].云南冶金, 2014, 43(2):66-70.HUANG Hui, CHEN Fu-liang, RONG Hui, DUO Yun-feng, YANG Zhi-hong.The current situation of domestic molybdenum resources and molybdenum smelting analysis[J].Yunnan Metallurgy, 2014, 43(2):66-70.
[2] 吴海瀛.2013年国际市场走势及近期估计[J].中国钼业, 2014, 38(3):51-58.WU Hai-ying.International molybdenum market summary and recent assessments in 2013[J].China Molybdenum Industry, 2014, 38(3):51-58.
[3] 胡磊, 肖连生, 张贵清, 曾理.从高杂质低品位钼焙砂中苏打高压浸出钼的试验研究[J].矿冶工程, 2012, 32(6):66-70.HU Lei, XIAO Lian-sheng, ZHANG Gui-qing, ZENG Li.Experimental study on leaching molybdenum at high pressure with Soda from low grade molybdenum calcine with high impurities[J].Mining and Metallurgical Engineering, 2012, 32(6):66-70.
[4] 杨洪英, 俞娟, 佟琳琳, 罗文杰.低品位复杂钼精矿的提纯工艺[J].中国有色金属学报, 2013, 23(7):2012-2018.YANG Hong-ying, YU Juan, TONG Lin-lin, LUO Wen-jie.Purification process of low-grade complex molybdenite concentrate[J].The Chinese Journal of Nonferrous Metals, 2013, 23(7):2012-2018.
[5] 张文钲.从低品位钼精矿或钼中间产品生产工业氧化钼、二钼酸铵和纯三氧化钼[J].中国钼业, 2004, 28(4):33-35.ZHANG Wen-zheng.Production of technical molybdenum oxide, ammonium dimolybdate and pure molybdenum trioxide from low grade molybdnite concentrates or molybdenum intermediate product[J].China Molybdenum Industry, 2004, 28(4):33-35.
[6] 张启修, 赵秦生.钨钼冶金[M].北京:冶金工业出版社, 2005:26-32.ZHANG Qi-xiu, ZHAO Qin-sheng.Metallurgy of tungsten and molybdenum[M].Beijing:Metallurgical Industry Press, 2005:26-32.
[7] MANOJ K, MANKHAND T R, MURTHY D S R, MUKHOPADHYAY R, PRASAD P M.Refining of a low-grade molybdenite concentrate[J].Hydrometallurgy, 2007, 86(3):56-62.
[8] 彭建蓉, 杨大锦, 陈加希, 阎江峰.原生钼矿加压碱浸试验研究[J].稀有金属, 2007, 31(6):110-113.PENG Jian-rong, YANG Da-jin, CHEN Jia-xi, YAN Jiang-feng.Experimental study on alkaline leaching of crude molybdenite under pressure of oxygen[J].Chinese Journal of Rare Metals, 2007, 31(6):110-113.
[9] KETCHAM J.Pressure oxidation process for the production of molybdenum trioxide from molybdenite.United States Patent, US6149883[P].2000-11-21.
[10] VICLOR J.Pressure oxidation process for the production of molybdenum trioxide from molybdnite.US6149883[P].2000-11-21.
[11] CAO Zhan-fang, ZHONG Hong, LIU Guang-yi, FU Jian-gang, WANG Shuai, QIU Yun-ren.Electric-oxidation kinetics of molybdenite concentrate in acidic NaCl solution[J].The Canadian Journal of Chemical Engineering, 2009, 87(6):939-944.
[12] FU Jian-gang, ZHONG Hong.Electro-oxidation process for molybdenum concentrates[J].Journal of Central South University of Technology, 2005, 12(2):134-140.
[13] 曹占芳, 钟宏, 姜涛, 刘广义, 王帅.德兴铜矿辉钼矿精矿的选择性电氧化浸出与分离过程[J].中国有色金属学报, 2013, 23(8):2290-2295.CAO Zhan-fang, ZHONG Hong, JIANG Tao, LIU Guang-yi, WANG Shuai.Selective electric-oxidation leaching and separation of Dexing molybdenite concentrates[J].The Chinese Journal of Nonferrous Metals, 2013, 23(8):2290-2295.
[14] 符剑刚, 钟宏, 黄永平, 卜向明.Mn3+/Mn2+间接电氧化法分解辉钼矿[J].中南大学学报(自然科学版), 2004, 35(5):797-801.FU Jian-gang, ZHONG Hong, HUANG Yong-ping, PU Xiang-ming.Indirect electro-oxidation of molybdenite by Mn3+/Mn2+[J].Journal of Central South University of Technology (Science and Technology), 2004, 35(5):797-801.
[15] WARREN I H, MOUNSEY D M.Factors influencing the selective leaching of molybdenum with sodium hypochlorite from copper/molybdenum sulphide minerals[J].Hydrometallurgy, 1983, 10(3):343-357.
[16] ANTONIJEVIC M M, PACOVIC N V.Investigation of molybdenite oxidation by sodium dichromate[J].Minerals Engineering, 1992, 5(2):223-233.
[17] ROMANO P, BLÁZQUEZ M L, ALGUACIL F J, MUÑOZ J A, BALLESTER A, GONZÁLEZ F.Comparative study on the chalcopyrite bioleaching of a molybdenite concentrate with mesophilic and thermophilic bacteria[J].FEMS Microbilology Letters, 2001, 196(1):71-75.
[18] OLSON G J, CLARK T R.Bioleaching of molybdenite[J].Hydrometallurgy, 2006, 82(3):133-136.
[19] 向铁根.钼冶金[M].长沙:中南大学出版社, 2002:1-20.XIANG Tie-gen.Molybdenum metallurgy[M].Changsha:Central South University Press, 2002:1-20.
[20] 甘敏, 范晓慧, 张麟, 邱冠周, 王勇, 邓琼, 陈许玲.低品位钼精矿氧化焙烧过程的反应行为[J].中国有色金属学报, 2014(12):3115-3122.GAN Min, FAN Xiao-hui, ZHANG Lin, QIU Guan-zhou, WANG Yong, DENG Qiong, CHEN Xu-ling.Reaction behavior of low grade molybdenum concentrates in oxidation roasting process[J].The Chinese Journal of Nonferrous Metals, 2014(12):3115-3122.
[21] 俞娟, 杨洪英, 陈燕杰, 范有静.低品位钼精矿的钼提取研究[J].东北大学学报(自然科学版), 2011, 32(8):1141-1144.YU Juan, YANG Hong-ying, CHEN Yan-jie, FAN You-jing.Extraction of molybdenum from low-grade molybdenum concentrates[J].Journal of Northeastern University (Nature Science), 2011, 32(8):1141-1144.
[22] 李飞, 陈星宇, 何利华, 吴金玲.氢氧化钠分解不溶性钼酸盐的浸出热力学[J].中国有色金属学报, 2014(11):2921-2927.LI Fei, CHEN Xing-yu, HE Li-hua, HU Jin-ling.Leaching thermodynamics of decomposing sparingly soluble molybdate by sodium hydroxide[J].The Chinese Journal of Nonferrous Metals, 2014(11):2921-2927.
[23] 彭俊, 王学文, 王明玉, 肖彩霞, 施丽华.从镍钼矿中提取镍钼的工艺[J].中国有色金属学报, 2012, 22(2):553-559.PENG Jun, WANG Xue-wen, WANG Ming-yu, XIAO Cai-xia, SHI Li-hua.Extraction process of molybdenum and nickel from Ni-Mo ore[J].The Chinese Journal of Nonferrous Metals, 2012, 22(2):553-559.
(编辑龙怀中)
Extraction of molybdenum from low grade molybdenum concentrates by calcium-based roasting and acid leaching process
CHEN Xu-ling1, WANG Hai-bo1, GAN Min1, 2, FAN Xiao-hui1, ZHANG Lin2, DENG Qiong1, WANNG Yong2, ZENG Jin-lin1
(1.School of Minerals Processing and Bioengineering, Central South University, Changsha 410083, China;2.Daye Non-Ferrous Metals Group Holdings Co., Ltd., Huangshi 435100, China)
The mechanism of chemical reactions was studied on the oxidation of low grade molybdenum concentrate with addition of calcium oxide by the methods of XRD and TG-DSC, and the optimum conditions of calcium-based roasting and acid leaching were determined.The result of TG-DSC shows that the reactions are composed mainly of decomposition of Ca(OH)2, oxidization of MoS2, re-oxidization of MoO2and the formation of molybdate.The products are MoO2, MoO3, CaMoO4and CaSO4in the process of oxidation roasting.The XRD result shows that the diffractions of low valence state molybdenum can not disappear completely until roasting temperature exceeds 600℃ and roasting time is longer than 90 min.The main phases are CaMoO4and CaSO4in molybdenum calcine, and the molybdenite can be oxidized completely.The retaining ratio of sulfur can reach 91.49% under the conditions of mass ratio of Ca(OH)2to molybdenum concentrate 1:1, roasting temperature 650℃ and roasting time 90min.The test shows that the leaching rate of molybedenum can reach 99.12% under the suitable conditions of leaching temperature 90℃, leaching time 2 h, sulfuric acid 70 g/L, the ratio of liquid to solid 5:1.
low grade molybdenum concentrate;calcium-based roasting;acid leaching;phase transformation
TF841.2
A
1004-0609(2015)10-2913-08
中国博士后科学基金特别资助项目(2014T70691);中国有色矿业集团总公司科技项目(2013KJJH06)
2014-12-09;
2015-06-18
甘敏,讲师;电话:13467517674;E-mail:csuganmin@126.com
