离子液体在天然活性物质提取中的应用研究进展
2015-11-18李明英
李明英
(浙江杭州绿城心血管病医院药剂科,浙江 杭州 310012)
离子液体在天然活性物质提取中的应用研究进展
李明英*
(浙江杭州绿城心血管病医院药剂科,浙江 杭州 310012)
查阅近年来国内外相关文献,并进行分析、归纳和总结,综述离子液体在天然活性物质提取中的应用研究进展。离子液体作为一种绿色溶剂,并以其独特性质,近年来在天然活性物质提取领域的应用研究备受关注。不过,目前用于天然活性物质提取的离子液体大多仅为咪唑类型,且尚未发现不同类型离子液体对不同种类天然活性成分的提取效率具有明显的特异性和规律性,这有待进一步深入研究。
离子液体;天然活性物质;提取
离子液体一般是由结构不对称、体积相对较大的有机阳离子与体积相对较小的无机阴离子构成,在室温或接近室温时呈液态,又称低温熔融盐、室温离子液体或液态有机盐等。最初,离子液体主要用于电化学研究,而近年来发现其是一种极具应用潜力的环境友好溶剂,故被称之为绿色溶剂。人类发现的第1个离子液体为硝基乙胺,至今已有百年历史。但真正标志性的离子液体的诞生是在1975年,Koch等研制出N-丁基吡啶阳离子熔融盐。到1992年,咪唑四氟硼酸盐的出现使离子液体得到迅速发展。目前,离子液体的应用研究已涉及合成反应、催化反应、电化学、萃取分离等各个领域[1]。
离子液体因其优良的溶剂性能,如高黏度、低蒸汽压、热稳定性好、溶解性能好以及低可燃性等,受到研究人员的广泛关注[2-3],并在有机化学、分析化学、生物化学、物理化学等领域应用广泛,尤其在分析化学领域,作为液-液萃取、微波辅助提取、超声辅助提取和液相微萃取中的萃取溶剂,其应用发展迅速。近年来,离子液体用作高速逆流色谱和高效液相色谱(HPLC)的流动相以及HPLC和气相色谱吸附剂的改性剂或固定相的研究,也有相应报道[4-8]。
1 离子液体的结构
离子液体种类繁多,通过不同阴阳离子间的组合,能设计出不同的离子液体。离子液体中常见阳离子有N,N-二烷基取代咪唑阳离子、N-烷基吡啶阳离子、烷基季铵阳离子和烷基季膦阳离子,而在提取分离中应用最广泛的为咪唑类离子液体,如表1所示;阴离子主要分为AlCl3型和非AlCl3型,前者遇水和空气不稳定,后者常见的有卤素阴离子、BF4-、PF6-、CF3SO3-、CF3COO-、SbF6-、(CF3S02)2N-等[9]。
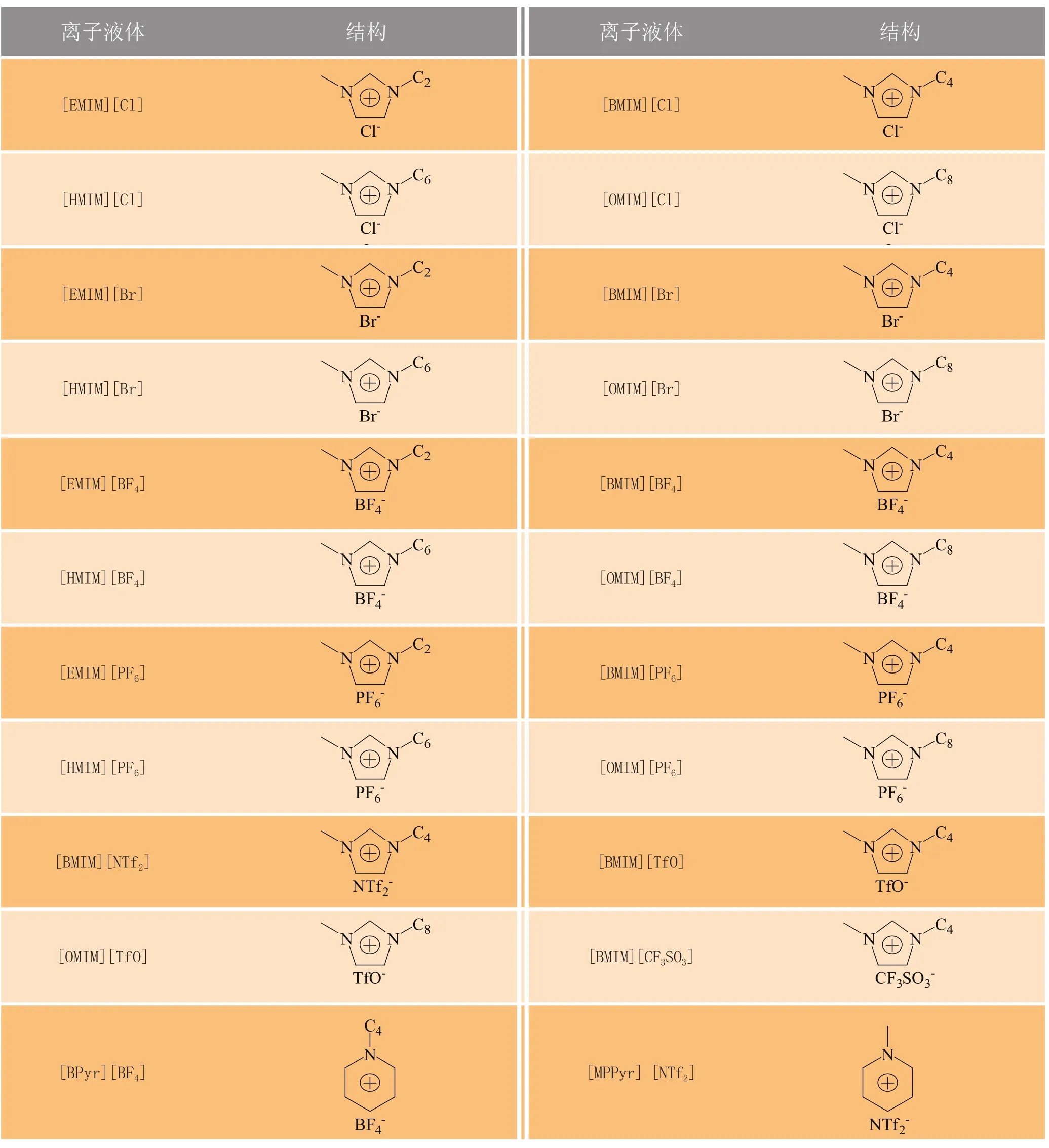
表1 常用于提取分离天然活性物质的离子液体及其结构Table 1 Ionic liquids commonly used in the extraction and separation of natural active compounds and their structures
2 离子液体的特性
离子液体具有自身特殊性质,如可设计性、热稳定性、不挥发性、高黏度、高密度等,与传统有机溶剂存在较大差异,在分析化学领域得到广泛关注。
2.1 可设计性
离子液体是一种可设计性溶剂,可通过对阴阳离子的调整,得到不同功能和溶解性的离子液体,从而满足其与不同物质之间的相互作用,因此离子液体作为提取和分离复杂生物活性化合物的溶剂独具优势[10]。离子液体与生物活性分子之间的相互作用是萃取的主要机制。相关研究结果表明,疏水性强的离子液体对香豆素的萃取能力较好,且对疏水性较强的嘌呤类化合物的萃取效果也较好,而氨基酸酯离子液体对嘌呤类成分(如茶碱、可可碱、咖啡因等)也有很强的萃取能力。离子液体中烷基取代基的碳链长度对提取效率的影响较大,如用离子液体提取牛蒡子中牛蒡苷和牛蒡苷元时,随着离子液体中碳链的延长,其提取效率也随之提高,这是由于碳链的延长增强了离子液体的疏水性。此外,咪唑类阳离子与牛蒡苷、牛蒡苷元间存在氢键、离子键、π-π跃迁等作用力,这些作用力有助于离子液体溶解目标化合物,从而提高提取效率[10]。
此外,离子液体的水溶性与其阴离子种类有关,如具有相同阳离子的[OMIM][BF4]和[OMIM][Br],前者与水不相溶,而后者完全溶于水,可溶于水的离子液体一般以水溶液形式用于天然活性成分的提取。
2.2 热稳定性
离子液体作为一种萃取介质,需要能承受目标产物提取过程的操作温度,故热稳定性成为其一项重要性能指标。离子液体的热稳定性主要受到其阴阳离子的组成、杂原子-碳原子之间和杂原子-氢键之间作用力以及含水量的影响[1]。其中,阴离子的结构和性质对离子液体热稳定性的影响最为明显,阴离子的配位性和亲核性越弱,其组成的离子液体的热分解温度越高;而随着阴离子亲水性的增强,相应的离子液体的热分解温度降低[11]。咪唑类离子液体的热稳定性顺序是(按所含阴离子排序):[Cl]-、[Br]-、[I]-<[BF4]-<[CF3SO3]-<[NTf2]-<[PF6]-。差示扫描量热法(differential scanning calorimeter,DSC)分析结果显示大多数离子液体的热分解温度接近于400 ℃[10,12],此温度高于一般提取过程的操作温度。
2.3 不挥发性
离子液体由于完全由离子组成,故其蒸汽压几乎为零,即离子液体具有不挥发性。因此,当离子液体与水或者有机溶剂形成两相进行目标产物分离时,若被萃取物质具有挥发性,可以通过蒸馏回收的方法获得被萃取物质,使离子液体得到循环利用,且其难挥发性能极大减少对环境的污染[13]。2.4 高黏度
离子液体的另一个重要性质是高黏度,主要受氢键和范德华力等分子间相互作用力的影响,其黏度要高于一般有机溶剂,是水的几十倍甚至几百倍。当离子液体中阳离子烷基链增长时,其黏度也随之增大。同样,离子液体中阴离子的类型和对称性对其黏度的影响也较大,如25℃时,[BMIM][PF6]的黏度为450 CP(1 CP= 1 mPa.s),而[BMIM][NTf2]的黏度仅为69 CP;在25℃电离平衡的水中,[BMIM][PF6]的黏度为397 CP,而[BMIM][ NTf2]的黏度仅27 CP,可见水的存在明显影响离子液体的黏度[14]。
2.5 高密度
大多数离子液体的密度都要高于有机溶剂,一般在0.9~1.7 g·cm-3之间,主要受其阳离子和阴离子结构的影响。其中,阴离子的影响更明显,因为阴离子的分子质量对离子液体的分子结构体积(即分子实际体积)和自由体积(即分子间空隙和分子表面空穴体积)具有决定性作用,通常离子液体密度随阴离子体积的增大而增大;而阳离子的作用恰好相反,碳链越长,阳离子体积越大,离子液体密度越小。在设计和制备离子液体时,可选择相应的阴离子来确定离子液体密度的大致范围,再选择阳离子进行微调[15]。
3 离子液体在天然活性物质提取中的应用
部分离子液体难溶于水,因此能与水形成两相体系,利用溶质在两相中的分配系数的不同而达到分离天然活性化合物的目的,而且因其不挥发性,可以通过蒸馏的方法将挥发性产物从离子液体中分离出来,而低挥发性的有机化合物可通过超临界流体CO2萃取。相比于常用的有机溶剂,离子液体在提取天然活性物质方面具有巨大潜力,它的应用可简化样品的预处理、提高萃取效率、减少对环境的污染等。因此,近年来,离子液体已成功应用于天然药物中活性化合物的提取,且一般与液-液萃取、超声辅助提取(UAE)、微波辅助提取(MAE)、高速逆流色谱(HSCCC)、负压空化提取(PNEC)、超高压提取(UPE)等技术联用(见表2)。
另外,由于离子液体的黏性较大,因此在提取天然活性物质中其水溶液的应用较多。但也有一些文献报道了纯离子液体的应用,不过这些离子液体大多是自己合成的,且黏度较低。

表2 离子液体在提取天然活性物质中的应用实例Table 2 Examples for the applications of ionic liquids in extraction of natural active compounds

续表2
由表2数据可见,相对于水、乙醇、石油醚等常规溶剂,离子液体在天然活性成分提取方面具有较大优势。植物细胞壁主要由纤维素、半纤维素和果胶组成,纤维素容易产生分子内氢键及纤维素链之间的分子间氢键,并聚集形成纤维素微纤丝。传统的植物提取方法是采用甲醇、丙酮等作为提取溶剂,这些有机溶剂只能通过溶解细胞膜中脂质,增大穿透性,在一定程度上对植物组织造成机械性破坏,从而达到萃取目的。而离子液体则能竞争性地与纤维素形成氢键,更大程度地破坏纤维素微纤丝的氢键网状结构,溶解纤维素,更易进入植物细胞,显著提高萃取效率。另外,与水相比,离子液体与纤维素形成的氢键键能提高了3倍,表明离子液体对纤维素的活性位点具有更强的亲和力,而这种作用力能够改变纤维素的特性而破坏它的三级结构[45]。可见,相比于甲醇等常规溶剂,离子液体对植物细胞壁具有更强的破坏能力,故其对天然活性物质的提取效率也就更高。
3.1 黄酮类化合物的提取
离子液体在黄酮类化合物的提取中得到了较为广泛的应用。王阳光等[16]在微波辅助提取柽柳中芦丁的实验中,分别采用[BMIM][Br]、[BMIM][BF4]、[HMIM][Br]、[HMIM][BF4]等4种离子液体为萃取剂,比较了不同离子液体对芦丁萃取效率的影响,结果发现[BMIM][Br]比另外3种离子液体更有优势,表明离子液体中的阴阳离子对提取效率均有影响,且离子液体与芦丁分子之间有多种作用力,如氢键、静电作用等,有助于芦丁溶解在离子液体中。另外,该实验还将离子液体与传统溶剂甲醇、水和乙醇的微波辅助提取芦丁效率进行了比较,结果发现离子液体对柽柳中芦丁的萃取效率比水提高了68.8%,提示离子液体对微波具有较强的吸收和转化能力,致使样品和溶剂迅速升温,从而提高了对芦丁的提取效率。Yang等[23]比较了纯水、0.5 mol·L-1NaCl溶液、80%甲醇、0.5 mol·L-1[BMIM][Br]对甘草中甘草苷、异甘草素和甘草酸的提取效果,结果显示,[BMIM][Br]对3种目标产物的平均提取率比纯水提高了63.4%,比NaCl溶液提高了83.3%。
3.2 生物碱类化合物的提取
在生物碱类化合物的提取中,离子液体也明显体现出了相对于其他溶剂的优势。为筛选出最适宜的离子液体,提取前一般会考察不同阴阳离子对活性成分的提取效率,而阴阳离子的选择也决定了该离子液体的亲水性大小。如利用[BMIM][BF4]从白胡椒中提取胡椒碱时,由于胡椒碱的疏水性,离子液体与胡椒碱之间的疏水作用力成为提取过程的主要驱动力,经预实验考察发现,构成此类离子液体的4种阴离子中,能增强离子液体疏水性的阴离子顺序为:[PF6]->[ H2PO4]-> [Br]->[BF4]-,[BMIM][BF4]对胡椒碱的提取效率比75%甲醇提高了83.4%[30]。另一方面,随着离子液体中阳离子碳链的增长,其亲水性减弱,而且碳链上的取代基团对离子液体的亲水性有明显的影响,如磺酸基能降低离子液体的亲水性以及氢键的强度。Yang等[32]在利用离子液体提取喜树翅果中的喜树碱时,考察了[EMIM]+、[PMIM]+、[AMIM]+、[BMIM]+、[HMIM]+和[OMIM]+对喜树碱提取效率的影响,结果发现,离子液体中阳离子碳链上碳原子大于8时,其亲水性降低,且当碳链从乙基增长到辛基,离子液体的提取效率随之增加。Wang等[46]在利用[BMIM][Br]从黄柏中提取3种生物碱——小檗碱、药根碱和巴马汀时,考察发现,此离子液体在阴离子不变而仅延长阳离子碳链后,其对3种生物碱的提取效率均随之呈现逐渐下降的趋势。这表明,离子液体中阳离子烷基链的长度与其亲脂性相关,从而影响其提取效率。
3.3 萜类化合物的提取
一般萜类化合物亲脂性强,难溶于水,易溶于脂溶性有机溶剂。但萜类的苷化合物具有一定的亲水性,能溶于热水,不溶于亲脂性溶剂,如人参皂苷具有水溶性。Lin等[39]利用离子液体对人参中8种人参皂苷进行提取,结果发现,离子液体中咪唑类阳离子的烷基链长度对其提取效率有明显影响,即随着烷基链由丙基增长至己基,相应离子液体对总皂苷的提取效率急剧下降,这是因为随着烷基链含碳量的增加,离子液体的水溶性降低所致。Fan等[41]利用[BMIM][Cl]微波辅助提取广藿香中的广藿香醇,结果提取率达1.94%,相比于乙醇微波辅助提取法提高了166%,比超声辅助提取法和索氏提取法提高123%,比24 h乙醇常温浸提法提高234%,这是因为离子液体能够溶解纤维素,极大地促进了植物细胞壁通透性的增加,继而显著提高其提取效率[40]。
3.4 木脂素类化合物的提取
植物中的木脂素是亲脂性成分,多呈游离型,少数与糖结合成糖苷。因此木脂素易溶于氯仿、乙醚等极性小的有机溶剂,但是极性小的溶剂又难以透入植物细胞,故离子液体在木脂素的提取方面具有较大优势。Ma等[35]将离子液体成功应用于五味子中木脂素的提取,相对于3 h的水蒸气蒸馏法和4 h的回流提取法,离子液体微波辅助提取法将提取时间缩短至40 min,提取效率也有所提高,而且采用离子液体作为提取溶剂,也减少了对环境的污染。王迪等[36]以[C12MIM][Br]为提取溶剂,采用超高压技术从牛蒡子中提取牛蒡苷和牛蒡苷元,避免了热效应造成的有效成分损失,在很大程度上缩短了提取时间,减少了杂质成分的溶出,并可降低能耗。其间,该研究小组采用烷基链较长的[C12MIM]+作为离子液体中阳离子,使得离子液体疏水性增强,极性减弱,而且咪唑类阳离子与目标产物之间可产生π-π跃迁、离子键、氢键等作用力,有助于目标化合物的溶解,从而提高提取效率。
3.5 香豆素类化合物的提取
香豆素类化合物部分溶于热水,易溶于有机溶剂,而香豆素苷类化合物可溶于甲醇、乙醇和水,难溶于低极性有机溶剂。秦皮甲素和秦皮乙素属于香豆素苷类,所以当离子液体的烷基链碳数目大于4时,其对这两个目标产物的提取效率降低。这是因为随着离子液体中阳离子的烷基链增长,其极性降低,空间位阻增大,使离子液体与目标化合物之间的作用力减弱,从而使此类离子液体的提取效率降低[37]。
3.6 有机酸类化合物的提取
近年来,逐渐有研究者将离子液体水溶液应用于有机酸的提取,探究离子液体对此类化合物提取的特异性和规律性。Liu等[42]尝试用一系列溴化咪唑盐离子液体对迷迭香中鼠尾草酸和迷迭香酸进行提取,结果,通过单因素优化发现,[OMIM]Br对目标产物的提取率最高;而且,与传统提取方法相比,微波辅助离子液体的提取方法能在很大程度上提高目标化合物的回收率,缩短提取时间。Lou等[18]采用[BMIM]Br作为提取溶剂,超声/微波辅助提取牛蒡叶中的咖啡酸和绿原酸,结果显示,与70%乙醇热回流提取方法相比,此法对咖啡酸和绿原酸的回收率分别提高了7.7%和8.1%,提取时间也从5 h缩短至30 s。
3.7 多类成分同时提取
药用植物中一般含有大量不同种类的活性成分,用常规提取溶剂只能提取到类似极性的物质,而离子液体具有广泛的溶解能力,能够同时提取不同结构类型以及不同极性的化合物[11]。迷迭香富含鼠尾草酸、迷迭香酸等优良抗氧化剂,被广泛用于医药、食品等物质的保存,并含有用于食品调味剂的挥发油,其中,鼠尾草酸和挥发油属于脂溶性物质,而迷迭香酸属于水溶性酚酸类化合物。Liu等[42]将离子液体联合微波辅助提取方法应用于迷迭香中鼠尾草酸、迷迭香酸和挥发油的提取,其间,比较了离子液体与传统有机溶剂对这3种物质的回收率。结果发现,在相同微波条件下,[OMIM]Br对鼠尾草酸的提取率为(33.29±0.69) mg·g-1,而水仅为(1.09±0.03) mg·g-1,且此离子液体对迷迭香酸和挥发油的提取率也较水分别提高了33.7%和16.2%;相比于85%乙醇水溶液,[OMIM]Br对鼠尾草酸和迷迭香酸的提取率分别提高了17.6%和2.6%,对挥发油的提取率也达到了(21.5±0.83) mg·g-1;此外,离子液体的使用在很大程度上缩短了提取时间,减少了对热敏性物质的破坏。
4 结语与展望
离子液体因其独特的性质,在天然活性物质提取领域得到广泛关注。离子液体对纤维素的溶解性极强,能够迅速破坏植物细胞壁,加速有效成分的溶出,从而缩短提取时间,提高提取效率;而且,离子液体和天然活性化合物之间产生的氢键、π-π、范德华力、库仑力等作用力,能加强二者的结合,促进离子液体提取效率的提高;另外,与普通有机溶剂不同的是,离子液体作为一种设计型溶剂,可以通过调整阴阳离子来调节其溶解性,以满足与不同物质之间的相互作用,继而扩大了其提取目标化合物的应用范围;再者,离子液体几乎没有蒸汽压,故其具有不挥发性,可通过蒸馏回收其提取的具有挥发性的目标成分,使离子液体得以循环利用,也减少了对环境的污染。此外,离子液体与MAE和UAE的联合使用,能保护热敏性物质免遭破坏,并缩短提取时间,故在天然活性成分提取领域也广受欢迎。然而,离子液体也存在一些缺陷,如其较广的溶解范围给目标化合物的进一步分离纯化带来不小麻烦,而且因其不挥发性,也导致不可能对其中提取的不挥发性成分进行浓缩。
离子液体种类繁多,但目前使用较多的为咪唑类离子液体,如本文所述,其对天然活性物质具有良好的提取性能,而其他类型的离子液体是否也具有相似良好的提取性能,值得进一步研究。另外,目前尚未发现不同类型离子液体对不同种类天然活性成分的提取效率有明显的特异性和规律性,这有待更深入的研究。
[1]Passos H, Freire M G, Coutinho J A. Ionic liquid solutions as extractive solvents for value-added compounds from biomass[J]. Green Chem,2014, 16(12): 4786-4815.
[2]Han X, Armstrong D W. Ionic liquids in separations [J]. Acc Chem Res,2007, 40(11): 1079-1086.
[3]Anderson J L, Armstrong D W, Wei G T. Ionic liquids in analytical chemistry [J]. Anal Chem, 2006, 78(9): 2892-2902.
[4]Wanigasekara E, Perera S, Crank J A, et al. Bonded ionic liquid polymeric material for solid-phase microextraction GC analysis[J]. Anal Bioanal Chem, 2010, 396(1): 511-524.
[5]Liu F, Wang D, Wang X, et al. Ionic liquid-based ultrahigh pressure extraction of five tanshinones from Salvia miltiorrhiza Bunge[J]. SepPurif Technol, 2013, 110: 86-92.
[6]Yang Q, Xing H, Su B, et al. Improved separation effi ciency using ionic liquid-cosolvent mixtures as the extractant in liquid-liquid extraction: a multiple adjustment and synergistic effect[J]. Chem Eng J, 2012,181/182: 334-342.
[7]Bogdanov M G, Svinyarov I R, Keremedchieva, et al. Ionic liquidsupported solid-liquid extraction of bioactive alkaloids. I. New HPLC method for quantitative determination of glaucine in Glaucium fl avum Cr. (Papaveraceae)[J]. Sep Purif Technol, 2012, 97: 221-227.
[8]Tang B, Bi W, Tian M, et al. Application of ionic liquid for extraction and separation of bioactive compounds from plants[J]. J Chromatogr B,2012, 904: 1-21.
[9]Wei Z, Zu Y, Fu Y, et al. Ionic liquids-based microwave-assisted extraction of active components from pigeon pea leaves for quantitative analysis[J]. Sep Purif Technol, 2013, 102: 75-81
[10]张丹丹, 谭婷, 刘鄂湖, 等. 离子液体在中药提取、分离与分析中的应用[J]. 中国药科大学学报, 2013, 44(4): 380-384.
[11]Huddleston J G, Visser A E, Matthew Reichert W, et al. Characterization and comparison of hydrophilic and hydrophobic room temperature ionic liquids incorporating the imidazolium cation[J]. Green Chem, 2001, 3: 156-164.
[12]Fredlake C P, Crosthwaite J M, Brennecke J F, et al. Thermophysical properties of imidazolium-based ionic liquids[J]. Chem Eng Data, 2004,49 (4): 954-964.
[13]汪雁, 宋航, 贾春梅, 等. 离子液体在天然药物活性成分提取中的应用[C]//2012年中国药学大会暨第十二届中国药师周论文集. 南京:中国药学会, 2012: 2213-2218.
[14]Seddon K R, Stark A, Torres M J. Influence of chloride, water, and organic solvents on the physical properties of ionic liquids[J]. Pure Appl Chem, 2000, 72(12): 2275-2287.
[15]Larsen A S, Holbrey J D, Reed C A, et al. Designing ionic liquids: imidazolium melts with inert carborane anions[J]. Am Chem Soc, 2000,122(30): 7264-7272.
[16]王阳光, 欧阳小琨, 杨立业, 等. 离子液体微波辅助萃取柽柳中芦丁的研究[J]. 高校化学工程学报, 2011, 25(3): 411-415.
[17]Fan J P, Cao J, Zhang X H, et al. Optimization of ionic liquid based ultrasonic assisted extraction of puerarin from Radix Puerariae Lobatae by response surface methodology[J]. Food Chem, 2012, 135(4): 2299-2306.
[18]Lou Z, Wang H, Zhu S, et al. Ionic liquids based simultaneous ultrasonic and microwave assisted extraction of phenolic compounds from burdock leaves[J]. Anal Chim Acta, 2012, 716: 28-33.
[19]Li X, Guo R, Zhang X, et al. Extraction of glabridin using imidazoliumbased ionic liquids[J]. Sep Purif Technol, 2012, 88: 146-150.
[20]Liu Y, Yang L, Zu Y, et al. Development of an ionic liquid-based microwave-assisted method for simultaneous extraction and distillation for determination of proanthocyanidins and essential oil in Cortex cinnamomi[J]. Food Chem, 2012, 135(4): 2514-2521.
[21]Duan M H, Luo M, Zhao C J, et al. Ionic liquid-based negative pressure cavitation-assisted extraction of three main flavonoids from the pigeonpea roots and its pilot-scale application[J]. Sep Purif Technol,2013, 107: 26-36.
[22]Xu L, Li A, Sun A, et al. Preparative isolation of neomangiferin and mangiferin from Rhizoma anemarrhenae by high-speed countercurrent chromatography using ionic liquids as a two-phase solvent system modifi er[J]. J Sep Sci, 2010, 33(1): 31-36.
[23]Yang L, Li L L, Liu T T, et al. Development of sample preparation method for isoliquiritigenin, liquiritin, and glycyrrhizic acid analysis in licorice by ionic liquids-ultrasound based extraction and highperformance liquid chromatography detection[J]. Food Chem, 2013,138(1): 173-179.
[24]马飞跃, 段开放, 王希清, 等. 离子液体微波辅助提取降香檀叶中鹰嘴豆芽素A和染料木素[J]. 植物研究, 2013, 33(4): 494-498.
[25]Du F Y, Xiao X H, Li G K. Application of ionic liquids in the microwave-assisted extraction of trans-resveratrol from Rhizma Polygoni Cuspidati[J]. J Chromatogr A, 2007, 1140(1): 56-62.
[26]陈君, 周光明, 杨远高, 等. 离子液体-超声辅助萃取/高效液相色谱法测定白花杜鹃叶中的黄酮[J]. 分析测试学报, 2013, 32(3): 341-345.
[27]朱晓娜, 曹伟伟, 李明静. 离子液体优化高速逆流色谱法分离槐花中的黄酮类化合物[J]. 天然产物研究与开发, 2012, 24(12): 1833-1836.
[28]Xiao Y, Wang Y, Gao S, et al. Determination of the active constituents in Arnebiae uchroma (Royle) Johnst. by ionic liquid-based ultrasonicassisted extraction high-performance liquid chromatography[J]. J Chromatogr B, 2011, 879(20): 1833-1838.
[29]Bi W, Tian M, Row K H. Ultrasonication-assisted extraction and preconcentration of medicinal products from herb by ionic liquids[J]. Talanta, 2011, 85(1): 701-706.
[30]Cao X, Ye X, Lu Y, et al. Ionic liquid-based ultrasonic-assisted extraction of piperine from white pepper[J]. Anal Chim Acta, 2009,640(1): 47-51.
[31]Ma C H, Wang S Y, Yang L, et al. Ionic liquid-aqueous solution ultrasonicassisted extraction of camptothecin and 10-hydroxycamptothecin from Camptotheca acuminate samara[J]. Chem Eng Process, 2012, 57/58(1): 59-64.
[32]Yang L, Wang H, Zu Y, et al. Ultrasound-assisted extraction of the three terpenoidindole alkaloids vindoline, catharanthine and vinblastine from Catharanthus roseus using ionic liquid aqueous solutions[J]. Chem Eng J, 2011, 172(2): 705-712.
[33]马文燕. 天然来源有效成分的微波辅助及离子液体微波辅助萃取技术应用研究[D]. 杭州: 浙江大学, 2010.
[34]Ma W, Lu Y, Hu R, et al. Application of ionic liquids based microwaveassisted extraction of threealkaloids N-nornuciferine, O-nornuciferine,and nuciferine from lotus leaf[J]. Talanta, 2010, 80(3): 1292-1297.
[35]Ma C H, Liu T T, Yang L, et al. Ionic liquid-based microwave-assisted extraction of essential oil and biphenyl cyclooctene lignans from Schisandra chinensis Baill fruits[J]. J Chromatogr A, 2011, 1218(48): 8573-8580.
[36]王迪, 耿岩玲, 王晓, 等. 超高压辅助离子液体提取/HPLC分析牛蒡子中牛蒡苷与牛蒡苷元[J]. 分析测试学报, 2013, 32(2): 218-222.
[37]Yang L, Liu Y, Zu Y G, et al. Optimize the process of ionic liquid-based ultrasonic-assisted extraction of aesculin and aesculetin from Cortex fraxini by response surface methodology[J]. Chem Eng J, 2011, 175(22): 539-547.
[38]Jin R, Fan L, An X. Microwave assisted ionic liquid pretreatment of medicinal plants for fast solvent extraction of active ingredients[J]. Sep Purif Technol, 2011, 83: 45-49.
[39]Lin H, Zhang Y, Han M, et al. Aqueous ionic liquid based ultrasonic assisted extraction of eight ginsenosides from ginseng root[J]. Ultrason Sonochem, 2013, 20(2): 680-684.
[40]Fan L, Jin R, Liu Y, et al. Enhanced extraction of patchouli alcohol from Pogostemon cablinby microwave radiation-accelerated ionic liquid pretreatment[J]. J Chromatogr B, 2011, 879(30): 3653-3657.
[41]李万华, 王小刚, 范代娣. 离子液体提取皂角刺白桦脂酸衍生物的研究[J]. 化学工程, 2012, 40(11): 1-3.
[42]Liu T, Sui X, Zhang R, et al. Application of ionic liquids based microwave-assisted simultaneous extraction of carnosic acid, rosmarinic acid and essential oil from Rosmarinus offi cinalis [J]. J Chromatogr A,2011, 1218(47): 8480-8489.
[43]Jiao J, Gaq Y I, Fu Y J, et al. Microwave-assisted ionic liquids treatment followed by hydro-distillation for the effi cient isolation of essential oil from Fructusforsy thiaseed[J]. Sep Purif Technol, 2013, 107: 228-237.
[44]张之达, 陈吉平, 李长平,等. 离子液体微波辅助萃取川芎中内酯类化合物[J]. 过程工程学报, 2010, 10(3): 498-502.
[45]Bogdanov M G, Svinyarov I. Ionic liquid-supported solid-liquid extraction of bioactive alkaloids. II. Kinetics, modeling and mechanism of glaucine extraction from Glaucium fl avum Cr. (Papaveraceae) [J]. Sep Purif Technol, 2013, 103: 279-288.
[46]Wang W, Li Q, Liu Y, et al. Ionic liquid-aqueous solution ultrasonicassisted extraction of three kinds of alkaloids from Phellodendron amurense Rupr and optimize conditions use response surface[J]. Ultrason Sonochem, 2015, 24: 13-18.
Application Progress of Ionic Liquids in Extraction of Natural Active Compounds
LI Mingying
(Department of Pharmacy, Zhejiang Greentown Cardiovascular Hospital, Hangzhou 310012, China)
Through retrieval, analysis and generalization of the related literatures published at home and abroad in recent years, the application progress of ionic liquids in the extraction of natural active compounds was reviewed. The application researches of ionic liquids as a kind of green solvents with their own unique properties in the extraction of natural active compounds have attracted much attention in recent years. However, most of the ionic liquids currently used in the extraction of natural active compounds are imidazolium types. In addition, the signifi cant specifi city and regularity of different types of ionic liquids to the extraction effi ciencies of different natural active components haven’t been revealed, which needs further investigations.
ionic liquid; natural active compound; extraction
TQ413; R284.2
A
1001-5094(2015)06-0437-09
接受日期:2015-04-10
*通讯作者:李明英,主管药师;
研究方向:临床药学,药物分析;
Tel:0571-88857888-80225; E-mail:limingying2015@163.com
