高能量密度液流电池的研究进展
2015-11-14贾传坤
贾传坤,王 庆
(新加坡国立大学材料科学与工程系,新加坡 117576)
随着世界经济的快速发展和人口的增多,能源和环境之间的矛盾日益加剧,因此以太阳能和风能为代表的新型清洁能源被大力开发[1-2]。由于风能和太阳能的发电过程存在不稳定性和不连续性,导致其很难安全并入电网[3-4],因此需要配备低成本高效率的电能转化和储存装置。另外,智能电网的发展也需要一种可靠的储能装置来调节电网的功率输入输出,以达到最高的效率。在众多储能技术中氧化还原液流电池(液流电池)以其结构设计灵活、储能规模大、可快速充放电、响应速度快和安全性能高等优点成为最有发展潜力的大规模储能装置[5-7]。近年来各种新型的液流电池体系被提出并广泛研究。本文主要对最近5年高能量密度液流电池的研究趋势进行归纳和总结,并对液流锂电池的工作原理及关键问题进行重点介绍。
1 氧化还原液流电池
1974年,Thaller[8]在第九届学会间能量转换工程会议上首次提出了氧化还原液态流体电池——“液流电池”的概念。液流电池与传统电池不同,其能量不是储存在电池内部,而是储存在与电池分离的电解液中。这样的电池结构使其功率输出和能量储存彼此独立。如图1所示,液流电池的基本组成包括正负两个储液罐、正负极材料、隔膜以及电池壳体。在外接循环泵的驱动下,正负极电解液分别在储液罐和两个半电池室之间循环流动,并在电极上发生氧化和还原半反应。电子通过集流体经外电路传递给负载,完成化学能和电能间的能量转换。液流电池具有设计灵活的优点,可以通过改变正负极电解液的量来满足储能容量的需求,也可以通过改变电堆中单电池串并联数量和有效作用面积,来满足不同的功率需求[9-10]。根据电解液的不同,液流电池分为水系和有机系液流电池。下文将对两类液流电池分别进行简单地介绍。

图1 氧化还原液流电池示意图Fig.1 Schematic illustration of redox flow batteries
2 水系液流电池
在水系液流电池中,氧化还原活性物质溶解在水溶液里。因此,水系液流电池工作电位窗口一般很窄(< 2 V)。水系液流电池最早被广泛研究,世界范围内有许多大型示范性电池系统。其中包括铁/铬液流电池、全钒液流电池、溴/多硫化物液流电池以及溴/醌液流电池等,见表1。

表1 水系液流电池对比表Table 1 Summary of different aqueous redox flow batteries
1974年,美国航天局(NASA)的Thaller[11-12]首次提出铁/铬液流电池。其正负极电解液中的氧化还原电对分别为Fe2+/3+和Cr2+/3+。电池的工作电压在0.90~1.20 V,这类电池具有大约15 W·h/kg的比能量。2014年EnerVault公司展示了1 MW·h/250 kW的电池系统。但是两个问题制约着它的发展[13]:首先是铬半电池中铬氧化还原电对的可逆性差,影响了电池的寿命和性能;另外正负极电解液通过隔膜扩散渗透,导致其交叉污染,从而增大了电池的自放电,降低了电池的库仑效率。
1988年,Skyllas-Kazacos和Rychcik成功地展示了第一个全钒液流电池。它与其它液流电池的不同之处在于,钒电池的电解液为单一钒离子的硫酸溶液,这使得正负极电解液的交叉污染风险降低很多。工作时,正负极电解液中的VO2+/VO2+和V3+/V2+电对分别在正负极上发生氧化还原反应,与此同时质子通过隔膜传递以保持两个半电池室的物质和电荷平衡,完成电能和化学能的可逆转换。钒电池的电池电压约为1.25 V,其能量密度一般为25 W·h/L。近年来,在世界范围内包括中国建立了很多大规模的钒电池的示范工程。但其商业化面临着高成本和低能量密度的考验[14-17]。
1983年,Remick和Ang[18-19]首次提出了溴/多硫化物液流电池。之后Regenesys公司用NaBr和Na2S4作为正负极的电解液,钠离子膜作为隔膜组装了电池。这类电池的开路电压为1.74 V,其能量密度达到20~30 W·h/L。虽然Aberthaw Power Station在英国成功展示了1 MW的电池系统,但由于这类电池的工作电压高,容易造成水分解。另外硫和溴会在隔膜上富集,产生H2S和Br2,带来安全隐患。除此之外,活性物质的交叉污染也需要解决[20-21]。
2014年,哈佛大学的Aziz等[22]报道了一类非金属溴/醌(bromine-quinone)液流电池。这类电池利用Br2/Br−和蒽醌磺酸盐(9,10-anthraquinone-2, 7-disulphonic acid, AQDS)作为正负极氧化还原对,开路电压为0.86 V。由于其氧化还原反应的电子数是2,并且活性物质的浓度比较高,溴/醌液流电池的能量密度接近钒电池。这类电池的一个主要优点是它使用低成本的正负极电解液,因此电池系统的预期成本要低于钒电池。此外,由于醌在碳电极上的反应速度很快,电池能够在较高的功率密度下工作。溴/醌液流电池的缺点是其正极使用腐蚀性很强的溴作为活性物质,因此电池的稳定性和安全性有待解决。
3 非水系液流电池
液流电池的能量密度与电池电压(V)、活性物质浓度(Ca)、有效电子数(n)以及电解液体积(Vt)相关[23]

式中,F为法拉第常数。从式(1)可以看出,提高电池电压和活性物质的有效浓度是提高液流电池能量密度的有效方法。水系液流电池由于水分解的影响,其电压很难达到2 V。因此,非水系液流电池在最近几年得到了广泛研究。
1988年Matsuda等[24]报道了第一个非水系的液流电池。这种电池利用钌的配合物,如[Ru(bpy)3]2+/3+作为活性物质,乙腈作为溶剂,电池电压达到2.60 V。随后,特别在过去5年间,很多有机金属分子作为活性物质被应用在非水系液流电池中,如Ru(acac)3[25]、Cr(acac)3[26]、[Ni(bpy)3]0/2+、[Fe(bpy)3]2+/3+[27]、Mn(acac)3[28]、VO(acac)2[29]、[V(mnt)3]2−[30]以 及[Fe(phen)3]2+/3+和[Co(phen)3]2+/3+[31]等。虽然这类电池的电压较高,但它的能量密度严重受限于分子在有机溶剂里的溶解度,而其一般低于1 mol/L。另外,由于H+在非水体系中无法使用,在充放电时碱金属离子(如Li+)常被用作电荷平衡离子,以保持两个半电池室间的电平衡。因此,这类电池需要一个既有高的锂离子电导率,又可以阻挡其它电解质成分透过的膜材料。而目前还没有这种高离子电导率和高选择透过性的膜可供使用。
4 混合液流电池
用高容量、低电位的金属材料代替低浓度的负极电解液,用作负极的储能介质,虽然牺牲了部分液流电池的工作特点,但可以极大地提高液流电池的能量密度。这种在正极半电池保持液流电池的工作模式,而负极半电池使用传统电池的工作模式的液流电池结构,叫做混合液流电池。现在研究最多的混合液流体系是基于金属锌和金属锂的混合液流电池。表2中总结了常见的各种混合液流电池体系,下文只对最常见的锌基和锂基混合液流电池进行简单介绍。

表2 金属基混合液流电池对比表Table 2 Summary of metal-based hybrid redox flow batteries
4.1 锌基混合液流电池
锌基液流电池的负极是金属锌板和辅助电解液,正极是流动的活性电解液。在充放电时,金属锌在负极上可逆地沉积、溶解(图2)。锌/溴液流电池是研究最多、最成熟的一种混合液流电池体系。它在20世纪70年代由Exxon公司最早展示出来,现在世界各地有多家企业在进行商业化开发。这类电池利用Br2/Br-和Zn0/2+在正负极的氧化还原反应,电池电压为1.85 V,能量密度可以达到39 W·h/L。但这类电池的产业化必须解决锌沉积形成枝晶以及高电位水分解的问题。另外,Br2蒸气的腐蚀性也考验着电池的长期稳定性。另一种锌基液流电池是基于锌/铈的液流体系,由英国Plurion公司在2004年开发出来。锌/铈液流电池利用Ce3+/4+和Zn0/2+的反应,使用甲基磺酸作为溶剂,电池的开路电压可以达到2.43 V,能量密度为37.5~120 W·h/L。
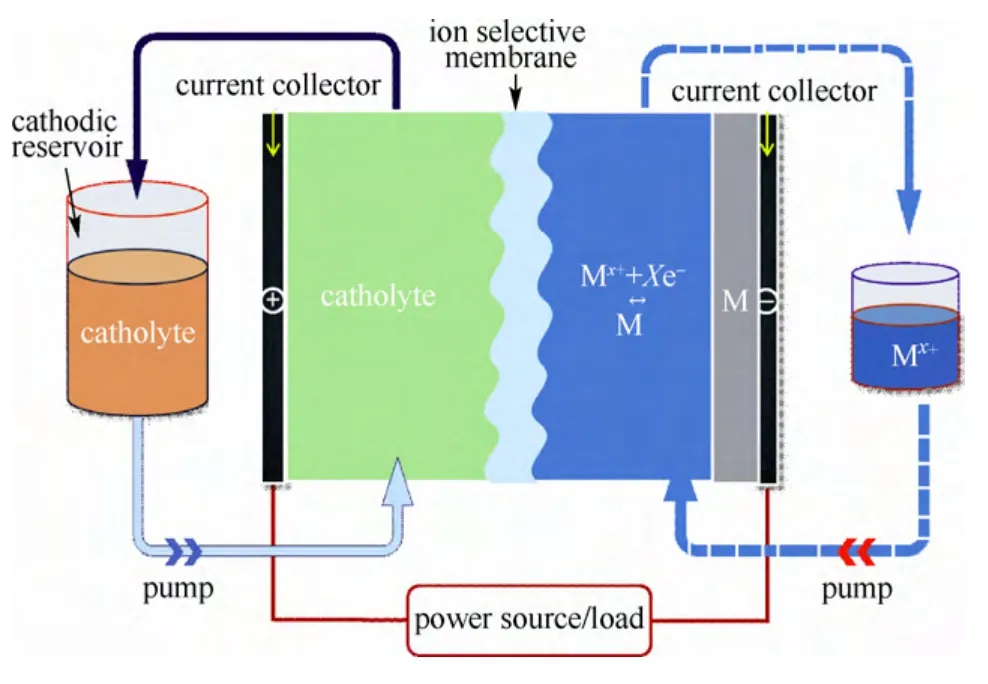
图2 金属基混合液流电池示意图Fig.2 Schematic illustration of metal-based hybrid redox flow battery
2015年美国西北太平洋国家实验室(PNNL)报道了一种高能量密度的锌/碘液流电池[23]。这类液流电池利用I-和Zn0/2+的氧化还原反应,电池的电压为1.22 V。由于其电极反应的有效电子数为2,而碘离子的浓度可以达到5~7 mol/L,这类电池的能量密度远远高于钒电池,实际测量达到167 W·h/L。在报道中Nafion 115被用作Zn2+的传递膜,但由于其离子选择性和电导率很低,造成电池实际工作中的极化比较大,所以电池的功率密度较低。因此,开发一种低成本的Zn2+传导膜是这类电池能否产业化的关键。此外,金属锌电极的循环稳定性及正极的腐蚀性问题都将影响电池的循环寿命并增加运行成本。
4.2 锂基混合液流电池
锂基混合液流电池是近来的一个研究热点。由于碱金属特别是金属锂具有很低的电极电位,与其它高电位的氧化还原对组合在一起可以获得很高的工作电压,进而能显著提高电池系统的能量密度。此外,Li+导电膜的发展是锂基混合液流电池研究的另一个驱动力。2011年,Goodenough和周豪慎研究组几乎同时报道了用锂片作负极,[Fe(CN)6]3+/4+或Fe2+/3+的水溶液为正极电解液,正负极半电池用Li+导电陶瓷膜隔开的锂基混合液流电池[42-43]。此后,其它类似的体系不断地被报道出来。如锂/碘和锂/溴液流电池[36,44],分别用I3-/I-或Br2/Br-的水溶液作为正极电解液,电池电压分别为3.60 V和3.90 V,能量密度和比能量分别达到了550 W·h/L和1000 W·h/kg。根据报道,这类电池具有很高的循环稳定性,前50周只有很小的容量衰减。但需要指出的是,以上的电池测量多数在静态下进行,并且使用的电解液量非常少。考虑到在实际大规模应用中,陶瓷膜的成本高且易碎,而且正极使用腐蚀性高的碘或溴,这类电池在正极电解液流动条件下的长期稳定性以及安全性需要进一步被证实。
非水系的正极电解液与金属锂有更好的相容性,与水系相比它对隔膜的要求低得多。2014年,Yu等[39]利用二茂铁的DMF溶液作为正极电解液,电池表现出较好的循环容量保持率和能量效率。2014年,PNNL的Wang等[40]也报道了一种锂/改性二茂铁液流电池。这类电池用二茂铁的离子盐作为正极活性物质,它在碳酸酯中的溶解度可以达到0.80 mol/L,因此电池的能量密度达到了50 W·h/L。2015年,PNNL的同一研究组报道了一种锂/ TEMPO液流电池[38]。它利用TEMPO的碳酸酯溶液作为正极活性物质,浓度可以达到2.0 mol/L。因此这类电池可以获得远高于其它液流电池的能量密度188 W·h/L。
随着锂硫电池的发展,锂/多硫化物液流电池是近来研究较多的一种锂基混合液流电池[45]。它利用锂片作为负极,可溶解的锂多硫化物作为正极活性物质。这类电池理论能量密度为190 W·h/L,实际电池的能量密度在5 mol/L Li2S8条件下能够达到108 W·h/L。循环500次后,这类电池的容量保持率在75%左右。在非水系锂基混合液流电池中,金属锂上生成的钝化膜(SEI膜)可以作为天然的Li+导电膜,阻挡正极活性分子的透过,但其循环稳定性还有待证实。另外,锂枝晶以及锂片在循环中的粉化等问题并没有得到解决。因此这种锂基混合液流电池的实际应用,还有很长的路要走。
在以上讨论的各种液流电池体系中,电池的能量密度除了受限于电解质溶液中氧化还原对的浓度以外,电解液中的电荷平衡离子的浓度,如水系中的H+、非水系中常用的Li+等也是限制电池能量密度的一个因素。这些电荷平衡离子需要和活性物质的浓度相匹配,才能发挥液流电池的全部容量。
5 半固态流体电池
半固态流体电池(semi-solid flow battery)最早由麻省理工学院的Yet-Ming Chiang研究组[46]在2007年提出。如图3所示,这种电池把固体活性物质、导电添加剂与电解液的混合物做成可以流动的浆料,在循环泵的驱动下流过正负极半电池室,电极上的电子通过导电添加剂形成的导电网络完成电能在固体活性物质中的储存和释放。与氧化还原液流电池相比,由于半固态浆料的交叉污染风险较低,半固态流体电池不需要昂贵的离子交换膜,一定厚度的微孔膜即可以阻挡活性物质的透过。以研究最多的半固态流体锂电池为例,其正极活性浆料使用锂离子电池常用的正极材料,如LiCoO2、LiFePO4、LiNi0.5Mn1.5O4或 0.3Li2MnO3·0.7LiMO2(M=Mn、Co、Ni)等,这些活性材料中可以脱出的Li+浓度分别为25.6、22.8、24.1、39.2 mol/L;负极浆料使用锂离子电池常用的负极材料,如Li4Ti5O12、石墨或硅等,其可嵌入的Li+浓度分别为22.6、21.4和87.0 mol/L,都远远高于液流电池中氧化还原对的浓度。另外,由于电池电压与锂离子电池接近,半固态流体锂电池能够展现出远高于传统液流电池的能量密度。
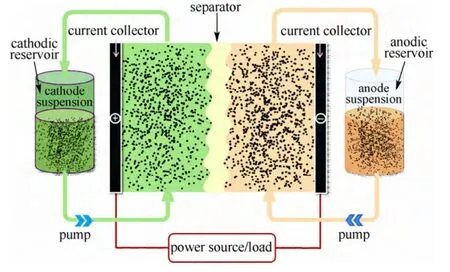
图3 半固态流体电池示意图Fig.3 Schematic illustration of semi-solid flow battery
近年来,Chiang研究组展示了不同锂离子电池正负极材料的半固态流体锂电池。如在一个典型的LiCOO2-Li4Ti5O12半固态流体电池中,它的正极活性浆料由体积比为10%的Li4Ti5O12和2%的炭黑组成,负极浆料由体积比为20%的LiCoO2和1.5%的炭黑组成。当正负极浆料中的LiCoO2和Li4Ti5O12体积比为40%时,电池的能量密度可以达到397 W·h/L。如果用相同体积比的LiCoO2-石墨作为活性物质,电池的能量密度能进一步提高到615 W·h/L。
锂硫电池以其高的比容量和比能量而被广泛研究。借助于高容量的锂硫电池活性材料,2015年Lu等[47]报道了半固态的锂硫电池,它的正极浆料由不同体积比的硫和炭黑组成。使用20%硫和26%炭黑做成正极浆料,电池的体积容量能够达到294 A·h/L,100周循环的库仑效率和能量效率分别高于90%和80%。但由于该工作使用的电解液只有100 L,电池在实际应用过程中的长期循环寿命还有待验证。
另一种类似的半固态流体电池是美国阿贡国家实验室(ANL)提出的“nanoelectrofuel”流体电池。据报道,他们使用活性物质的纳米颗粒与水系或非水系的电解液混合形成浆料,在提高活性物质比例的同时,保持了浆料的高流动性。
虽然理论上半固态流体电池可以做到很高的能量密度,但实际中高比例的活性物质将导致正负极浆料的黏度很高,使得它们在电池中的流动性很差,需要消耗更多循环泵的能量,从而影响电池的工作效率。因此,半固态流体电池只有在一定规模以上才可能形成竞争力,而其最终会成为一个工程问题。另外,为提高活性物质在浆料中的比例,减少导电添加剂的量也将限制电池的功率密度。
6 基于“氧化还原靶向反应”的液流电池体系
如上所述,传统液流电池的活性物质溶解在电解液中,其浓度很难提高到10 mol/L以上(尤其在非水体系中);而活性物质浓度高的半固态流体电池又面临浆料的低流动性问题。因此,如何兼顾传统液流电池电解液的好流动性以及半固态流体电池正负极浆料的高活性物质浓度,成为发展下一代高能量密度液流电池的一个关键。这里一个可能的选择是基于“氧化还原靶向反应”的液流电池体系。
6.1 液流锂电池
2006年,本文作者课题组[48]提出了电极材料的“氧化还原靶向反应”(redox targeting reaction):即利用电位合适的氧化还原媒介分子,与分散在电解液中的固体活性物质进行可逆的氧化还原反应。通过这样一个化学过程,可以实现固体活性物质的可逆充放电,而不需要像传统电池中的一样将活性物质涂在电极片上。利用锂离子电池的电极材料,2011年我们研究组[49]首次将这一原理引入到液流电池中,发展了新一代高能量密度的氧化还原液流锂电池(redox flow lithium battery,RFLB)。
如图4所示,在一个典型的半电池结构中负极为锂片,正极使用高电位的二溴二茂铁(FcBr2)和低电位的二茂铁(Fc)作为“氧化还原靶向反应”的媒介分子,正极活性物质LiFePO4储存在一个分离的储能罐内。① 在充电过程中,Fc和FcBr2首先在电极上被氧化成Fc+和FcBr2+;② 在循环泵的驱动下,FcBr2+随着电解液流进储能罐,与其中的LiFePO4发生化学脱锂反应;③ FcBr2+被还原为FcBr2,反应后的FcBr2随着电解液流回电池内部,在电极上被重新氧化成FcBr2+,经过多次循环,直到罐内的LiFePO4被全部转化为FePO4,充电过程完成;④ 放电过程与充电过程类似,溶液中FcBr2+和Fc+首先在电极上被还原为FcBr2和Fc,随着电解液的流动,Fc进入储能罐并与其中的FePO4发生化学嵌锂反应;⑤ Fc被氧化为Fc+,反应后的Fc+随着电解液流回电池内部,在电极上被重新还原为Fc。经过多次循环,直至罐内的FePO4全部转化为LiFePO4,放电过程结束。
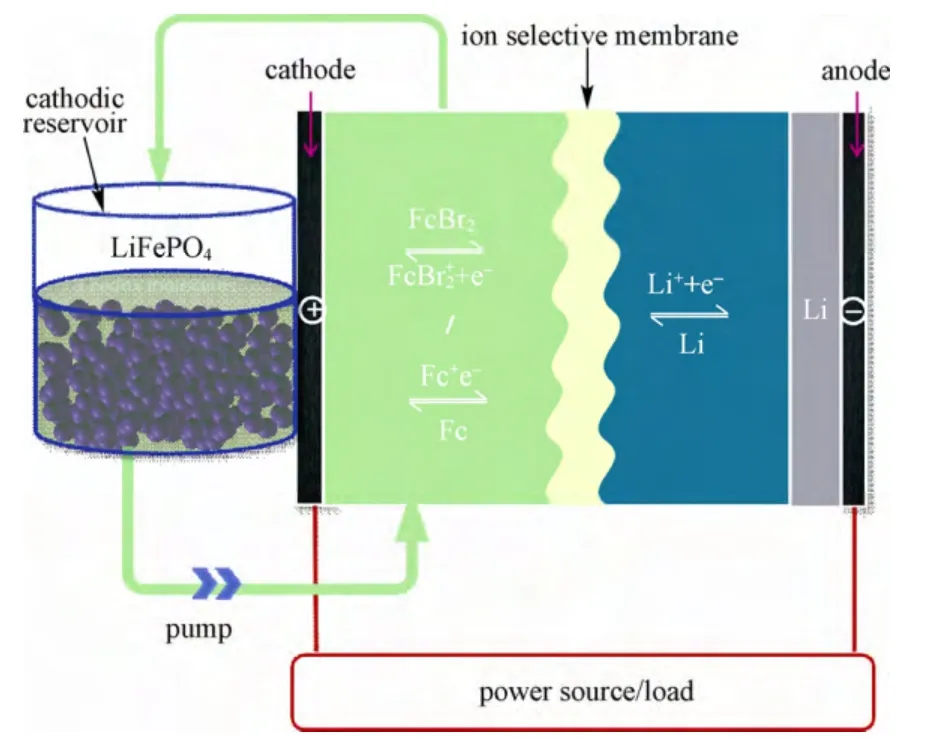
图4 液流锂电池半电池示意图Fig.4 Schematic illustration of redox flow lithium battery half-cell
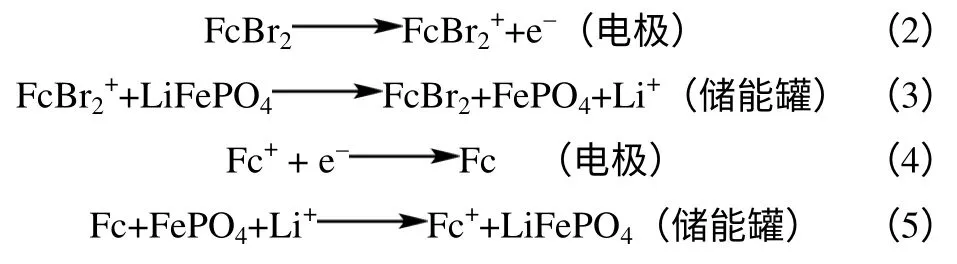
这个半电池的放电电压为3.25~3.40 V。考虑到实际应用中LiFePO4固体需要一定的孔隙率以保证电解液流过,当空隙率为50%时,储能罐中Li+的有效浓度为11.4 mol/L,此时这种RFLB半电池的能量密度能够达到1000 W·h/L。
同样地,液流锂电池的半电池也可以用低电位的材料(如TiO2)作为活性物质,用十甲基二茂钴 (CoCp*2)和二茂钴(CoCp2)作“氧化还原靶向反应”的媒介分子,按照下列反应步骤进行可逆地充放电[50]
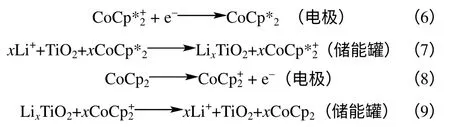
结合以上的两个半电池,分别用LiFePO4和TiO2作为储能罐中的正负极活性物质,20 mmol/L的Fc/FcBr2和(CoCp*2)/(CoCp2)作正负极反应的媒介分子,本文作者等[51]构建了一个液流锂电池的全电池,如图5所示。这个全电池避免了半电池中金属锂的循环稳定性问题,考虑到储能罐中固体活性物质的孔隙率,其能量密度能达到250 W·h/L以上。这种液流锂电池兼具液流电池和锂离子电池的优点,同时避免了二者的缺点。与全钒液流电池 相比,液流锂电池的能量密度高一个数量级。与锂离子电池相比,储能罐中的固体活性物质不需要任何导电添加剂和黏结剂,大大简化了电池的组装,并能进一步提高电池的能量密度;液流锂电池对活性材料在脱嵌锂过程的体积变化有更高的忍耐度,有利于提高电池的循环寿命;另外,由于固体活性物质储存在分离的储能罐中,大大降低了大电池组过充电和过放电的危险。与半固态流体锂电池相比,由于固体活性物质在储能罐中静置,可以更致密,从而获得更高的能量密度;工程上流动介质的黏度以及流体的复杂性也大大降低。
现阶段氧化还原液流锂电池的发展主要受限于膜材料的Li+电导率,因此其功率密度还远远低于水系液流电池。另外,这种电池对储锂材料的选择有较高的要求。由于媒介分子与活性物质的氧化还原反应伴随着电子的转移,所以这些固体物质的表面不能存在厚的SEI膜。在解决以上问题的同时,作为一个新的储能技术,液流锂电池独特的工作原理也启发我们发展其它着眼于近期、更成熟的储能系统。另外我们要看到的是,电极材料的“氧化还原靶向反应”提供了一个多样化的平台。它不仅仅局限于以上提到的锂离子电池的电极材料,通过媒介分子的标靶作用,理论上所有的传统电池都可以转化成液流电池的工作模式,从而发展出“液流X-电池”(redox flow X-battery,X表示各种不同的电池化学),实现用低浓度的氧化还原对完成高密度的能量存储。

图5 锂离子液流全电池示意图Fig.5 Schematic illustration of redox flow lithium battery full cell
6.2 液流锂空气电池
近年来,锂空气电池由于其极高的能量密度而被广泛研究。但非水系锂空气电池面临的一个很大问题是,它的放电产物Li2O2沉积在阴极上,造成电极催化剂的钝化和电极材料的堵塞。借鉴“氧化还原靶向反应”的原理,本团队发展了一种液流锂空气电池,可以有效地解决以上问题[52]。
液流锂空气电池利用一对氧化还原分子作为氧化还原反应(ORR)和析氧反应(OER)的媒介,从而使Li2O2的生成和分解从电池内部转移到一个分离的气体扩散罐 (gas diffusion tank,GDT)中,成功地解决了电极的钝化和阻塞问题。液流锂空气电池的结构和工作原理如图6所示。在放电过程中,ORR分子首先在电极上还原,如式(10)所示,在循环泵的驱动下,还原态分子随着电解液流进GDT罐与Li+和O2发生化学反应,见式(11),生成的Li2O2沉积在气体扩散罐中

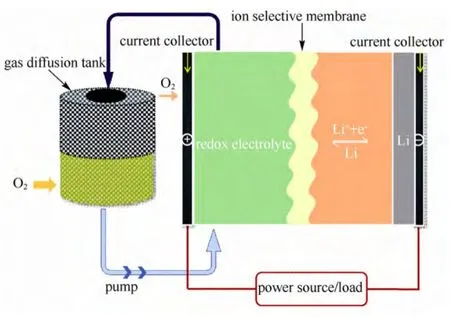
图 6 液流锂空气全电池示意图Fig.6 Schematic illustration of redox flow lithium oxygen battery
在充电过程中,OER分子首先在电极上氧化,如式(12)所示,氧化态分子随着电解液流进GDT罐与放电过程中生成的Li2O2进行反应,释放O2,见式(13)
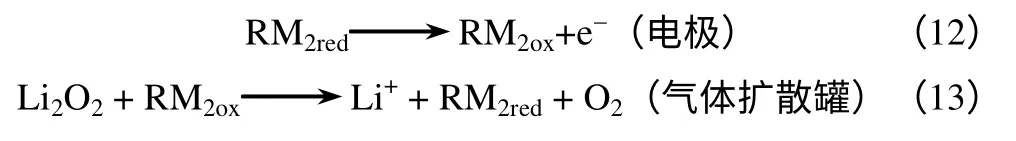
这类液流锂空气电池具有能量密度高,设计简单灵活等优点。目前本课题组在筛选合适的ORR以及OER反应的媒介分子,以进一步提高电池的循环稳定性,并降低电池的充电过电位。
7 结语与展望
液流电池以其特殊的工作模式,在大规模储能方面吸引了越来越多的关注, 许多液流电池的大型示范系统近年来在世界各地出现。另一方面,液流电池的研究力度在过去5年中变得更大,许多新的体系和研究手段不断被报道出来。综述近几年的进展,高能量密度液流电池的研究经历着从水系到非水系,从全液流到混合液流,从液相到半固相,再到全固相的发展阶段。
图7总结了近来研究的各种液流电池体系。从图7可以看出,大多数水系液流电池由于电压的限制,其单个储液罐的能量密度一般低于50 W·h/L。以钒电池为代表的水系液流电池还面临着成本高和工作温度区间窄的缺点,阻碍了这类电池的产业化发展。而近年来广泛研究的非水系液流电池,虽然电池电压一般高于2 V,但由于活性物质的溶解度较低,并且缺乏合适的离子导电膜,短期内还看不到应用前景。半固态流体电池以悬浮的固体物质浆料作为活性材料,具有发展高能量密度流体电池的潜力,但由于浆料的流动性差,有很多工程上的问题需要解决。基于“氧化还原靶向反应”的液流电池体系结合了传统液流电池和半固态流体电池的优点,为发展高能量密度的液流电池提供了一个新途径。这种电池独特的工作原理,使得它可应用于不同电池体系,从而发展出更接近实用的液流电池系统。有望在较短的时间内完成从基础研究到工程展示的转化。

图7 各类液流电池能量密度对比图Fig.7 Summary of the reported tank energy densities of various redox flow batteries
[1]Masmoudi Abdelkarim,Abdelkafi Achraf,Krichen Lotfi.Electric power generation based on variable speed wind turbine under load disturbance[J].Energy,2011,36(8):5016-5026.
[2]Wang Hongyan(王红岩),Li Jingming(李景明),Zhao Qun(赵群),Lin Yingji(林英姬).Resources and development of new energy in China[J].Acta Petrolei Sinica(石油学报),2009,30(3):469-474.
[3]Niknam Taher,Kavousifard Abdollah,Tabatabaei Sajad,Aghaei Jamshid.Optimal operation management of fuel cell/wind/photovoltaic power sources connected to distribution networks[J].Journal of Power Sources,2011,196(20):8881-8896.
[4]Xiao Ying(肖英).On the problems and countermeasures of China’s new energy technology progress[J].Science and Technology Progress and Policy(科技进步与对策),2008,25(2):82-85.
[5]Johnson David A,Reid Margaret A.Chemical and electrochemical behavior of the Cr (III)/Cr (II) half-cell in the iron-chromium redox energy storage system[J].Journal of the Electrochemical Society,1985,132(5):1058-1062.
[6]Dong Quanfeng(董全峰),Zhang Huamin(张华民),Jin Minggang(金明钢),Zheng Mingsen(郑明森),Zhan Yading(詹亚丁),Sun Shigang(孙世刚),Lin Zugeng(林祖赓).Research progresses in a flow redox battery[J].Electrochemistry(电化学),2005,11(3):237-243.
[7]Zhang Huamin(张华民).高效大规模化学储能技术研究开发现状及展望[J].Chinese Journal of Power Sources(电源技术),2007,31(8):587-591.
[8]Thaller Lawrence H.9th Intersociety Energy Conversion Engineering Conference[M].New York:American Society of Mechanical Engineers,1974:924-928.
[9]Zhao Ping,Zhang Huamin,Zhou Hantao,Chen Jian,Gao Sujun,Yi Baolian.Characteristics and performance of 10 kW class all-vanadium redox-flow battery stack[J].Journal of Power Sources,2006,162(2):1416-1420.
[10]Nozaki Ken,Kaneko Hiroko,Negishi Akira,Ozawa Takeo.In Proceedings of the Intersociety Energy Conversion Engineering Conference[M].Las Vegas:Institute of Electrical and Electronics Engineers,1983:1641-1646.
[11]Johnson D A.Department of energy conservation and renewable energy:Division of energy storage systems[R].Washington:National Aeronautics and Space Administration,1982.
[12]Hagedorn Norman H,Thaller Lawrence H.Redox storage systems for solar applications[R].Cleveland:National Aeronautics and Space Administration,Lewis Research Center,1980.
[13]Gahn Randall F,Hagedorn Norman H,Johnson Jerome A.Cycling performance of the iron-chromium redox energy storage system[R].Washington:National Aeronautics and Space Administration,1985.
[14]Chen Jinqing(陈金庆),Wang Qian(汪钱),Wang Baoguo(王保国).Research progress in key materials for all vanadium redox flow battery[J].Modern Chemical Industry(现代化工),2006,26(9):21-24.
[15]Yang Zhenguo,Zhang Jianlu,Kintner-Meyer Michael C W,Lu Xiaochuan,Choi Daiwon,Lemmon John P,Liu Jun.Electrochemical energy storage for green grid[J].Chemical Reviews,2011,111(5):3577-3613.
[16]Skyllas-Kazacos M,Chakrabarti M H,Hajimolana S A,Mjalli F S,Saleem M.Progress in flow battery research and development[J].Journal of the Electrochemical Society,2011,158(8):R55-R79.
[17]Jia Chuankun,Liu Jianguo,Yan Chuanwei.A significantly improved membrane for vanadium redox flow battery[J].Journal of Power Sources,2010,195(13):4380-4383.
[18]Remick Robert J,Ang Peter G P.Electrically rechargeable anionically active reduction-oxidation electrical storage-supply system:US,4485154A[P].1984-11-27.
[19]De Leon C P,Frías-Ferrer A,González-García José,Szánto D A,Walsh Frank C.Redox flow cells for energy conversion[J].Journal of Power Sources,2006,160(1):716-732.
[20]Walsh F C.Electrochemical technology for environmental treatment and clean energy conversion[J].Pure and Applied Chemistry,2001,73(12):1819-1837.
[21]Leung Puiki,Li Xiaohong,De León Carlos Ponce,Berlouis Leonard,Low C T J,Walsh Frank C.Progress in redox flow batteries, remaining challenges and their applications in energy storage[J].RSC Advances,2012,2(27):10125-10156.
[22]Huskinson Brian,Marshak Michael P,Suh Changwon,Er Süleyman,Gerhardt Michael R,Galvin Cooper J,Chen Xudong,Aspuru-Guzik Alán,Gordon Roy G,Aziz Michael J.A metal-free organic-inorganic aqueous flow battery[J].Nature,2014,505(7482):195-198.
[23]Li Bin,Nie Zimin,Vijayakumar M,Li Guosheng,Liu Jun,Sprenkle Vincent,Wang Wei.Ambipolar zinc-polyiodide electrolyte for a high- energy density aqueous redox flow battery[J].Nature Communications,2015,6,doi:10.1038/ncomms7303.
[24]Matsuda Y,Tanaka K,Okada M,Takasu Y,Morita M, Matsumura-Inoue T.A rechargeable redox battery utilizing ruthenium complexes with non-aqueous organic electrolyte[J].Journal of Applied Electrochemistry,1988,18(6):909-914.
[25]Chakrabarti M H,Dryfe R A W,Roberts E P L.Evaluation of electrolytes for redox flow battery applications[J].Electrochimica Acta,2007,52(5):2189-2195.
[26]Liu Qinghua,Shinkle Aaron A,Li Yongdan,Monroe Charles W, Thompson Levi T,Sleightholme Alice E S.Non-aqueous chromium acetylacetonate electrolyte for redox flow batteries[J].Electrochemistry Communications,2010,12(11):1634-1637.
[27]Kim Jae Hun,Kim Ki Jae,Park Min Sik,Lee Nam Jin,Hwang Uk,Kim Hansu,Kim Young Jun.Development of metal-based electrodes for non-aqueous redox flow batteries[J].Electrochemistry Communications,2011,13(9):997-1000.
[28]Sleightholme Alice E S,Shinkle Aaron A,Liu Qinghua,Li Yongdan,Monroe Charles W,Thompson Levi T.Non-aqueous manganese acetylacetonate electrolyte for redox flow batteries[J].Journal of Power Sources,2011,196(13):5742-5745.
[29]Herr T,Noack J,Fischer P,Tübke J.1,3-dioxolane, tetrahydrofuran,acetylacetone and dimethyl sulfoxide as solvents for non-aqueous vanadium acetylacetonate redox-flow-batteries[J].Electrochimica Acta,2013,113:127-133.
[30]Cappillino Patrick J,Pratt Harry D,Hudak Nicholas S,Tomson Neil C,Anderson Travis M,Anstey Mitchell R.Application of redox non-innocent ligands to non-aqueous flow battery electrolytes[J].Advanced Energy Materials,2014,4(1):doi:10.1002/aenm.201300566.
[31]Xing Xueqi,Zhang Dapeng,Li Yongdan.A non-aqueous all-cobalt redox flow battery using 1, 10-phenanthrolinecobalt (II) hexafluoro- phosphate as active species[J].Journal of Power Sources,2015,279:205-209.
[32]Lim H S,Lackner A M,Knechtli R C.Zinc-bromine secondary battery[J].Journal of the Electrochemical Society,1977,124(8):1154-1157.
[33]Tang Chao,Zhou Debi.Methane sulfonic acid solution as supporting electrolyte for zinc-vanadium redox battery[J].Electrochimica Acta,2012,65:179-184.
[34]Leung P K,De León C Ponce,Walsh F C.An undivided zinc-cerium redox flow battery operating at room temperature (295 K)[J].Electrochemistry Communications,2011,13(8):770-773.
[35]Pan Junqing,Ji Lizhong,Sun Yanzhi,Wan Pingyu,Cheng Jie,Yang Yusheng,Fan Maohong.Preliminary study of alkaline single flowing ZnO2battery[J].Electrochemistry Communications,2009,11(11):2191-2194.
[36]Zhao Yu,Wang Lina,Byon Hye Ryung.High-performance rechargeable lithium-iodine batteries using triiodide/iodide redox couples in an aqueous cathode[J].Nature Communications,2013,4: 1896.
[37]Zhao Yu,Byon Hye Ryung.High-performance lithium-iodine flow battery[J].Advanced Energy Materials,2013,3(12):1630-1635.
[38]Wei Xiaoliang,Xu Wu,Vijayakumar Murugesan,Cosimbescu Lelia,Liu Tianbiao,Sprenkle Vincent,Wang Wei.TEMPO-based catholyte for high-energy density nonaqueous redox flow batteries[J].Advanced Materials,2014,26(45):7649-7653.
[39]Zhao Yu,Ding Yu,Song Jie,Li Gang,Dong Guangbin,Goodenough John B,Yu Guihua.Sustainable electrical energy storage through the ferrocene/ferrocenium redox reaction in aprotic electrolyte[J].Angewandte Chemie International Edition,2014,53(41):11036-11040.
[40]Wei Xiaoliang,Cosimbescu Lelia,Xu Wu,Hu Jianzhi,Vijayakumar M,Feng Ju,Hu Mary Y,Deng Xuchu,Xiao Jie,Liu Jun,Sprenkle Vincent,Wang Wei.Towards high-performance nonaqueous redox flow electrolyte via ionic modification of active species[J].Advanced Energy Materials,2015,5(1):doi:10.1002/aenm.201400678.
[41]Takechi Kensuke,Kato Yuichi,Hase Yoko.A highly concentrated catholyte based on a solvate ionic liquid for rechargeable flow batteries[J].Advanced Materials,2015,27(15):2501-2506.
[42]Wang Yarong,Wang Yonggang,Zhou Haoshen.A Li-liquid cathode battery based on a hybrid electrolyte[J].Chem.Sus.Chem.,2011,4(8):1087-1090.
[43]Lu Yuhao,Goodenough John B.Rechargeable alkali-ion cathode-flow battery[J].Journal of Materials Chemistry,2011,21(27):10113-10117.
[44]Zhao Yu,Ding Yu,Song Jie,Peng Lele,Goodenough John B,Yu Guihua.A reversible Br2/Br-redox couple in the aqueous phase as a high-performance catholyte for alkali-ion batteries[J].Energy & Environmental Science,2014,7(6):1990-1995.
[45]Manthiram Arumugam,Fu Yongzhu,Su Yusheng.Challenges and prospects of lithium-sulfur batteries[J].Accounts of Chemical Research,2012,46(5):1125-1134.
[46]Chiang Yet Ming,Carter William Craig,Duduta Mihai,Limthongkul Pimpa.High energy density redox flow device:US,12/970 773[P].2014-05-13.
[47]Chen Hongning,Zou Qingli,Liang Zhuojian,Liu Hao,Li Quan,Lu Yichun.Sulphur-impregnated flow cathode to enable high-energy- density lithium flow batteries[J].Nature Communications,2015,6:doi:10.1038/ncomms6877.
[48]Wang Qing,Zakeeruddin Shaik M,Wang Deyu,Exnar Ivan,Grätzel Michael.Redox targeting of insulating electrode materials:A new approach to high-energy-density batteries[J].Angewandte Chemie International Edition,2006,45(48):8197-8200.
[49]Huang Qizhao,Li Hong,Grätzel Michael,Wang Qing.Reversible chemical delithiation/lithiation of LiFePO4:Towards a redox flow lithium-ion battery[J].Physical Chemistry Chemical Physics,2013,15(6):1793-1797.
[50]Pan Feng,Yang Jing,Huang Qizhao,Wang Xingzhu,Huang Hui,Wang Qing.Redox targeting of anatase TiO2for redox flow lithium-ion batteries[J].Advanced Energy Materials,2014,4(15):doi:10.1002/aenm.201400567.
[51]Huang Qizhao,Wang Qing.Next-generation, high-energy-density redox flow batteries[J].Chem.Plus.Chem.,2015,80(2):312-322.
[52]Zhu Yunguang,Jia Chuankun,Yang Jing,Pan Feng,Huang Qizhao,Wang Qing.Dual redox catalysts for oxygen reduction and evolution reactions:Towards a redox flow LiO2battery[J].Chemical Communications,2015,51(46):9451-9454.
