定量结构—保留相关关系辅助气相色谱—质谱法和气相色谱红外光谱法定性分析香精中的醛酮酯类化合物
2015-11-03黄翼飞等
黄翼飞等


摘 要 构建了简单的醛酮酯类化合物定量结构-保留相关关系(Quantitative structure-retention relationship, QSRR),结合气相色谱-质谱/气相色谱-红外光谱(GC-MS/GC-IR)方法建立快速、准确的香精样品中醛酮酯类化合物定性分析方法。以醛酮酯标样保留时间tR为因变量,分子拓扑指数0Q为自变量进行多元线性回归拟合(MLR)得到tR=0Q×A+B的QSRR模型;混合标样预测集得到QSRR模型为tR=0.9090 0Q-5.279(醛酮)和tR=0.82360Q-7.422(酯),相关系数R2=0.997,测试集化合物预测值与实验值的相对误差小于5%;结合GC-MS/GC-IR分析方法检测和谱库检索化合物类别,快速准确定性分析香精样品中醛酮酯类化合物,为复杂基体中醛酮酯类同系物和同分异构体分析提供了快速、准确的定性方法。
关键词 定量结构-保留相关关系; 香精; 醛; 酮; 酯; 气相色谱-质谱; 气相色谱-红外光谱
1 引 言
气相色谱-质谱联用(GC-MS)技术结合了GC高效分离和MS定性专属性强的优势,具有灵敏度高、分析速度快和鉴别能力强的特点,可同时完成待测组分的分离鉴定,适用于混合物中未知组分的定性和定量分析,在食品[1]、环境[2]、医药[3]、化工[4]等领域中应用广泛。但气相色谱的色谱柱容量有限,同系物或异构体化合物的色谱保留时间相近或一致[5]。虽然GC-MS配置的NIST数据库中已包含超过20万张化合物的EI质谱图谱,但在含有较多同系物和同分异构体的复杂样品分析中,有些化合物在EI(与GC常联用的离子化方式)电离方式下不产生分子离子峰;利用谱库检索一般只能给出某个成分的可能匹配物质,一些结构异构体的EI质谱图较为相似,仅仅依靠GC-MS得到的结果对化合物进行定性并不十分充分,需要通过其它电离技术获得分子量信息,或采用多级质谱(MSn)技术获得结构信息。研究者常通过与其它定性方法联用、建立指纹图谱[6]或化学计量学[7]的手段来弥补NIST数据库在同系物和异构体鉴定分析中的不足。气相色谱-红外光谱(GC-IR)联用技术结合了GC良好的分离能力和IR结构鉴定的优势,适合复杂未知物成分分离及其定性定量分析。另一方面,定量结构保留相关关系(QSRR)是直接利用分子结构信息关联和预测有机物的色谱保留时间[8]。多元线性回归模型是QSRR中应用广泛的一种经典建模方法,它对自变量和因变量加以线性拟合得到最小二乘意义下的最佳结果,在环境、食品、化工等领域未知化合物的分离分析中得到广泛应用[9~15]。
香精香料是食品香味的主要来源之一,它们使制造食品的香味能够与传统手工制作的食品相媲美。香精香料已经广泛应用到食品生产的各个领域,它能改善食品质量、降低生产成本、增加食品的色香味,大大提高了人民的生活质量和品味,同时促进了食品工业的快速发展[16]。醛酮酯类化合物是重要的工业原料、药物原料、合成中间体,也是合成香精香料的重要组成之一[17]。目前,醛酮酯类化合物的QSRR方面的相关研究已多有报道[18~24]。
本研究采用QSRR辅助GC-MS/IR方法快速定性分析饱和醛酮酯同系物及其同分异构体。以醛酮酯标样保留时间tR为因变量,分子拓扑指数0Q为自变量,构建简单醛酮酯类化合物定量结构-保留相关关系(QSRR),采用本方法辅助GC-MS/IR方法建立快速、准确的香精样品中醛酮酯类化合物定性分析方法。
2 实验部分
2.1 仪器与试剂
GC 6890N气相色谱(美国Agilent公司);IR 6170红外光谱联用仪(美国Thermo Fisher Scientific公司),另配有FID检测器;6890/5790气相色谱-质谱联用仪(GC-MS,美国Agilent公司)。
2-戊酮、3-戊酮、2-己酮、4-庚酮、5-甲基-2-己酮、3-辛酮、正己醛、1-辛醛、丙酸乙酯、丁酸甲酯、丁酸乙酯、乙酸异戊酯、丁酸丙酯、丁酸丁酯、丁酸异戊酯、丁酸正戊酯、异戊酸异戊酯、丁酸己酯、乙酸戊酯、己酸乙酯、癸酸乙酯、十二酸乙酯、十四酸乙酯、十五酸乙酯、棕榈酸甲酯、三醋酸甘油酯(纯度≥99.5%,阿拉丁试剂公司);正己烷(色谱纯,百灵威公司(上海))。香精等样品由某企业提供。
各标准品以正己烷为溶剂,配制成1000 mg/L储备液备用;单标使用液和混标使用液根据需要由储备液用正己烷稀释而成。
2.2 分析条件
2.2.1 GC-MS条件
色谱柱: Agilent HP-VOC(60 m × 0.32 mm × 1.80 μm); 进样口温度: 260℃; 质谱接口温度270℃,离子源温度230℃,电离方式为 EI,电子轰击能量 70 eV;载气为高纯He,柱流速1.0 mL/min;进样量1 μL,分流进样,分流比为25∶1;程序升温:以5℃/min的速率从70℃升至270℃。
2.2.2 GC-IR/FID条件 Agilent HP-VOC色谱柱 (60 m × 0.32mm × 1.80 μm);进样口温度: 260℃,FID检测器温度:250℃;载气为高纯He,柱流速1.0 mL/min;进样量1 μL,分流进样,分流比为5:1;程序升温:以5℃/min的速率从70℃升至270℃;红外光谱分辨率:16 cm1,扫描次数:8次;GC-IR接口传输线温度:270℃,光管温度:270℃。
2.3 样品处理
在0.2 mL香精样品中加入0.5 mL 正己烷,振荡2 min后,用1 mL 注射器吸取上清液,重复3次,得到1 mL萃取液,备用。
2.4 分子拓扑指数0Q
3 结果与讨论
3.1 GC-MS和GC-FID/IR中醛酮酯化合物的保留时间
结合GC-IR可对未知物进行官能团鉴定的特点,辅助GC-MS定性分析复杂样品中的醛酮酯类化合物。本研究首先考察了醛酮酯类化合物在不同方法中的色谱保留时间(表1)。结果表明,采用同一方法和同型色谱柱,由于GC-IR接口构造特殊,馏出物在气红接口中滞留时间较长,导致醛酮酯化合物在GC-MS和GC-IR/FID中保留时间不同,但色谱保留时间顺序基本一致,相应化合物的保留时间差值近似为常数,这为GC-IR辅助GC-MS用于复杂样品中未知物的分析鉴定奠定了基础。
3.2 QSRR模型建立
将17种饱和酯类化合物分为两类,其中7种乙酯类同系物(丙酸乙酯、丁酸乙酯、己酸乙酯、癸酸乙酯、十二酸乙酯、十四酸乙酯、十五酸乙酯)作为训练集,推测对应关系式;剩余的不同取代基的其它酯类化合物作为预测集,用于检验方法准确性。饱和酯类化合物的Q值、在GC-MS方法中保留时间实验值见表2。由表2可知,乙酯类同系物的色谱保留时间与其分子结构参数Q值间存在良好的线性关系,相关系数为0.997。由于这些乙酯类同系物都是直链羧酸基乙酯,在GC中存在良好的碳数规律。因此,本对应关系式与同系物碳数规律结果一致。此对应关系式对其它酯类化合物的保留时间预测值也列于表2。
由于作为预测集的酯类化合物与训练集的乙酯类化合物的结构存在较大差异,单独采用保留时间碳数规律无法得到良好的预测。但经过分子拓扑结构处理后的结果表明,酯类化合物的保留时间与其对应的Q值能很好地符合此线性关系,预测值与实验值的偏差不超过5%。
对于醛酮类化合物,以2-戊酮、3-戊酮、2-己酮、4-庚酮及5-甲基-2-己酮作为训练集,将醛酮化合物在不同方法上的色谱保留时间(tR)与相应化合物的0Q进行多元线性回归分析。结果表明,tR与0Q具有良好的相关性,其相关系数R2=0.997。其中醛酮化合物在GC-MS方法中色谱保留时间(tR)与0Q的拟合方程为:
tR=0.9090Q-8.141(4)
以4-庚酮、3-辛酮、1-辛醛和4-壬酮为测试集,用公式(4)对测试集在GC-IR方法中的色谱保留时间进行预测,所得预测值及其与实验值的相对偏差见表3。结果表明,测试集化合物的预测值与实验值的相对偏差小于3.4%,表明模型预测能力较强。
3.3 QSRR辅助GC-MS/IR方法在复杂样品醛酮酯类化合物鉴定中的应用
3.3.1 香精样品1#分析 采用GC-MS分析香精样品1#的正己烷萃取液(图1A)。通过NIST质谱图谱库搜索,其中9、16、19和24号峰可能为醛酮类化合物,相应化合物及其匹配度见表4。
由图1A可见,3号和16号谱峰的匹配度并不高,而24号谱峰不仅质谱匹配度低,而且给出了相似匹配度的不同化合物。本研究进一步采用GC-IR分析该样品(图1B),结合IR谱库鉴定结果,可以基本确定谱峰9和19为醛酮类化合物,峰3为酯类化合物,但具体结构无法确定。
为了准确确定这些醛酮酯类化合物的同系物结构,采用QSRR模型进一步处理。表5给出了6~14个碳直链饱和醛的0Q值及其根据已知模型中拟合公式得到的色谱保留时间预测值。
为壬醛。而24号峰(十三醛和十四醛)相应的色谱保留时间预测值与实验值相对误差相当大,初步判断MS谱库推荐的两个可能结果均不正确。根据保留时间预测值与实际色谱保留时间判断,24号谱峰应为十一醛。通过标准样品对预测结果进行核实, 3号峰为丁酸乙酯;16号峰为壬醛;24号峰为十一醛,证明采用QSRR结合GC-MS/IR能准
确判断未知化合物的结构。
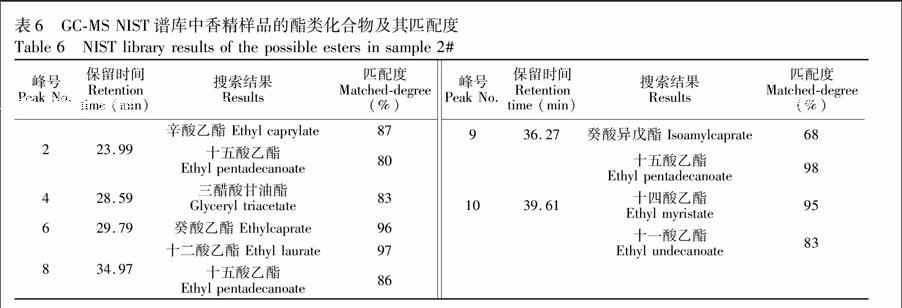
3.3.2 香精样品2#分析 香精样品2#经正己烷处理后的GC-MS分析结果见图2,通过NIST质谱谱库搜索给出的相应化合物及其匹配度见表6。
结果表明,虽然GC-MS NIST谱库和GC-IR都显示香精样品2#中含有多个酯类化合物,但GC-MS对多个酯类化合物的同系物给出了匹配度相近的可能结果,单独通过GC-MS或通过GC-IR辅助MS难以准确简单酯类化合物同系物的结构。为此,本研究通过NIST推荐的化合物的0Q值并结合QSRR已建立的模型进行预测。结果表明,辛酸乙酯、十二酸乙酯、癸酸异戊酯和十五酸乙酯的预测保留时间与实验中2, 8, 9和10号峰的保留时间吻合度较好,进一步采用相应标准样品进行对比,最终确定预测结果与实际结果一致。
4 结 论
根据分子拓扑指数0Q和色谱保留时间关系,建立了醛酮酯类化合物的QSRR模型tR=0QA+B,该模型因变量、自变量具有较好的线性相关性,预测能力良好。采用GC-MS、GC-IR对香精样品分离分析并进行初步定性,利用所建立的tR-0Q模型对初步定性结果辅助定性确定准确的定性结果,确立了快速、准确判定香精香气等复杂样品中未知化合物结构的分析方法。本方法中气相色谱采用的色谱柱均为HP-VOC柱,在其它色谱柱体系,本方法并不适用。另外,本方法的tR-0Q模型对脂肪族饱和醛酮酯类化合物的能够准确定性,但对苯系物或不饱和化合物的定性误差较大。
References
1 Pacioni G, Cerretani L, Procida G, Cichelli A. Food Chem., 2014, 146: 30-35
2 Bonansea R I, Amé MV, Wunderlin D A. Chemosphere, 2013, 90(6): 1860-1869
3 Emond P, Mavel S, Adoud N, Nadal-Desbarats L, Montigny F, Bonnet-Brilhault F, Barthélémy C, Merten M, Sarda P, Laumonnier F, Vourc H P, Blasco H, Andres C R. Anal. Bioanal. Chem., 2013, 405(15): 5291-5300
4 Zhang M, Resende F L P, Moutsoglou A. Fuel, 2014, 116: 358-369
5 HUANG Jian. Identification of 7 Kinds of BTEX in Industrial Additives by Headspace Gas Chromatography-Mass Spectrometry, Jilin University Master′s Thesis, 2014
黄 鉴. 工业助剂中7种苯系物的顶空气相色谱-质谱定性分析, 吉林大学硕士论文, 2014
6 HUANG Ying-Feng. Study on the Analysis of Flavor and Flavor Material for Tobacco, Zhejiang University Master′s Thesis, 2007
黄映凤. 烟用香精香料的分析研究, 浙江大学硕士论文, 2007
7 He M, Yan J, Cao D, Liu S, Zhao C, Liang Y, Li Y, Zhang Z. Talanta, 2013, 103: 116-122
8 QUAN Mei-Ping. Chinese Journal of Spectroscopy Laboratory, 2013, 30(5): 2288-2293
权美平. 光谱实验室, 2013, 30(5): 2288-2293
9 Kaliszan R. Chem. Rev., 2007, 107(7): 3212-3246
10 Héberger K. J. Chromatogr. A, 2007, 1158(1-2): 273-305
11 Ebrahimi-Najafabadi H, Mcginitie T M, Harynuk J J. J. Chromatogr. A, 2014, 1358: 225-231
12 Dashtbozorgi Z, Golmohammadi H, Konoz E. Microchem. J., 2013, 106: 51-60
13 Yan J, Cao D, Guo F, Zhang L, He M, Huang J, Xu Q, Liang Y. J. Chromatogr. A, 2012, 1223: 118-125
14 Ghavami R, Sepehri B. J. Chromatogr. A, 2012, 1233: 116-125
15 Qin L, Liu S, Chen F, Xiao Q, Wu Q. Chemosphere, 2013, 90(2): 300-305
16 CAI Pei-Dian, BAI Wei-Dong, QIAN Min. China Condiment, 2010, (2): 35-38
蔡培钿, 白卫东, 钱 敏. 中国调味品, 2010, (2): 35-38
17 LIU Mei-Sen, HE Wei-Ping. China Food Additives, 2003, (5): 6-10
刘梅森, 何唯平. 中国食品添加剂, 2003, (5): 6-10
18 Souza S, Kuhnen C A, Junkes B D S, Yunes R A, Heinzen V E F. J. Chemometr., 2009, 23(5): 229-235
19 Gupta V K, Khani H, Ahmadi-Roudi B, Mirakhorli S, Fereyduni E, Agarwal S. Talanta, 2011, 83(3): 1014-1022
20 Souza S,Kuhnen C A, Junkes B D S, Yunes R A, Heinzen V E F. J. Mol. Graph. Model., 2009, 28(1): 20-27
21 ZHOU Cong-Yi, NIE Chang-Ming, TIAN Wan-Fu, DAI Yi-Min, PENG Guo-Wen. J. Instrum. Anal., 2007, (6): 802-807
周丛艺, 聂长明, 田万福, 戴益民, 彭国文. 分析测试学报, 2007, (6): 802-807
22 LIU Feng-Ping, LIANG Yi-Zeng, CAO Chen-Zhong. Chinese J. Anal. Chem, 2007, 35(2): 227-232
刘凤萍, 梁逸曾, 曹晨忠. 分析化学, 2007, 35(2): 227-232
23 DU Xi-Hua, GU Ju-Guan. Chinese J. Anal. Chem., 2005, 33(4): 553-556
堵锡华, 顾菊观. 分析化学, 2005, 33(4): 553-556
24 Junkes B D S, Amboni R D D M, Yunes R A, Heinzen V E F. J. Brazil. Chem. Soc., 2004, 15(2): 183-189
25 DU Xi-Hua. Chemistry, 2001, 8: 508-512
堵锡华. 化学通报, 2001, 8: 508-512
