石榴花多糖醇提工艺的响应曲面法优化及其抗氧化活性研究
2015-10-24柯春林李作美路滨宇钱时权蚌埠学院生物与食品工程系安徽蚌埠33030复旦大学药学院上海003
柯春林,李作美,路滨宇,钱时权,张 斌,袁 静(.蚌埠学院生物与食品工程系,安徽蚌埠33030;.复旦大学药学院,上海003)
石榴花多糖醇提工艺的响应曲面法优化及其抗氧化活性研究
柯春林1,李作美1,路滨宇2,钱时权1,张 斌1,袁 静1
(1.蚌埠学院生物与食品工程系,安徽蚌埠233030;2.复旦大学药学院,上海201203)
以石榴花为原料,用热水浸提法提取其多糖。在单因素实验的基础上,运用Box-Behnken实验设计,采用响应曲面法对石榴花多糖的醇提条件进行优化。结果表明最佳工艺为:提取时间4h,温度76℃,料液比1∶52,在此基础上进行验证实验,实测多糖得率为6.35%。同时,不同的体外抗氧化实验结果表明石榴花多糖具有适度的还原力,较强的清除亚硝酸盐(NO2-)和超氧自由基(O2-)的清除效果,较好的螯合金属离子能力,而且石榴花多糖的抗氧化活性随着多糖浓度的提高而增强。
石榴花,多糖,响应曲面,提取优化,抗氧化活性
石榴为石榴科石榴属植物,在我国己有2000多年的栽培历史。据不完全资料统计,我国石榴栽培面积达11万余公顷,居世界第1位。石榴全身是宝,它的各个部分都含有丰富的活性物质,表现出很强的生物活性,然而对石榴活性物质的研究和开发多集中于石榴叶、石榴皮和石榴籽,对石榴花的研究报道较少[1-3]。石榴花红色花朵居多,也有玛瑙、粉红、黄色和白色等,具有良好的观赏价值和文化价值,同时石榴花营养丰富,具有较高的药用价值,渐渐成为人们研究该植物的热点[4]。石榴花为中药和维吾尔常用药,性平、涩,作为中药可用于治疗中耳炎、鼻衄、创伤出血。在维吾尔族医学中素以“古丽娜”之称而入药,用于退翳,治神经衰弱和恶心[5]。已有的研究内容表明石榴花具有多种化学成分,如多酚类、黄酮类、三萜类、糖类、皂苷、花青素等多种化合物[6-8]。石榴花具有抗氧化活性、降血脂和降血糖作用[8-11]。据报道,石榴花中有多糖成分[12]。但目前很少有关于石榴花多糖制备技术的报道,也没有关于其生物活性研究的报道。基于以上研究背景,本研究探索了石榴花多糖醇提工艺及其抗氧化活性,以期为石榴花的资源开发提供理论依据。
1 材料与方法
1.1 材料与仪器
石榴花(红玛瑙籽,红花) 安徽怀远;菲洛嗪美国Sigma公司;葡萄糖、对氨基苯磺酸、盐酸萘乙二胺、三羟甲基氨基甲烷(Tris)、邻苯三酚 国药集团化学试剂有限公司;无水乙醇、苯酚、浓硫酸、磷酸氢二钠、磷酸二氢钠、柠檬酸、铁氰化钾、三氯化铁、三氯乙酸、浓盐酸、氯化亚铁、亚硝酸钠等 均为分析纯。
WFZUV-2000型紫外-可见光分光光度计 上海尤尼柯仪器有限公司;SHB-Ⅲ型循环水式多用真空泵 郑州长城仪器有限公司;RE-51AA型旋转蒸发仪 上海亚荣生化仪器厂;BL-220H型分析天平 日本Shimadzu公司;FW 100型粉碎机 天津市泰斯特仪器有限公司;800B型低速离心机 上海安亭科学仪器厂;DZF-6030A型真空干燥箱 上海齐欣科学仪器有限公司;PHB-4型酸度计 上海雷磁仪器厂;HH-4型恒温水浴锅 江苏国华电器有限公司等。
1.2 实验方法
1.2.1 石榴花多糖提取工艺 工艺流程:石榴花→干燥→粉碎、过60目筛→乙醇索氏提取回流至无色→残渣晾干→水浴浸提4h→减压过滤→Sevage法脱蛋白→剧烈振荡→静置分离→浓缩至15mL左右→乙醇沉淀→减压过滤→丙酮溶剂洗涤3次→低温干燥→石榴花多糖备用[13]。
1.2.2 多糖的测定 采用苯酚-硫酸法测定样品中石榴花多糖的含量[14],多糖得率(%)=[粗多糖质量(g)/原料质量(g)]×100。
1.2.3 单因素实验 石榴花多糖为水溶性多糖,易溶与水,本实验主要考察提取时间、提取温度和料液比对石榴花多糖得率的影响。初始条件为:料液比1∶60(g/m L)、提取温度60℃、浸提时间2h、提取次数1次、pH7.0和醇沉浓度70%。取5份3g干燥后的石榴花粉末,保持初始条件的其他条件不变:设置提取时间1、2、3、4、5h,提取温度45、55、65、75、85℃,料液比为1∶30、1∶40、1∶50、1∶60和1∶70进行单因素实验。
1.2.4 响应曲面实验 在单因素实验的基础上,确定影响石榴花多糖提取效果的主要因素。以各因素为自变量,运用Design Expert 7.1.3软件进行Box-Behnken设计,采用响应面法并以石榴花多糖得率为响应值(因变量Y),对料液比(A)、提取时间(B)和提取温度(C)的3因素3水平进行提取条件优化,设计方案见表1。

表1 实验因素与水平设计Table 1 Factors and levels in response surface analysis design
1.2.5 抗氧化实验
1.2.5.1 还原力的测定 参照文献[15]的方法,取不同浓度样品溶液1.0m L于试管中,分别加入1.0m L磷酸盐缓冲液和1.0m L K3(Fe(CN)6)溶液,混匀,在50℃水浴中加热20min,取出后迅速冷却,加入1.0m L三氯乙酸混匀后,再加入0.2m L FeCl3溶液,混匀,10m in后测定700nm吸光值,3次重复。以水代替FeCl3溶液作空白对照。以吸光值(A1-A2)表示样品还原力,A1—表示样品管吸光值,A2—表示样品空白管吸光值。
1.2.5.2 对亚硝酸盐(NO2·-)的清除作用 参照文献[16]的方法,分别吸取不同浓度的样品液3m L于25m L容量瓶,加入5μg/m L的亚硝酸钠2m L。柠檬酸-柠檬酸盐缓冲液5m L,37℃水浴中反应15min后,立即加入0.4%对氨基苯磺酸溶液2m L,混匀静置5m in,加入0.2%盐酸萘乙二胺溶液1m L,用蒸馏水定容至25m L。15m in以后,然后以空白试剂作对照测定吸样的品光度A538nm,重复做3次实验,取平均值。空白组:以蒸馏水代替样品。按下式计算清除率:NO2-清除率=(A1-A2)/A1×100。A1—未加样品时吸光值;A2—加样品后吸光值。
1.2.5.3 对超氧自由基(O2-·)的清除作用 采用邻苯三酚自氧化法[17],取0.05mol/L pH为8.2的Tris-HCl缓冲液6m L加入盛有2.2m L蒸馏水的试管中。置于25℃水浴中预热20m in。分别精确吸取不同浓度的多糖溶液0.5m L。即加入在25℃水浴中预热过的邻苯三酚1m L,立即混匀。在25℃水浴中准确反应4m in后,加入8mol/L的HCl溶液0.1m L终止反应。然后以空白作对照测定样品在325nm处的吸光度,做3次平行实验,取平均值。按下式计算清除率:O2-·清除率=(A1-A2)/A1× 100。其中:A1—空白管吸光值;A2—样品管吸光值。
1.2.5.4 螯合金属离子能力 根据文献[18]的方法稍作改进,取不同浓度样品溶液1.0m L于试管中,分别加入0.05m L FeCl2溶液、0.2m L菲洛嗪溶液、2.75m L水,混匀,10m in后测吸光度A562nm,重复3次,取平均值。以水代替FeCl2溶液做空白对照。螯合率(%)=[A0-(A1-A2)]/A0×100其中:A0—水代替样液时的吸光值;A1—样品管吸光值;A2—样品空白管吸光值。
2 结果与分析
2.1 单因素实验
由图1(a)可知在1~4h时随着时间的延长,多糖得率增加的幅度较大,4h后多糖得率增加不明显,这时多糖在固-液之间的浓度基本达到了平衡;如图1(b)所示,在45~75℃时随着温度的提高多糖得率逐渐升高,75℃时达到峰值;75℃时以后,温度继续增加,多糖得率反而下降,可能的原因是多糖在温度过高时会降解;从图1(c)可以看出,在料液比1∶30~1∶50时随着提取溶剂的增加,多糖得率上升,继续增加提取溶剂,料液比超过1∶50后提取效果有降低的趋势,可能此浓度下,石榴花和热水组成的溶液体系中,溶质饱和,多糖已基本溶解,石榴花多糖不能充分溶解析出,而且提取溶剂过多的情况下不利于后续的浓缩纯化过程。所以本实验选取3个主要影响因素提取时间、提取温度和料液比,对应的水平分别为:3、4、5h;65、75、85℃;1∶40、1∶50和1∶60。
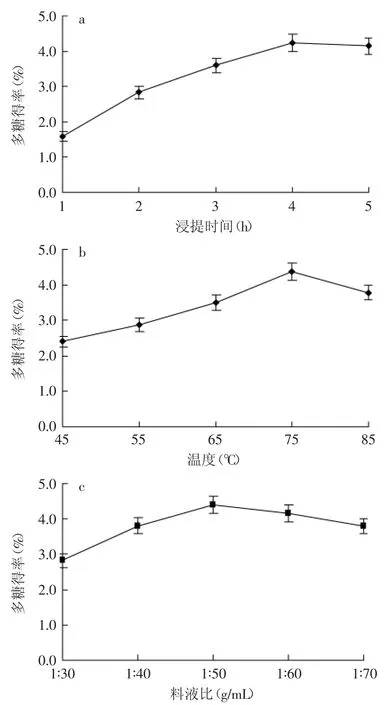
图1 浸提时间(a)、温度(b)和料液比(c)对多糖得率的影响Fig.1 Effect of extraction time,temperature and solvent/ material ratio on polysaccharides yields
2.2 响应曲面实验
2.2.1 Box-Behnken实验结果 以多糖得率为响应值,响应面实验结果见表2,方差分析结果表明(表3):模型极显著(p<0.0001),失拟项不显著(p=0.0552>0.05)。模型的校正系数R2adj=0.9899,说明该模型可以解释98.99%的响应值的变化,相关系数为R2=0.9956,表明该模型与实际拟合非常好,实验误差小。其中提取时间以及料液比对响应值具有极显著的影响(p<0.0001),提取温度对响应值的影响不显著(p>0.05)。时间和温度、时间和料液比间的交互作用对响应值影响极显著(p<0.0001),温度和料液比之间的交互影响对响应值极显著(p<0.01)。将所得实验数据进行多元回归拟合,得到各因素对石榴花多糖得率Y的回归方程:

2.2.2 响应曲面分析 根据拟合函数,固定一个因素在“0”水平处理,分析另外2个因素对多糖得率的影响,做响应面分析,得到各因子交互作用响应面图(图2)。由图2(a)、图2(b)和图2(c)可知,它们的等高线图为椭圆形,而且曲率半径较大,表示交互作用很明显。所以提取时间和料液比、提取温度和料液比、提取温度和时间对石榴花多糖得率的交互作用极显著。

表2 Box-Behnken Design实验设计与实验响应结果Table 2 Box-Behnken designmatrix and the response values for the yield of polysaccharides
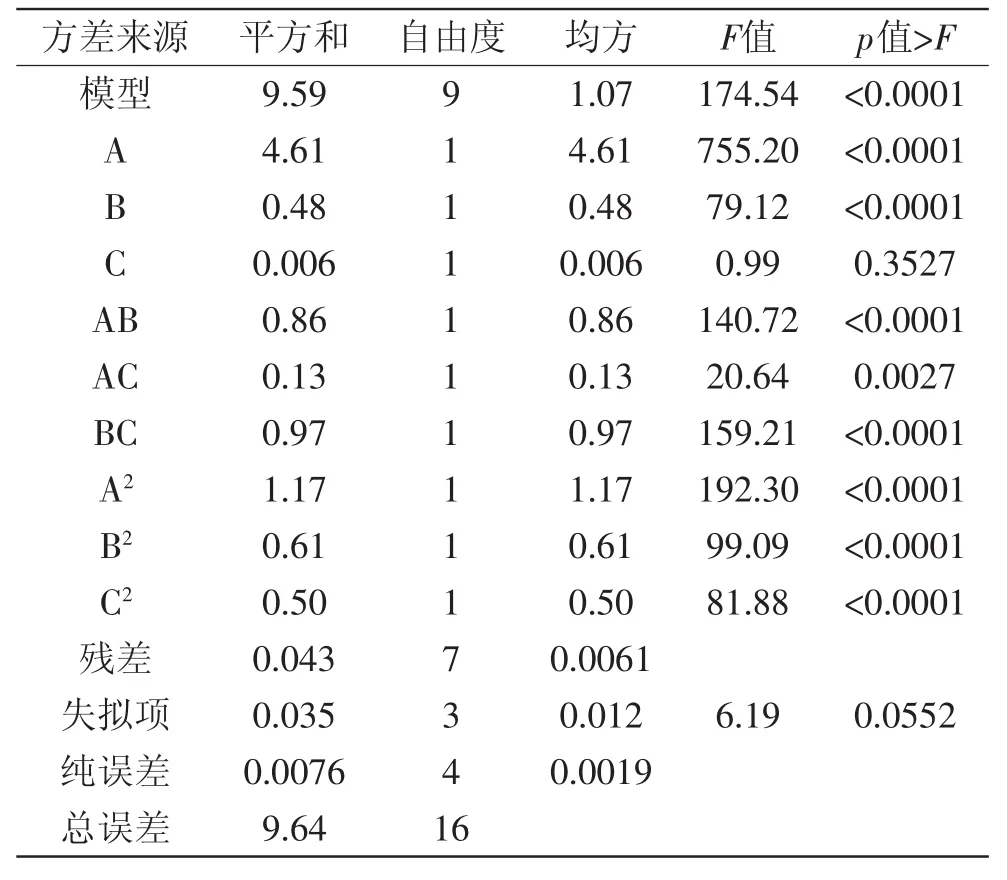
表3 回归模型方差分析结果Table 3 Analysis of variance for the response surface quadraticmodel
2.2.2 验证实验 根据响应曲面实验结果并结合实际得出最佳提取工艺:料液比(1∶52)、温度(76℃)、时间(4h)和乙醇浓度(70%),理论计算多糖得率为6.35%。在此基础上进行验证实验,共计3次,实测多糖得率为6.35%,虽然低于11号实验组的6.496%,但节约了1h,料液比下降了8个点,明显降低了成本。即在确定的优化工艺条件下,能够获得较大石榴花多糖得率。
2.3 抗氧化实验结果
2.3.1 还原力 多糖还原力是其潜在抗氧化能力的一个重要衡量指标[19]。由图3看出,当石榴花多糖的浓度在0.052~0.260mg/m L范围内时,随着多糖浓度的增加,多糖溶液总还原力也在明显增强,也即在此浓度范围内,多糖能将反应溶液中的Fe3+还原为Fe2+,表明石榴花多糖具有较好的还原能力。

图2 浸提时间和料液比(a)、浸提温度和料液比(b)、浸提温度和时间(c)对多糖得率的影响Fig.2 Effects of time and solvent/material ratio(a),temperature and solvent/material ratio(b),temperature and time(c)on polysaccharides yield
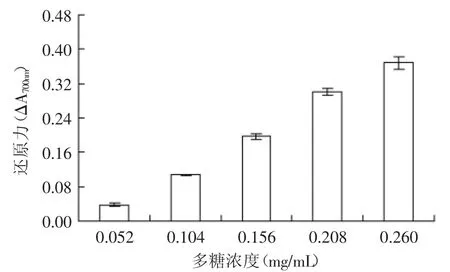
图3 石榴花多糖的还原力Fig.3 The reductive potential by polysaccharides from pomegranate flowers
2.3.2 对亚硝酸盐(NO2-)的清除能力 图4为石榴花多糖清除亚硝酸盐的情况。在0.009~0.044mg/m L浓度范围内,石榴花多糖清除亚硝酸盐的活性具有剂量依赖关系。尤其在0.009~0.017mg/m L随着样品浓度的增大,多糖对亚硝酸盐的清除能力快速增长。在0.044mg/m L浓度时,多糖对亚硝酸盐的清除率达到49.1%。本结果说明石榴花多糖具有明显的清除亚硝酸盐的能力。
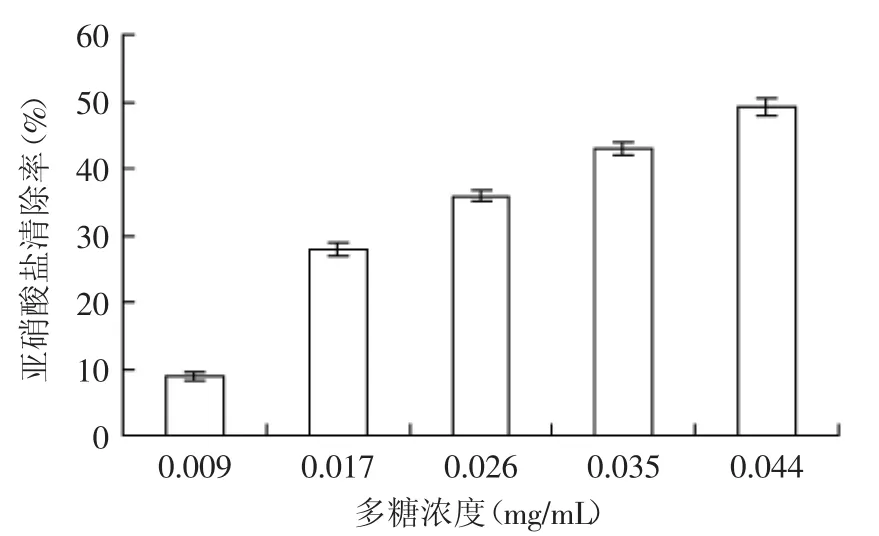
图4 石榴花多糖对亚硝酸盐的清除能力Fig.4 The nitrite scavenging effectby polysaccharides from pomegranate flowers
2.3.3 对超氧自由基(O2-·)的清除效果 由图5可知,在0.022~0.067mg/m L范围内,石榴花多糖对O2-·清除作用显著提高,但是当石榴花多糖的浓度在0.067~0.112mg/m L范围内时,多糖对O2-·清除活性只是缓慢增长。在石榴花多糖的浓度达到0.112mg/m L时石榴花多糖对超氧自由基(O2-·)的清除率达到53.08%。由此可见石榴花多糖对O2-·具有一定的清除作用。
2.3.4 螯合金属离子的能力 螯合金属离子的能力是抗氧化活性的一种表现[18]。如图6可知,随着多糖浓度的增加,石榴花多糖对金属离子的螯合率逐渐加强,在0.055~0.109mg/m L随着样品浓度的增大,多糖螯合率显著增加,显示出较好的螯合亚铁离子能力。样品浓度在0.164~0.273mg/m L之间,螯合率逐渐增长。
3 结论
采用响应面分析法优化石榴花多糖的醇提条件,结果表明最佳提取工艺为:时间4h,温度76℃,料液比1∶52。在此基础上进行验证实验,实测多糖得率为6.35%。通过不同的体外抗氧化实验方法测定石榴花提取液中多糖的抗氧化性活性,结果显示石榴花多糖具有适度的还原力,较强的清除亚硝酸盐(NO2-)和超氧自由基(O2-·)的清除效果,较好的螯合金属离子能力,而且石榴花多糖的抗氧化活性随着多糖浓度的提高而增强。
Study on optimization of extraction conditions for polysaccharide from pomegranate flowers and its antioxidant activities
KE Chun-lin1,LIZuo-mei1,LU Bin-yu2,QIAN Shi-quan1,ZHANG Bin1,YUAN Jing1
(1.Department of Biotechnology and Food Engineering,Bengbu College,Bengbu 233030,China;2.School of Pharmacy,Fudan University,Shanghai201203,China)
Pomegranate flowers as row material were used for extraction polysaccharide with hot water. On thebasis of single factor experiments,the optimized extraction conditions for polysaccharides were determined byusing response surface methodology through the Box -Behnken design. The optional conditions were as follows:extraction time 4 hours,temperature 76℃,ratio of raw material to solvent 1∶52. Under the conditions,the yield of6.35% was obtained by the verification experiment. And the polysaccharides from pomegranate flowersshowed moderate reducing power,strong clearance rate of nitrite(NO2-)and super oxygen free rad ical(O2-)and the ability to chelate metal ions,and the antioxidant activity of polysaccharides increased with the improvement of the polysaccharide concentration.
pomegranate flowers;polysaccharides;response surface analysis;extraction optimization;antioxidant activity
TS281.1
B
1002-0306(2015)08-0286-05
10.13386/j.issn1002-0306.2015.08.051
2014-04-14
柯春林(1976-),男,博士,副教授,主要从事糖生物学和糖生物工程方面的研究。
安徽省自然科学基金项目(1408085MH209);安徽省高等学校省级自然科学基金项目(KJ2012B094);安徽省大学创业训练计划项目(AH20141305065)。
