臭氧多脱过程中残留臭氧的分解试验研究
2015-10-24林法伟朱燕群徐超群马强王智化周俊虎岑可法
林法伟,朱燕群,徐超群,马强,王智化,周俊虎,岑可法
(浙江大学能源清洁利用国家重点实验室,浙江杭州310027)
臭氧多脱过程中残留臭氧的分解试验研究
林法伟,朱燕群,徐超群,马强,王智化,周俊虎,岑可法
(浙江大学能源清洁利用国家重点实验室,浙江杭州310027)
为了实现臭氧氧化多种污染物协同脱除反应后残留臭氧的近零排放,通过实验室模拟某300 MW锅炉烟气臭氧多脱条件,开展残余臭氧的分解试验研究。研究不同水浴温度、喷淋温度、添加剂种类、添加剂浓度等关键参数对脱硫塔及烟囱尾部烟道中残余臭氧分解特性的影响.试验结果表明,水浴温度和喷淋温度越高,残余臭氧的分解效果越好;喷淋液中加入还原性物质对残余臭氧的分解有很明显的促进作用;添加剂浓度在一定程度上影响残余臭氧的分解效果.使用CaSO3+(NH4)2SO4或Na2SO3+Na NO2复合型添加剂最终实现超低残余臭氧排放体积分数为0.03×10-6~0.04×10-6,满足了国家环境空气质量标准0.047×10-6.
臭氧多脱技术;残留臭氧分解;添加剂
近年来,随着国内外对环保的要求越来越严格,继脱硫脱硝后,重金属污染物排放的控制已摆上议程,燃煤电厂往往需要投入巨资来逐项实现各种污染物的排放标准.相比于由SCR、活性炭喷射和湿法脱硫组成的烟气综合治理技术,臭氧多脱技术(臭氧氧化多种污染物协同脱除)因可实现烟气中多种污染物协同脱除而具有明显优势,近年来已成为国内外烟气综合治理领域的一大研究热点[1-5].
对于燃煤锅炉烟气NOx排放,其中难溶于水的NO体积分数为90%~95%[1].考虑到湿法脱硫已广泛应用于大型燃煤锅炉的烟气净化,向尾部烟道烟气中通入臭氧,利用臭氧的强氧化性将烟气中NO和重金属等污染物氧化成具有较强水溶性的高价态氧化物(NO2、N2O5、Hg2+等),从而实现在脱硫塔中与SO2的协同脱除[2].这是本文所提到的“臭氧多脱技术”.目前,臭氧多脱技术在低温环境下已经开展了较多的研究工作[6-11],实验室中已经取得了96%的脱硝效率和100%的脱硫效率.在工程应用中,为了保证烟气中NOx、Hg、二恶英等污染气体较好的氧化降解吸收效率,喷入臭氧的化学当量比往往大于1,导致少量的臭氧残留.
残留的臭氧是一种污染物,它对人的呼吸道、神经、皮肤和免疫机能都会产生危害.我国的环境空气质量标准(GB 3095-2012)[12]和居住区大气中臭氧卫生标准(GB18066-2000)[13]中规定环境空气中臭氧质量浓度一级标准为0.1 mg/m3(0.047× 10-6).臭氧发生器安全与卫生标准(GB28232-2011)[14]中规定臭氧对水和空气处理后排放的质量浓度不得超过0.16 mg/m3(0.074×10-6).鉴于国家标准的限制和臭氧的危害,有必要对臭氧多脱过程中残留臭氧进行分解脱除,实现烟气中多种污染物的近零排放.
关于废水中臭氧分解机理的研究已取得较多成果[15-16].目前普遍遵循的机理有2个,即Staehelin等[17-20]提出的SHB机理和Tomiyasu等[21]提出的TFG机理.国内外学者已开展大量针对臭氧在空气中的热分解特性的研究[22].但大部分工作仅针对体积分数小于10-6[23]的臭氧分解开展试验.在实际电站锅炉中,在除尘器后脱硫塔前喷入臭氧,对烟气中的多种污染物进行高效氧化,之后残余臭氧将通过尾部脱硫塔和烟囱等尾部烟道最终排入大气。本文通过模拟脱硫塔和尾部烟道运行环境,开展残余臭氧的热分解试验研究,以实现烟气中多种污染物协同脱除,同时避免臭氧的二次污染.
1 试验系统及方法
试验系统如图1所示.臭氧采用氧气经一台臭氧发生器(型号CF-G-3-10g,青岛国林实业股份有限公司,臭氧产量≥10 g/h)产生.产生臭氧后与氮气混合(N2和O2均采用杭州今工特种气体有限公司提供的体积分数为99.999%的N2和O2),混合气的流量由质量流量计MFC(D08系列,北京七星华创)进行控制,混合气一部分进入臭氧分析仪1(型号为IN2000,美国IN公司,量程为0~10-2,精度为10-6),剩余进入喷淋塔.塔后气体进入模拟烟囱后最终排出,模拟烟囱的温度通过水浴恒温槽(型号为HH-S,常州澳华仪器有限公司,控温范围为室温~300℃,精度为±1℃)控制,不同位置的残留臭氧体积分数通过臭氧分析仪2(型号为Model205,美国2B公司,量程为10-9~100×10-6,精度为10-9)进行测量.
一般,臭氧分解与时间、温度有关,试验中通过选择合适的管径、管长和流量,以满足所需达到的停留时间.喷淋温度通过喷淋塔温控装置控制,沿程温度通过水浴加热控制.
试验中所用喷淋塔内径为33.5mm,高度为200 mm,体积为0.176 L,喷淋液体积流量为0.2 L/min,喷淋塔内停留时间4.8 s.配制喷淋液所用试剂(CaSO3、Na2SO3、NaNO2、(NH4)2SO4)均为分析纯级.为了使试验条件更接近工程实际,以某电厂300 MW锅炉为例,烟囱高度为210 m,底部内径为15 m,出口内径为7 m,两台锅炉共用一根烟囱。假定烟气总体积流量为260万m3/h(单台为130万m3/h(标准状况)).两台锅炉同时运行时,经计算得到烟气在烟囱内的停留时间为22.3 s.试验中用于模拟烟囱的聚四氟乙烯管内径为3.8 mm,体积流量为2.2 L/min的O2/O3/N2混合气为模拟烟气.燃煤锅炉烟气臭氧多脱技术中最主要的臭氧消耗来自于NO的氧化,按烟气中NO初始体积分数为250× 10-6计算,工程应用中O3与NO的摩尔比常取1~1.5[9](O3初始体积分数为250×10-6~375×10-6).由于反应温度和混合情况不同,在试验中测得氧化反应后的残留臭氧体积分数为10-5~8×10-5.为了确保最终实现残留臭氧的近零排放,试验中取残留臭氧初始体积分数为10-4~1.5×10-4.
图1中6个阀门分别对应不同的热分解时间,依次是0、1、4、8、16和23 s,当打开任一阀门时,其余阀门保持关闭.通过检测不同停留时间,来表征臭氧随时间梯度变化的分解特性.通过模拟实际的运行环境,研究不同烟囱温度(调节水浴温度)、喷淋塔条件(喷淋塔内温度、喷淋添加剂种类、添加剂浓度)等关键参数对尾部烟道(脱硫塔及烟囱)中残余臭氧分解特性的影响.
针对喷淋塔内臭氧分解率(简称“塔内分解率”, Rt)、水浴加热段内随加热时间变化的臭氧分解率(简称“沿程分解率”,Rw)和综合臭氧塔内分解和沿程分解得出的臭氧总分解率Ra,对臭氧分解率的计算采用下式:

图1 残留臭氧分解试验系统图Fig.1 Scheme of residual ozone decomposition test system
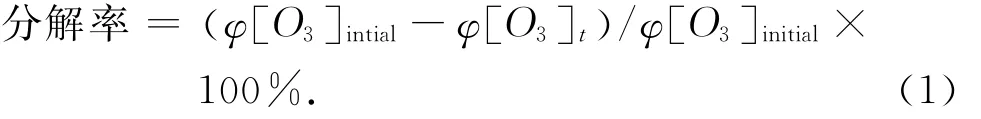
式中:φ[O3]initial为分解段内残留臭氧的初始体积分数,φ[O3]t为水浴加热段内随停留时间t而变化的臭氧体积分数,即φ[O3]0、φ[O3]1、φ[O3]4、φ[O3]8、φ[O3]16和φ[O3]23分别表示加热停留0、1、4、8、16和23 s后的臭氧体积分数.当计算塔内分解率Rt时,式(1)中φ[O3]initial取喷淋塔入口残留臭氧体积分数φ[O3]inlet,φ[O3]t取φ[O3]0.计算沿程分解率Rw时,式(1)中的φ[O3]initial取φ[O3]0, φ[O3]t取相应停留时间后的残留臭氧体积分数.计算总分解率Ra时,式(1)中的φ[O3]initial取喷淋塔入口残留臭氧体积分数φ[O3]inlet,φ[O3]t取φ[O3]23.
2 试验结果与讨论
2.1 水浴温度的影响
考虑到工程实际中烟气经过脱硫塔后的温度为70~90℃,通过试验研究了经过不喷淋的喷淋塔后,水浴温度分别为70、80和90℃时的臭氧沿程分解率,如图2所示.
由图2可见,在无喷淋作用下,即使臭氧体积分数较低时,分解率仍大体上与停留时间呈线性关系,这和前言所述的臭氧热分解经验公式[22]是匹配的;随着水浴温度的升高,臭氧分解率不断升高,即温度越高,臭氧分解速率越快[24];经过23 s这一充分长停留时间后,臭氧分解率最高只能达到约18.40%.可见,若烟气经臭氧氧化后不通过湿式洗涤塔喷淋,仅靠臭氧的自然分解,烟囱出口臭氧的体积分数是不会达标的,还必须采取其他措施促进臭氧分解.

图2 水浴温度对臭氧沿程分解的影响Fig.2 Effect of bath temperature on ozone decomposition along way
2.2 水喷淋的影响
实际电厂臭氧氧化后的烟气都要经过湿式洗涤塔喷淋,为了揭示喷淋液对臭氧塔内分解和沿程分解的影响,首先以水为喷淋介质,研究喷淋温度变化对臭氧塔内分解影响的试验.研究得到40~80℃下臭氧塔内分解率随水喷淋温度T的变化规律,如图3所示.由图3可见,喷淋温度的提高有利于臭氧塔内分解,当喷淋温度为60℃时臭氧塔内分解率为25.03%,试验中使臭氧从喷淋塔入口体积分数105×10-6降至出口体积分数78.72×10-6.此外,塔内分解率基本上与喷淋温度呈线性关系.导致这一变化趋势的原因在于:一方面温度升高促进臭氧分解;另一方面温度升高导致湿度增加,臭氧与水的反应(反应式2)增强,从而导致臭氧快速分解[25].
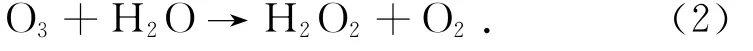

图3 喷淋温度对臭氧塔内分解的影响Fig.3 Effect of spray temperature on ozone decomposition in spray tower
为了揭示水喷淋对臭氧沿程分解的影响,于水浴温度90℃下,选定水喷淋温度分别为40和60℃的工况进行臭氧沿程分解试验,结果如图4所示.从图4可以看出,在水喷淋的情况下,臭氧沿程分解率比相同水浴温度下无喷淋时高(即与图2中的90℃工况对比).原因归结于水喷淋可以有效地提高沿程烟气湿度,沿程臭氧气体与水蒸气发生均相反应(反应式(2)),提高反应速率,进而促进臭氧分解.此外,图4中2个喷淋温度所得的效果显示高喷淋温度能够提高臭氧沿程分解率,这是由于喷淋温度提高导致烟气出塔后的含湿量增加,有利于残留臭氧的分解.当喷淋温度为60℃时,臭氧沿程末端分解率(23 s)为30.59%,可将上述臭氧塔体出口体积分数78.72×10-6降至54.64×10-6,仍显著高于国家标准.
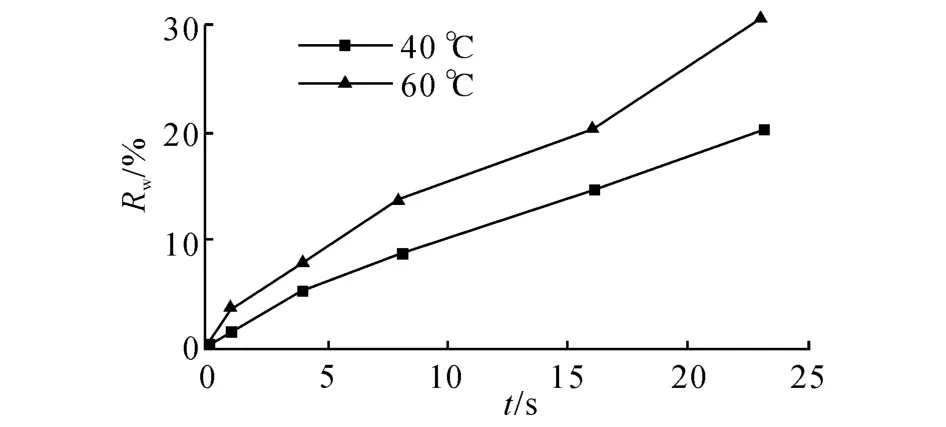
图4 喷淋温度对臭氧沿程分解的影响Fig.4 Effect of spray temperature on ozone decomposition along way
2.3 添加剂种类的影响
目前,对于促进臭氧分解的研究主要集中于催化臭氧分解.对于燃煤烟气臭氧多脱技术,烟气经臭氧氧化后进入脱硫塔,脱硫浆液吸收SO2和NOx后生成亚硫酸根和亚硝酸根等还原性离子.同时,为了提高NOx脱除率,往往需要在喷淋浆液中添加一些还原性物质促进吸收.利用臭氧多脱+湿法洗涤工艺综合协同脱除燃煤烟气中的多种污染物之后,需要对循环洗涤后的浆液进行无害化处理,旨在将吸收SO2和NOx后产生的亚硫酸根和亚硝酸根等离子氧化提纯,烟气中残留的臭氧可以起到这一作用.
为了揭示喷淋液中添加剂种类对残余臭氧的塔内分解效果,往喷淋水中分别加入浓度为0.04 mol/L的CaSO3、Na2SO3、NaNO2、CaSO3+(NH4)2SO4和Na2SO3+Na NO2作为喷淋介质.当喷淋温度为60℃时,研究喷淋液中添加剂种类对臭氧塔内分解的影响.将试验结果与无喷淋、水喷淋进行比较,如图5所示.图中,混合1表示CaSO3+(NH4)2SO4的混合溶液,混合2表示Na2SO3+NaNO2的混合溶液.
从图5可得如下结论。1)臭氧塔内的分解效果从高到低顺序为添加剂喷淋>水喷淋>无喷淋,原因在于臭氧与水的反应[17-21]本身可以促进臭氧分解,添加剂中的还原性离子与臭氧发生氧化还原反应可以进一步促进臭氧分解.加入Na2SO3后喷淋液与臭氧主要发生反应(3)~(6),加入CaSO3后喷淋液与臭氧主要发生反应(4)~(7),加入Na NO2后喷淋液与臭氧主要发生反应(8)、(9).2)添加剂种类对促进臭氧分解效果的顺序为Na2SO3> Na2SO3+NaNO2>CaSO3+(NH4)2SO4>NaNO2>CaSO3.这是两方面因素综合作用的结果.其一是p H值的影响,p H值越高越有利于臭氧分解,根本原因可由TFG机理[21]中的反应(10)说明.除CaSO3+(NH4)2SO4外,其余4种添加剂(即Na2SO3、Na2SO3+NaNO2、NaNO2和CaSO3)溶液的p H值的大小关系恰好与上述臭氧分解效果的顺序相同.CaSO3和(NH4)2SO4混合溶液对臭氧的分解效果优于CaSO3单一溶液,原因将在2.5节详细分析.其二是溶液中可以与臭氧进行氧化还原反应的还原性离子的影响,亚硫酸根的还原性强于亚硝酸根.CaSO3由于溶解度较低而不太利于分解臭氧;3)4种添加剂喷淋液均可使臭氧塔内分解率高达91%以上.尤其是加入Na2SO3后塔内臭氧分解率可以高达99.49%,试验中使臭氧从喷淋塔入口体积分数110×10-6降至出口体积分数0.56× 10-6.可见喷淋液中添加Na2SO3后已可使塔体出口臭氧体积分数降至很低水平,但仍达前述0.047× 10-6的10倍以上,尚需进一步采取措施.

图5 添加剂种类对臭氧塔内分解的影响Fig.5 Effect of additives species on ozone decomposition in spray tower

为了揭示喷淋液中添加剂种类对臭氧沿程分解的影响,往喷淋水中分别加入0.04 mol/L的CaSO3、Na2SO3、Na NO2作为喷淋介质.在喷淋温度为60℃,水浴温度为90℃的工况下,研究喷淋塔后残余臭氧在水浴加热段的沿程分解效果,并与水喷淋进行比较.试验结果如图6所示.
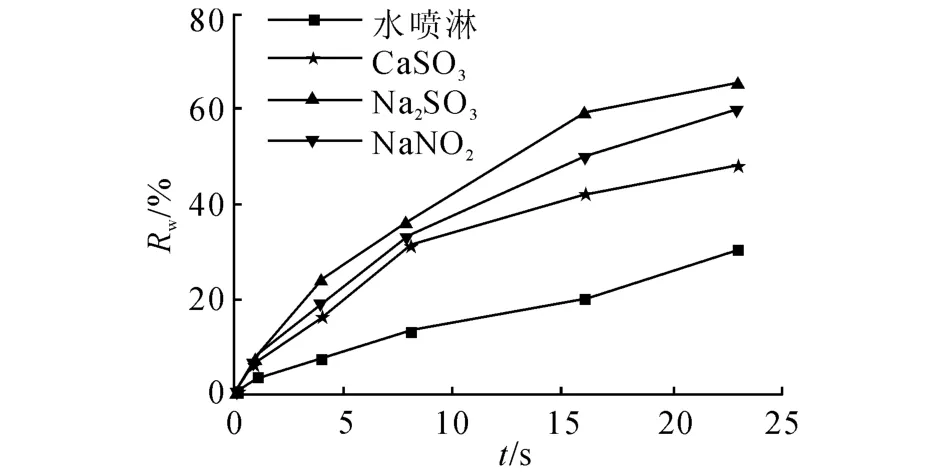
图6 添加剂种类对臭氧沿程分解的影响Fig.6 Effect of additives species on ozone decomposition along way
从图6可以看出,与水喷淋相比,3种添加剂的加入均对臭氧沿程分解有促进作用,这应归功于喷淋液中还原性离子被烟气携带进入水浴加热段,将在水浴加热作用下进一步将残余臭氧还原而分解.不同添加剂对臭氧沿程分解的促进效果的顺序与塔内相同,这也验证了上述分析.加入添加剂后,流出塔外的残余臭氧的沿程分解率大致与停留时间呈线性关系.对于分解臭氧效果最好的Na2SO3添加剂,经喷淋塔后残余臭氧沿程分解率最高达到65.76%,可将上述0.56×10-6的塔体出口体积分数降至0.19×10-6,仍稍高于排放限值0.047×10-6.
2.4 添加剂浓度的影响
为了研究添加剂浓度对塔内臭氧分解的影响,选取Na2SO3和Na NO2为目标添加剂。在喷淋温度为60℃的工况下,得到臭氧塔内分解率随添加剂浓度c(添加剂)的变化曲线,如图7所示.
对于NaNO2添加剂,臭氧塔内分解率随添加剂浓度升高而持续增大;对于Na2SO3添加剂, Na2SO3浓度对臭氧塔内分解率的影响不显著,加大添加剂浓度,臭氧塔内分解率(均在99%以上)仅是起初略有升高,随后趋于平稳.此外,Na2SO3添加剂对臭氧塔内的分解效果明显优于NaNO2.为了排除2种添加剂喷淋液因p H值不同带来的影响,在2种添加剂浓度相同的情况下,通过加入NaOH使2种添加剂喷淋液的p H值相同,发现Na2SO3对应臭氧塔内分解率为99.71%,NaNO2对应臭氧塔内分解率为96.10%.这说明NaNO2本身对臭氧的分解效果比Na2SO3差,这是因为亚硫酸根的还原性强于亚硝酸根.这验证了2.3节所陈述的观点.

图7 添加剂浓度对臭氧塔内分解的影响Fig.7 Effect of concentration of additives on ozone decomposition in spray tower
2.5 最终排放的体积分数比较
为了确保臭氧排放体积分数达到所要求的0.047×10-6安全值,试验中对无喷淋、水喷淋、0.04 mol/L CaSO3喷淋液、0.04 mol/L CaSO3+0.04 mol/L(NH4)2SO4复合喷淋液、0.04 mol/L Na2SO3+0.04 mol/L NaNO2复合喷淋液5种工况下的臭氧最终排放的体积分数和分解率进行研究.试验是在喷淋温度为60℃、水浴温度为90℃和停留时间为23 s的工况下进行测量的,所得的测量结果如表1所示.可见,与无喷淋和水喷淋相比,喷淋液中加入可与臭氧反应的还原性物质可以大幅度降低臭氧的最终排放的体积分数.采用2种复合型添加剂时,残留臭氧经湿式洗涤塔内喷淋液洗涤和塔后23 s的沿程分解,最终排放的体积分数均可降至0.047×10-6以下.以CaSO3+(NH4)2SO4为添加剂时臭氧最终排放的体积分数之所以能够比单一CaSO3添加剂时降低,主要是因为反应(11)、(12)的存在,生成溶解度高的(NH4)2SO3和NH4HSO3。这样可以提高CaSO3的传质速率,增加溶液中可溶性S(IV)的存在[2],有利于对臭氧的还原分解.Na2SO3+NaNO2的效果优于两者单独存在时效果的原因在于喷淋液中还原性离子的浓度和种类增加,可以提高进入模拟烟道的还原性离子的浓度和种类,促进臭氧沿程分解.


表1 臭氧最终排放的体积分数和分解率比较Tab.1 Comparison of concentration and decomposition rate of final ozone emissions
3 结 论
(1)提高水浴温度可以提高臭氧沿程分解率.与无喷淋相比,水喷淋可以提高臭氧分解率,且喷淋水温度提高,臭氧塔内和沿程分解率均提高.
(2)往喷淋液中加入还原性添加剂后,喷淋塔内的不同添加剂对臭氧的分解效果遵循Na2SO3>Na2SO3+NaNO2>CaSO3+(NH4)2SO4>NaNO2>CaSO3的顺序.
(3)添加剂浓度的提高明显有利于NaNO2喷淋液对臭氧的分解,但对可高效分解臭氧的Na2SO3喷淋液不明显.
(4)在喷淋温度为60℃、水浴温度为90℃和停留时间为23 s的工况下,分别采用2种复合型添加剂CaSO3+(NH4)2SO4和Na2SO3+NaNO2,臭氧最终排放的体积分数均能够达到0.03×10-6~0.04× 10-6,达到了0.047×10-6的安全值.在实际工业应用中,有望实现燃煤烟气多种污染物协同脱除的同时不引起因残余臭氧体积分数过高而造成的二次污染.
[1]WANG Zhi-hua,ZHOU Jun-hu,ZHU Yan-qun,et al.Simultaneous removal of NOx,SO2and Hg in nitrogen flow in a narrow reactor by ozone injection:experimental results[J].Fuel Processing Technology,2007, 88(8):817- 823.
[2]张相,朱燕群,王智化,等.臭氧氧化多种污染物协同脱除及副产物提纯的试验研究[J].工程热物理学报, 2012,33(7):1259- 1262.
ZHANG Xiang,ZHU Yan-qun,WANG Zhi-hua,et al.Experimental research for multi-pollution control by ozone and by-product purification[J].Journal of Engineering Thermophysics,2012,33(7):1259- 1262.
[3]SKALSKA K,MILLER J S,WILK M,et al.Nitrogen oxides ozonation as a method for NOx emission abatement[J].Ozone:Science and Engineering,2012, 34(4):252- 258.
[4]SKALSKA K,MILLER J S,LEDAKOWICZ S.Kinetics of nitric oxide oxidation[J].Chemical Papers,2010, 64(2):269- 272.
[5]MOK Y S,LEE H J.Removal of sulfur dioxide and nitrogen oxides by using ozone injection and absorption:reduction technique[J].Fuel Processing Technology, 2006,87(7):591- 597.
[6]王智化.燃煤多种污染物一体化协同脱除机理及反应射流直接数值模拟DNS的研究[D].杭州:浙江大学, 2005.
WANG Zhi-hua.Mechanism study on multi-pollution control simultaneously during coal combustion and direct numerical simulation of reaction jets flow[D].Hangzhou:Zhejiang University,2005.
[7]STAMATE E,IRIMIEA C,SALEWSKI M.Investigation of NOxreduction by low temperature oxidation using ozone produced by dielectric barrier discharge[J].Japanese Journal of Applied Physics,2013,52(5):3E-5E.
[8]ZHANG Jia,ZHANG Rui,CHEN Xin,et al.Simultaneous removal of NO and SO2from flue gas by ozone oxidation and NaOH absorption[J].Industrial and Engineering Chemistry Research,2014,53(15):6450- 6456.
[9]DORA J.Parametric studies of the effectiveness of oxidation of NO by ozone[J].Chemical and Process Engineering,2009,30(4):621- 634.
[10]SKALSKA K,MILLER J S,LEDAKOWICZ S.Intensification of NOxabsorption process by means of ozone injection into exhaust gas stream[J].Chemical Engineering and Processing:Process Intensification, 2012,61:69- 74.
[11]WANG Zhi-hua,CEN Ke-fa,ZHOU Jun-hu,et al.Simultaneous multi-pollutants removal in flue gas by ozone[M].Berlin:Springer,2014.
[12]GB 3095-2012,环境空气质量标准[S].北京:中国环境科学出版社,2012.
[13]GB18066-2000,居住区大气中臭氧卫生标准[S].北京:中华人民共和国国家质量监督检验检疫总局, 2000.
[14]GB28232-2011,臭氧发生器安全与卫生标准[S].北京:中华人民共和国卫生部,2011.
[15]BELTRÁN F J.Ozone reaction kinetics for water and wastewater systems[M].[S.l.]:CRC,2004.
[16]WEISS J.Investigations on the radical HO2in solution[J].Transactions of the Faraday Society,1935,31(1):668- 681.
[17]STAEHELIN J,HOIGNE J.Decomposition of ozone in water:rate of initiation by hydroxide ions and hydrogen peroxide[J].Environmental Science and Technology,1982,16(10):676- 681.
[18]STAEHELIN J,HOIGNE J.Decomposition of ozone in water in the presence of organic solutes acting as promoters and inhibitors of radical chain reactions[J].Environmental Science and Technology,1985,19(12):1206- 1213.
[19]BUHLER R,STAEHELIN J,HOIGNE J.Ozone decomposition in water studied by pulse radiolysis 1.HO2/O2and HO3/O3as intermediates correction[J].The Journal of Physical Chemistry,1984,88(22):2560 -2564.
[20]STAEHELIN J,BÜHLER R E,HOIGNÉJ.Ozone decomposition in water studied by pulse radiolysis.2.hydroxyl and hydrogen tetroxide(HO4)as chain intermediates[J].The Journal of Physical Chemistry, 1984,88(24):5999- 6004.
[21]TOMIYASU H,FUKUTOMI H,GORDON G.Kinetics and mechanism of ozone decomposition in basic aqueous solution[J].Inorganic Chemistry, 1985,24(19):2962- 2966.
[22]福奇曼E G,布朗宁R G..臭氧消毒(国际臭氧学会第三次国际会议论文集)[M].北京:中国建筑工业出版社,1983.
[23]李艳菊.室内臭氧污染变化规律研究[D].天津:天津大学,2005.
LI Yan-ju.Study on the changing laws of indoor ozone contamination[D].Tianjin:Tianjin University,2005.
[24]SEASE W S.Ozone mass transfer and contact systems[C]//Proceedings of the 2nd International Symposium on Ozone Technology.New York:International Ozone Institute,Syracuse,1976:1- 14.
[25]石志平,王文生.相对湿度变化对臭氧分解速率的影响[J].保鲜与加工,2004,4(6):24- 25.
SHI Zhi-ping,WANG Wen-sheng.Effect of different relative humidity on decomposable rate of ozone[J].Storage and Process,2004,4(6):24- 25.
Experimental study on residual ozone decomposition in process of multi-pollutants removal by ozone
LIN Fa-wei,ZHU Yan-qun,XU Chao-qun,MA Qiang,WANG Zhi-hua, ZHOU Jun-hu,CEN Ke-fa
(State Key Laboratory of Clean Energy Utilization,Zhejiang University,Hangzhou 310027,China)
The observation of residual ozone decomposition with the purpose of near-zero gas emission was conducted during the process of simultaneous multi-pollutants removal by ozone.A 300 MW boiler flue gas conditions were simulated.The effects of bath temperature,spray temperature,additives species and concentration of additives were attentively employed to conduct the residual ozone decomposition.The increase of bath temperature and spray temperature can improve the residual ozone decomposition.The residual ozone decomposition can be obviously promoted in spray tower when the spray liquid containing reductive substances.Concentration of additive had a positive effect on ozone decomposition.Compound additive(CaSO3+(NH4)2SO4or Na2SO3+NaNO2)achieved the highest decomposition among them.The ozone emission at the exit was 0.03×10-6~0.04×10-6,which could satisfy the national emission limit of 0.047×10-6.
multi-pollutants removal by ozone;residual ozone decomposition;additive
10.3785/j.issn.1008-973X.2015.07.007
X 701
A
1008- 973X(2015)07- 1249- 06
2014- 05- 30. 浙江大学学报(工学版)网址:www.journals.zju.edu.cn/eng
脱硫脱硝技术及其产业化科技创新团队资助项目(2011R50017);国家“973”重点基础研究发展规划资助项目(2012CB214906).
林法伟(1993-),男,博士生,从事臭氧氧化多种污染物协同脱除的研究.ORCID:0000-0001-5461-8277.
E-mail:linfawei@zju.edu.cn
朱燕群,女,工程师.ORCID:0000-0002-0981-2078.E-mail:yqzhu@zju.edu.cn
