石墨烯量子点功能化多壁碳纳米管构建日落黄和酒食黄同时检测的电化学传感器
2015-10-18徐利斌尹争志曾延波
徐利斌, 尹争志, 曾延波, 李 蕾*,
(1.常州大学石油化工学院食品学院,江苏常州 213016;2.嘉兴学院生物与化学工程学院,浙江嘉兴 314001)
人工合成色素被广泛用作食品添加剂,但其对生命体存在潜在威胁。世界卫生组织和国际粮农组织对每一种色素的使用量做了明确的规定[1],我国也制定了相应的严格规定[2]。日落黄(SY)和酒食黄(TZ)是两种典型色素,被用于饮料、酒水、糖果等食物[3,4],但过量食用会对人体造成严重危害[5],TZ更会影响到神经系统[6]。但SY和TZ具有价格低廉的绝对优势,依然被过量添加使用。因此,准确、快捷、灵敏检测SY和TZ对保障人们的生命安全至关重要。SY和TZ长期共存且含量低,给检测带来一定的难度。在已有的检测方法[7,8]中,电化学方法由于其简便、灵敏、成本低等优势而备受关注[9 - 13],而发展制备可以同时检测SY和TZ的电化学传感器,具有潜在的应用价值。
碳纳米管(CNTs)具备独特的物理、化学、机械性能,用作电极材料时可以加快电子传递速率、提高检测灵敏度[14]。杜学萍等[15]利用电聚合方法制备了聚次甲基蓝/多壁碳纳米管修饰玻碳电极,该电极测定叶酸时检测限达1.6×10-6mol·L-1。石墨烯量子点(GQDs)的荧光性能得到广泛地研究,但其电化学性能的研究较少,因此,研究GQDs与CNTs的复合物及其电化学性能,具有十分重要的意义。本实验以阳离子型高分子聚二烯丙基二甲基氯化铵(PDDA)为中介,将GQDs吸附到多壁碳纳米管(MWNTs)表面,制得GQDs功能化的MWNTs(GQDs-MWNTs)。该复合物修饰玻碳电极(GCE)后,表现了良好的导电性能,以及对SY和TZ的显著电催化性能。
1 实验部分
1.1 仪器与试剂
CHI660D电化学工作站(上海辰华仪器有限公司);CARY 5000紫外光谱仪(美国,瓦里安公司);S-4800扫描电子显微镜(SEM)(日本,日立公司)。
HNO3、KMnO4、HCl、H2O2、NaNO3、H2SO4、氨水、乙醇、石墨粉、日落黄(SY)和酒食黄(TZ),均购自上海化学试剂厂;聚二烯丙基二甲基氯化铵(PDDA)购自Sigma公司;MWNTs购自中科院成都化学所,使用前经混酸纯化处理。其它试剂均为分析纯,实验用水为二次去离子水。
实际样品购自大型超市。
1.2 石墨烯量子点的合成
采用Hummer方法[16]合成氧化石墨烯(GO):将石墨粉(1.5 g)、NaNO3(1.5 g)和H2SO4(69 mL)混合,在冰浴条件下搅拌,缓慢加入9 g KMnO4,然后缓慢升温至室温并搅拌1 h,缓慢加入100 mL水,温度升至90 ℃,搅拌30 min,加入300 mL水和100 mL 30%的H2O2,然后再用水洗涤、离心直至中性。最后把过滤物置于烘箱中干燥过夜得到GO,将其配制成4 mg·mL-1的溶液,待用。
将40 mL 30%的H2O2和10 mL 25%~28%的氨水加入5 mL GO溶液中,在80 ℃、强烈搅拌下反应24 h,在65 ℃时旋转蒸发,除去过量的氨水和H2O2,乙醇洗涤后,制得GQDs。
1.3 GQDs-MWNTs复合物修饰玻碳电极的制备
10 mL(0.5 mg·mL-1)酸处理的MWNTs分散到0.25%的PDDA(含0.5 mol·L-1NaCl)中,超声2 h,离心除去多余的PDDA,得到的复合物分散于水中形成溶液。加入25 mg GQDs后,混合超声8 h,离心洗涤除去多余的GQDs。取10 μL 1 mg·mL-1的GQDs-MWNTs复合物滴涂于洁净的GCE表面,静置干燥后,得到GQDs-MWNTs/GCE。该修饰电极可在0.2 mol·L-1NaAc缓冲溶液中用于检测SY和TZ。
1.4 电化学测定方法
以0.2 mol·L-1的HAc-NaAc缓冲溶液(pH=4.3)作为电解质溶液,搅拌条件下,在0.2 V富集待测物240 s后,于0.3~1.2 V范围内进行示差脉冲伏安(DPV)扫描,记录电化学信号。
2 结果与讨论
2.1 修饰材料的扫描电镜及紫外-可见吸收光谱表征
从材料的扫描电镜(SEM)图可以看出,MWNTs表面光滑,呈现彼此错综交织、多孔的分布状态,可以提高电极的比表面积(图1a)。GQDs的尺寸约为2 nm,当将GQDs复合固定到MWNTs表面后,复合物呈现胶状表面,但同样呈现多孔的三维分布状态(图1b)。
图2为各种材料的紫外-可见吸收光谱图,GQDs在230 nm处的特征吸收峰,对应于石墨烯结构中的C=C的π→π*电子跃迁吸收(曲线a);MWNTs在278 nm处的特征吸收峰,对应其π→π*电子跃迁(曲线b)。将GQDs和MWNTs复合后,在230 nm和278 nm处出现了两个吸收峰,分别对应GQDs和MWNTs的特征吸收(曲线c)。说明GQDs已成功复合到MWNTs表面。

图1 MWNTs(a)和GQDs-MWNTs(b)的扫描电镜(SEM)图
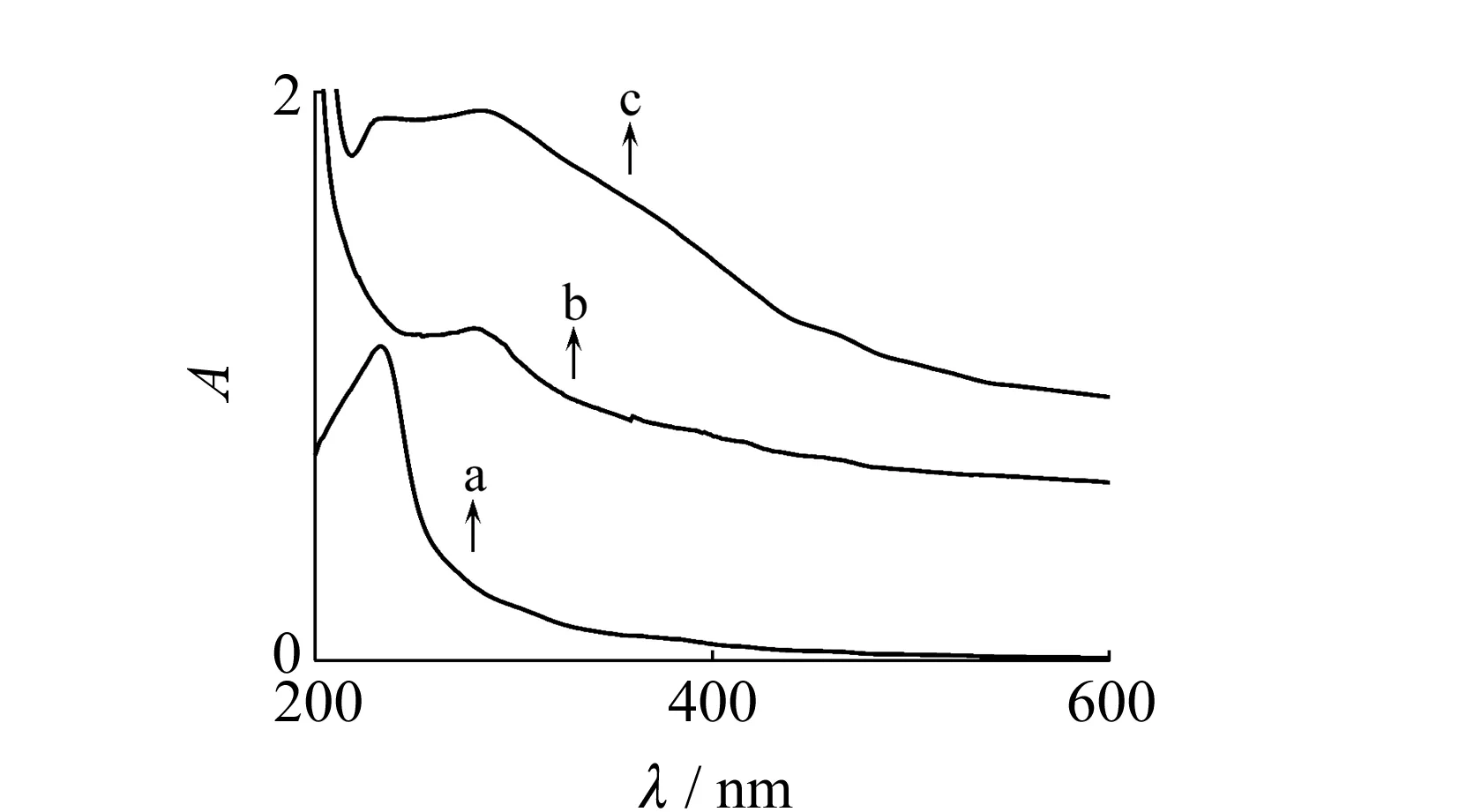
图2 GQDs(a)、MWNTs(b)和GQDs-MWNTs(c)的紫外-可见(UV-Vis)吸收光谱图
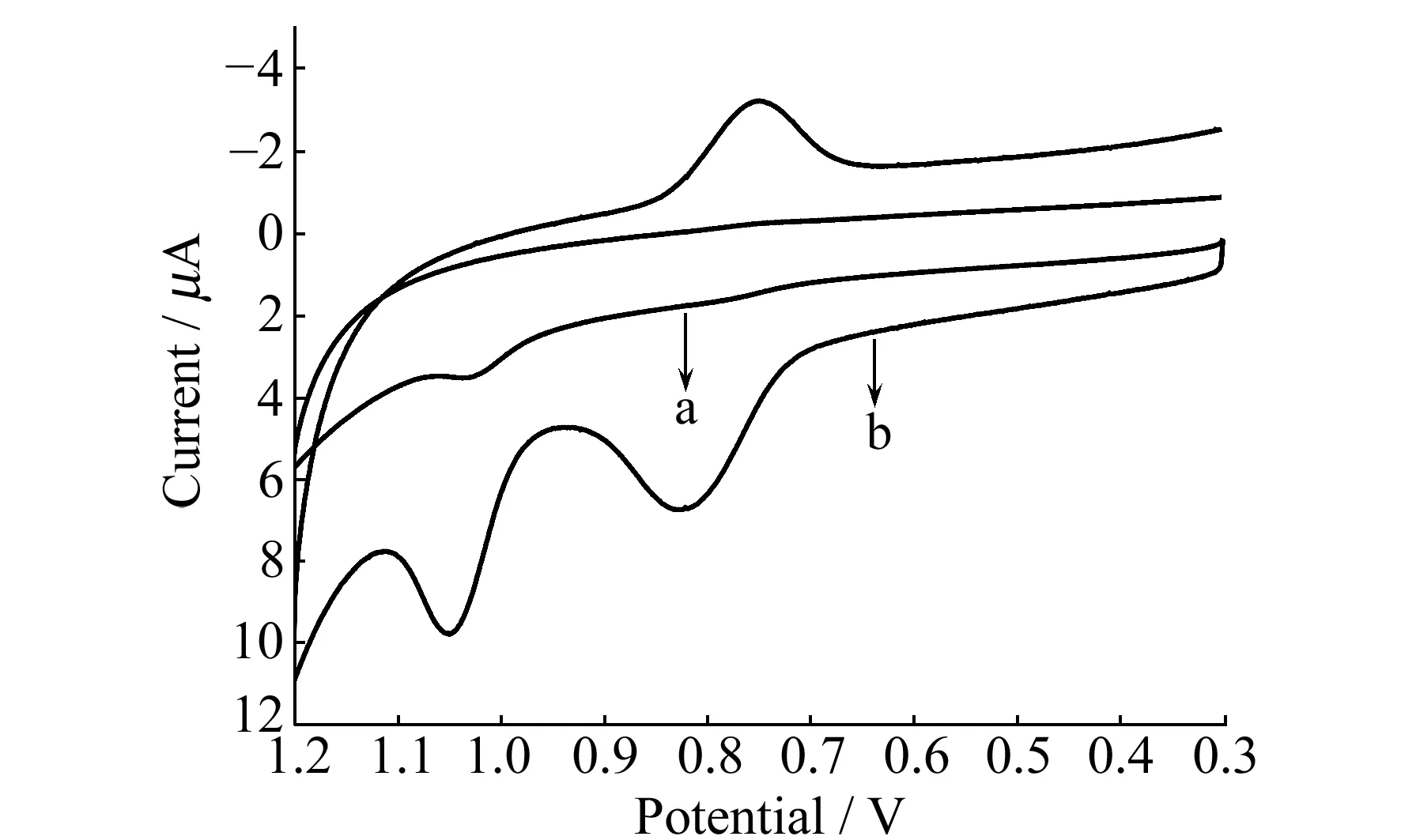
图3 1 μg·mL-1酒食黄和0.1 μg·mL-1日落黄在不同电极上的循环伏安图
2.2 修饰电极对日落黄和酒食黄的电化学响应
MWNTs/GCE对SY和TZ的响应如图3a所示,在1.035 V处出现一个不明显的氧化峰。用GQDs-MWNTs/GCE对相同体系进行电化学扫描,结果发现在0.825 V和0.752 V处出现一对氧化还原峰,在1.055 V处出现明显的氧化峰(图3b),两个氧化峰的峰电位差为230 mV。说明该修饰电极可以用于SY和TZ的同时检测。
2.3 电沉积富集前处理条件的选择
以0.1 μg·mL-1SY和1 μg·mL-1TZ为检测对象,研究了待测物在不同沉积电位(-0.1~0.5 V,富集时间为240 s)时对检测信号的影响。实验结果表明:沉积电位对两者的峰电流影响较小,因此为方便起见,沉积电位选择为0.2 V。沉积时间对SY和TZ的响应信号影响较大,对于SY和TZ,在30~240 s的沉积时间内,其峰电流随沉积时间呈现上升的线性关系,但随着沉积时间的继续增加,峰电流趋于稳定,表明达到了饱和吸附。考虑到灵敏度,选用240 s作为沉积时间。
2.4 SY和TZ的电化学行为及其机理
图4分别为MWNTs/GCE、GQDs-MWNTs/GCE对TZ和SY的电化学响应图。检测SY时,MWNTs/GCE在0.78 V出现了微弱的氧化峰,且随着扫描次数的增多,峰电流逐渐减小,可能是由于SY的氧化产物覆盖在了电极表面,使其表面钝化。在GQDs-MWNTs/GCE上,于0.825 V和0.752 V处出现了明显的氧化还原峰。检测TZ时,GQDs-MWNTs/GCE表现出了比MWNTs/GCE明显得多的催化性能。这可能是由于MWNTs和GQDs提供了丰富的富集表面、结合位点、电催化界面,起到了富集待测物和加快电子传递的作用。在0.2 mol·L-1的HAc-NaAc缓冲溶液中,实验了不同pH值时SY和TZ的峰电流响应。实验结果显示:在pH=3.8~6.9范围内,随着pH的增大,SY和TZ的氧化峰电位逐渐减小,表明在SY和TZ的氧化过程中有质子的参与,并且氧化峰电位与pH呈现良好线性关系:Epa(SY)=-0.03018pH+0.98681(R2=0.9941);Epa(TZ)=-0.04149pH+1.26136(R2=0.9942)。其中,当pH=4.3时,SY的峰电流最为明显,因此选用pH=4.3的 0.2 mol·L-1的缓冲溶液为电解质溶液。
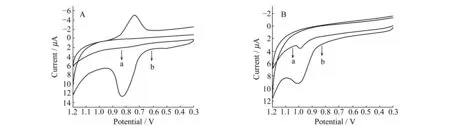
图4 (A) MWNTs/GCE(a)、GQDs-MWNTs/GCE(b)对日落黄的CVs响应;(B)MWNTs/GCE(a)、GQDs-MWNTs/GCE(b)对酒食黄的CVs响应
对于SY,当扫速从50 mV·s-1增至300 mV·s-1时,峰电位几乎没有变化,表明该过程为吸附控制过程。对于TZ,当扫速从50 mV·s-1增至300 mV·s-1,阳极峰电流(Ipa)与扫速(v)的平方根呈现很好的线性关系。线性回归方程为:Ipa(μA)=-1.735v1/2(v:mV·s-1)+6.415(R2=0.9991),表明该过程属于扩散控制过程,与此同时,氧化峰电位(Ep)随着扫描速率(v:mV·s-1)的增大而增大。SY与TZ的电化学过程机理与文献报道[17]一致。
2.5 传感器的线性范围和检测限
SY和TZ两种色素共存时的检测结果如图5所示。当TZ的浓度低于3 500 ng·mL-1时,不会干扰SY的检测,SY的线性响应范围为30~230 ng·mL-1,线性方程为:I(μA)=-0.0017c(ng·mL-1)-0.000838616(R2=0.9980),检测限为4.05 ng·mL-1(图5A)。当SY浓度低于800 ng·mL-1时,不会干扰TZ的检测,TZ的线性响应范围为40~600 ng·mL-1,线性方程为:I(μA)=-0.00394c-0.06318(R2=0.9953),检测限为8.06 ng·mL-1(图5B)。
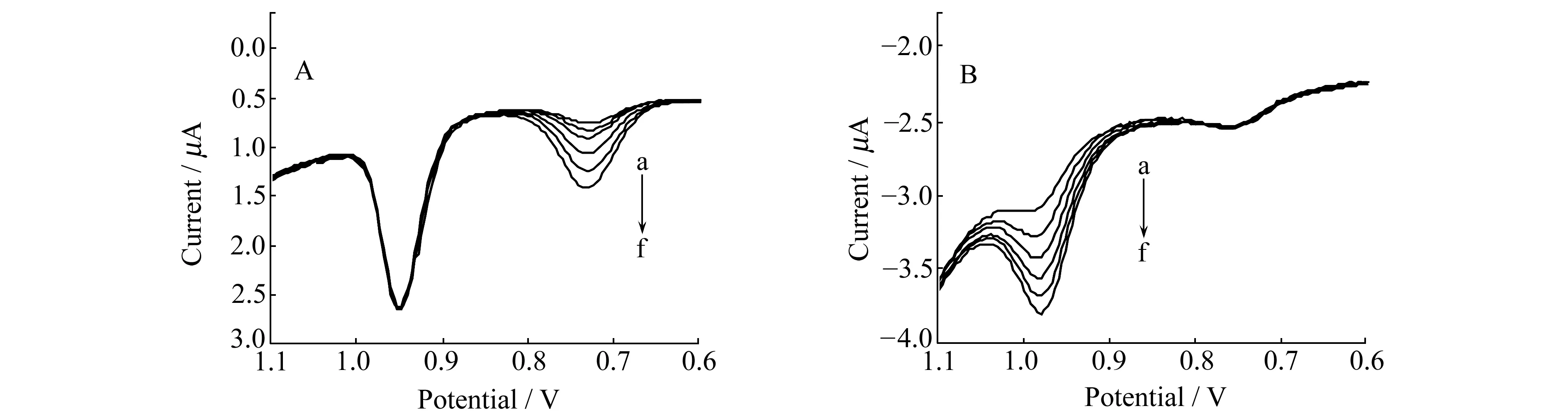
图5 (A)1 μg·mL-1酒食黄与不同浓度日落黄共存时的示差脉冲伏安(DPV)图;(B)0.02 μg·mL-1日落黄与不同浓度酒食黄共存时的DPV图
2.6 重现性、稳定性和干扰实验
研究了传感器的重现性和稳定性。以0.1 μg·mL-1的SY和TZ为检测对象,其结果的相对标准偏差(RSD)分别为2.4%(SY)和2.8%(TZ)。把该传感器置于空气中放置1个月后,对0.1 μg·mL-1的SY和TZ进行检测,RSD分别为3.6%(SY)和4.1%(TZ)。由此可见,所制备的GQDs-MWNTs/GCE具有较好的稳定性与重现性。当体系中100倍的Fe3+、Ca2+、Fe2+,1 000倍的葡萄糖存在时,对SY和TZ的检测均无影响。
2.7 实际样品分析
将该传感器用于市售饮料佳得乐中的SY及醒目中TZ的检测,在5 mL pH=4.3的HAc-NaAc缓冲溶液中,分别加入10 μL佳得乐、50 μL醒目以及三个不同量的标准品,在最佳条件下进行检测。实验结果如表1所示,TZ和SY的平均回收率分别为98.4%、96.1%,以及小于4%的RSD,说明该传感器可以用于实际样品中TZ和SY的测定。

表1 检测饮料中的日落黄和酒食黄
3 结论
制备了GQDs-MWNTs功能化的新型复合物,并用于修饰GCE。该修饰电极可用于日落黄和酒食黄的同时检测,GQDs和MWNTs的协同效应增强了修饰电极的导电性、检测灵敏度、稳定性和抗干扰能力,可用于饮料中日落黄和酒食黄的检测。
