BCLC B期肝癌术后行索拉非尼治疗的疗效分析
2015-10-13庄磊魏永刚宋其同施红旗张启瑜李波
庄磊,魏永刚,宋其同,施红旗,张启瑜,李波
(1.四川大学华西医院 肝脏外科,四川 成都 610000;2.温州医科大学附属第一医院 肝胆外科,浙江温州 325015)
BCLC B期肝癌术后行索拉非尼治疗的疗效分析
庄磊1,2,魏永刚1,宋其同2,施红旗2,张启瑜2,李波1
(1.四川大学华西医院肝脏外科,四川成都610000;2.温州医科大学附属第一医院肝胆外科,浙江温州325015)
目的:探讨手术切除后服用索拉非尼治疗巴塞罗那临床肝癌分期系统(BCLC)B期肝细胞肝癌(以下简称肝癌)的临床疗效。方法:回顾性收集2011年1月至2013年12月因BCLC B期肝癌在四川大学华西医院肝脏外科接受手术切除并于术后服用索拉非尼的患者资料,以及同期仅行手术切除的患者资料,1∶2配对,做病例对照研究,比较2组患者的生存时间及肿瘤复发时间。共纳入63例病例,观察组21例,对照组42例。结果:2组中位生存时间分别为25.0个月和17.7个月,差异有统计学意义(P=0.025);肿瘤复发时间分别为9.6个月和5.7个月,差异无统计学意义(P=0.574)。结论:手术切除联合索拉非尼治疗BCLC B期肝癌是安全的,并且可以延长患者的中位生存时间,是一种值得考虑的治疗方案。
癌,肝细胞;手术切除;索拉非尼
肝细胞肝癌(以下简称肝癌)是全球常见的恶性肿瘤之一,我国的肝癌发病率在癌症中占第三位,死亡率为第二位[1]。巴塞罗那临床肝癌分期系统(Barcelona Clinic Liver Cancer Classification,BCLC)B期肝癌的治疗方式国内外存在较大争议:欧美的临床实践指南建议行经导管肝动脉化疗栓塞(transcatheter arterial che-moembolization,TACE)治疗[2-3];而亚太地区的指南认为可手术切除[4-6]。研究[7-8]表明,索拉非尼能使中晚期肝癌患者的中位生存时间以及疾病进展时间获得显著延长。目前手术切除联合索拉非尼治疗BCLC B期肝癌的研究不多,笔者在此做回顾性病例对照研究,探讨其临床价值。
1 资料和方法
1.1一般资料 收集2011年1月至2013年12月因BCLC B期肝癌在四川大学华西医院肝脏外科接受手术切除,并于术后服用索拉非尼的患者资料。纳入标准:符合手术切除指征并行手术切除;术中发现或术后病理证实为BCLC B期肝癌;术后2周及大于2周影像学检查未见确切残留病灶;接受索拉非尼治疗前CT或MRI检查未见肿瘤复发。排除标准:接受过其他分子靶向药物治疗或其他系统性治疗;曾行肝移植术;服用索拉非尼前肝癌复发;合并其他肿瘤;病历资料不齐全或失访。收集患者病史资料、血液学检查、影像学检查、手术记录、术后病理报告等。共纳入63例资料齐全的病例,其中术后行索拉非尼治疗者21例(观察组),仅行手术切除者42例(对照组)。配对条件包括性别、年龄以及是否有肝硬化。2组基线资料比较差异无统计学意义(P >0.05),见表1。
1.2治疗
1.2.1肝切除术:所有患者均行术中超声探查,确定手术切除范围,尽量保留足够多的剩余肝脏。
1.2.2索拉非尼:所有患者经手术医师评估,于术后可耐受索拉非尼时开始服用。初始口服剂量为400 mg,每天2次,如有不良反应可酌情减量至200 mg,每天2次。发现肿瘤进展或复发时停止服用。
1.3疗效评价 肿瘤复发时间:患者手术切除至影像学检查发现肿瘤复发或转移的时间。总体生存时间:患者手术切除至患者死亡的时间。不良反应评价:根据美国国立癌症研究所不良事件通用标准3.0版(CTCAE 3.0)记录索拉非尼的不良反应。
1.4随访 通过电话、邮件等方式随访,随访内容包括索拉非尼服用时间、不良反应、 疾病复发转移情况,以及患者生存时间和死亡原因等。随访截止日期为2015年6月30日。
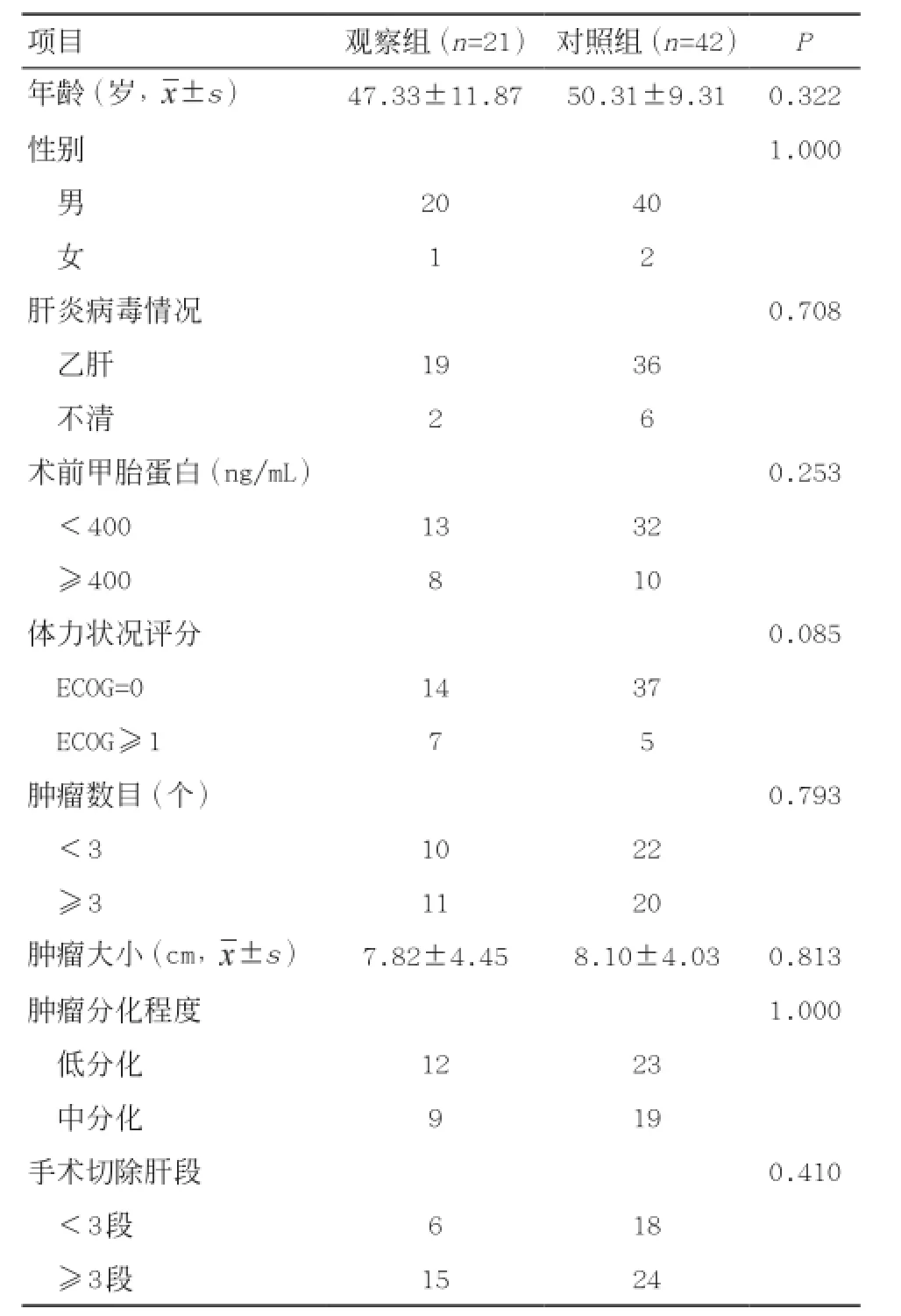
表1 患者临床病理特征
1.5统计学处理方法 采用SPSS 19.0统计学软件进行统计学分析。至观察终点记录肿瘤复发时间及患者生存时间,计量资料以±s或M描述,Kaplan-Meier法做生存曲线分析,2组生存率比较采用Log-Rank法。P<0.05为差异有统计学意义。
2 结果
2.1短期结果 术后并发症发生率为12.7%(8/ 63),具体如下:腹水4例,呼吸系统感染2例,膈下积液1例,胆漏1例。术后30 d及90 d内均无患者死亡。
2.2长期结果 观察组在术后17.8 d(6~52 d)开始联合索拉非尼治疗,平均服用6.3个月(1.9~17.0个月)。直至观察终点,共43例患者死亡,其中观察组11例,对照组32例。观察组和对照组的中位生存时间分别为25.0个月(95% CI:21.3,28.7个月)和17.7个月(95% CI:16.0,19.3个月),2组比较差异有统计学意义(P=0.025)。见图1。观察组和对照组的肿瘤复发时间分别为9.6个月和5.7个月,差异无统计学意义(P=0.574)。
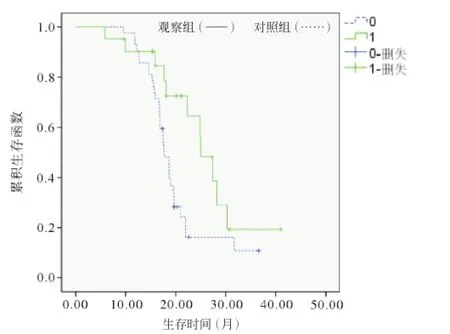
图1 2组中位生存时间比较
2.3药物不良反应 本次研究未观察到4级及以上不良反应。其中5例患者因难以耐受药物不良反应,减量至200 mg,每天2次后可以耐受。药物常见的不良反应包括手足皮肤反应、腹泻、脱发、高血压、体质量减轻等。其中3级手足皮肤反应5例,腹泻3例;2级手足皮肤反应10例、腹泻6例、脱发4例、高血压1例。其余均为1级不良反应。
3 讨论
肝癌是我国最常见的恶性肿瘤之一,根治性手术切除依然是其最有效的治疗方法。随着手术技术和麻醉技术的不断提高,肝癌通过手术切除治疗的安全性也逐步提高。研究表明,手术前仔细评估手术的可行性,术中精细操作,控制出血,保留足够的剩余肝脏,并予以恰当的营养支持,可以有效地降低围手术期病死率,确保手术治疗的安全性,令患者从中获益。Torzilli等[9]在研究中纳入737例BCLC B期肝癌患者,手术后1年生存率为88%;而在Zhong等[10]的研究中,中晚期肝癌患者手术切除后的1、3、5年生存率分别为88%、62%和39%。Wang等[11]在一回顾性的研究中纳入了3 892例不同分期的肝癌患者,指出BCLC B期肝癌的术后1、3、5年生存率分别是81.5%、64.4%和50.5%。这些研究的疗效令人满意,但肝癌术后的高复发性仍严重影响患者的生存质量及预后。
肝癌是一种富血供的肿瘤,发病机制很复杂,其发生、进展和转移与基因的突变、细胞信号转导通路和新生血管增生异常等密切相关,RAF-MEK-ERK通路与肝癌的发展密切相关[12]。而索拉非尼能抑制RAF-MEK-ERK通路,降低VEGFR、PDGFR、Flt-3、c-Kit等多种受体型酪氨酸激酶的活性,有着抑制肿瘤血管生成作用和减少肿瘤细胞增殖的双重作用,在抑制肝癌的增殖、转移、复发方面有一定的疗效。Bruix等[13]在SHARP试验的基础上做了关于索拉非尼治疗BCLC B期和BCLC C期的疗效及安全性的亚组分析,其中BCLC B期服用索拉非尼的54例,其中位生存时间和肿瘤复发时间分别为14.5个月和6.9个月。在SOFIA研究[14]中,纳入了74例BCLC B期患者和222例BCLC C期患者,接受索拉非尼治疗后2组的中位生存时间分别为20.6个月和8.4个月(P<0.0001)。索拉非尼治疗中晚期肝癌的疗效已受到广泛认可。
上述研究有一共同点即治疗手段单一,患者生存获益有限,因此多种治疗方案联合应用的疗效值得关注。有学者报道肝癌切除联合术后索拉非尼能够延缓肝癌复发[15]。而在我们的前期研究[16]中,手术联合索拉非尼治疗中晚期肝癌已取得一定的成效。因此,手术切除联合索拉非尼治疗中晚期肝癌的疗效值得进一步研究。本研究中,BCLC B期肝癌患者术后服用索拉非尼的中位生存时间高于对照组,这一结果与近期国内外研究结果类似。
本研究中,观察组并未发生4级或4级以上的药物不良反应。出现严重不良反应的患者通过药物减量即可耐受,其他患者通过对症处理后均能好转。因此手术联合索拉非尼治疗是可耐受的。考虑到BCLC B期肝癌生物学特性特殊且复杂,仍有很多因素影响患者的生存预后,且本次研究病例数较为有限,难以做多因素分析,我们希望能在以后做更深入的研究。
综上所述,手术切除并于术后联合索拉非尼治疗肝功能良好、肝脏储备功能良好的BCLC B期肝癌患者,疗效较为满意,不良反应可以耐受,值得扩大病例进一步研究。
[1]Jemal A, Muray T, Ward E, et al. Cancer statistics, 2005[J]. CA Cancer J Clin, 2005, 55(1): 10-30.
[2]Bruix J, Sherman M. Management of hepatocellular carcinoma[J]. Hepatology, 2005, 42(5): 1208-1236.
[3]European association for the study of the liver. EASLEORTC clinical practice guidelines: management of hepatocellular carcinoma[J]. J Hepatol, 2012, 56(4): 908-943.
[4]叶胜龙, 秦叔逵, 吴孟超, 等. 原发性肝癌规范化诊治的专家共识[J]. 临床肝胆病杂志, 2009, 25(2): 83-92.
[5]Kudo M, Izumi N, Kokudo N, et al. Management of hepatocellular carcinoma in Japan: Consensus-Based Clinical Practice Guidelines proposed by the Japan Society of Hepatology (JSH) 2010 updated version[J]. Dig Dis, 2011, 29 (3): 339-364.
[6]Omata M, Lesmana LA, Tateishi R, et al. Asian Pacific Association for the Study of the Liver consensus recommendations on hepatocellular carcinoma[J]. Hepatol Int, 2010,4(2): 439-474.
[7]Llovet JM, Ricci S, Mazzaferro V, et al. Sorafenib in advanced hepatocellular carcinoma[J]. N Engl J Med, 2008,359(4): 378-390.
[8]Cheng AL, Kang YK, Chen Z, et al. Efficacy and safety of sorafenib in patients in the Asia-Pacific region with advanced hepatocellular carcinoma: a phase III randomised,double-blind, placebo-controlled trial[J]. Lancet Oncol,2009, 10(1): 25-34.
[9]Torzilli G, Belghiti J, Kokudo N, et al. A snapshot of the effective indications and results of surgery for hepatocellular carcinoma in tertiary referral centers: is it adherent to the EASL/AASLD recommendations?: an observational study of the HCC East-West study group[J]. Ann Surg, 2013, 257 (5): 929-937.
[10] Zhong JH, Ke Y, Gong WF, et al. Hepatic resection associated with good survival for selected patients with intermediate and advanced-stage hepatocellular carcinoma[J]. Ann Surg, 2014, 260 (2): 329-340.
[11] Wang JH, Changchien CS, Hu TH, et al. The efficacy of treatment schedules according to Barcelona Clinic Liver Cancer staging for hepatocellular carcinoma-Survival analysis of 3892 patients[J]. Eur J Cancer, 2008, 44(7): 1000-1006.
[12] Semela D, Dufour JF. Angiogenesis and hepatocellular carcinoma[J]. J Hepatol, 2004, 41(5): 864-880.
[13] Bruix J, Raoul JL, Sherman M, et al. Efficacy and safety of sorafenib in patients with advanced hepatocellular carcinoma: subanalyses of a phase III trial[J]. J Hepatol, 2012, 57 (4): 821-829.
[14] Iavarone M, Cabibbo G, Piscaglia F, et al. Field-practice study of sorafenib therapy for hepatocellular carcinoma: A prospective multicenter study in Italy[J]. Hepatology, 2011,54(6): 2055-2063.
[15] Wang SN, Chuang SC, Lee KT. Efficacy of sorafenib as adjuvant therapy to prevent early recurrence of hepatocellular carcinoma after curative surgery: a pilot study[J]. Hepatol Res, 2014, 44(5): 523-531.
[16] 庄磊, 魏永刚, 杨家印, 等. 中晚期肝细胞肝癌术后行索拉非尼治疗的疗效分析[J]. 中国普通外科杂志, 2014, 23 (7): 882-886.
(本文编辑:吴健敏)
R735.7
B DOI: 10.3969/j.issn.2095-9400.2015.12.018
2015-09-03
庄磊(1989-),男,浙江瑞安人,住院医师,博士。
李波,教授,博士生导师,Email:cdhxlibo@126. com。
