BDE-47在土壤矿物质与有机质上的吸附解吸特征
2015-10-12张美芳樊孝俊
张美芳,樊孝俊
南昌市环境监测站,江西 南昌 330038
多溴联苯醚(PBDEs)作为一种持久性有机污染物,具有高毒性、持久性、生物积累性和亲脂憎水性[1]。PBDEs分布广泛,在各类环境介质中都有分布,其中土壤作为PBDEs的主要汇和再释放源,对PBDEs的时空分布和地球化学循环过程具有非常重要的作用[2]。PBDEs与土壤之间的吸附和解吸作用是其进入土壤介质后发生的最快速、最直接的环境过程,因而该过程是影响其后续迁移行为和生物降解过程的关键。当前,对PBDEs在土壤中的解吸与吸附行为特征研究均是基于土壤本身[3-4],对其中参与影响PBDEs在土壤中行为的土壤组分并没有进行单独深入探究。土壤主要由有机质和无机矿物组分构成,腐殖酸在土壤有机质中含量较高,较稳定,是土壤胶体吸附过程中最活跃的多相和多分散物质,是土壤有机质的主要吸附中心[5]。石英砂作为土壤中硅酸盐类物质的代表,是土壤矿物的主要骨架组分。高岭土具有较高的孔隙率和比表面积,是土壤中黏土矿物的代表。本研究以土壤中检出浓度及频率较高的 2,2',4,4'-四溴联苯醚(BDE-47)为研究对象,选择石英砂、高岭土作为土壤中的无机矿物组分的代表,选择腐殖酸作为有机质组分代表,分别进行独立吸附与解吸实验,通过吸附与解吸实验,识别影响BDE-47在土壤中吸附的关键组分,并以吸附容量、吸附非线性、解吸滞后因子等为考察指标,探讨了BDE-47的吸附与解吸特性。
1 实验部分
1.1 试剂及样品
BDE-47的标准固体样品(WI纯度大于98%,Aldrich Chemical Co.Inc.Milwaukee);甲醇、正己烷(色谱纯,USA);叠氮化钠、八水合氯化钙、高岭土、石英砂、腐殖酸(分析纯,中国)。
采集来源于3个不同地区的不同土地利用类型(果园、林地、农田)的3种土壤作为受试土壤。土壤样品经室温风干后,去除石块、植物残体等一系列杂质,通过2 mm孔径的金属筛进行筛分后,避光。
1.2 吸附实验
在60 mL棕色样品瓶中,各加入一定质量的吸附剂(土壤、高岭土、石英砂各50 mg,腐殖酸1 mg)和40 mL含一定浓度BDE-47的背景电解液(含 0.01 mol/L CaCl2和 200 mg/L NaN3),混匀后在(25±1)℃、120 r/min下振荡平衡72 h。平衡后静置4 h,取20 mL上清液用于BDE-47浓度测试。每组实验分别设置3个平行样,每个浓度梯度设置1个对照组。
取20 mL上清液,以正己烷为萃取溶剂,采用2次液液萃取方式萃取上清液中的 BDE-47。BDE-47浓度用GC-MS进行检测[6]。
1.3 解吸实验
每次提取出20 mL含BDE-47的上清液后,重新向体系内加入20 mL背景溶液,再次密封,按吸附实验方法振荡24 h后取出,重复解吸步骤,样品共进行3次解吸。
1.4 吸附/解吸系数测定
利用Freundlich等温吸附和解吸公式对实验数据进行拟合分析。Ce为每次吸附或解吸后BDE-47在液相的平衡浓度;Qe为每次吸附或解吸后BDE-47在吸附剂上的固相平衡浓度;KF为吸附或解吸系数;N为吸附或解吸非线性系数(以Ns或 Nd表示)。
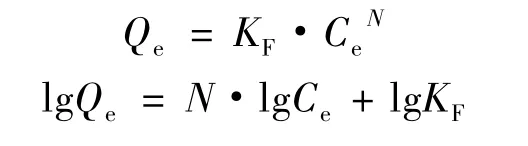
2 结果与讨论
2.1 吸附剂特性表征
对石英砂、高岭土、土壤和腐殖酸进行简单的表征,结果列于表1中。从比表面积来看,高岭土的比表面积是石英砂的450多倍,意味着高岭土相比石英砂会有更多的吸附位点;3种土壤的比表面积为16.93~19.94 m2/g,土壤的比表面积主要由其粒径分布和孔隙结构所贡献,而其内部孔隙可能来自于矿物质或者矿物-有机物聚合体的孔隙或微孔有机组分,而腐殖酸的比表面积很小,仅有1.91 m2/g,说明其孔隙结构相对土壤不够发达。3种土壤的总有机碳质量分数为0.13%~0.70%,不同的土地利用类型可能造成土壤有机质来源与形成过程差异。
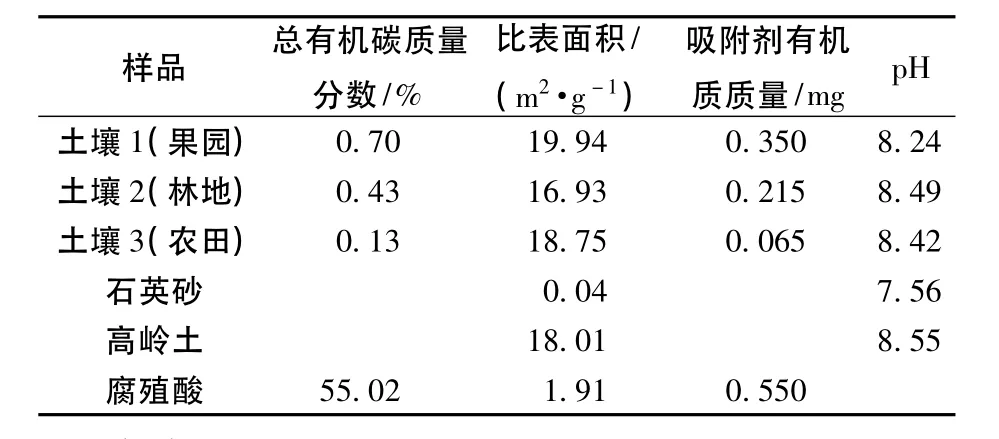
表1 吸附剂的基本理化性质
2.2 吸附特性分析
图1为腐殖酸、石英砂、高岭土和3种土壤对BDE-47的Freundlich吸附等温线拟合结果,所有拟合参数均列于表2中。分析结果表明,土壤、石英砂、高岭土和腐殖酸对 BDE-47的吸附用Freundlich吸附模型拟合所得的 R2分别为0.963、0.993、0.962、0.962、0.991、0.920,具有较好的拟合度。吸附系数KF表征吸附剂对吸附质的吸附能力大小。高岭土和石英砂的KF远小于土壤和腐殖酸的 KF,相比于腐殖酸、土壤对BDE-47的吸附能力,作为土壤典型无机矿物质组分的石英砂和高岭土对BDE-47的吸附能力非常微弱。高岭土对BDE-47的吸附能力强于石英砂,可能因为高岭土的比表面积大于石英砂,使高岭土能有更多的吸附位点用于吸附BDE-47。
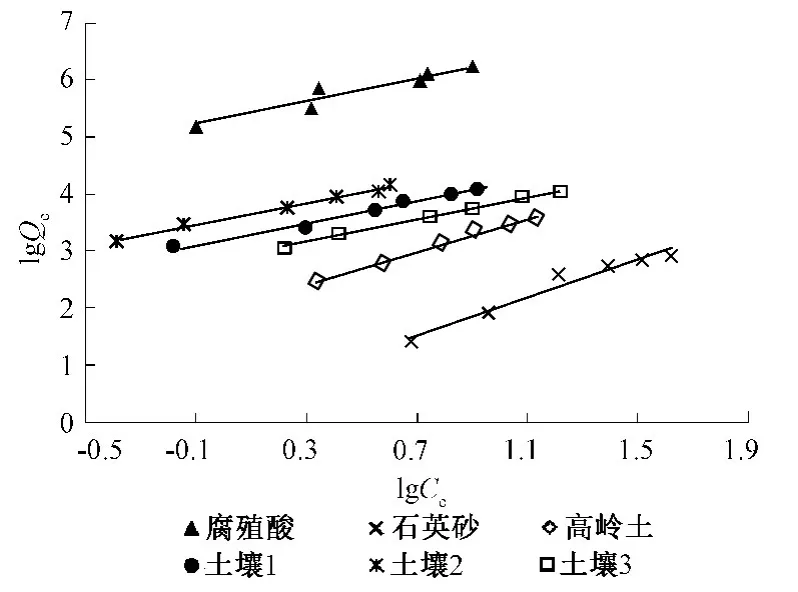
图1 土壤、无机矿物和腐殖酸对BDE-47的Freundlich吸附等温线
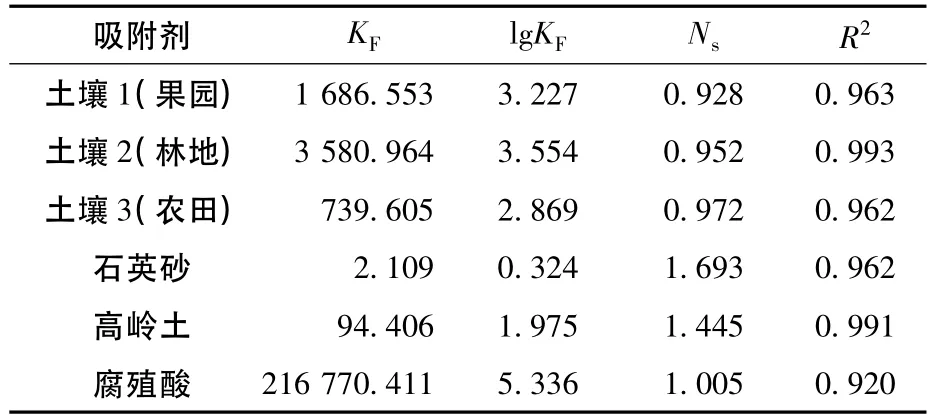
表2 土壤、无机矿物和腐殖酸对BDE-47的Freundlich吸附等温线拟合参数
本研究认为,作为典型土壤重要有机质组分的腐殖酸,在对BDE-47的吸附中起到了重要作用。这与之前一些研究指出的土壤中有机质对类似PBDEs的疏水性有机污染物有着重要影响的结论相符[7]。
然而,单纯比较KF的大小不能有效地比较土壤与腐殖酸的吸附能力的高低,故引入KFOC作为表征因子。KFOC为有机碳归一化后的吸附系数(单位有机质吸附系数),通过比较KFOC的大小,能有效地反映除有机质含量这个因子外,其他特性因素对吸附能力的影响。图2为单位有机质的土壤及腐殖酸对BDE-47的Freundlich吸附等温线结果,拟合所得参数列于表3。
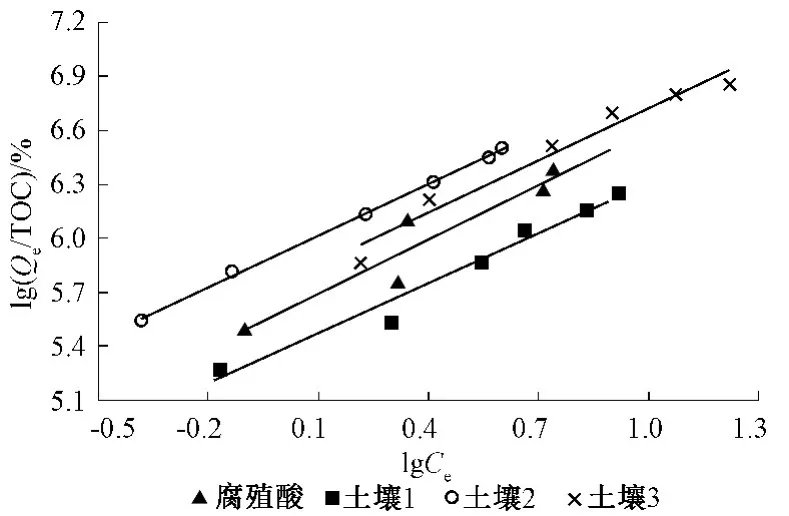
图2 单位有机质土壤及腐殖酸对BDE-47的Freundlich吸附等温曲线
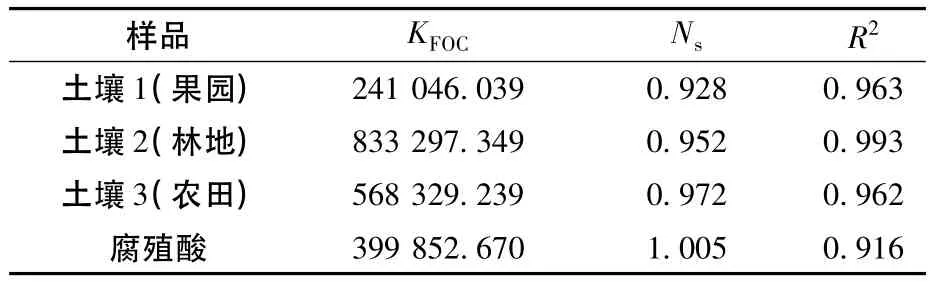
表3 单位有机质土壤及腐殖酸对BDE-47的Freundlich吸附等温线拟合参数
3种土壤的KFOC是腐殖酸的KFOC的0.612~2.115倍,说明排除有机质含量因素影响后,不同土壤对BDE-47的吸附能力仍存在差异。这与土壤中有机质的构成与表面特性有关。Heyas等[8]研究指出,腐殖酸中有机质的芳香性并没有土壤中的强,因此,土壤中可能因存在芳香性更高或空隙结构更为发达的其他有机组分而具有更强的π-π键作用能力或微孔吸附能力。这也可以解释当对比单位有机碳吸附剂的吸附能力时,土壤对BDE-47的吸附能力会比腐殖酸强的现象。虽然腐殖酸吸附BDE-47能力较强,但在土壤中,还存在黑碳等其他有机质对BDE-47有较强吸附作用[9]。
2.3 解吸特性分析
图3为在不同BDE-47初始浓度条件下BDE-47在腐殖酸上解吸的Freundlich解吸等温线拟合结果,拟合参数列于表4。可以看出,腐殖酸对BDE-47的解吸过程可以用Freundlich模型较好地拟合与表达。
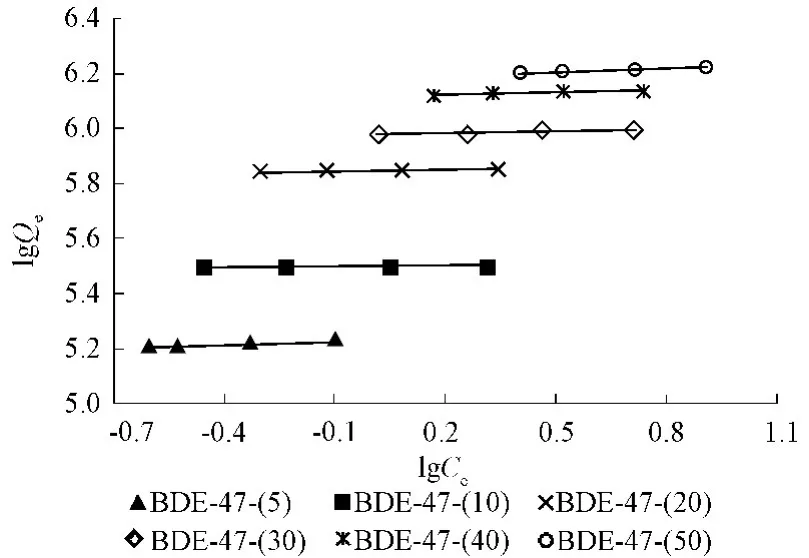
图3 腐殖酸对不同浓度BDE-47下的Freundlich解吸曲线
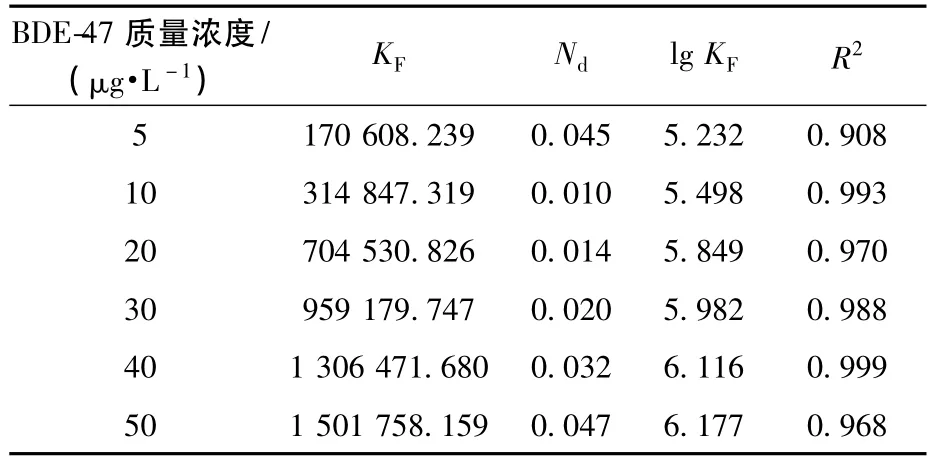
表4 腐殖酸对BDE-47不同浓度下的Freundlich解吸等温线拟合结果
为了表征BDE-47在腐殖酸上的解吸滞后性质,选择解吸非线性系数Nd与吸附非线性系数Ns的比值(解吸滞后因子HI)进行表征分析,HI越小,表明解吸滞后越显著[10]。另外,通过计算每次循环解吸后的解吸率来分析BDE-47在腐殖酸上的滞后性变化,结果见表5。
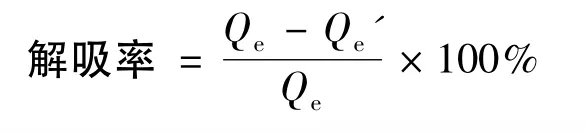
式中Qe为第K次解吸(K=0时为吸附)后腐殖酸上的BDE-47平衡浓度,Qe'为第K+1次解吸后腐殖酸上的BDE-47平衡浓度。
由表5可以看出,BDE-47在腐殖酸上的解吸滞后非常显著。当吸附质BDE-47浓度越小时,BDE-47在腐殖酸上的解吸滞后越显著。疏水性有机污染物在土壤有机组分上出现的解吸滞后现象可能由以下原因导致[11]:化学键形成或和特定吸附位点的不可逆结合;吸附质被吸附剂分子捕获;慢解吸速率;结构或孔隙变形机制。而在BDE-47起始质量浓度为5 μg/L时出现的HI突然变大的情况,可能是由于吸附质剩余浓度过低,浓缩后的BDE-47浓度仍然低于实验所用GC-MC仪器的测量范围,从而出现较大误差。辛佳等[12]对BDE-47在土壤中的解吸行为进行研究发现,对于设置的 5、10、20、30、40、50 μg/L 6 组起始BDE-47质量浓度的解吸实验,对应的滞后因子分别为 1.269、0.482、0.311、0.208、0.107、0.203,均大于本研究所用的纯腐殖酸,说明BDE-47在腐殖酸上的解吸滞后性显著强于在土壤上的解吸滞后性。
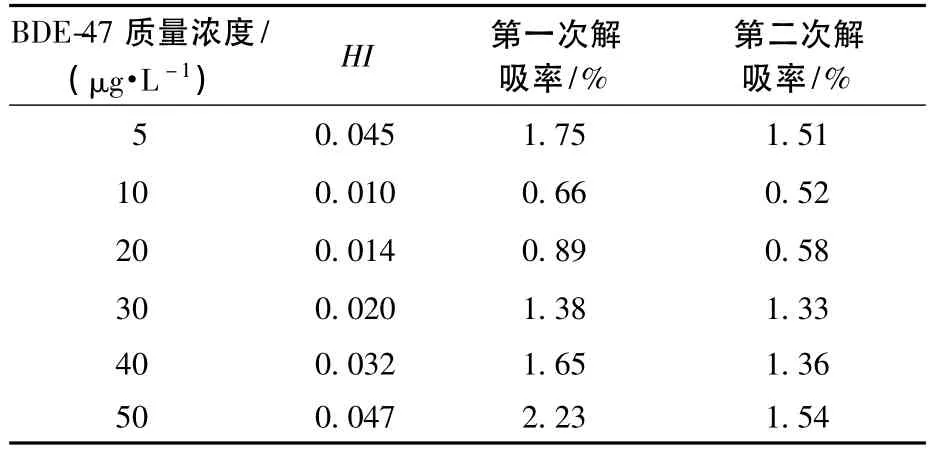
表5 不同浓度BDE-47在腐殖酸中吸附的滞后性参数
从解吸率的角度分析发现,在测试的所有浓度中,BDE-47从腐殖酸上第一次解吸下来的解吸率均比第二次从腐殖酸上解吸下来的解吸率要大。由于BDE-47刚被吸附时优先吸附到高能位点,而当高能位点趋近饱和时,BDE-47开始向低能位点吸附。而在解吸初始阶段,因为BDE-47与低能位点的吸附力较弱,因此优先被解吸下来,而高能位点与BDE-47之间的较强作用力导致之后解吸的滞后和困难,从而也解释了为什么第一次解吸循环的解吸率要高于二次解吸循环的解吸率。
3 结论
定量对比土壤、矿物质和有机质对BDE-47吸附能力后发现,矿物组分虽然是土壤构成的优势组分,但其对BDE-47的吸附能力很弱,而有机质对BDE-47在土壤中的吸附具有重要的调控作用。在土壤中,有机碳含量不是影响土壤有机质吸附BDE-47的惟一因素,还与有机质的构成及表面结构特性有关。在BDE-47的解吸行为中,BDE-47在腐殖酸上呈现了强烈的解吸滞后性,且解吸率随着解吸循环的进行而逐渐降低。
[1]汤保华,祝凌燕,周启星.多溴二苯醚(PBDEs)对环境的污染及其生态化学行为[J].生态学杂志,2008(1):96-104.
[2]刘宗峰,郎印海,曹正梅,等.环境中多溴联苯醚(PBDEs)分布特征研究进展[J].土壤通报,2007(6):1 227-1 233.
[3]Olshansky Y,Polubesova T,Vetter W,et al.Sorptiondesorption behavior of polybrominated diphenyl ethers in soils[J].Environmental Pollution,2011,159(10):2 375-2 379.
[4]Liu W,Cheng F,Li W,et al.Desorption behaviors of BDE-28 and BDE-47 from natural soils with different organic carbon contents[J].Environmental Pollution,2012,163:235-242.
[5]曹罡,莫汉宏,安凤春.除草剂2,4-D在胡敏酸上的吸附[J].环境科学学报,2002(1):120-122.
[6]Xin J,Liu X,Jiang L,et al.BDE-47 sorption and desorption to soil matrix in single-and binary-solute systems[J].Chemosphere,2012,87(5):477-482.
[7]崔兆杰,宋善军,刘静.多氯联苯在土壤中的吸附规律及其影响因素研究[J].生态环境学报,2010(2):325-329.
[8]Hayes M H B,Swift R S,Wardle R E,et al.Humic materials from an organic soil: A comparison of extractants and of properties of extracts[J].Geoderma,1975,13(3):231-245.
[9]Huang W,Peng P,Yu Z,et al.Effects of organic matter heterogeneity on sorption and desorption of organic contaminants by soils and sediments[J].Applied Geochemistry,2003,18(7):955-972.
[10]Doretto K M,Rath S.Sorption of sulfadiazine on Brazilian soils[J].Chemosphere,2013,90(6):2 027-2 034.
[11]彭剑飞,饶俊文,沈咏美等.天然土壤中典型多溴联苯醚解吸过程的初步研究[J].农业环境科学学报,2009(7):1 404-1 409.
[12]辛佳,刘翔.多溴联苯醚BDE-47在土壤中的吸附及解吸行为研究[C].哈尔滨:持久性有机污染物论坛2011暨第六届持久性有机污染物全国学术研讨会,2011.
