3-(1,1-双吲哚基)乙基香豆素的合成
2015-10-12宋庆宝
林 燕,宋庆宝
(浙江工业大学 化学工程学院,浙江 杭州 310014)
医药化工
3-(1,1-双吲哚基)乙基香豆素的合成
林燕,宋庆宝
(浙江工业大学化学工程学院,浙江杭州310014)
以水杨醛和乙酰乙酸乙酯为起始原料合成3-乙酰基香豆素,再通过3-乙酰基香豆素和吲哚反应合成3-(1,1-双吲哚基)乙基香豆素。该方法具有操作简便、条件温和、反应时间短、收率高等优点。
双吲哚;香豆素;合成
双吲哚类衍生物是一类及其重要的化合物,因为很多天然产物和药物中均含有该结构单元[1]。近几年来,临床医学研究发现,双吲哚类物质有显著的药理活性,如抗乳腺癌、抗肝癌、抗前列腺癌等活性,可作为研制抗癌药的先导物[2]。此外,双吲哚类化合物还具有抗菌[3]、消炎[4]、止泻[5]等作用。由于多数双吲哚类衍生物具有优越的生物活性,因而通过有效的方法合成双吲哚类化合物受到了学术界的普遍关注。虽然对双吲哚类衍生物的合成已有不少文献报道,但已报道的方法具有反应步骤较多,收率较低,条件复杂等缺点。
研究表明,香豆素类化合物具有明显的药理活性,如抗HIV、抗癌、抗凝血、抗炎及平滑肌松弛等[6]。吲哚和香豆素都是很好的活性药效团,同时含有吲哚和香豆素的化合物可能有更好的生物及药理活性。本研究从廉价易得的原料出发,希望构建同时含有吲哚和香豆素的骨架,得到双吲哚-香豆素衍生物。寻找绿色环保的合成方法及开发具有更多活性药效团的新型化合物具有重要的理论意义,并为以后的药学研究奠定基础。
1 实验部分
1.1试剂与仪器
所用试剂均为分析纯;熔点用SGW X-4显微熔点仪测定,温度计未校正;1HNMR由德国Bruker公司Bruker DRX 500 MHz核磁共振仪测定;有机反应用薄层硅胶板(TLC 60 F-254)跟踪,紫外灯检测。
1.23-乙酰基香豆素的合成
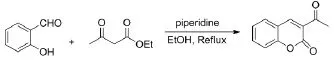
将水杨醛 (1.22 g,10 mmol),乙酰乙酸乙酯(1.43 g,11 mmol),哌啶(0.085 g,10 mol%),无水乙醇(20 mL)加入到50 mL单口圆底烧瓶中,回流搅拌2 h。TLC点板跟踪,反应结束后冷却至室温,抽滤,乙醇:水=1:1(5 mL×2)洗涤,干燥得3-乙酰基香豆素粗品1.70 g,产率:90%。粗品用无水乙醇重结晶,过滤、干燥后直接用于下一步反应。3-乙酰基香豆素参考文献[7]类似方法合成,熔点122°C~124°C。
1.33-(1,1-双吲哚基)乙基香豆素的合成
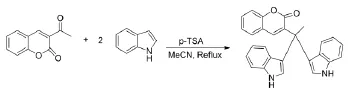
取上述3-乙酰基香豆素(0.188 g,1 mmol),吲哚(0.234 g,2 mmol),p-TSA·H2O(0.019 g,10 mol%)和乙腈(5 mL)加入到25 mL圆底烧瓶中,反应回流4 h。TLC点板跟踪,反应结束后冷却至室温,抽滤,乙醇(5 mL×2)洗涤,干燥得白色固体0.344 g,产率:85%。粗产品用无水乙醇重结晶,熔点253℃~255℃。1H NMR(500 MHz,DMSO)δ 10.93(s,2H),7.65(s,1H),7.52(t,J=8.4 Hz,1H),7.42~7.37(m,3H),7.35(d,J =8.3 Hz,1H),7.29(d,J=8.1 Hz,2H),7.20(t,J=7.5 Hz,1H),7.03(t,J=7.5 Hz,2H),6.90(d,J=2.0 Hz,2H),6.82(t,J=7.5 Hz,2H),2.34(s,3H)。
2 结果与讨论
2.1溶剂对3-(1,1-双吲哚基)乙基香豆素合成反应的影响

表1 溶剂反应的影响a
在3-(1,1双吲哚基)乙基香豆素的合成反应中,考察了不同溶剂对反应产率的影响,结果如表一所示。与乙醇、甲醇、异丙醇、乙酸乙酯、二氯甲烷相比,乙腈做溶剂具有明显的优越性,反应时间短,收率高。因此,以乙腈作为溶剂。
2.2催化剂对3-(1,1-双吲哚基)乙基香豆素合成反应的影响
接着考察了在乙腈回流条件下,加入10 mol%不同催化剂以探索催化剂对反应的影响。如表二所示,p-TSA作催化剂时,反应时间最短,收率最高。当使用CAN,ZnCl2,NiCl·26H2O等其他路易斯酸催化剂时,需要更长时间才能反应完全,而且产率较低。因此,该反应中选用p-TSA为催化剂。

表2 催化剂反应的影响a
3 结论
以水杨醛和乙酰乙酸乙酯为起始原料,在乙醇回流、哌啶催化下反应合成3-乙酰基香豆素。再以3-乙酰基香豆素和吲哚为模板反应,通过一系列的实验,找到了合成3-(1,1-双吲哚基)乙基香豆素的最佳反应条件。反应具有操作简便、时间短、收率高等优点。
[1]Ge X,Rennert S G,Gruener N.3,3'-Diindolyl-methane induces apoptosis in human cencer cells[J].Biochemical and Biophysical Research Communications,1996,228:153-158.
[2]Kamal A,SrikanthY V V,Ashraf M.Synthesis of 3,3-diindolyl oxyindolesefficietly catalyzed by FeCl3and their in vitro evaluation for anticancer activity[J].Bioorganic& Medicinal Chemistry Letters,2010,20:5229-5231.
[3]Bolotov V V,Drugovina V V,YakovlevaL V.Facile synthesis of 3,3-di(heteroaryl)indolin-2-one derivatives[J]. Khimiko-FarmatsevticheskiiZhurnal,1982,16:58-61.
[4]Pajouhesh H,Parsons R,Popp F D.Potential anticonvulsants VI:Condensation of isatins with cyclohexanone and other cyclic ketones[J].Journal of Pharmaceutical Sciences,1983,72:318-321.
[5]Garrido F,Ibanez J,Gonalons E.Facile synthesis of 3,3-di(heteroaryl)indolin-2-one derivatives catalyzed by ceric ammonium nitrate(CAN)under ultrasound irradiation[J]. European Journal of Medicinal Chemistry,1975,10:143-149.
[6]Xia Y,Fan C D,Zhao B X,et a1.Synthesis and structure -activity relationships of novel 1-arylmethyl-3-aryl-1H-pyrazole-5-carbohydra-zide hydrazine derivatives as poten tial agents against A549 lung cancer cells[J].European Journal of Medicinal Chemistry,2008,43:2347.
[7]Rao H S P,Sivakumar S.Condensation of α-Aroylketene Dithioacetals and 2-Hydroxy-arylaldehydes Results in Facile Synthesis of a Combinatorial Library of 3-Aroylcoumarins[J].Journal of Organic Chemistry,2006,71: 8715-8723.
附:
Synthesis of 3-(1,1-Di(1H-indol-3-yl)ethyl)-2H-chromen-2-one
LIN Yan,SONG Qing-bao
(College of Chemical Engineering,Zhejiang University of Technology,Hangzhou,Zhejiang 310014,China)
Using salicylaldehyde and ethyl acetoacetate as starting material to synthesize 3-acetyl coumarin,then 3-(1,1-di(1H-indol-3-yl)ethyl)-2H-chromen-2-one was synthesized viathe reation of 3-acetyl coumarin and indole.The method has the merits of simple operation,mild reactioncondition,high yield and short reaction time.
bisindole;coumarin;synthesis

1006-4184(2015)12-0009-03
2015-05-10
林燕(1987-),女,福建龙岩人,硕士研究生,主要从事有机合成研究。E-mail:ydly16@163.com。
