气相色谱法同时测定白酒中的8种物质
2015-10-10符传武
洪 薇,符传武
(广西柳州食品药品检验所,广西柳州545006)
气相色谱法同时测定白酒中的8种物质
洪薇,符传武
(广西柳州食品药品检验所,广西柳州545006)
采用气相色谱法测定白酒中的乙酸乙酯、己酸乙酯、乳酸乙酯、丁酸乙酯、丙酸乙酯和甲醇、正丙醇、β-苯乙醇8种物质,寻求最佳色谱条件。采用DB-624UI(60 m×0.32 mm×1.8 μm)毛细管色谱柱,氢火焰离子化检测器(FID)进行测定。8种物质在0~0.08%范围内的线性关系均良好,相关系数R2均在0.990以上。精密度试验的相对标准偏差(RSD)为0.03%~0.60%,检出限为0.001~0.025 g/L。加标回收率在82.22%~103.83%,RSD为0.2%~1.8%。结果表明,该方法实现了8种物质的良好分离,满足检测的要求。
气相色谱法;白酒;8种物质;同时测定
白酒的主要成分是乙醇和水,还有少量醇类、酯类等成分,构成了白酒不同的风格和口感。醇类是白酒中的主要助香成分,是醇甜主要物质来源,具有衬托酯香的作用。但醇类含量过高会导致酒味苦涩,导致饮酒者身体不适,易醉酒甚至中毒,因此醇类含量需要严格控制。酯类以不同的成分含量使白酒呈现特殊的香型,比如米香型白酒的主体香为乳酸乙酯,还有乙酸乙酯及适量的β-苯乙醇;浓香型白酒的主体香为己酸乙酯,还有适量的乳酸乙酯、乙酸乙酯及丁酸乙酯;清香型白酒的主体香是乙酸乙酯。各种香型的白酒中这些呈香成分的含量都有一定的要求,并且国家标准对其检测也推荐了相应的方法[1-2]。
GB/T 5009.48—2003《蒸馏酒及配制酒卫生标准的分析方法》中有甲醇和正丙醇的检测方法,GB/T 10345—2007《白酒分析方法》中有乙酸乙酯、己酸乙酯、乳酸乙酯、丁酸乙酯、丙酸乙酯、正丙醇、β-苯乙醇的检测方法。该试验则对色谱柱和气相色谱条件进行筛选优化[3-16],选择最佳条件,建立了同时测定上述8种物质的气相色谱分析方法,满足检验工作的需要,也更方便、快捷。
1 材料与方法
1.1材料与试剂
1.1.1样品
10批白酒检品:SP20140484、SP20140487、SP20140491、SP20140522、SP20140622、SP20140643、SP20140662、SP 20140945、SP20141010、SP20141050,包括米香型、清香型和浓香型白酒。分别为柳州、来宾市食品药品监督管理局委托检验样品。
1.1.2试剂
乙酸乙酯(99.9%)、甲醇(99.9%)均为色谱纯:赛默飞世尔科技(中国)有限公司;丙酸乙酯(99.0%)、丁酸乙酯(99.0%)、乳酸乙酯(99.0%)、己酸乙酯(99.0%)、正丙醇(99.0%)均为色谱纯:百灵威科技有限公司;β-苯乙醇(99.0%):阿拉丁试剂有限公司;乙酸正戊醇(95%):天津市光复精细化工研究所。
体积分数60%乙醇:用乙醇(色谱纯)加水(一级纯化水)配制。
1.2仪器与设备
7890A气相色谱仪:美国安捷伦科技公司;摩尔实验室超纯水器:上海摩勒生物科技有限公司。
1.3方法
1.3.1色谱条件
检测器:氢火焰离子化检测器(flame ionization ditector,FID);色谱柱:DB-624UI(60 m×0.32 mm×1.8 μm);柱温:初始温度为80℃,以3℃/min升至110℃,再以45℃/min升至200℃,保持8 min;进样口温度为220℃,进样量为1 μL,分流比为10∶1;检测器温度为220℃,氢气(H2)∶空气(O2)∶尾吹气(N2)=40∶400∶30;载气流速为2.5 mL/min。
1.3.2内标溶液的制备
精密量取乙酸正戊醇2.0 mL,置于100 mL容量瓶中,用体积分数60%乙醇稀释至刻度,摇匀,作为内标溶液。
1.3.3标准溶液的制备
精密量取乙酸乙酯、己酸乙酯、乳酸乙酯、丁酸乙酯、丙酸乙酯、甲醇、正丙醇、β-苯乙醇各2.0 mL,置于100 mL容量瓶中,用体积分数60%乙醇稀释至刻度,摇匀,作为标准储备溶液。该标准储备液各组分体积分数分别为2%。
精密吸取上述标准储备溶液1.0 mL,移入100 mL容量瓶中,加入内标溶液1.0 mL,用体积分数60%乙醇溶液稀释至刻度,摇匀,作为标准工作溶液。
1.3.4样品溶液的制备
吸取样品10.0 mL置于10 mL容量瓶中,加入内标溶液0.10 mL,摇匀,作为样品溶液。
1.3.5标准曲线的绘制
精密量取标准储备溶液0、0.25 mL、0.50 mL、1.00 mL、2.00 mL、4.00 mL,置于100 mL容量瓶中,分别加入内标溶液1.0 mL,用体积分数60%乙醇溶液稀释至刻度,摇匀,制备成体积分数为0、0.005%、0.010%、0.020%、0.040%、0.080%的标准溶液。
1.3.6计算方法
(1)校正因子(f值)的计算:
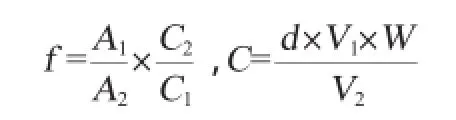
式中:f为各物质的相对校正因子;A1为内标物的峰面积;A2为被测组分标样的峰面积;C1为内标物的质量浓度,g/mL;C2为被测组分标样的质量浓度,g/mL;C为内标物或被测组分标样的质量浓度,g/mL;d为内标物或被测组分的密度;W为内标物或被测组分标样的纯度;V1为内标物或被测组分标样的取样量,mL;V2为内标物或被测组分标样的定容体积,mL。
(2)各物质含量的计算:
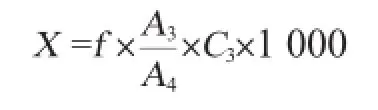
式中:X为样品中各物质的含量,g/L;A3为样品中被测组分的峰面积;A4为添加于样品中内标的峰面积;C3为添加于样品中内标的质量浓度,g/mL。
2 结果与分析
2.1色谱柱的选择
试验中分别将HP-INNOWAX(30m×0.32mm×0.25μm)、DB-FFAP(30m×0.32mm×0.25μm,30m×0.32mm×1.0 μm)和DB-624UI(60 m×0.32 mm×1.8 μm)色谱柱进行对比试验。当使用HP-INNOWAX和DB-FFAP色谱柱时,样品中杂质与某些被测成分不能完全分离,而选用DB-624UI时能把杂质和被测成分很好地分离,并且具有良好的灵敏度。
2.2色谱条件的选择
试验考察了不同的初始温度(35℃、40℃、50℃、60℃、80℃、100℃)与不同分流比组合色谱条件对被测成分分离度的影响,得到最佳色谱条件。即柱温:初始温度为80℃,以3℃/min升至110℃,再以45℃/min升至200℃,保持8 min;进样口温度为220℃,进样量为1 μL,分流比为10∶1;检测器温度为220℃,氢气(H2)∶空气(O2)∶尾吹气(N2)=40∶400∶30;载气流速为2.5 mL/min。
2.3系统适用性考察
精密吸取标准工作溶液和样品溶液(SP20140484)各1 μL注入气相色谱仪,按“1.3.1”中色谱条件测定,记录色谱图,结果见图1。由图1可知,各被测组分理论塔板数均达到5 000以上,标准溶液和样品溶液中被测组分均能良好分离。
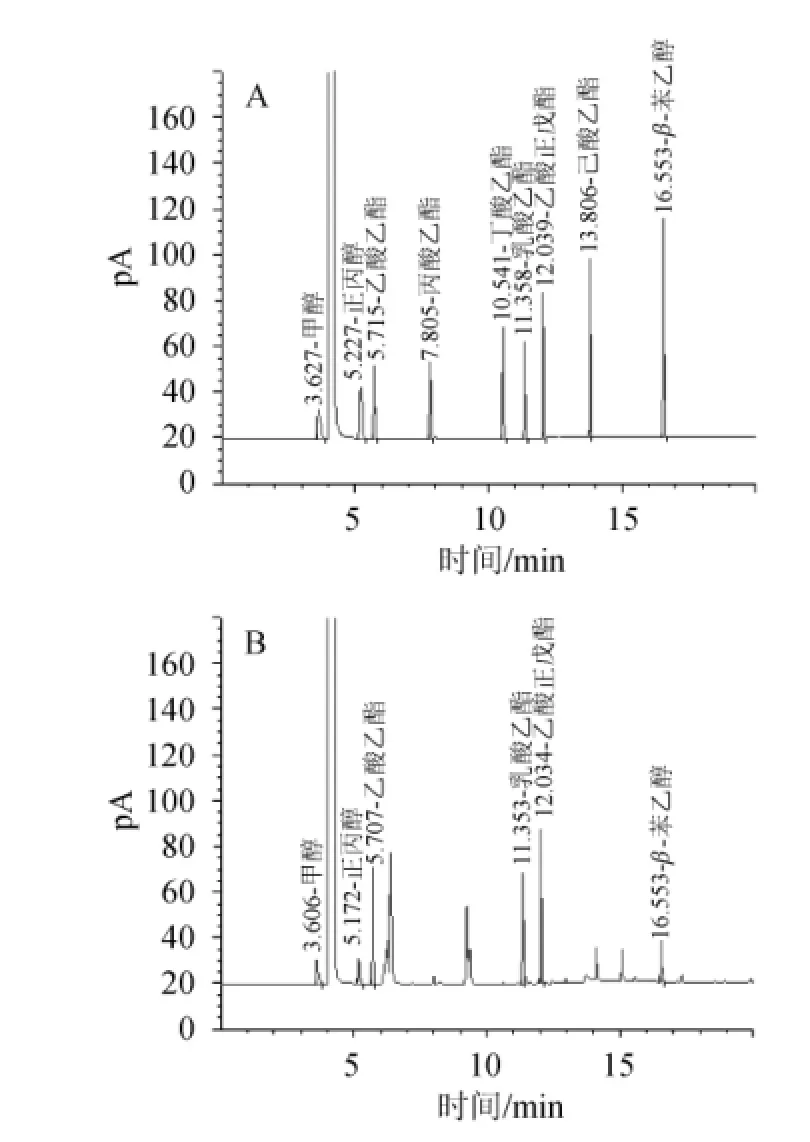
图1 标准溶液(A)和样品溶液(B)的气相色谱图Fig.1 GC chromatograms of standard solution(A)and sample solution(B)
2.4校正因子(f值)的测定
精密吸取标准工作溶液1μL注入气相色谱仪,按“1.3.1”项下色谱条件测定,得到各组分的保留时间、平均校正因子及相对标准偏差(relative standard deviation,RSD)见表1。

表1 各组分的保留时间及平均校正因子(n=3)Table 1 The retention time and the mean correction factor of components(n=3)
由表1可知,8种被测组分在20 min内出峰,大大缩短了检测时间,且各组分平均校正因子RSD均<2.0%。
2.5线性关系考察
分别精密吸取不同体积分数的标准溶液1 μL注入气相色谱仪,测定。以各组分的体积分数(%)作为横坐标(x),各组分峰面积与乙酸正戊酯峰面积的比值作为纵坐标(y),制作标准曲线,各组分线性回归方程及相关系数R2结果见表2。

表2 各组分线性方程Table 2 The linear equation of components
由表2可知,各组分在0~0.08%范围内,各组分相关系数R2≥0.998 7,表明二者线性关系均良好。
2.6精密度试验
精密吸取标准工作溶液1 μL,连续进样6次,结果见表3。由表3可知,各组分的RSD值在0.03%~0.60%,表明该法精密度良好。
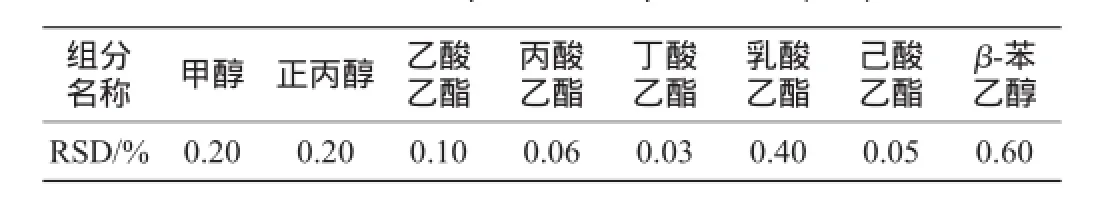
表3 精密度试验结果(n=6)Table 3 Results precision experiments(n=6)
2.7检出限的测定
将标准储备溶液稀释进样测定,检出限按3倍信噪比计算,结果见表4。
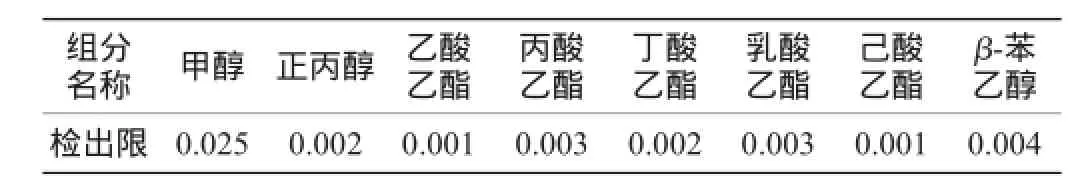
表4 被测组分的检出限Table 4 Detection limits of componentsg/L
2.8加标回收率试验
将标准储备溶液稀释至体积分数为0.025%,分别吸取1mL、2mL、3mL加入10mL容量瓶中,用样品(SP20140484)稀释至刻度,并加入内标溶液0.10 mL,混匀,制成回收样品溶液。分别精密吸取1 μL注入气相色谱仪,记录峰面积,计算回收率,结果见表5。

表5 加标回收率测定结果Table 5 Determination results of adding standard recovery rate
由表5可知,各组分回收率为82.22%~103.83%,RSD为0.2%~1.5%,说明该法准确度高,能满足检测需要。
2.9样品的测定
10批白酒检品,按照“1.3.4”中的方法制备样品溶液,分别精密吸取1 μL注入气相色谱仪,记录色谱图。按内标法计算各组分含量,结果见表6。
由表6可知,10批样品中均未检出丙酸乙酯,其他被测组分则在不同香型白酒中含量各有高低,体现了不同醇类、酯类在不同香型白酒中的呈香作用。
2.10讨论
GB/T 10345—2007《白酒分析方法》中建议使用的毛细管柱为LZP-930白酒分析专用柱或FFAP毛细管柱或其他具有同等分析效果的毛细管柱,根据已有的毛细管柱,在试验中对HP-INNOWAX(30 m×0.32 mm×0.25 μm)、DB-FFAP(30m×0.32mm×0.25μm,30m×0.32mm×1.0μm)和DB-624UI(60 m×0.32 mm×1.8 μm)色谱柱进行了比较,结果发现DB-624UI色谱柱分析效果最佳,于是选定该柱进行测定。在色谱柱选择过程中,同时进行了色谱条件的筛选,并着重进行了初始温度的选择。不同的初始温度对低沸点物质的分离有较大的影响,考察了初始温度分别为35℃、40℃、50℃、60℃、80℃、100℃时的分离效果,最终选定80℃为初始温度。
3 结论
本试验建立了同时测定白酒中乙酸乙酯、己酸乙酯、乳酸乙酯、丁酸乙酯、丙酸乙酯和甲醇、正丙醇、β-苯乙醇8种物质的气相色谱方法,研究表明,该方法简单快捷、分离效果好、准确度高,能满足白酒风味成分检测的需要。
[1]中华人民共和国国家质量监督检验检疫总局.GB/T 10345—2007白酒分析方法[S].北京:中国标准出版社,2007.
[2]中华人民共和国卫生部.GB/T 5009.48—2003蒸馏酒及配制酒卫生标准的分析方法[S].北京:中国标准出版社,2003.
[3]郑校先,陈丽花,方逸群.气相色谱分析黄酒中β-苯乙醇、醛类及酯类的研究[J].中国酿造,2009,28(12):121-123.
[4]李支星.应用大口径毛细管柱气相色谱法检测白酒中醇类和酯类成分[J].食品安全导刊,2012(8):46-47.
[5]张雅琪,贾梅珍,杨天宝,等.毛细管气相色谱法同时检测白酒中31种微量成分的研究[J].农产品加工·学刊,2014(8):35-37.
[6]王宇.气相色谱(内标)法测定酒中甲醇、高级醇含量[J].现代预防医学,2010,37(1):90-91.
[7]霍权恭.毛细管气相色谱分析白酒中醇类与酯类[J].食品科学,2012,33(18):243-245.
[8]孟佩俊,梁青青,张丽萍,等.气象色谱法分析白酒中甲醇、杂醇油和乙酸乙酯的含量[J].包头医学院学报,2011,27(6):27-29.
[9]王延云,胡强,李超豪,等.气相色谱测定白酒中乙酸乙酯含量的方法[J].食品研究与开发,2013(8):91-93.
[10]任玉兰,田密,李春彦,等.白酒中微量组分的气相色谱分析[J].中国酿造,2011,30(7):177-179.
[11]韩深,刘伟华,古瑾,等.气相色谱法测定蒸馏酒中多种风味成分[J].现代仪器与医疗,2013,19(1):9-15.
[12]王健,艾涛波,岳清洪.固相萃取和同位素内标法检测白酒中氨基甲酸乙酯[J].中国酿造,2015,34(1):115-117.
[13]霍丹群,张苗苗,侯长军,等.基于主成分分析和判别分析的白酒品牌鉴别方法[J].农业工程学报,2011,27(2):297-301.
[14]张丽敏,胡永刚,史静霞,等.清香型白酒陈酿过程中微量成分变化规律研究[J].山西大学学报:自然科学版,2002,25(4):334-337.
[15]李莹.白酒中甲醇分析方法的研究[J].酿酒,2010,37(2):77-78.
[16]伊雄海,郭德华,邓晓军,等.多维气相色谱法检测酒中甲醇[J].分析化学研究简报,2011,39(5):705-708.
Simultaneous determination of eight compounds in Chinese liquor by GC
HONG Wei,FU Chuanwu
(Guangxi Liuzhou Institute for Food and Drug Control,Liuzhou 545006,China)
The concentration of ethyl acetate,ethyl hexanoate,ethyl lactate,ethyl butyrate,ethyl propanoate,methanol,n-propanol,and β-phenylethanol in Chinese liquor were determined by GC.The samples were separated by DB-624UI(60 m×0.32 mm×1.8 μm)capillary column,and then detected by FID detector.The method had a good linearity in the range of 0.00%-0.08%(v/v),theR2were all over 0.990.The relative standard deviation(RSD)ofprecisionwas0.03%-0.60%,andthedetectionlimitsofcomponentswere0.001-0.025g/L.Therecoverieswerebetween82.22%-103.83%,with the RSD from 0.2%to 1.8%.The results showed the method has realized a good separation,which was suitable for the determination of eight compounds in liquor.
gas chromatography;Chinese liquor;eight compounds;simultaneous determination
O657.71
A
0254-5071(2015)10-0134-04
10.11882/j.issn.0254-5071.2015.10.030
2015-09-15
洪薇(1982-),女,主管中药师,本科,主要从事食品药品检测工作。
