p38/ATF-2通路参与C反应蛋白诱导的内皮细胞活化*
2015-09-18刘少军李沅美刘慰华熊龙根刘世明广州医科大学附属第二医院广州心血管疾病研究所心内科广东广州5060广东药学院生命科学与生物制药学院广东广州50006
刘少军,李沅美,刘慰华,熊龙根,刘世明△(广州医科大学附属第二医院广州心血管疾病研究所/心内科,广东广州5060;广东药学院生命科学与生物制药学院,广东广州50006)
p38/ATF-2通路参与C反应蛋白诱导的内皮细胞活化*
刘少军1,李沅美2,刘慰华1,熊龙根1,刘世明1△
(1广州医科大学附属第二医院广州心血管疾病研究所/心内科,广东广州510260;2广东药学院生命科学与生物制药学院,广东广州510006)
目的:考察p38 MAPK/ATF-2通路在C反应蛋白(CRP)诱导的内皮细胞活化中的作用。方法:采用培养的人冠状动脉内皮细胞(HCAEC)第3~7代用于实验。CRP刺激诱导内皮细胞活化,给予p38抑制剂SB203580和SB202190干预。免疫印迹法检测p-eNOS、p-p38和p-ATF2的水平;ELISA法测定HCAEC分泌的黏附分子ICAM-1、VCAM-1和MCP-1的变化。结果:CRP呈浓度依赖性地抑制p-eNOS水平,CRP诱导HCAEC分泌ICAM-1、VCAM-1和MCP-1;CRP激活p38/ATF-2通路;SB203580和SB202190部分恢复p-eNOS水平和抑制CRP诱导的ICAM-1、VCAM-1和MCP-1分泌。结论:p38 MAPK/ATF-2通路参与CRP诱导的HCAEC活化。
p38 MAPK/ATF-2通路;C反应蛋白;内皮细胞活化;动脉粥样硬化
[ABSTRACT]AIM:To investigate the role of p38 MAPK/ATF-2 pathway in C-relative protein(CRP)-induced endothelial cell activation.METHODS:Human coronary artery endothelial cells(HCAEC)were cultured and were used between passages 3 and 7.CRP served as a stimulus for endothelial cell activation.Western blotting was performed to determine the expression and phosphorylation of eNOS,p38 and ATF2.ELISA was carried out to detect the levels of ICAM-1,VCAM-1 and MCP-1 released from HCAEC.Pharmacological p38 inhibitors SB203580 and SB202190 were used to determine the effect of p38/ATF-2 pathway.RESULTS:CRP reduced the p-eNOS level in a concentration-dependentmanner and induced the release of ICAM-1,VCAM-1 and MCP-1.The p38/ATF-2 pathway was activated by CRP treatment.SB203580 and SB202190 partially rescued p-eNOS level and suppressed the secretion of ICAM-1,VCAM-1 and MCP-1.CONCLUSION:p38MAPK/ATF-2 pathway participates in CRP-induced endothelial activation.
[KEY WORDS]p38 MAPK/ATF-2 pathway;C-relative protein;Endothelial activation;Atherosclerosis
动脉粥样硬化(atherosclerosis,AS)被视为是一种炎症性的疾病[1]。C反应蛋白(C-reactive protein,CRP)是机体在炎症或组织损伤后而产生的急性期反应蛋白和非特异性的炎症标志物[2]。近来研究表明CRP还可作为AS、心肌梗死等的心血管疾病危险的预测因子[3-4]。CRP在AS中重要作用之一是诱导内皮型(endothelial cell,EC)活化。EC活化被认为是AS的起始环节。活化的EC表现为内皮型一氧化氮合酶(endothelial nitric oxide synthase,eNOS)的活性降低,细胞间黏附分子1(intercellular adhesionmolecule-1,ICAM-1)、血管细胞黏附分子1(vascular cell adhesion molecule-1,VCAM-1)、E-selectin和单核细胞趋化蛋白1(monocyte chemoattractant protein-1,MCP-1)分泌增加[3,5]。目前CRP诱导内皮细胞活化的分子机制尚未完全清楚。本研究主要考察p38 MAPK/ATF-2通路在CRP诱导的人冠状动脉内皮细胞(human coronary artery endothelial cells,HCAEC)活化中的作用。
材料和方法
1材料
培养基EGM-2购自Lonza;CRP购自Trichem Rsources和Calbiochem;除抗体GAPDH购自Santa Cruz外,其余抗体均购自Cell Signaling;抑制剂SB203580和SB202190分别购自Enzo Life Sciences和Calbiochem;ICAM-1和VCAM-1的ELISA试剂盒购于eBioscience;MCP-1的ELISA试剂盒购于BD。
2方法
2.1HCAEC的培养HCAEC(Cell Applications)的培养按照说明书进行。本实验使用的HCAEC介于3~7代之间。实验处理细胞之前,使用含0.1%胎牛血清、不含细胞因子的EGM-2基础培养基培养24 h。
2.2免疫印迹(Western blotting)检测参照已经发表的文章进行[5-6]。各组细胞裂解后定量(Bio-Rad Laboratories)。用Laemm li buffer(62.5 mmol/L Tris-HCl,pH 6.8,2%SDS,10%glycerol,50 mmol/L dithiothreitol,0.1%bromphenol blue)上样,用8%或者12%的SDS-PAGE进行蛋白分离,然后转印到PVDF膜(GE Healthcare)上。5%的脱脂奶粉(Bio-Rad)封闭后,相应的抗体孵育4℃过夜。孵育HRP标记的II抗后进行ECL曝光。
2.3ELISA检测HCAEC处理后收集细胞培养液。离心后回收上清液。按照eBioscience或者BD Biosciences的说明书进行操作。最后在酶标仪上以450 nm的波长进行读数。
3统计学处理
检测的数据采用SPSS 13.0统计软件包进行统计分析,多组比较用单因素方差分析、LSD法,两组间比较用t检验。统计数据以均数±标准差(mean ±SD)表示。以P<0.05为差异有统计学意义。
结果
1CRP诱导EC活化
内皮细胞活化的主要标志是eNOS活性下降和黏附分子(ICAM-1、VCAM-1和MCP-1等)的分泌。Ser1177位的磷酸化调控是eNOS活性调节的最重要的一种方式,因此p-Ser1177水平能够反映eNOS的活性。我们首先观察到各浓度CRP(0、12.5、25、50和100 mg/L)刺激后HCAEC细胞形态没有明显改变。免疫印迹结果表明,eNOS的Ser1177位磷酸化水平呈浓度依赖性下降,表明CRP抑制eNOS活性。同时ELISA检测表明,与对照组相比,CRP(50 mg/ L)处理组的ICAM-1、VCAM-1和MCP-1的表达水平分别是对照组的2.83、4.80和2.03倍,见图1。这些结果表明,CRP活化内皮细胞,与之前的报道一致[6-8]。

Figure 1.CRP induced HCAEC activation.A:typical images of cellular morphology;B:the phosphorylation of eNOS detected by Western blotting;C:HCAEC culture supernatantwas analyzed by ELISA.Mean±SD.n=3.*P<0.05 vs control.图1 CRP诱导HCAEC活化
2CRP激活p38/ATF2通路
免疫印迹实验观察到CRP呈浓度依赖性地诱导p38的Thr180/Tyr182磷酸化水平(p-p38)增加,而p38的总蛋白表达不变。同时,p38的底物ATF2的Thr69/71磷酸化水平(p-ATF2)增加,见图2。这表明CRP激活p38/ATF2通路。
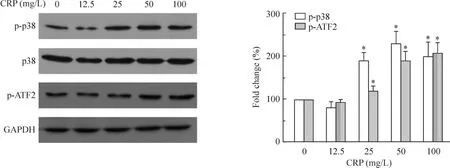
Figure 2.CRP activated p38 MAPK/ATF2 pathway in the HCAEC.Mean±SD.n=3.*P<0.05 vs control.图2 CRP激活p38/ATF2通路
3p38/ATF2部分参与CRP诱导的eNOS活性下降
用2个p38抑制剂SB203580和SB202190进行干预,结果发现SB203580和SB202190在抑制CRP诱导的p-p38和p-ATF2增加的同时,还增加p-eNOS的表达水平,见图3。这说明抑制p38/ATF2能够部分恢复eNOS的活性。
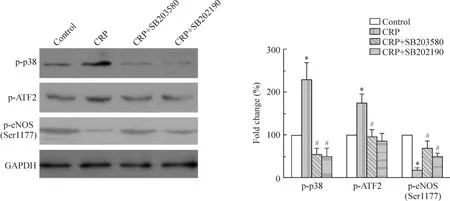
Figure 3.p38 inhibitors partially recovered the phosphorylation level of eNOS at Ser1177 in the HCAEC.Mean±SD.n=3.*P<0.05 vs control;#P<0.05 vs CRP.图3 p38抑制剂部分恢复p-eNOS水平
4p38抑制剂对黏附分子分泌的影响
ELISA结果显示,SB203580和SB202190能够有效抑制CRP诱导的ICAM-1、VCAM-1和MCP-1分泌,见图4。综合上述结果,p38/ATF2部分介导CRP诱导的eNOS活性下调和黏附分子(ICAM-1、VCAM-1和MCP-1)的分泌,即p38/ATF2参与CRP诱导的内皮细胞活化过程。
讨论
大量的研究表明CRP是心血管疾病强有力的、独立的预测因子[3-4]。流行病学调查、临床药物试验和实验室研究都表明CRP在AS的发生发展中发挥重要作用。CRP能够活化EC、造成内皮功能障碍、促进血管平滑肌细胞的增殖和迁移、诱导黏附分子分泌进而募集单核细胞入侵血管壁等等[3,5];CRP对EC的损伤主要是抑制eNOS活性、促进黏附分子分泌、产生活性氧簇以及促进氧化型低密度脂蛋白的摄取等[3,9]。

Figure 4.Inhibition of VCAM-1,ICAM-1 and MCP-1 releases from the HCAEC by p38 inhibitors.Mean±SD.n= 3.*P<0.05 vs control;#P<0.05 vs CRP.图4 SB203580和SB202190抑制黏附分子的分泌
本研究主要探讨CRP诱导EC活化的分子机制,重点集中在p38/ATF2通路上。我们观察到p38抑制剂SB203580和SB202190在抑制CRP诱导的p38/ATF2激活同时,还能部分恢复eNOS活性和抑制黏附分子(ICAM-1、VCAM-1和MCP-1)分泌,表明p38/ATF2通路部分介导了CRP诱导的EC活化。
p38 MAPK是一个在真核生物中高度保守的丝裂原蛋白激酶家族。p38信号通路在细胞外界应激反应中发挥极其重要的作用,几乎所有有害的外部刺激或内部损伤均可以激活p38信号通路。本研究证实p38/ATF2通路参与CRP诱导的EC活化过程,为揭示EC损伤的分子机制甚至寻找AS的防治靶点提供有益线索。事实上,他汀类药物可以通过降低p38 MAPK信号通路的活性[10],发挥抑制CRP诱导的内皮细胞损伤的效应[11]。
本研究不足之处在于没有探讨p38通路激活与EC活化的内在机制,即p38/ATF2激活与抑制eNOS活性,以及与促进ICAM-1、VCAM-1和MCP-1分泌之间的直接分子关系。已有报道表明CRP通过CD32受体激活p38激酶,进而激活NF-κB促进黏附分子VCAM-1的表达[12-14]。p38/NF-κB通路在CRP诱导的EC活化中的作用也是我们后续的研究内容之一。
[1]Ross R.Atherosclerosis:an inflammatory disease[J].N Engl JMed,1999,340(2):115-126.
[2]Du Clos TW.Function of C-reactive protein[J].Ann Med,2000,32(4):274-278.
[3]Ferri C,Croce G,Cofini V,etal.C-reactive protein:interaction with the vascular endothelium and possible role in human atherosclerosis[J].Curr Pharm Des,2007,13 (16):1631-1645.
[4]Koenig W.Predicting risk and treatment benefit in atherosclerosis:the role of C-reactive protein[J].Int JCardiol,2005,98(2):199-206.
[5]Liu SJ,Liu WH,Zhong Y,et al.Glycogen synthase kinase-3βis involved in C-reactive protein-induced endothelial cell activation[J].Biochemistry(Mosc),2013,78 (8):915-919.
[6]Liu SJ,Zhong Y,You XY,et al.Insulin-like growth factor 1 opposes the effects of C-reactive protein on endothelial cell activation[J].Mol Cell Biochem,2014,385(1-2):199-205.
[7]Pasceri V,Willerson JT,Yeh ET.Direct proinflammatory effectof C-reactive protein on human endothelial cells[J].Circulation,2000,102(18):2165-2168.
[8]LiHY,Wang J,Wu YX,etal.Topological localization of monomeric C-reactive protein determines proinflammatory endothelial cell responses[J].J Biol Chem,2014,289 (20):14283-14290.
[9]Bian F,Yang X,Zhou F,et al.C-reactive protein promotes atherosclerosis by increasing LDL transcytosis across endothelial cells[J].Br JPharmacol,2014,171(10): 2671-2684.
[10]陈埏芳,钟健,汤绍辉,等.辛伐他汀通过抑制p38 MAPK活化降低肝硬化门静脉高压大鼠门静脉压力[J].中国病理生理杂志,2013,29(2):205-209.
[11]钟钧琳,彭隆,罗艳婷,等.瑞舒伐他汀抑制C-反应蛋白诱导的晚期内皮祖细胞炎症因子的表达[J].中国病理生理杂志,2013,29(4):597-602.
[12]Kawanami D,Maemura K,Takeda N,et al.C-reactive protein induces VCAM-1 gene expression through NF-κB activation in vascular endothelial cells[J].Atherosclerosis,2006,185(1):39-46.
[13]Liang YJ,Shyu KG,Wang BW,et al.C-reactive protein activates the nuclear factor-κB pathway and induces vascular cell adhesion molecule-1 expression through CD32 in human umbilical vein endothelial cells and aortic endothelial cells[J].JMol Cell Cardiol,2006,40(3):412-420.
[14]Qamirani E,Ren Y,Kuo L,et al.C-reactive protein inhibits endothelium-dependent NO-mediated dilation in coronary arterioles by activating p38 kinase and NAD(P)H oxidase[J].Arterioscler Thromb Vasc Biol,2005,25 (5):995-1001.
p38 MAPK/ATF-2 pathway is involved in C-relative protein-induced endothelial cell activation
LIU Shao-jun1,LIYuan-mei2,LIUWei-hua1,XIONG Long-gen1,LIU Shi-ming1
(1Department of Cardiology,Guangzhou Institute of Cardiovascular Disease,Second Affiliated Hospital of Guangzhou Medical University,Guangzhou 510260,China;2College of Life Science and Bio-pharmaceutics,Guangdong Pharmaceutical U-niversity,Guangzhou 510006,China.E-mail:gzliushiming@126.com)
R541
A
10.3969/j.issn.1000-4718.2015.05.007
1000-4718(2015)05-0808-04
2014-11-20[修回日期]2015-01-04
国家自然科学基金资助项目(No.81300151);广东省自然科学基金重点项目(No.S2011020002143)
△通迅作者Tel:020-34153522;E-mail:gzliushiming@126.com
