shRNA靶向沉默HSV—2 UL54基因在HEK293细胞内的表达
2015-09-09吕延成潘晓瑜黄畅等
吕延成 潘晓瑜 黄畅等

摘要:根据乙型单纯疱疹病毒(HSV-2)UL54基因序列,设计并合成特异性的小干扰片段,将其定向克隆至真核表达载体pGPU6/GFP/Neo中,经脂质体介导转染HEK293细胞,倒置荧光显微镜和流式细胞仪检测转染效率,MTT法检测HEK293细胞的存活率,RT-PCR检测UL54基因mRNA的表达,Western blot检测UL54基因编码蛋白质的表达,终点滴定法测定细胞上清液中的病毒感染滴度。结果显示, shRNA1081能抑制UL54 基因mRNA和蛋白质的表达,能显著降低子代病毒滴度,提高细胞的存活率。表明本研究构建的重组表达载体pGPU6/GFP/Neo-UL54 shRNA能在HEK293细胞中表达,并抑制HSV-2复制。
关键词:UL54基因;RNA干扰;短发夹RNA;真核表达载体;2型单纯疱疹病毒
中图分类号:R373 文献标识码:A 文章编号:0439-8114(2015)15-3779-05
DOI:10.14088/j.cnki.issn0439-8114.2015.15.052
Abstract: In search of new anti-virus strategy,targeting herpes simplex virus type 2 (HSV-2) UL54 gene and based on the rule of shRNA design, DNA fragment targeting conserved sequences of UL54 was synthesized and cloned into a plasmid vector pGPU6/GFP/Neo, and then transferred into human embryonic kidney(HEK) 293 cells by lipofectamine. Parameters including transfection efficiency,cell survival rate, expression level of UL54 mRNA and protein, and viral titer in supernatants collected from HSV-2 infected cell, were detected by fluorescence microscopy and flow cytometry,MTT,real-time fluorescent quantitative PCR, western blotting, and end-point assay respectively. The results showed that, shRNA1081 inhibited UL54 mRNA expression and significantly decreased target gene protein expression, markedly reduced TCID50 in HSV-2 infected cells at 48 hours post-infection, and increased survival rate of cells. It revealed that pGPU6/GFP/Neo-UL54 shRNA could express in HEK 293 cells and inhibit HSV-2 replication.
Key words:UL54 gene; RNA interference; shRNA; eukaryotic expression vector; herpes simplex virus type 2
生殖器疱疹(Genital herpes, GH)是一种反复发作、难以控制的溃疡性疾病,主要由2型单纯疱疹病毒(Herpes simplex virus,HSV-2)引起,目前还无特效药物控制HSV-2的感染和复发。
RNA干扰(RNA interference,RNAi)是一种特异性基因沉默技术,能够使mRNA发生降解而导致基因表达沉默,它为靶向防治HSV-2提供了新思路。目前国内外运用RNAi技术特别是针对HSV-2的研究报道较少,其中绝大多数都是直接应用化学合成的siRNA(Small interfering RNA)针对HSV-2进行干扰[1,2],但是化学合成的siRNA通过脂质体介导进入细胞易被RNase降解,沉默效应持续的时间较短。本试验采用的是通过构建带有RNA聚合酶Ⅲ启动子的重组表达载体,转录出具有发夹结构的双链RNA(Small hairpin RNA, shRNA)。shRNA在Dicer酶作用下转化成21~25 nt的siRNA,可使构建载体在细胞内表达的siRNA持续时间长,稳定性强,是一种较理想的RNAi研究方法。
HSV-2是双链线性DNA,基因组约为150 kb,编码70多种蛋白质。HSV-2基因组表达具有很高的时序性,按照基因表达的先后顺序可将HSV-2病毒基因分为立即早期基因、早期基因和晚期基因,其中有多个基因在病毒复制和繁殖的过程中发挥重要作用,这些主要功能基因都可能成为RNAi抑制HSV-2的靶基因。立即早期基因编码5种细胞感染蛋白质(Infect cell protein,ICP),包括ICP0、ICP4、ICP22、ICP27、ICP47。UL54基因属于HSV-2立即早期基因,编码的ICP27蛋白质是HSV-2病毒复制所必需的一种关键多功能蛋白质,主要调节病毒和宿主细胞mRNA的合成与成熟,运输细胞核的mRNA到细胞质中[3,4],能激活病毒晚期基因的表达,并与ICP0、ICP4一起调控早期基因和晚期基因的表达[5-7],刺激病毒转录翻译[8]。有研究证明,ICP27蛋白质一旦突变可影响病毒在宿主内的复制[9,10],在病毒的激活过程中可以激活p38与JNK信号通路而使细胞发生调亡,因此ICP27被认为在病毒激活过程中起着重要作用。所以编码ICP27蛋白质的UL54基因应是特异siRNA干扰的考虑位点。因此,针对HSV-2 UL54基因筛选设计合适的干扰位点,构建4个shRNA重组表达载体,建立pGPU6/GFP/Neo-UL54 shRNA在人胚胎肾细胞(HEK293)中高表达的模型,筛选出有效抑制UL54基因表达的shRNA干扰序列,为进一步研究利用RNA干扰技术抑制HSV-2复制作用奠定了基础。
1 材料与方法
1.1 材料
HSV-2 333标准株来源于美国细胞收藏中心,HEK293和Escherichia coli DH5α由遵义医学院中心实验室提供,质粒pGPU6/GFP/Neo为上海吉玛制药技术有限公司产品,限制性内切酶BamH Ⅰ、BbsⅠ、Pst Ⅰ为美国Fermentas公司产品,T4 DNA连接酶为杭州碧云天生物技术研究所产品,RNA提取试剂TRIzol、SYBR?誖 PrimeScript?誖 RT-PCR Kit为宝生物工程(中国大连)有限公司产品,DMEM培养基为美国GIBCO公司产品,新生牛血清为杭州四季青公司产品,转染试剂Lipofectamine2000为Invitrogen公司产品,鼠抗ICP27单抗为Abcam公司产品,PCR引物由上海生物工程技术服务有限公司合成。
1.2 短发夹RNA(shRNA)靶序列的设计
从GenBank上获得HSV-2(NC_001798)UL54基因序列,按照shRNA设计原则,针对HSV-2的UL54基因序列保守区域各筛选设计、合成4条干扰靶序列,分别命名为UL54 shRNA1081、UL54 shRNA1092、UL54 shRNA1276、UL54 shRNA1407,同时设计不针对任何基因的序列为阴性对照(Negative control,NC)。所设计的寡核苷酸链由上海吉玛制药技术有限公司化学合成,详见表1。
1.3 pGPU6/GFP/Neo-UL54 shRNA表达载体的构建和鉴定
合成编码发夹结构shRNA的正义链和反义链分别用无核酸酶的无菌水稀释成50 mol/L,按照退火缓冲液的说明配制退火反应体系(Nuelease-free water 40 μL,退火缓冲液20 μL,50 μmol/L的shRNA的正义链和反义链各20 μL)。退火反应步骤为:95 ℃ 2 min,每8 s下降1 ℃,降至25 ℃。退火产物储存于-20 ℃。取pGPU6/GFP/Neo空载体用BamH Ⅰ、Bbs Ⅰ于37 ℃酶切2 h,酶切后产物进行琼脂糖凝胶电泳回收,电泳鉴定后与siRNA小片段进行连接,16 ℃连接过夜,连接产物转化E. coli DH5a感受态细胞,涂布于含Kana抗性的LB平板上,37 ℃恒温培养箱中培养过夜,挑取单克隆菌落接种于含Kana抗性的LB培养液中,37 ℃恒温摇床培养过夜,收集菌液,小量快速抽提质粒DNA,提取的质粒分别用BamHⅠ、PstⅠ双酶切鉴定。
1.4 细胞培养和质粒转染
HEK293细胞用含10%小牛血清的DMEM完全培养基在37 ℃、5%CO2及饱和湿度条件下进行常规的细胞培养,每隔2 d换液。选取对数生长期的HEK293细胞,转染前1 d,在24孔细胞培养板里接种500 μL的HEK293细胞(0.8×105~1.0×105个细胞/mL),37 ℃、5%CO2培养箱中培养至单层细胞汇合度为70%~80%时即可进行转染。质粒和lipofectamin2000转染试剂的比例为0.8 μg∶2.0 μL,转染48 h后在倒置荧光显微镜下观察荧光表达情况并利用流式细胞仪检测转染效率。
1.5 病毒的接种及子代病毒滴度的检测
HSV-2感染HEK293细胞,并于显微镜下观察细胞病变,用终点滴定法检测子代病毒滴度。按Reed-Muench法计算能引起50%细胞发生病变的病毒最高稀释度(50% tissue culture infective dose, TCID50),即为病毒滴度。
1.6 MTT法检测HEK293细胞存活率
按0.5×105~1.0×105个细胞/mL细胞密度接种到96孔培养板进行培养,每孔体积100 μL,接种病毒48 h后弃上清,每孔加MTT溶液(5 mg/mL) 10 μL,继续孵育4 h,终止培养,吸去孔内培养上清液,每孔加入100 μL DMSO,脱色摇床上振荡10 min,使结晶物充分溶解。以无细胞孔作为空白对照(仅加入MTT和DMSO),利用酶标免疫检测仪在波长492 nm下测定各孔光吸收值,计算细胞存活率。细胞存活率=(A实验组-A空白组)/(A对照组-A空白组)×100%。
1.7 实时荧光定量PCR检测UL54 基因mRNA的表达
Trizol提取细胞总RNA,逆转录为cDNA用于后续PCR扩增。采用引物设计软件PrimerPremier 5.0设计UL54基因和管家基因GAPDH的上下游引物,以GAPDH基因作为内参对照检测各组细胞内mRNA表达水平,引物由上海生物工程技术服务有限公司合成,PAGE纯化,浓度为0.5 μmol/μL。引物序列如下:UL54基因上游引物:5′-CCAGGACCCTATCATCGGAACG-3′,下游引物:5′-AGTATTTCAATGAGACCCGCCAT-3′;GAPDH基因上游引物:5′-AGAAGGCTGGGGCTCATTTG-3′,下游引物:5′-AGGGGCCATCCACAGTCTTC-3′。进行PCR反应:95 ℃预变性5 min,95 ℃变性15 s,60 ℃退火15 s,72 ℃延伸32 s(共40个循环)。采用Comparative delta-delta相对定量法计算各组mRNA的表达量。
1.8 Western blot检测蛋白质表达
提取细胞总蛋白质,采用BCA(Bicinchoninic acid)法测定细胞总蛋白质浓度,Western blot法检测蛋白质表达,以GAPDH基因为内参,Western blot条带经Quantity One定量分析软件进行分析。
1.9 统计学处理
利用SPSS 13.0软件进行统计分析,所有数据采用平均数±标准差(x±s)表示,多组间比较采用方差分析,两两组间比较采用LSD-t检验。
2 结果与分析
2.1 表达载体pGPU6/GFP/Neo-shRNA酶切鉴定结果
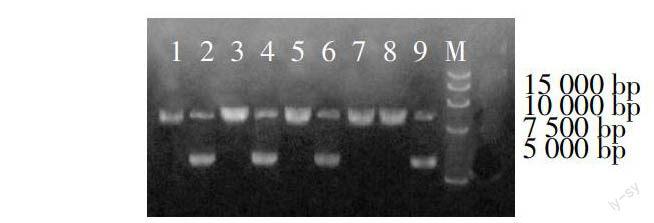
pGPU6/GFP/Neo质粒上有Bbs Ⅰ和BamH Ⅰ酶切位点,在这两个酶切位点之间还有一个Pst Ⅰ酶切位点。shRNA模板成功插入到质粒pGPU6/GFP/Neo上时, Pst Ⅰ酶切位点被置换,因此重组质粒能被BamH Ⅰ酶切开,不能被Pst Ⅰ酶切。Pst Ⅰ酶切结果显示有2条带,分别为超螺旋的SC构型和质粒的松弛开环OC构型,这两条带表明重组质粒不能被Pst Ⅰ酶切。重组体被BamH Ⅰ单酶切而线性化,条带在5 100 bp左右,如图1所示。
2.2 细胞转染效率测定结果
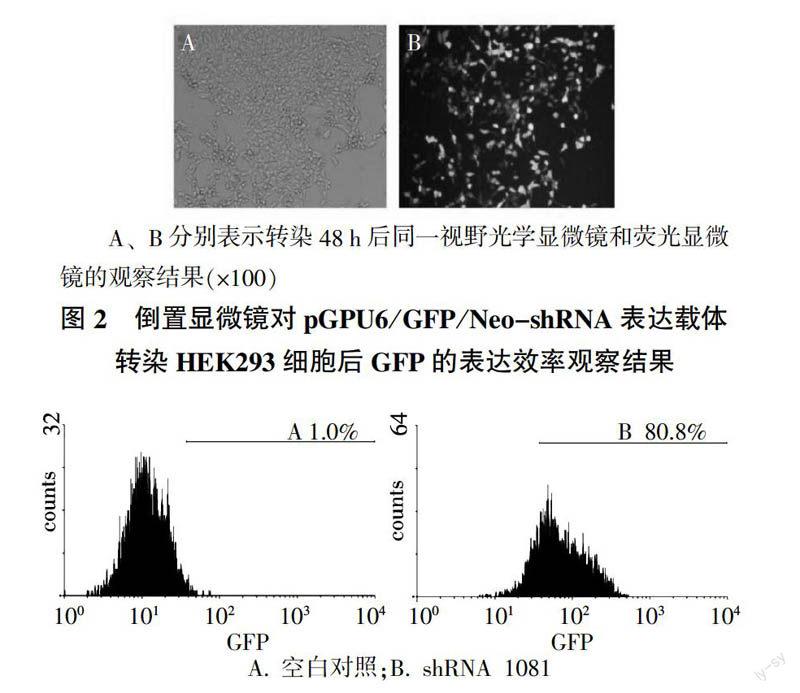
pGPU6/GFP/Neo-shRNA表达载体转染HEK293细胞48 h后,绿色荧光蛋白质(GFP)的表达达到高峰。倒置荧光显微镜观察质粒转染细胞情况如图2所示,流式细胞仪测得转染48 h后转染效率如图3所示,转染效率最高达80.8%。
2.3 HSV-2转染后子代的病毒滴度检测结果
细胞接种HSV-2 48 h后,收集各组病毒上清液进行病毒滴度的测定,病毒滴度用TCID50计算。通过终点滴定法测定HSV-2的TCID50,以确定感染细胞所需的病毒量。结果(表2)显示,空白对照组TCID50为10-5.5±0.5 TU/(100 μL),其含义为将该病毒液稀释10的(5.5±0.5)倍,接种100 μL能使50%细胞发生病变。与空白对照组(空载体)相比,干扰组UL54 shRNA1092、UL54 shRNA1276病毒滴度虽有下降,但差异不显著(P>0.05);其余两干扰组病毒滴度也均有不同程度下降,差异达极显著水平(P<0.01),其中UL54 shRNA 1081组病毒滴度下降最显著。
2.4 UL54基因mRNA表达的实时荧光定量PCR检测结果
接种HSV-2 48 h后,提取各组细胞内HSV-2总RNA,利用实时荧光定量PCR法进行目的基因的mRNA表达水平的检测,结果(表3)显示,UL54 shRNA1081组和UL54 shRNA1407组对UL54基因的mRNA表达抑制率分别为69.61%和51.46%,与空白对照(空载体)组相比,具有显著性差异(P<0.05),而转染对照组(阴性对照组)与空白对照组相比,无显著性差异(P>0.05),UL54 shRNA1081对mRNA表达抑制率最高。
2.5 HEK293细胞存活率的MTT法检测结果
MTT法检测HEK293细胞存活率,结果(图4)表明,UL54 shRNA1081组细胞存活率最高,与对照组的细胞存活率相比,差异显著(P<0.05)。
2.6 HSV-2 UL54基因蛋白质表达的Westernblot 检测结果
Western blot检测结果显示,UL54基因表达的ICP27蛋白质条带位于63 ku位置(图5A)。ICP27蛋白质相对表达量用ICP27条带的灰度值与内参基因GAPDH的灰度值的比值表示,与空白对照组相比,UL54基因各干扰组的蛋白质表达均有不同程度的降低,UL54 shRNA1081组蛋白质表达下降最显著(P<0.05),其次是UL54 shRNA1276组(图5B)。
3 讨论
本研究针对HSV-2 UL54基因筛选设计合适的4个干扰靶位点,构建shRNA重组表达载体,该载体有GFP表达,便于观察和检测转染效率。经酶切鉴定验证,成功构建了4个pGPU6/GFP/Neo-UL54 shRNA真核表达载体。HEK293细胞是HSV-2的易感细胞,通过脂质体介导的pGPU6/GFP/Neo-UL54 shRNA真核表达载体转染HEK293细胞,利用倒置荧光显微镜和流式细胞仪检测到大量绿色荧光蛋白质表达,表明装载到质粒上的基因片段通过脂质体的介导成功转染到HEK293细胞,且转染效率达到80%左右,达到试验要求。结果表明,UL54基因特异性的shRNA1081表达载体能有效抑制HEK293细胞中mRNA和ICP27蛋白质的表达,与空载体相比,mRNA抑制率为69.61%,对蛋白质表达的抑制效果最显著。此外,本研究还通过观察子代病毒滴度的变化来反映病毒的复制情况,但是肉眼观察带有一定的主观性,所以还通过MTT法来检测细胞的存活率,考察shRNA表达载体对宿主细胞的保护情况,与空载体组相比,shRNA1081表达载体能明显降低子代的病毒滴度,细胞的存活率也最高。证实UL54 shRNA1081表达载体干扰效果较好,说明该shRNA1081真核表达载体能特异降低UL54基因的表达,在一定程度上还抑制病毒的复制,因此UL54基因是一个潜在的有效的抗HSV-2的药物靶点。另外,RNAi并不能完全阻断基因的表达,对阻断基因mRNA的表达有一定的限度[11],siRNA在细胞内与RISCs(RNA-induced silencing complexes)结合后,通过其识别并沉默相应的mRNA,RISCs有一定的饱和度,过多的siRNA反而可能抑制其活性,也不可能无限增大siRNA的浓度。因此将两种基因或者多个基因的分子靶向治疗相结合有可能治疗效果更好。因此,本试验通过筛选出最有效抑制UL54基因表达的shRNA干扰序列,和前期研究针对不同的病毒关键基因如UL29[12]、UL27[13]、ICP4[14]以及已报道的UL30[15]进行多个靶点shRNA的设计、筛选,为下一步利用最有效干扰序列进行联合干扰HSV-2复制作用奠定了基础。
参考文献:
[1] 刘继峰,关翠萍,唐 旭,等.siRNA对单纯疱疹病毒2型ICP4基因抑制作用的研究[J].中华实验和临床病毒性杂志,2010, 24(3):199-201
[2] STEINBACH J M, WELLER C E, BOOTH C J, et al. Polymer nanoparticles encapsulating siRNA for treatment of HSV-2 genital infection[J]. J Control Release,2012,162(1):102-110.
[3] SEDLACKOVA L,RICE S A. Herpes simplex virus type 1 immediate-early protein ICP27 is required for efficient incorporation of ICP0 and ICP4 into virions[J].Virol,2008,82(1):268-277.
[4] MALIK P,TABARRAEI A,KEHLENBACH R H, et al. Herpes simplex virus ICP27 protein directly interacts with the nuclear pore complex through Nup62, inhibiting host nucleocytoplasmic transport pathways[J]. Biol Chem,2012,287(15): 12277-12292.
[5] SANDRI-GOLDIN R M.The many roles of the regulatory protein ICP27 during herpes simplex virus infection[J]. Front Biosci,2008,13(5):5241-5256.
[6] QING G,WEILI W, FANQIN Z,et al. Research of UL54-specific siRNA on herpes simplex virus type II replication[J]. Int J Dermatol,2011,50(3):362-366.
[7] HARGETT D, MCLEAN T, BACHENHEIMER S L, et al. Herpes simplex virus ICP27 activation of stress kinases JNK and p38[J].Virol,2005,79(13):8348-8360.
[8] ZHAO L,ZHU W B,DING Q,et al. The herpes simplex virus type multiple function protein ICP27[J]. Virol,2008,23(6):399-405.
[9] SANDRI-GOLDIN RM. The many roles of the highly interactive HSV protein ICP27, a key regulator of infection[J]. Future Microbiol,2011,6(11):1261-1277.
[10] KALAMVOKI M,ROIZMAN B. The histone acetyltransferase CLOCK is an essential component of the herpes simplex virus 1 transcriptome that includes TFIID,ICP4,ICP27,and ICP22[J]. Virol,2011.85(18):9472-9477.
[11] JACKSON A L,BARTZ S R,SCHELTER J,et al. Expression profiling reveals off-target gene regulation by RNAi[J]. Nature Biotech,2003,21(6):635-637.
[12] 黄 畅,潘晓瑜,袁俊杰,等.单纯疱疹Ⅱ型病毒UL29基因shRNA表达载体的干扰效应[J].实用医学杂志,2014,30(5):691-694.
[13] 吕延成,潘晓瑜,周丹丹,等.靶向UL27 shRNA抑制Ⅱ型单纯疱疹病毒在HEK293细胞中的复制[J].中国生物化学与分子生物学报,2013,29(8):759-766.
[14] 袁俊杰,吕延成.shRNA表达载体对HSV-2 ICP4基因的干扰效应[J].遵义医学院学报,2013,36(1):21-24.
[15] 冯 海,张 浩,屠 静,等.敲减单纯疱疹病毒Ⅱ型(HSV-2)UL30蛋白表达可抑制HSV-2复制[J].中国生物化学与分子生物学报,2007,23(12):1025-1030.
