等离子改性CNT/TiO2电极吸附去除水中苯酚的研究
2015-08-30杨文浩杨灵芳湖南大学水工程与科学系湖南长沙410082
施 周,杨文浩,杨灵芳,邓 林 (湖南大学水工程与科学系,湖南 长沙 410082)
等离子改性CNT/TiO2电极吸附去除水中苯酚的研究
施 周*,杨文浩,杨灵芳,邓 林 (湖南大学水工程与科学系,湖南 长沙 410082)
利用电感耦合空气等离子体对涂覆法制备的CNT/TiO2复合电极进行射频放电改性处理.复合电极的表面形貌、润湿性及元素成分分别通过扫描电镜(SEM)、接触角测试仪、x射线光电子能谱(XPS)进行了表征.结果表明,改性后有利于苯酚吸附,电极比表面孔隙、亲水性、TiO2及含氧官能团均得以增加;循环伏安测试(CV)表明改性后电极比电容提高 54%;改性后复合电极对苯酚的吸附量较改性前提高了45%.且等离子改性CNT/TiO2电极对苯酚的去除量随电压、苯酚初始浓度的增加而增加,吸附过程符合准二级动力学方程,吸附等温线符合Langmuir等温吸附模型.
等离子活化;CNT/TiO2复合电极;苯酚;电吸附
苯酚具有较强的腐蚀性和毒性,对人类健康和环境生态危害显著[1].目前国内外主要采用光催化氧化法[2]、化学氧化法[3]、生物法[4]和吸附法[5]处理苯酚废水,但成本高、操作复杂、回收再生困难.电吸附技术是一种基于双电层电容理论的新型水处理技术,它以电势差为驱动力,迫使离子向带有相反电荷的电极移动而被吸附,具有能耗低和无二次污染等优点[6-8].碳纳米管(CNT)以其良好的导电性、较大的比表面积和良好的化学惰性成为电极材料的研究热点,但由于其本身的憎水性和粘结剂的疏水性[9]导致碳纳米管电极的润湿性能差,电极的使用效率低.对碳纳米管材料接枝亲水性基团[10]或添加亲水性氧化物如TiO2[11-13]可有效改善其润湿性.等离子活化技术在改善比表面积、增加官能团、提高材料润湿性能方面有显著作用[14-15].目前文献有关等离子体改性碳纳米管电极的报道很少见,且改性多在N2条件下进行.本研究采用空气等离子活化技术改性 CNT/TiO2电极,探讨其电极特性和对苯酚的电吸附性能.
1 实验部分
1.1材料及预处理
主要材料为: 多壁碳纳米管CNTs: 型号LMWNT-2040(长度<2μm,直径 20~40nm),购自深圳纳米港有限公司;纳米TiO2: Degussa P25,购自广州市华力森贸易有限公司;聚四氟乙烯(PTFE)乳液:含量(60±2)%,广东化学试剂有限公司;实验苯酚废水按如下方法人工配制:准确称量200mg苯酚晶体溶解于 1L容量瓶配制成200mg/L苯酚溶液,置于密闭冰箱中保存.
实验采用KOH对CNTs进行预处理.首先将CNTs和KOH分析纯固体以质量比1:4比例混合,在氮气保护下以850℃温度煅烧2h,清洗干净并烘干后作为实验的碳纳米管的原材料.
1.2CNT/TiO2电极制备及等离子改性
采用涂覆法制备碳纳米管复合电极.按重量比为70:10:10:10称取CNTs、TiO2、导电炭黑、PTFE,在研钵中研磨均匀后均匀地涂覆在306不锈钢丝网(30mm×50mm)上,置于110℃烘箱中烘烤24h后,冷却至室温,采用10MPa压力压制10min得到碳纳米管复合电极,记为CNT/TiO2电极.
等离子改性试验装置见文献[16]:采用SY型500W射频功率源和SP-Ⅱ型射频匹配器作为等离子引发器,等离子体反应器采用石英玻璃管,外置线圈为螺旋型铜线圈.本实验改性工艺条件为:管内空气压力为10Pa,电流为130mA,电压650V,频率13.56MHz.等离子活化时间3min,处理后电极记为P-CNT/TiO2.
1.3电吸附装置及实验装置
电吸附装置参见文献[16].电极对由 2块60mm×50mm×2mm的玻璃基板和2块50mm×15mm×3mm的条形分隔板组装而成,碳纳米管电极平整粘贴在玻璃基板上,电极之间的间距d=3mm.
实验参数如下:含苯酚水样总体积为200mL,初始苯酚浓度为 200mg/L (支持电解质 Na2SO4浓度 0.05mol/L),电极电压为 600mV,电极间距3mm,溶液流速 4mL/min,水浴恒温 20℃,取样间隔时间为30min.
1.4分析测试方法
水样中的苯酚浓度采用直接分光光度法[17](日立U-3900型紫外分光光度计)测试.采用扫描电镜SEM(日立S-4800扫描电镜,日本)观察等离子体改性前后电极的微观形貌变化;通过接触角测试(KRVSS DSA100,德国)测量电极的亲水性能;采用X射线光电子能谱仪XPS(Kratos Amicus,英国)对电极表面成分进行表征;采用循环伏安法CV(电化学工作站CHI660D,上海)对电极的电化学性能进行表征.
利用公式(1)计算等离子体改性前后CNT/TiO2复合电极对苯酚的吸附量.
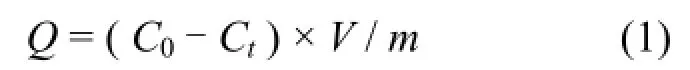
式中: Q为吸附量,mg/g; C0和Ct分别为溶液中苯酚的初始浓度和t时刻浓度,mg/L; V为水样总体积,L; m为工作电极的质量,g.
2 结果与讨论
2.1电极的表面特性

图1 CNT/TiO2(a)和P-CNT/TiO2(b)电极的SEM形貌图Fig.4 SEM images of CNT/TiO2electrode (a) and P-CNT/TiO2electrode (b)
由图 1可知,未经等离子改性的 CNT/TiO2电极呈现较为平整的电极表面,且表面材质主要是碳纳米管.而经过等离子改性后,电极表面变得粗糙,碳纳米管之间孔洞间距和数量增加,根据前期碳纳米管电极等离子改性的研究[18]表明:等离子体改性能改善碳纳米管电极的比表面积、孔容和孔结构分布.对比等离子改性前后图片,碳纳米管表面白色颗粒状附着物的量明显增加,这可能是在等离子体改性过程中TiO2负载到了碳纳米管表面,从而使得TiO2材料的亲水性能和电化学性能可以更有效地利用.
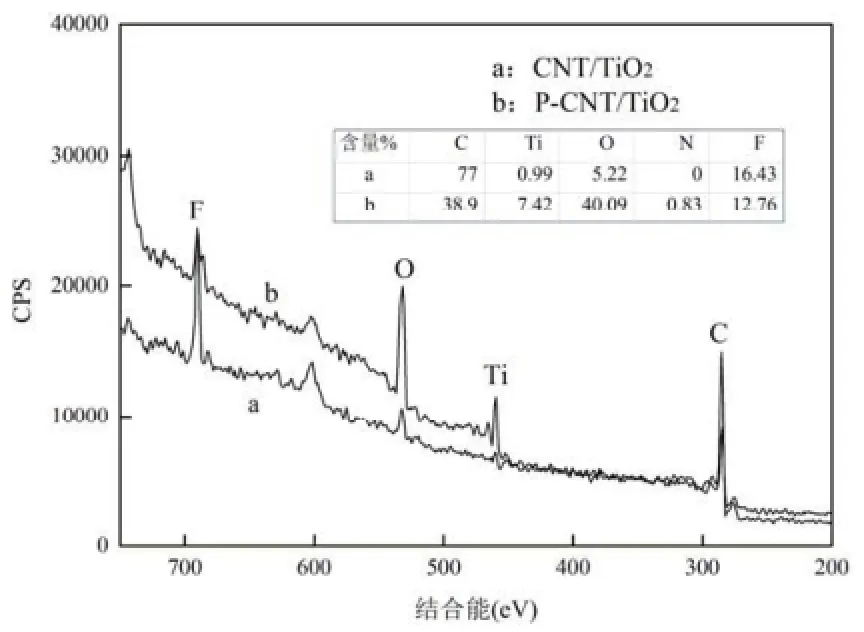
图2 CNT/TiO2(a)和P-CNT/TiO2(b)电极XPS谱图Fig.4 XPS of CNT/TiO2electrode(a) and P-CNT/TiO2electrode(b)
由图2可知,等离子改性前后电极表面的Ti 和O的含量发生了较大变化: Ti的含量从0.99%提高到了 7.42%,O的含量从 5.22%提高到了40.09%.进一步证实了SEM图片(图1)的分析结果,即等离子改性后的 TiO2表面负载量增加.据报道,二氧化钛对电极性能提高具有明显改善作用[13],而通过等离子改性处理后,二氧化钛主要集中负载在电极的表面,可以大大提高这种材料的利用率.此外,XPS结果显示 O:Ti的比例远远超2:1,且改性后该比例进一步增大,主要有2种原因:二氧化钛在表面的负载提高了电极表面的含氧量;等离子过程中,空气中的氧被激活后在电极表面引入了含氧官能团[18].等离子改性后,电极中的氮含量有所增加,说明在改性过程中还接枝引入了含氮官能团.上述表面成分的变化是由于在等离子过程中,管内稀薄的空气会发生电离产生大量的离子、激发态分子、自由基等多种活性粒子和紫外光等能量,可与电极材料之间发生相互作用形成新的结合键.
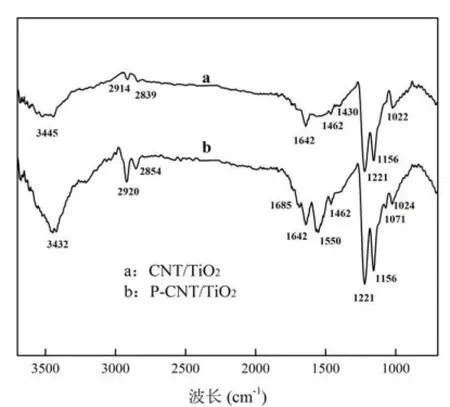
图3 CNT/TiO2(a)和P-CNT/TiO2(b)电极FTIR谱图Fig.4 FTIR of CNT/TiO2electrode(a) and P-CNT/TiO2electrode(b)
由图3可知, P-CNT/TiO2电极的谱图在波长 1685cm-1和 1071cm-1处出现了新的特征峰,此为 C=O和C—O—C的伸缩振动峰.波长3432cm-1处为O—H的伸缩振动峰.1642, 1221cm-1处分别为C—O—C和C—OH的特征吸收峰.另外,谱图在波长为1550cm-1处出现了C —N的新的特征峰[19].波长1430, 1024cm-1处为C —F的特征吸收峰[20].在波长 626, 710cm-1左右出现了Ti—O的伸缩振动峰[21].由此进一步证实了 XPS的测试结果,即通过等离子改性,复合电极表面引入了含氧官能团和含氮官能团(具体增加量见 XPS测试结果),这些极性官能团的引入能够大大改善电极表面的润湿性能和电化学性能,提高电极对苯酚的吸附量.
CNT/TiO2和 P-CNT/TiO2电极的接触角测试发现,接触角从等离子体改性前的(50±0.8)°降低至改性后的(20±0.5)°,说明等离子体改性处理有效改善了复合电极的润湿性能,结合XPS分析可知,这主要是通过促进二氧化钛负载到碳纳米管电极表面同时引入新含氧等官能团来实现的.
2.2电化学特性
采用循环伏安法(CV)对复合电极的电化学性能进行了表征,测试采用三电极系统,测试电极为工作电极,铂电极为对电极,饱和甘汞电极为参比电极,电解液采用实验所用200mg/L苯酚溶液,设置扫描电压范围-0.2~0.6V,扫描速率 10mV/s,结果如图4所示.其电容值的计算如下式:

式中, C为比电容(F/g), I为电流(A), V为电压(V),υ为扫描速率(mV/s), m为电极质量(g).
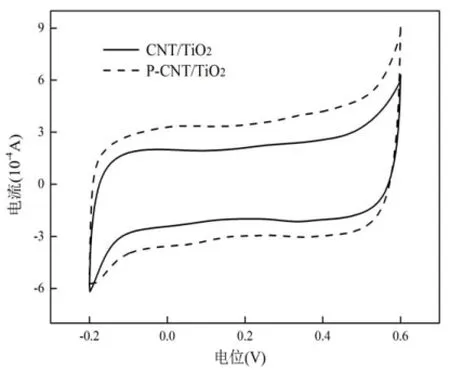
图4 CNT/TiO2和P-CNT/TiO2电极循环伏安曲线Fig.4 Cyclic voltammetry of CNT/TiO2electrode and P-CNT/TiO2electrode
由图4可知,在-0.2~0.6V范围内,CNT/TiO2和P-CNT/TiO2电极的CV曲线基本呈规则的矩形状,没有明显的氧化还原峰.表明在该电压范围内,苯酚的去除主要是通过双电层电容吸附而非发生氧化还原反应.根据图4曲线和公式(2)计算可得, CNT/TiO2和P-CNT/TiO2电极的比电容值分别为 18.97, 29.27F/g,即等离子活化处理后,复合电极的比电容值提高了 54%.这是因为作为一种过渡金属氧化物,二氧化钛的添加能促使电极电容变大[13].根据SEM、XPS和FTIR表征结果发现通过等离子活化处理后,二氧化钛负载到电极表面的含量显著提高且引入了含氧和微量的含氮官能团,这些元素的引入能大大提高电极的比电容值,改善电极的电化学性能,有助于复合电极对苯酚的电吸附.
2.3电吸附去除苯酚的性能
2.3.1电吸附去除苯酚动力学 如图5所示,复合电极对苯酚的吸附量随吸附时间的增加而增加,5h后基本趋于稳定,即达到平衡.平衡时CNT/TiO2和 P-CNT/TiO2电极电吸附苯酚的吸附量分别为172.21, 249.01mg/g,由此可确定等离子改性后吸附容量提高了45%.结合SEM、润湿性能、XPS和FTIR分析结果可知,等离子处理后电极具有更好的润湿性能、更大的比电容值使得电极对苯酚具有更大的吸附量.
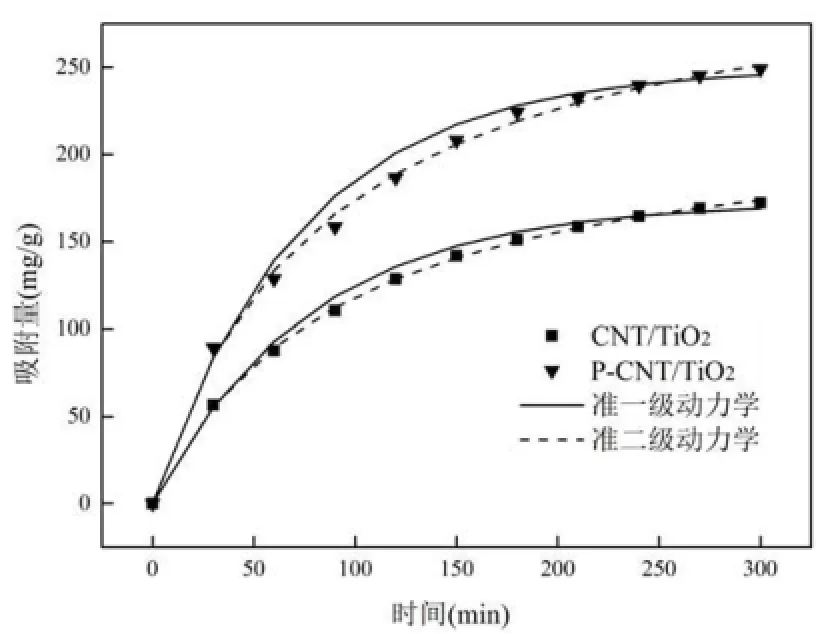
图5 CNT/TiO2和P-CNT/TiO2电极电吸附苯酚的动力学模型拟合Fig.4 Kinetics of electrosorption of phenol using CNT/TiO2and P-CNT/TiO2electrodes
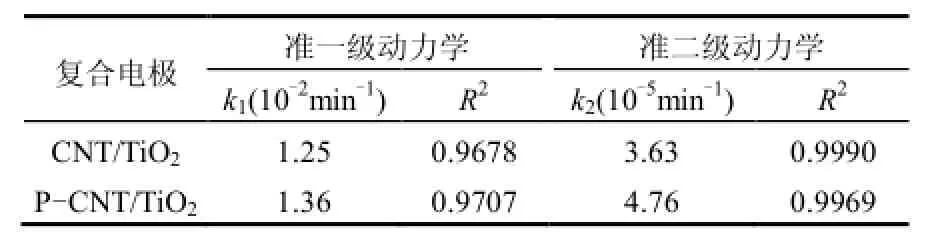
表1 准一级和准二级反应动力学拟合参数Table 1 Fitting parameters of pseudo-first-order and pseudo-second-order kinetics
由图5和表1可见, CNT/TiO2和P-CNT/ TiO2电极的准二级动力学拟合方程的R2都明显大于准一级动力学,且两种电极的吸附过程均与二级动力学拟合曲线有很好一致性,说明可用准二级动力学方程对2种电极电吸附苯酚的过程进行描述.
2.3.2电压对电吸附苯酚效果的影响 根据CV分析,在电压为600mV范围内,苯酚主要发生的是双电层吸附,因此选取该范围内的电压测试对苯酚去除的影响.由图 6可知,当电压为 200, 400, 600mV 时, 300min时的吸附量分别是188.42, 214.02, 249.01mg/g,可见,复合电极对苯酚的电吸附量随电压的增加而增加.相关研究表明,电压升高时电极表面的带电量也按比例增加,同时能耗也增加.后续实验的电压都选用600mV.
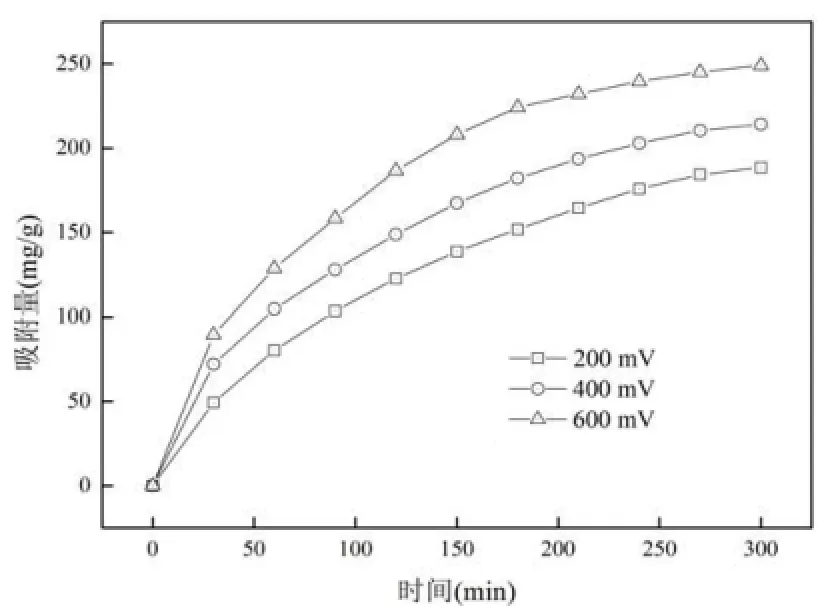
图6 电压对电吸附苯酚的影响Fig.4 Effect of applied voltage on electrosorption of phenol
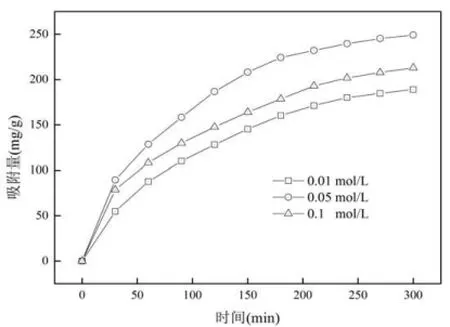
图7 Na2SO4浓度对电吸附苯酚的影响Fig.4 Effect of sodium sulphate concentration onelectrosorption of phenol
2.3.3盐对电吸附苯酚效果的影响 由于苯酚为弱电解质,电离能力较差,致使溶液导电能力较弱.而导电性是影响电吸附效果的一个重要因素.实验为了提高处理废水的导电性,采用向溶液中添加 Na2SO4来改变这一现状.由图 7可知, Na2SO4浓度为 0.05mol/L时苯酚电吸附效果最好.这是因为当 Na2SO4浓度低于 0.05mol/L时,由于电解质添加量比较少,不能最大限度地提高溶液的导电性, 因而苯酚的去除量随着 Na2SO4浓度的升高而增加.当 Na2SO4浓度高于0.05mol/L时,添加的电解质离子会与原溶液中苯酚离子形成竞争吸附,占据部分活性电位,从而影响苯酚的去除效果.因此,本研究选取 Na2SO4的浓度为0.05mol/L.
2.3.4苯酚浓度对电吸附苯酚效果的影响 由图8可知:随着苯酚初始浓度的增加,电极对苯酚的吸附容量也逐渐增加,直至趋于稳定,即电极达到饱和.结合表2和图8可知,Langmuir等温式拟合的R2明显大于Freundlich等温式,且实际吸附数据和Langmuir等温式拟合曲线有更好一致性,说明吸附过程更符合Langmuir等温模型.

表2 Langmuir和Freundlich吸附等温线拟合Table 1 Fitting parameters of Langmuir and Freundlich isotherms

图8 电吸附苯酚等温吸附模型拟合Fig.4 Adsorption isotherms of electrosorption of phenol
2.4电极的再生性能
电吸附的最大优点即电极再生容易,只需在电极上加上反向电压,吸附在电极上的离子在反向电场力作用下便会从电极上解吸下来,从而实现电极再生.本研究中当 P-CNT/TiO2电极吸附饱和之后改用蒸馏水进入流槽冲洗,同时将电极反向 10min,短接 60min,以完成电极再生.对P-CNT/TiO2电极6次循环再生数据表明,第1次再生时再生率(该次电极再生后的饱和吸附量与首次使用时饱和吸附量之比)为76.8%,之后电极的再生率在 72%~78%范围内波动(图 9),说明电极具有较好的可重复利用性.

图9 P-CNT/TiO2电极再生率Fig.4 Regeneration rate of the P-CNT/TiO2electrode
3 结论
3.1空气等离子活化法改性CNT/TiO2电极能够促使TiO2负载到电极表面并增加含氧官能团,从而提高电极的润湿性和电化学性能.
3.2经过等离子改性处理的P-CNT/TiO2电极对苯酚的吸附量较未改性的CNT/TiO2电极提高了 45%,吸附过程符合准二级动力学方程及Langmuir等温吸附模型.
3.3电压、电解质、初始浓度均对电极电吸附苯酚有影响:电极对苯酚的吸附量随电压、初始浓度的增加而增加;电解质 Na2SO4的最佳浓度为0.05mol/L.
3.4P-CNT/TiO2电极再生性能较好且稳定,其饱和吸附容量的再生率为 72%~78%,说明其可多次重复使用.
[1]段小月,刘 伟,李 想,等.活性碳纤维电吸附去除苯酚的动力学及热力学分析 [J]. 环境科学学报, 2011,31(3):505-510.
[2] Wei W, Yu C, Zhao Q F, et al. Ordered mesoporous carbon-based titania as a reusable adsorbent-catalyst for removing phenol from water [J]. Chinese Journal of Catalysis, 2013,34(6):1066-1075.
[3] 崔建国,刘幼琼,李 娜.高铁酸钾同时降解微污染水中苯酚和Cr (VI)的研究 [J]. 中国环境科学, 2011,31(9):1461-1465.
[4] Zhao Z Y, Jiang G Q, Jiang S Y, et al. Integrated anaerobic /aerobic biodegradation in an internal airlift loop reactor for phenol wastewater treatment [J]. Korean Journal of Chemical Engineering, 2009,26(6):1662-1667.
[5] Wu W T, Nie C F, Tan F I, et al. The Preparation of Palygorskite Clay Modified Woodceramics from Wheat Straw and the Absorption of Them to the Phenol Wastewater [J]. Polymers & Polymer Composites, 2013,21(9):565-572.
[6] Zou L D, Morri G, Qi D D. Using activated carbon electrode in electrosorptive deionisation of brackish water [J]. Desalination, 2008,225(1):329-340.
[7] Park K K, Lee J B, Park P Y, et al. Development of a carbon sheet electrode for electrosorption desalination [J]. Desalination, 2007, 206(1):86-91.
[8] Li H B, Pan L K, Lu T, et al. A comparative study on electrosorptive behavior of carbon nanotubes and graphene for capacitive deionization [J]. Journal of Electroanalytical Chemistry, 2011,653(1):40-44.
[9] Sung I H, Yu D M, Yoon Y J, et al. Preparation and properties of sulfonated poly(arylene ether sulfone)/hydrophilic oligomer-g-CNT composite membranes for PEMFC [J]. Macromolecular Research, 2013,21(10):1138-1144.
[10] Jin Z X, Sun X, Xu G Q, et al. Nonlinear optical properties of some polymer/multi-walled canbon nanotobe composites [J]. Chemical Physics Letters, 2000,318(6):505-510.
[11] Kim C, Lee J, Kim S, et al. TiO2sol-gel spray method for carbon electrode fabrication to enhance desalination efficiency of capacitive deionization [J]. Desalination, 2014,342(2):70-74.
[12] Chang L M, Duan X Y , Liu W. Preparation and electrosorption desalination performance of activated carbon electrode with titania [J]. Desalination, 2011,270(1-3):285-290.
[13] Liu P I, Chung L C, Shao H, et al. Microwave-assisted ionothermal synthesis of nanostructured anatase titanium dioxide/activated carbon composite as electrode material for capacitive deionization [J]. Electrochimica Acta, 2013,96:173-179.
[14] 罗 凡.低温等离子体改性碳材料吸附性能的研究 [D]. 杭州:浙江大学, 2009.
[15] 刘 勇.材料表面处理高频高压低温等离子体放电电源技术的研究 [D]. 杭州:浙江大学, 2006.
[16] Yang L F, Shi Z, Yang W H. Characterization of air plasma -activated carbon nanotube electrodes for the removal of lead ion [J]. Water Science & Technology, 2014,69(11):2272-2278.
[17] 魏复盛.水和废水监测分析方法(第四版) [M]. 北京:中国环境科学出版社, 2002:460-462.
[18] Yang L F, Shi Z, Yang W H. Enhanced capacitive deionization of lead ions using air-plasma treated carbon nanotube electrode [J]. Surface and Coatings Technology, 2014,251:122-127.
[19] Jiang X Y, Chen S D. Guide of infrared spectroscopy [M]. Tianjin:
Tianjin Sci. and Technol. Press, 1992:1-120.
[20] Lang X Q, Ma H Q, Tan X, et al. Surface activation and graft of the ultrafine PTFE particles [J]. Acta Physico-Chimico Sinica, 2005,21(7):703-706.
[21] Bezrodna T, Puchkovska G, Shymanovska V, et al. IR-analysis of H-bonded H2O on the pure TiO2surface [J]. Journal of Molecular Structure, 2004,700(1-3):175-181.
Electrosorption of phenol in aqueous solution using a plasma-activated CNT/TiO2electrode.
SHI Zhou*, YANG Wen-hao, YANG Ling-fang, DENG Lin (Department of Water Engineering and Science, Hunan University, Changsha 410082, China).
China Environmental Science, 2015,35(9):2664~2669
The CNT/TiO2composite electrode prepared by coating method was activated with radio frequency inductively coupled air-plasma. The surface morphology, wetting ability and surface elements of the plasma activated electrode were characterized by scanning electron microscopy (SEM), contact angle and X-ray photoelectron spectroscopy (XPS), respectively. It was found that the pore ratio, hydrophilic property, contents of TiO2and oxygen containing groups on the surface of the electrode increased after the activation, which facilitated the adsorption of phenol. Cyclic voltammetry (CV)result indicated that its specific capacity also increased by 54% with the plasma treatment. Further, phenol removal efficiency for the activated electrode was enhanced by 45% compared to that of the raw electrode, and the removal of phenol increased as the increase of applied voltage and initial concentration. The adsorption process followed the pseudo-second-order kinetic model and the equilibrium adsorption isotherm well fitted the Langmuir model.
plasma-activation;CNT/TiO2electrode;phenol;electrosorption
X703.1
A
1000-6923(2015)09-2664-06
2015-01-17
“十二五”国家科技支撑计划资助项目(2012BAJ24B03)
*责任作者, 教授, zhous61@163.com
施 周(1961-),男,湖南长沙人,教授,博士,主要从事水质净化与水污染控制方面的教学与研究及工程实践方面的工作.发表论文100余篇.
