健脾和胃颗粒质量标准的研究
2015-08-10许绍兰朱诗竟毛峻琴
赵 丹,许绍兰,李 蔚,朱诗竟,毛峻琴
·论 著·
健脾和胃颗粒质量标准的研究
赵 丹1,许绍兰1,李 蔚2,朱诗竟1,毛峻琴1
目的 研究并建立健脾和胃颗粒的质量标准。方法 采用TLC法对健脾和胃颗粒中的丹参、山楂和党参三味药进行定性鉴别;采用HPLC法测定健脾和胃颗粒丹参中的丹酚酸B含量,Agilent Eclipse Plus C18柱(4.6×250 mm,5 μm),以甲醇⁃乙腈⁃1.67%甲酸水溶液(27∶9∶64)为流动相;检测波长为286 nm,柱温25℃,流速1.0 mL/min,进样量10 μL。结果 试验采用TLC定性鉴别的三味药色谱斑点清晰,阴性对照无干扰;以HPLC法测定健脾和胃颗粒丹参中的丹酚酸B,丹酚酸B浓度在12.1856~389.94 μg/mL范围内与峰面积呈良好的线性关系,线性回归方程为Y=6.5459X-3.7811(r=0.9999,n=6),回收率为99.97%,RSD为1.07%。结论 本试验确定的方法操作简单、灵敏、准确,可用于健脾和胃颗粒的质量控制。
健脾和胃颗粒;丹参;山楂;党参;丹酚酸B;鉴别;含量测定
健脾和胃颗粒为解放军105医院自制制剂,是由丹参、党参、山楂等12味组成的复方制剂,具有健脾利湿、疏肝理气、清热活血等功效。为了提高该制剂的质量标准,本文使用TLC法对丹参、山楂和党参进行了定性鉴别,并采用HPLC法测定健脾和胃颗粒丹参中丹酚酸B含量,提高并完善了健脾和胃颗粒质量标准[1⁃3]。
1 仪器与试药
1.1 仪器 Agilent 1260高效液相色谱仪(安捷伦公司,四元泵,DAD检测器)、BT25S型电子分析天平(德国Sartorius)、KQ2200DB型数控超声波清洗器(昆山市超声仪器有限公司)、WD⁃9403型紫外分析仪(北京市六一仪器厂)、硅胶G薄层板(青岛海洋化工厂分厂)。
1.2 试药 健脾和胃颗粒(规格∶15g/袋,盒/10袋,解放军105医院制剂室,批号140721、140919、141205)、丹酚酸B对照品(中国药品生物制品检定所,批号∶111562⁃201313,含量为97.0%)、丹参对照药材(120923⁃201414)、山楂对照药材(121138⁃200905)和党参对照药材(121057⁃201206)均购自中国食品药品检定研究院,阴性对照品由本院自制,水为纯化水,甲醇、乙腈为色谱纯,其他试剂均为分析纯。
2 TLC鉴别
2.1 健脾和胃颗粒丹参鉴别 取健脾和胃颗粒与阴性对照样品各2.0 g,研细,分别加无水乙醚10 mL,振摇放置1 h,过滤并将滤液挥干,残渣加1 mL乙酸乙酯溶解,作为供试品溶液和阴性样品溶液;另取丹参药材、对照药材各1 g,同法制成药材、对照药材溶液。照文献[4]薄层色谱法试验,吸取上述四种溶液各10 μL,分别点于同一硅胶G薄层板上,以石油醚(60~90℃)-乙酸乙酯(4∶1)为展开剂展开,然后取出晾干。健脾和胃颗粒供试品在与对照药材色谱和对照品色谱相应的位置上,显相同颜色的斑点[5]。见图1。

图1 丹参薄层色谱图
2.2 健脾和胃颗粒山楂鉴别 取健脾和胃颗粒与本品阴性对照样品各3 g,研粉,分别加乙酸乙酯10 mL,超声处理15 min,滤过后取滤液浓缩成1 mL,作为供试品溶液和阴性样品溶液;另取山楂对照药材1 g,加乙酸乙酯4 mL,同法制成对照药材溶液。照文献[4]薄层色谱法试验,吸取上述溶液各10 μL,分别点于同一硅胶G薄层板上,以甲苯⁃乙酸乙酯⁃甲酸(20∶4∶0.5)为展开剂[6],展开,取出,晾干。喷以硫酸乙醇溶液(3→10),在80℃加热至斑点显色清晰。健脾和胃颗粒供试品,在与对照药材色谱相应的位置上,显相同颜色的斑点。见图2。
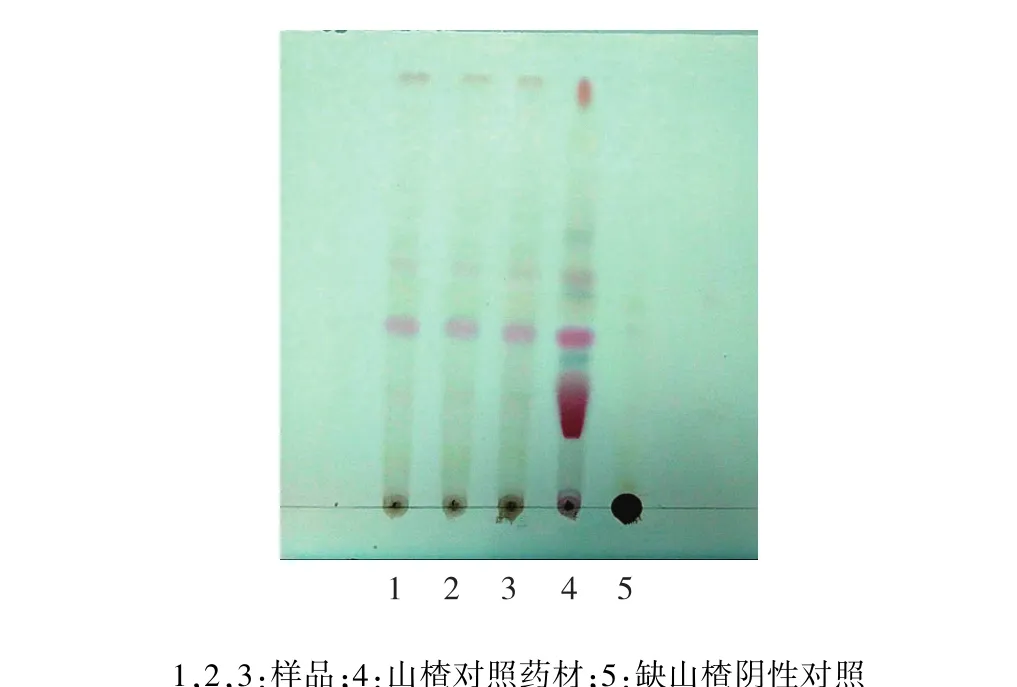
图2 山楂薄层色谱图
2.3 健脾和胃颗粒党参鉴别 取健脾和胃颗粒与本品阴性对照样品各20 g,研细,分别加甲醇超声提取两次(每次50 mL)每次30 min,滤过并将滤液浓缩至干,加水20 mL使溶解,加三氯甲烷50 mL提取,弃去三氯甲烷液,水溶液用水饱和正丁醇提取2次,每次25 mL,合并提取液,蒸干,残渣加含7%硫酸的45%乙醇溶液20 mL,加热回流1 h,取出,水浴蒸取乙醇,加三氯甲烷提取两次,每次25 mL,合并三氯甲烷液,用水50 mL振摇洗涤,弃去水洗液,三氯甲烷液蒸干,残渣加乙醇2 mL,分别作为健脾和胃颗粒供试品溶液和阴性样品溶液。再取党参对照药材1 g,同法制成对照药材溶液。照文献[4]薄层色谱法试验,吸取上述四种溶液各5 μL,分别点于同一硅胶G薄层板上,以正己烷⁃乙酸乙酯(1∶1)为展开剂,展开,取出,晾干后喷以10%硫酸乙醇溶液[7],加热至斑点清晰。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点。见图3。

图3 党参薄层色谱图
3 含量测定
3.1 色谱条件 色谱柱∶Agilent eclipse plus C18柱(4.6×250 mm,5 μm);流动相∶甲醇⁃乙腈⁃1.67%甲酸水溶液(27∶9∶64);检测波长为286 nm。柱温25℃;流速1.0 mL/min;进样量10 μL。
3.2 溶液的配制 ①对照品溶液的制备∶精密称取丹酚酸B对照品4.02 mg,置于10 mL量瓶中,加75%甲醇稀释至刻度,摇匀即得。②供试品溶液的制备∶取健脾和胃颗粒粉末2 g,置于锥形瓶中,加75%甲醇20 mL,称重,超声45 min,放冷,甲醇补足重量,摇匀,滤过,取滤液即得。
3.3 专属性(空白对照试验) 按照上述色谱条件,精密吸取对照品溶液、供试品溶液、阴性样品溶液各10 μL,注入高效液相色谱仪,测定丹酚酸B含量。结果显示,对照品溶液中丹酚酸B的保留时间为18.0 min,健脾和胃颗粒样品溶液中丹酚酸B的保留时间为17.8 min,阴性制剂供试品溶液在丹酚酸B对照品色谱的相应位置上无干扰。见图2。
3.4 线性关系考察 精密吸取对照品储备溶液1 mL,逐级稀释,摇匀。制得浓度分别为389.94 μg/mL,194.97μg/mL,97.485μg/mL,48.7425 μg/mL,24.3713 μg/mL,12.1856 μg/mL的对照品溶液系列,各取10 μL进行测定,进行回归分析。横坐标∶对照品浓度X(μg/mL),纵坐标∶峰面积Y,回归方程为∶
Y=6.5459X-3.7811(r=0.9999,n=6)
结果表明∶丹酚酸B含量在12.1856~389.94 μg/mL范围内线性关系良好。
3.5 精密度实验 精密吸取丹酚酸B对照品溶液10 μL,连续重复进样6次,记录峰面积,结果RSD为0.47%。

图2 专属性试验
3.6 稳定性试验 精密量取同一批号供试品溶液(批号∶140922),分别于配制后0、2、4、6、8 h测定峰面积,丹酚酸B RSD为0.86%(n=5)。结果表明,供试品溶液在8 h内稳定性良好。
3.7 重复性试验 取同一批号(批号∶140721)的健脾和胃颗粒6份,按“3.2”项下方法制备供试品溶液,并进行色谱测定。结果样品中丹酚酸B的平均含量为0.9552 mg/g,RSD为1.07%,表明此法重复性良好。
3.8 加样回收率试验 称取已知含量的同一批样品(批号∶140721)约0.5 g(9份),精密称定,分别置量瓶中,于①②③号量瓶中各精密加入丹酚酸B对照品溶液3 mL(每mL中含丹酚酸B 0.2328 mg),④⑤⑥号量瓶中各精密加入5 mL,⑦⑧⑨号量瓶中各精密加入7 mL,按“3.2”项下供试品溶液的制备方法,依色谱条件测定,记录峰面积,结果见表1。
3.9 样品含量测定 按“3.2”项下方法制备不同批号共3批健脾和胃颗粒供试品溶液,分别精密吸取供试品溶液10 μL进样,以峰面积计算样品中丹酚酸B的含量,结果见表2。

表1 加样回收率试验结果
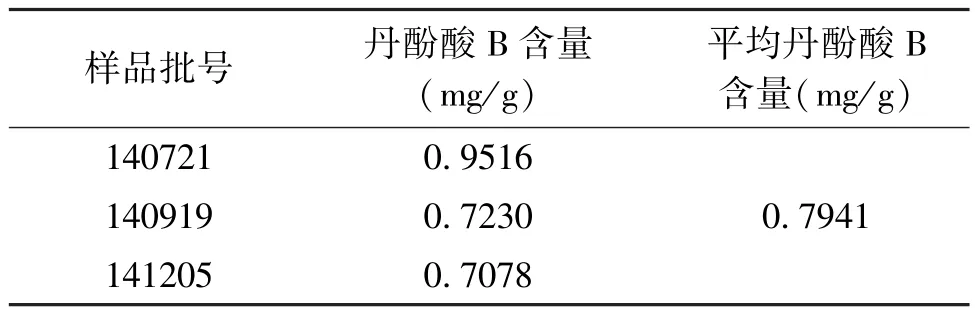
表2 丹酚酸B含量测定结果
3.10 提取方法的选择 精密称定同一批号(140721)的样品1.0 g若干份,分别加入10 mL 75%甲醇进行回流至不同的时间及超声提取不同时间的试验,按照前法处理制备供试品溶液后测定。试验结果(表3)表明∶超声提取要比回流提取效率高,因此选择超声提取,且超声45 min时的提取效率最高。

表3 提取方法的选择
4 讨 论
本试验中健脾和胃颗粒提取溶剂选用甲醇,因甲醇提取的效率最高[8]。经试验证实超声提取要比回流提取效率高[9],且超声45 min时的提取效率最高。本文参照《中国药典》2010版一部骨碎补中丹酚酸B的含量测定方法,选择甲醇⁃乙腈⁃1.67%甲酸水溶液(27∶9∶64)作为流动相,目标峰与杂质峰分离效果亦较好。
[1] 王 闰,孟 慧,许 勇.复方甘草软膏的制备及含量测定法的建立[J].东南国防医药,2015,17(4)∶389⁃391.
[2] 申 欣,查娅妮.风热感冒颗粒质量标准研究[J].中国药业,2008,17(9)∶25.
Study on the quality standard of Jianpihewei Granules
ZHAO Dan1,XU Shao⁃lan1,LI Wei1,ZHU Shi⁃jing1,MAO Jun⁃qin1. 1.Department of Pharmacy,85 Hospital of PLA,Shanghai 200052,China;2.Department of Pharmacy,105 Hospital of PLA,Hefei,Anhui 361000,China
Objective To study and establish the quality standard for Jianpihewei Granules.Methods TLC was used to i⁃dentify salvia miltiorrhizae,crataegus pinnatifida and codonopsis pilosula in Jianpihewei Granules.The content of salvianolic acid B in salvia miltiorrhizae was determined by HPLC.Methanol⁃acetonitrile⁃1.67%formic acid solution(27∶9∶64)was used for mobil phase of Agilent Eclipse Plus C18(4.6×250 mm,5 μm).The detection wavelength was 286 nm,flow rate was 1.0 mL/min and the temperature of column was 25℃.The injection volume was 10 μL.Results The spots on TLC are clear without negative sample interfrence.The concentration of salvianolic acid B in salvia miltiorrhizae determined by HPLC showed a good linear relationship withpeak area in the range of 12.1856-389.94 μg/mL of salvianolic acid B.The linear regression equation was Y=6.5459X-3.7811(r=0.9999,n=6).The recovery was 99.97%and RSD was 1.07%.Conclusion The method is simple,sensibility and accuracy,which can be used in quality control of Jianpihewei Granules.
Jianpihewei Granules;salvia miltiorrhizae;crataegus pinnatifida;codonopsis pilosula;salvianolic acid B
R286
A
10.3969/j.issn.1672⁃271X.2015.06.011
军队医疗机构制剂标准提高科研专项课题(14ZJZ03⁃1)
1.200052上海,解放军85医院药剂科;2.361000安徽合肥,解放军105医院药剂科
毛峻琴,E⁃mail∶xushaolan@126.com
