O-季铵化-N-(4-十二烷氧基)壳聚糖苯甲醛席夫碱 的制备及胶束pH 响应性
2015-07-25林意华李明春辛梅华陈燕燕
林意华,李明春,辛梅华,陈燕燕
(华侨大学材料科学与工程学院,环境友好功能材料教育部工程中心,福建 厦门 361021)
壳聚糖是无毒、生物相容性良好的天然多糖,近年来对壳聚糖进行各种亲/疏水改性制备智能化壳聚糖衍生物,用于药物增溶、药物控制释放等领域的研究不断深入[1]。
具有pH 响应的药物载体是根据人体病变部位细胞与正常细胞周围pH 值环境不同而设计的。亚胺(Schiff 碱)由于具有动态共价键的性质,可作为pH 响应位点应用于pH 敏感药物传输领域[2]。苯甲基亚胺由于苯环与C=N 共轭作用在生理pH 值环境下稳定性良好,而在弱酸环境下(如肿瘤细胞外环境)水解[3],并且苯甲基亚胺的合成反应条件温和,反应效率高[4],利用苯甲基亚胺的pH 敏感性构筑新型的pH 敏感药物载体引起了人们的关注。Ding 等[5]合成了两端带有苯甲醛基的温敏PEO-PPO-PEO 共聚物,将其与乙二醇基壳聚糖反应,制备了pH 值、温度双敏感可注射凝胶,并应用于包覆亲水药物和疏水药物。药物的释放速度可以通过改变pH 值和环境温度调节。Wang 等[6]以聚乙二醇-聚赖氨酸嵌段共聚物为主链接枝4-癸烷氧基苯甲醛,形成的双亲性的梳型聚合物分子链组装成聚合物胶束。该胶束在生理条件(pH 值为7.4)稳定,在一般肿瘤组织pH 值环境(pH 值为6.5)时由于苯甲基亚胺键断裂而解组装,从而实现了包载尼罗红的pH 值响应释放。Jiang 等[7]利用N-异丙基丙烯酰胺与香草醛改性壳聚糖,合成了具有pH值、温度双敏感性的壳聚糖衍生物,同样实现了药物的控制释放。本文制备了新型的壳聚糖衍生物O-季铵化-N-(4-十二烷氧基)壳聚糖苯甲醛席夫碱(QA-CS-DBA),见图1;考察了 QA-CS-DBA 胶束的形成以及在不同pH 值环境下的行为,为壳聚糖在难溶药物增溶以及药物缓释载体方面的应用提供依据。
1 实验部分
1.1 主要仪器与试剂
Bruker Avance III 型(500MHz)核磁共振波谱仪(Bruker);Nexusu 470 型傅里叶变换红外光谱仪(Nicolet);FD-1B-50 型冷冻干燥机(博医康实验仪器公司); Vario Micro 元素分析仪(Elementar); FLS920 型全功能稳态/瞬态荧光光谱仪(Edinburgh Instruments);ZEN3600 纳米激光粒度及 Zeta 电位分析仪(Malvern)。
1.2 O-季铵化-N-(4-十二烷氧基)壳聚糖苯甲醛席夫碱的制备
1.2.1 4-十二烷氧基苯甲醛的合成及表征
按照文献[8]的方法合成4-十二烷氧基苯甲醛(DBA)。用1H NMR 对产物进行表征。
1.2.2 N-(4-十二烷氧基)壳聚糖苯甲醛席夫碱的 合成
1g 壳聚糖分散于60mL 甲醇-水(体积比为1/1)中,升温至50℃。将上面制备的4-十二烷氧基苯甲醛4.30g 溶于10mL 甲醇后滴加于CS 甲醇-水中,50℃恒温反应24h,抽滤,乙醇索氏提取48h 以上,真空干燥得到CS-DBA 粉末。用FTIR 及元素分析进行表征。
1.2.3 O-季铵化-N-(4-十二烷氧基)壳聚糖苯甲醛席夫碱的合成
[9]的方法制备O-季铵化-N-(4-十二烷氧基)壳聚糖苯甲醛席夫碱(QA-CS-DBA)。操作如下: 1g CS-DBA 分散于70mL 异丙醇中,升温至70℃;将5.7g 2,3-环氧丙基三甲基氯化铵溶于6mL 水中滴加于上述溶液,70℃反应24h;抽滤,乙醇索提48h 以上,真空干燥得QA-CS-DBA 粉末;用FTIR 及元素分析表征。
1.3 临界胶束浓度测定
以芘为荧光探针,采用稳态荧光法测定O-季铵化-N-(4-十二烷氧基)壳聚糖苯甲醛席夫碱(QA-CS-DBA)的临界胶束浓度(CMC)值[10],激发波长339nm,扫描范围350~450nm,狭缝宽度0.7nm。

图1 DBA 与QA-CS-DBA 的合成路线
1.4 载药胶束制备
称取75mg QA-CS-DBA粉末溶于25mL 去离子水中,将75mg 酮洛芬溶于2.5mL 无水乙醇中,边搅拌边滴加到上述溶液中,滴加完毕超声30min,二次水透析12h 以上。透析袋中的载药胶束溶液离心后用0.45μm 滤膜过滤,得到载药胶束溶液,真空冷冻干燥得载药胶束冻干粉。同样操作制备QA-CS-DBA 空白胶束冻干粉。
1.5 载药量及包封率测试
取1mL 上述1.3 节制备的载药胶束溶液于25mL 容量瓶中,乙醇定容,振荡30min 后过滤,测定滤液在260nm 处的紫外吸光值A,根据酮洛芬乙醇溶液的线性方程 A=72.902C+0.0205(R2= 0.9994),C 为酮洛芬浓度,线性范围 0 ~0.025mg/mL,求得胶束内酮洛芬的质量。依照式(1)和式(2)计算QA-CS-DBA 载酮洛芬胶束的包封率和载药量。
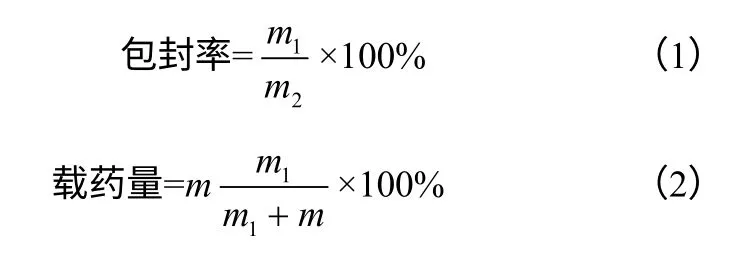
式中,m1为胶束内酮洛芬的质量,mg;m2为加入的酮洛芬总质量,mg;m 为载体的质量,mg。
1.6 载药胶束在不同pH 值的药物释放行为
测定胶束在生理条件(pH 值为7.40)以及一般肿瘤组织pH 值环境(pH 值为6.50)中的药物释放行为。称取20mg 载药胶束(载药量为39.37%)于透析袋中,分别置于含25mL pH 值为7.40 和pH值为6.50 的磷酸盐(PBS)缓冲溶液的锥形瓶,37℃恒温振荡,间隔一定时间取4mL 透析液,同时补充4mL 相同pH 值的PBS 缓冲液。透析液在260nm测定吸光值A,根据酮洛芬在pH 值为7.40 和pH值为 6.50 的 PBS 缓冲溶液中的线性方程 A= 61.184C+0.0101(R2= 0.9995)和A=61.574C+ 0.0129(R2=0.9990),式中C 为酮洛芬浓度,mg/mL,线性范围0~0.025mg/mL,计算酮洛芬的含量,绘制载药胶束在不同pH 值介质的释药量与时间关系 曲线。
2 结果与讨论
2.1 产物的红外分析
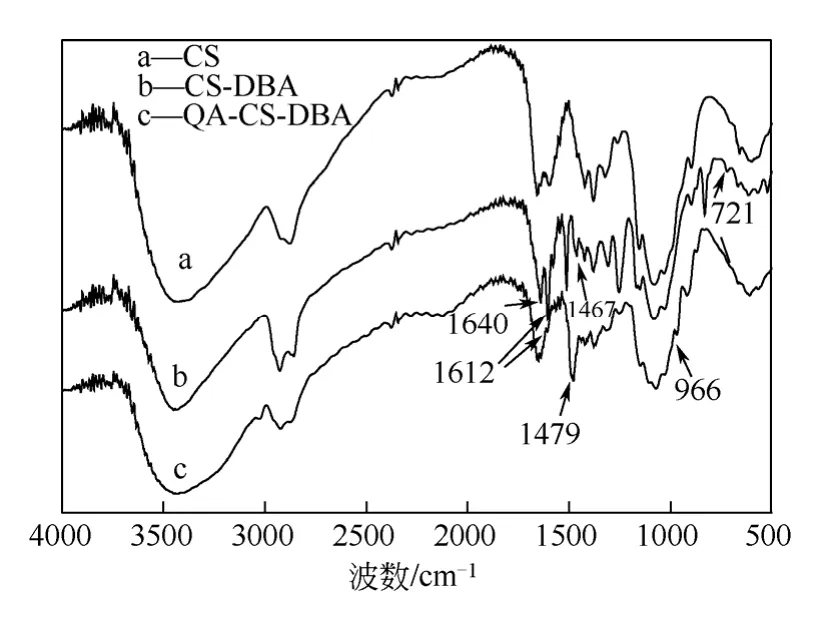
图2 原料和产物的FT-IR 图
采用KBr 压片法测得壳聚糖(CS)、N-(4-十二烷氧基)壳聚糖苯甲醛(CS-DBA)和 O-季铵化- N-(4- 十二烷氧基) 壳聚糖苯甲醛席夫碱(QA-CS-DBA)的红外光谱图如图2 所示。图2中a、b、c 分别为CS、CS-DBA 和QA-CS-DBA 的红外吸收谱线。与a 相比,b 在1640cm-1出现的新峰为C=N 吸收峰[11]; 1467cm-1为烷基链中亚甲基上的C—H 弯曲峰,721cm-1为n≥4 的(CH2)n基团的骨架振动峰[12],1467cm-1为苯环伸缩振动的特征峰。由红外谱图说明,DBA 已经接到壳聚糖的氨基上。c 与b 相比,c 在966cm-1的新峰为季铵盐吸收峰,1479cm-1为季铵盐基团中甲基的C—H 不对称伸缩峰[10],说明季铵盐基团已引入,由FTIR 图说明产物为QA-CS-DBA。
2.2 产物的1H NMR 分析
4-十二烷氧基苯甲醛(DBA)和O-季铵化- N-(4-十二烷氧基)壳聚糖苯甲醛席夫碱(QA-CS- DBA)分别溶于CD3Cl 和D2O 中,测定1H NMR如图3 所示。图3(a)为DBA 的1H NMR 图,其中δ9.87 为DBA 上羰基H 质子峰,δ7.82 与δ6.98 为苯环H 质子峰。δ3.94 为DBA 与O 相连亚甲基H 质子峰,δ1.82、δ1.29、δ1.33 为十二烷基链亚甲基H质子峰,δ0.90 为DBA 中长链烷基末端—CH3中H质子峰[13],由1H NMR 说明产物为DBA。图3(b)中δ4.50~3. 70 为壳聚糖骨架质子峰,δ3.33 为季铵盐氮上的3 个甲基质子峰[10],δ8.31 为—N=CH—中H的质子峰[14],δ7.52和δ6.66为苯环H质子峰,δ3.94为侧链DBA 与O 相连亚甲基H 质子峰,δ1.22、δ1.02、δ0.80 为侧链DBA 中长链烷基H 质子峰[13],由1H NMR 进一步说明产物为QA-CS-DBA。
2.3 QA-CS-DBA 的元素分析
采用元素分析法,由C/N 摩尔比计算产物的取代度[15],结果见表1。根据C/N 比计算原料壳聚糖的脱乙酰度为96.7%,4-(十二烷氧基)苯甲醛的取代度为43.1%,季铵化取代度为1.36%。季铵化度高可以提高产物的亲水能力使产物溶于水。
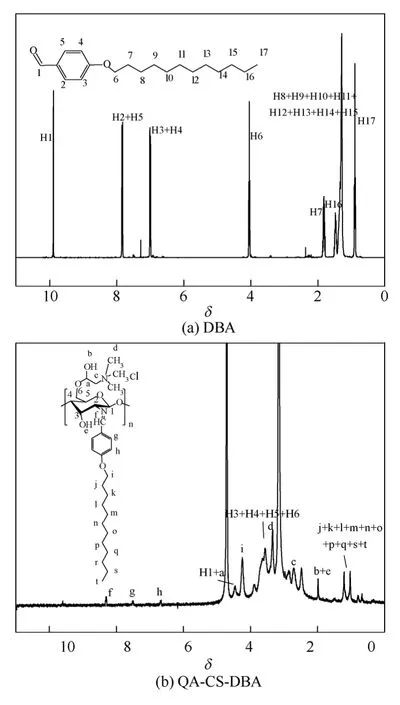
图3 产物的1H NMR 图
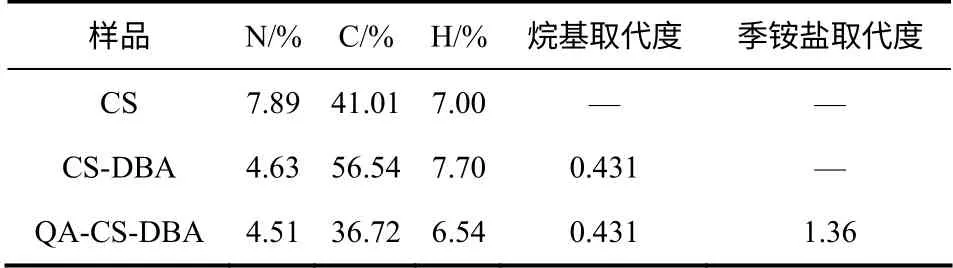
表1 产物的元素分析结果及取代度
2.4 胶束性能参数表征
2.4.1 临界胶束浓度
按照实验部分1.3 节的操作测得不同浓度QA-CS-DBA-芘的稳态荧光光谱如图4 所示。选取波长372nm 和383nm 处的荧光强度值I372和I383,计算其比值I372/I383,进一步计算并绘制lgC~I372/I383关系曲线如图5 所示。分段做曲线的切线,切线的交点对应的浓度即为QA-CS-DBA 的CMC值0.081mg/mL,该值远小于文献报道的壳聚糖基 药物载体材料的CMC 为0.714mg/m 和11~50μg/L[10,16]。临界胶束浓度小说明胶束具有很好的热力学稳定性,即使被稀释到很低的浓度也能维持其胶束结构[1]。这是因为疏水烷基链较长且柔顺性 好,有利于组装形成胶束,说明QA-CS-DBA 具有良好的双亲性结构。
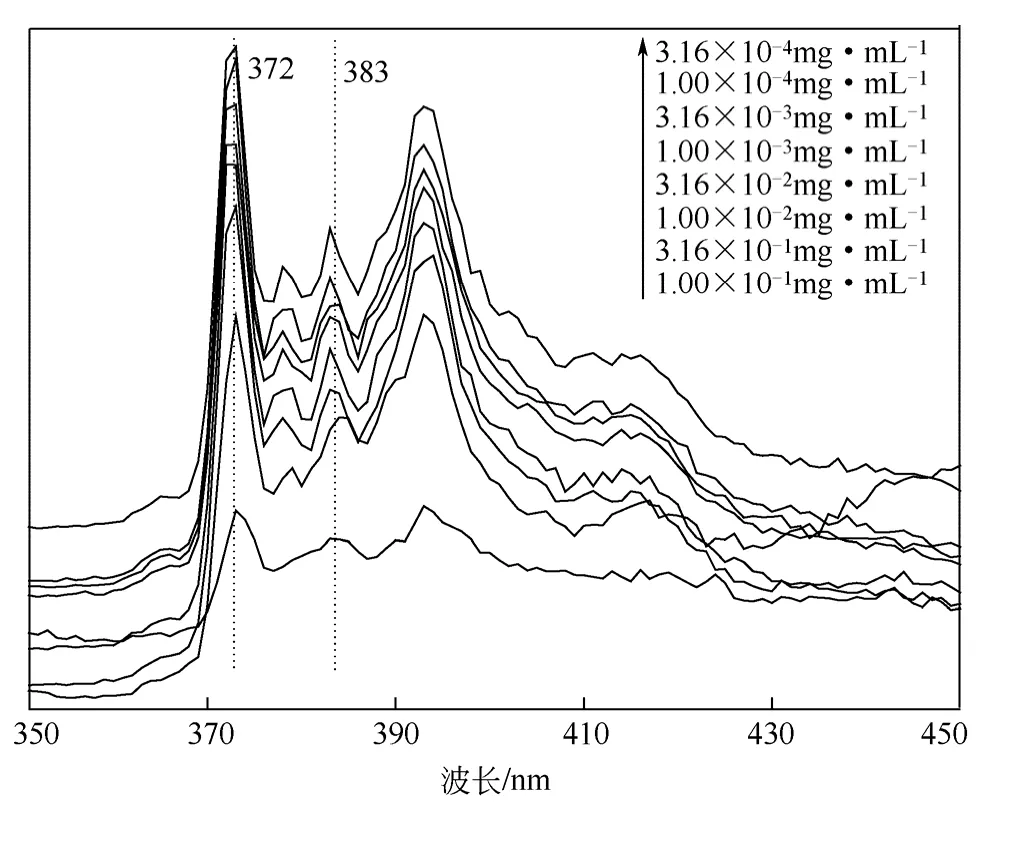
图4 不同浓度 QA-CS-DBA 水溶液中芘的稳态荧光光 谱图

图5 芘的荧光发射强度比(I372/I383)与 QA-CS-DBA 浓度关系曲线
2.4.2 胶束的载药量、包封率、粒径及Zeta 电位
按照1.5 节操作测得QA-CS-DBA 载酮洛芬胶束的载药量为39.37%,包封率为46.04%。
分别称取5mg 空白胶束及载酮洛芬胶束冻干粉复溶于5mL pH 值为7.4 的磷酸盐缓冲溶液中,测定平均粒径及Zeta 电位。测得空白胶束的平均粒径为285.0nm,如图6 所示,载药胶束(载药量39.37%)的平均粒径为341.0nm,比空白胶束粒径大,说明有酮洛芬载入胶束。空白胶束Zeta 电位为31.2mV,载药胶束Zeta 电位为30.8mV,Zeta 大于30mV,说明胶束具有较好的稳定性[15]。
2.4.3 QA-CS-DBA 胶束的形貌观察
将1.4 节制备的QA-CS-DBA 载药胶束冻干粉60℃真空干燥,用扫描电镜观察其形貌。由图7可以看出胶束粒径分布较为均匀,粒径比上述采用纳米激光粒度分析仪测得的341nm 略小,这可能是载药胶束在冷冻干燥过程中收缩并相互挤压造成。
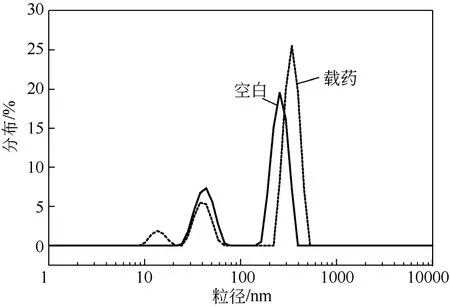
图6 空白胶束与载药胶束的粒径分布

图7 载药胶束的SEM 图
2.5 QA-CS-DBA 胶束的pH 响应性
2.5.1 胶束在不同pH 值条件下的Zeta 电位变化
参考文献[6]通过Zeta 电位变化表征胶束的pH响应性。将1.3 节中制备的空白胶束冻干粉溶解,用HCl 及NaOH 溶液交替调节pH 值,使pH 值在一般肿瘤组织环境pH 值为6.50 与生理环境pH 值为7.40 来回变化,分别测定溶液对应的Zeta 电位,结果如图8 所示。由图8 可见Zeta 电位在pH 值为7.40 比pH 值为6.50 高,这是因为pH 值为7.40 时,亚胺键(C=N)较为稳定,而pH 值为6.50 时,亚胺键断裂形成—NH3+,正电荷排斥导致胶束趋于不稳定,Zeta 电位变大[6]。由此可见,胶束在pH值为6.50~7.40 的较小范围内即有响应性。来回调节溶液pH 值,Zeta 电位发生响应变化,说明C=N键的形成与解离导致双亲性结构的形成与破坏,并最终导致了自组装胶束结构的组装与解组装,从分子水平解释了亚胺键的存在是导致 pH 响应的 原因。

图8 空白胶束的Zeta 电位随pH 值转变的关系
2.5.2 载药胶束在不同pH 值的药物释放行为
按照实验部分1.6 节的操作测定胶束在生理条件(pH 值为7.40)以及一般肿瘤组织pH 值环境(pH值为6.50)中的药物释放行为,结果见图9。由图9可见,QA-CS-DBA 载药胶束在pH 值为7.40 释放较为平缓,10h 后累积释放量为49.30%。而在pH值为6.50 的药物释放较快,在5h 左右基本达到平衡,48h 的累积释放量为74.99%,高于pH 值为7.40的累积释放量。这是因为在pH 值为6.50 时亚胺键断裂,DBA 解离使得胶束的通透性发生了改变,导致药物释放速率加快[14],比文献报道的通过席夫碱桥联药物的壳聚糖聚合物胶束在pH值为6.8的释放量66.7%要高[1],且高的释药量能够更好地杀灭癌细胞。并且在pH 值为6.50 时,载药胶束在3.5h 以内具有较快的释放速率,说明该载药胶束具有较快的响应速率。加快药物在肿瘤组织以及内含体内部弱酸环境中的释放有利于提高肿瘤组织及癌细胞内部的药物浓度,更好的发挥药物的作用。
3 结 论
通过制备O-季铵化-N-(4-十二烷氧基)壳聚糖苯甲醛席夫碱(QA-CS-DBA),并将其应用于载药胶束的制备,考察了pH 响应性能及药物释放性能。结果表明QA-CS-DBA 在溶液中能形成稳定的球形结构胶束,胶束具有较小的CMC。胶束Zeta 电位随pH 值不同而变化,具有pH 响应性。载药胶束在pH 值为7.40 时具有药物缓释效果,而在pH 值为6.50,即癌细胞周围pH 值时,具有快速释放效果,有望用于难溶抗癌药物的增溶及控释作用。

图9 载药胶束在不同pH 值介质中的释药量与时间关系
参 考 文 献
[1] 康爽明,胡海洋,胡婵娟,等. pH 敏感释药两亲性壳聚糖共聚物胶束的制备及其性质考察[J]. 沈阳药科大学学报,2011,28(1):6-11.
[2] Osowska Karolina,Miljanic O Š,et al. Oxidative kinetic self-sorting of a dynamic imine library[J]. Journal of the American Chemical Society,2011,133(4):724-727.
[3] 屈小忠,杨振忠. 苯甲酰亚胺动态共价键在构筑pH 响应性药物载体中的应用[J]. 高分子学报,2011(10):1118-1123.
[4] Yan X,Jinying Y. Schiff’s base as a stimuli-responsive linker in polymer chemistry[J]. Polymer Chemistry,2012,3(11):3045-3055.
[5] Ding C,Zhao L,Liu F,et al. Dually responsive injectable hydrogel prepared by in situ cross-linking of glycol chitosan and benzaldehyde-capped PEO-PPO-PEO[J]. Biomacromolecules,2010,11(4):1043-1051.
[6] Wang C,Wang G,Wang Z,et al. A pH-responsive superamphiphile based on dynamic covalent bonds[J]. Chem. Eur. J.,2011,17(12):3322-3325.
[7] Jiang J,Pan X,Cao J,et al. Synthesis and property of chitosan graft copolymer by RAFT polymerization with tosylic acid–chitosan complex[J]. International Journal of Biological Macromolecules,2012,50(3):586-590.
[8] 赵鸿斌,宁静恒,剑蔡,等. 系列长链烷氧基苯甲醛的合成研究[J]. 化学研究,2001,12(1):19-22.
[9] 刘臻,沈云,黄丹. O-季铵化-N-水杨醛壳聚糖席夫碱的合成及抗菌性研究[J]. 南通大学学报:自然科学版, 2011,10(4):48-52.
[10] 程萌萌,辛梅华,李明春,等. 季铵化-N-(4-咪唑甲基)壳聚糖的制备及其胶束形成[J]. 化工进展,2012,31(4):861-865.
[11] 李克让,徐民,张帅,等. 离子液体中壳聚糖磷酸吡哆醛席夫碱衍生物的合成与表征[J]. 化工学报, 2013,64(4):1499-1503.
[12] 裴立军,蔡照胜,商士斌,等. 碱性离子液体碱化制备N-十二烷基壳聚糖[J]. 精细化工, 2013,30(7):808-812.
[13] 刘捷频,杨德亮,曹华,等. meso-四(对烷氧基苯基)卟啉镁配合物的合成、表征和性能研究[J]. 有机化学,2012,32(4):709-713.
[14] Wang G,Wang C,Wang Z. Bolaform superamphiphile based on a dynamic covalent bond and its self-assembly in water[J]. Langmuir,2011,27(20):12375-12380.
[15] Huo M,Zhang Y,Zhou J,et al. Formation,microstructure,biodistribution and absence of toxicity of polymeric micelles formed by N-octyl-N,O-carboxymethyl chitosan[J]. Carbohydrate Polymers,2011,83(4):1959-1969.
[16] Liu J,Li H,Jiang X,et al. Novel pH-sensitive chitosan-derived micelles loaded with paclitaxe[J]. Carbohydrate Polymers,2010,82(2):432-439.
