精神分裂症患者代谢综合征与颈动脉内中膜厚度的相关性研究
2015-07-12朱景新
朱景新, 曲 伸
(1. 同济大学医学院,上海 200092; 2. 上海市奉贤区精神卫生中心,上海 201418;3. 同济大学附属第十人民医院内分泌科,上海 200072)
·临床研究·
精神分裂症患者代谢综合征与颈动脉内中膜厚度的相关性研究
朱景新1,2, 曲 伸3
(1. 同济大学医学院,上海 200092; 2. 上海市奉贤区精神卫生中心,上海 201418;3. 同济大学附属第十人民医院内分泌科,上海 200072)
目的 了解精神分裂症住院患者合并代谢综合征与颈动脉粥样硬化的关系。方法 检测150例住院精神分裂症患者腹围、血压、血糖、血脂、颈动脉B超等。结果 精神分裂症患者伴发代谢综合征的占34.7%,其颈动脉IMT值、颈动脉硬化和颈动脉斑块发生率均高于不伴有代谢综合征者(P<0.01)。伴发颈动脉硬化的占42%,其年龄、总病程、腹围、收缩压、FPG、TC、LDL明显大于不伴有颈动脉硬化者(P<0.05),但两组的住院时间、舒张压、TG、HDL-C差异无统计学意义(P>0.05);伴颈动脉硬化者的中心性肥胖、IFG、高血压、低HDL-C、代谢异常聚集患病率明显高于不伴颈动脉硬化者(P<0.05)、但在高TG的患病率上差异无统计学意义(P>0.05)。年龄、代谢异常聚集与颈动脉硬化有关(回归系数分别为: 1.339,1.971)。结论 长期住院的慢性精神分裂症患者代谢综合征、颈动脉硬化的患病率高,代谢综合征和颈动脉硬化密切相关,代谢综合征各组分间常协同存在,并共同在动脉粥样硬化发展过程中发挥重要作用。
精神分裂症; 代谢综合征; 动脉粥样硬化
精神分裂症患者常合并代谢异常,有研究显示精神分裂症患者的代谢综合征(metabolic syndrome, MS)发病率明显高于普通人群[1]。精神分裂症患者预期寿命比普通人缩短20%,心血管疾病是精神分裂症患者的首位死亡原因[2]。代谢综合征是一组代谢起源的相互关联的危险因素的集合,这些因素直接促成动脉粥样硬化性疾病,而颈动脉粥样硬化则作为全身动脉粥样硬化的早期反映和替代指标[3]。本研究旨在对住院精神分裂症患者合并代谢综合征及其各组分与颈动脉粥样硬化的关系进行探讨。
1 资料与方法
1.1 一般资料
对上海市奉贤区精神卫生中心2013年2月至2013年8月期间住院的186例精神分裂症患者进行调查。患者符合如下标准: (1) 符合《中国精神障碍分类与诊断标准第3版(CCMD-3)》精神分裂症诊断标准,年龄在20~75岁,首发或复发的患者;(2) 无心、肝、肾等重大脏器疾病史,非怀孕及哺乳期;(3) 连续应用抗精神病药物≥6个月。本组患者符合入组对象者150例。其中男性91例(60.7%),女性59例(39.3%),平均年龄(52.20±13.17)岁,男性平均年龄(49.82±13.40)岁,女性平均年龄(55.86±12.01)岁;平均病程(22.25±13.03)年,男性平均病程(20.77±12.93)年,女性平均病程(24.52±12.97)年。
1.2 方法
1.2.1 一般资料 自制调查表,对所有入组对象调查性别、年龄、病程、住院时间、治疗用药、疾病史等,检测包括身高、体质量、腰围、血压,并计算体质量指数(body mass index, BMI)=体质量(kg)/身高2(m2)。
1.2.2 实验室检查 所有患者禁食12h后于早晨6:00空腹抽取肘静脉全血4ml,检测血糖(FBG)、血浆总胆固醇(TC)、三酯甘油(TG)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)。上述检测由东芝TBA-40FR型生化分析仪完成。
1.2.3 颈动脉IMT测量 操作由专人负责。待测对象取仰卧位,颈后垫枕,头后仰,充分暴露颈前部,并偏向检查的对侧。取颈动脉长轴断面由近心端至远心端连续扫查,依次清晰显示颈总动脉近段、颈总动脉远段及颈总动脉窦部。同时注意观察颈动脉内膜是否光滑,动脉粥样硬化斑块的位置、数量及斑块性质等。测量心脏舒张期颈动脉后壁内中膜厚度(intima-media thickness, IMT)值。B超采用西门子超声波诊断仪(型号: ACUSON X1),探头频率2~5MHz。判断标准: IMT<1.0mm为正常;IMT增厚定义为≥1.0mm且<1.2mm;颈动脉粥样斑块定义为: 颈动脉系统任一血管节段存在突入管腔的回声结构,表面不光滑,或IMT≥1.2mm;颈动脉超声发现IMT增厚或颈动脉粥样斑块之一者即为患有颈动脉粥样硬化。
1.2.4 MS及代谢异常聚集诊断标准 代谢综合征诊断采用2005年美国国家胆固醇教育计划(NCEP)成人治疗组第三次指南(ATPⅢ修订版)的标准。符合以下3项及以上者: (1) 中心性肥胖: 男性腰围≥90cm,女性腰围≥80cm;(2) 高TG: TG≥1.7mmol/L或者已接受治疗者;(3) HDL-C降低: 男性HDL-C<1.03mmol/L,女性HDL-C<1.3mmol/L,或已接受治疗者;(4) 高血压: 血压≥130/85mmHg,或已诊断为高血压,或已接受治疗者;(5) 空腹血糖受损(impaired fasting glucose, IFG): FBG≥5.6mmol/L,或已诊断为糖尿病,及已接受治疗者。代谢异常聚集: 以MS组分异常≥2项定义为代谢异常集聚。
1.3 统计学处理
2 结 果
2.1 基本情况分析
150例精神分裂症患者MS、代谢异常聚集、中心性肥胖、高血压、IFG、高TG、低HDL-C的检出率分别为34.7%(52/150),56.0%(84/150),56.7%
(85/150),34.0%(51/150),21.3%(32/150),31.3%(47/150),42.0%(63/150)。颈动脉硬化63例,占42.0%(63/150),颈动脉粥样硬化斑块者38例,占25.3%(38/150),男、女颈动脉粥样硬化斑块检出率分别为25%和25.9%,差异无统计学意义(χ2=1.000,P>0.05)。
2.2 一般资料比较
精神分裂症患者有、无颈动脉硬化者的住院时间差异无统计学意义(P>0.05),男性患者颈动脉硬化患病率高于女性(P<0.01)。有颈动脉硬化者的年龄、总病程显著大于无颈动脉硬化者(P<0.01),进一步进行年龄、病程分层比较,不同年龄段之间颈动脉硬化的患病率差异有统计学意义(P<0.01),但不同病程之间患病率差异无统计学意义(P>0.05)。有颈动脉硬化者较无颈动脉硬化者中心性肥胖、IFG、高血压、低HDL-C、代谢异常聚集患病率明显增高(P<0.05)、但高TG的患病率差异无统计学意义(P>0.05),见表1。
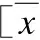
表1 有无颈动脉硬化者一般资料比较Tab.1 Comparison of general information between the patients with carotid AS and without carotid AS ±s,n(%)]

(续表1)
2.3 有无颈动脉硬化者部分体质参数及生化指标比较
伴颈动脉硬化的精神分裂症患者的腰围、收缩压、FBG、TC、LDL明显大于无颈动脉硬化的精神分裂症患者(P<0.05)。但舒张压、TG、HDL在两组间差异无统计学意义(P>0.05),见表2。
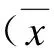
表2 有无颈动脉硬化者部分体质参数 及生化指标比较Tab.2 Comparison of physical parameters and biochemical index between two groups ±s)
1mmHg=0.133kPa
2.4 有无代谢综合征者颈动脉检查指标比较
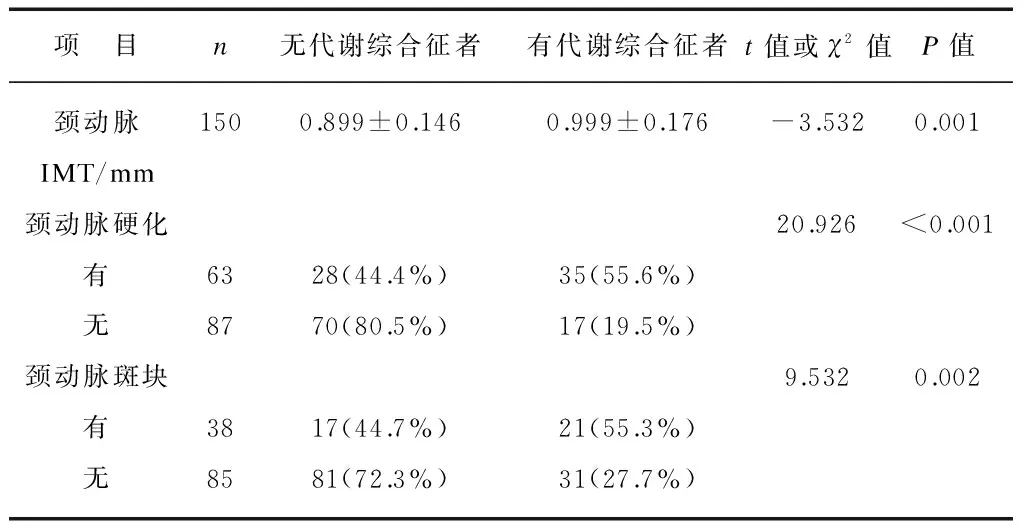
伴代谢综合征的精神分裂症患者颈动脉IMT显著大于无代谢综合征者(P<0.01),同时颈动脉硬化和颈动脉斑块的发生率均高于无代谢综合征者(P<0.05),见表3。
2.5 不同抗精神病药物颈动脉硬化患病率的比较
入组患者中单用一种抗精神病药物治疗者有90例,其中利培酮51例(占单一用药患者总数的56.67%),氯氮平8例(8.89%),奥氮平10例(11.11%),阿立哌唑10例(11.11%),喹硫平4例(4.44%),氯丙嗪5例(5.56%),奋乃静1例(1.11%),帕利哌酮1例(1.11%)。合并用药共60例(40%),多为利培酮合并氯氮平,或氯氮平合并阿立哌唑。将有无颈动脉硬化者的用药分为经典抗精神病药组和非经典抗精神病药组、氯氮平奥氮平组和其他药物组、单一用药组和合并用药组进行分组比较,各组之间两两比较患病率均差异无统计学意义(P>0.05),见表4。
表3 有无代谢综合征者颈动脉检查指标比较
Tab.3 Comparison of carotid artery index
between patients with MS and without MS

项 目n无代谢综合征者有代谢综合征者t值或χ2值P值颈动脉1500.899±0.1460.999±0.176-3.5320.001IMT/mm颈动脉硬化20.926<0.001有6328(44.4%)35(55.6%)无8770(80.5%)17(19.5%)颈动脉斑块9.5320.002有3817(44.7%)21(55.3%)无8581(72.3%)31(27.7%)
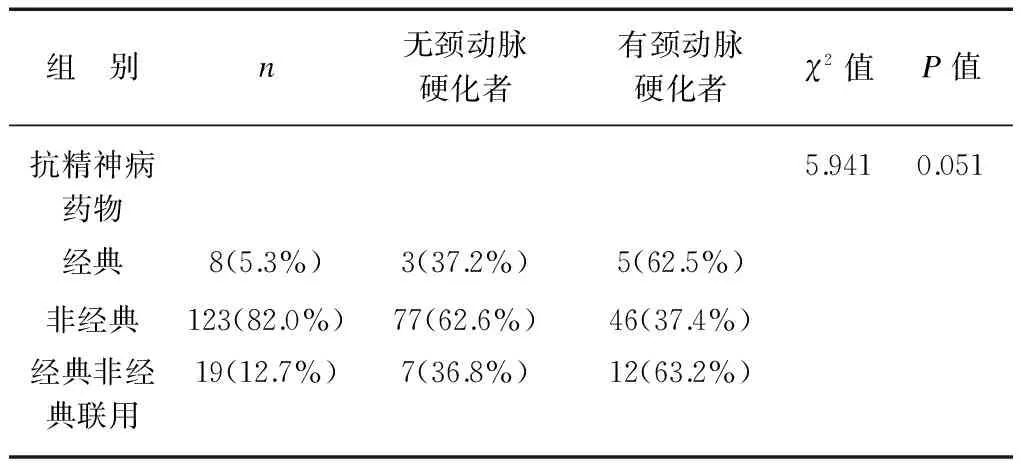
表4 应用不同抗精神病药物颈动脉硬化患病率的比较Tab.4 Comparison of the prevalence of carotid atherosclerosis in patients with different antipsychotic drugs [n(%)]

(续表4)
2.6 颈动脉硬化与代谢异常的logistic回归分析
logistic回归分析显示,年龄、代谢异常聚集与颈动脉硬化有关(P<0.05),提示这些因素为颈动脉硬化患病的独立危险因素;而性别、病程、中心性肥胖、高血压、IFG、低HDL-C与颈动脉硬化无明显相关性(P>0.05),见表5。
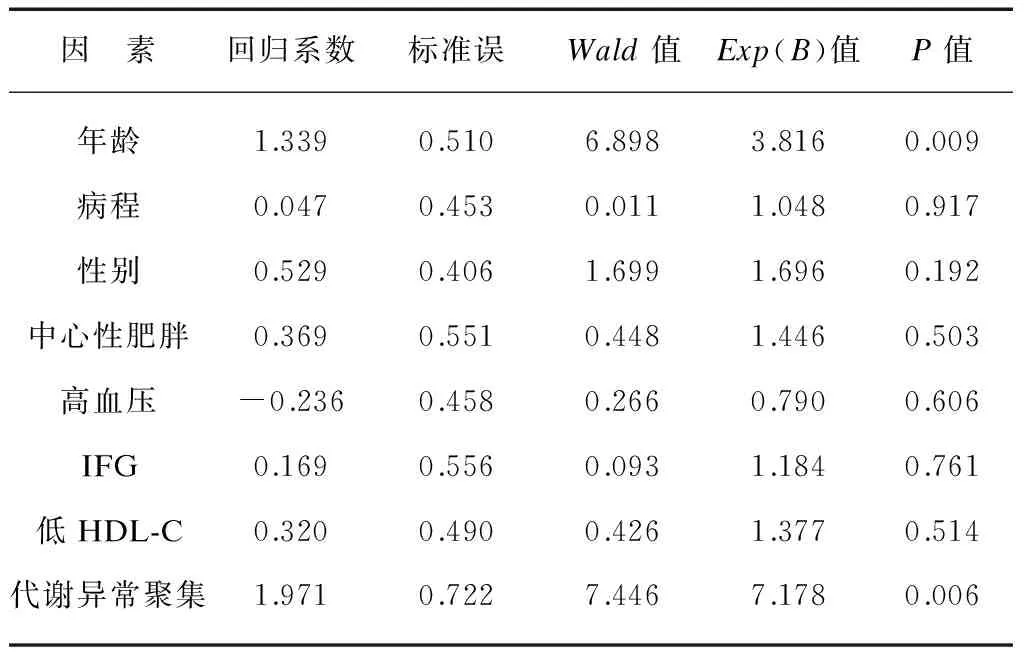
表5 影响精神分裂症患者伴发颈动脉硬化的 logistic分析结果Tab.5 Logistic analysis of the effect of carotid AS in patients with schizophrenia
3 讨 论
精神分裂症尤其长期服用抗精神病药物患者的体质量增加、MS及由此引起的心脑血管疾病的增加,已经引起临床医生高度重视。本研究结果显示,住院精神分裂症患者伴发MS患病率为34.7%,与国内多项研究结果接近,显著高于普通人群的17.14%[4-6]。住院精神分裂症患者颈动脉粥样硬化检出率为42%,是心脑血管疾病的高危人群。50岁以下人群颈动脉粥样硬化检出率为29.2%,随着年龄的增加,颈动脉粥样硬化检出率显著升高,50岁以上人群的检出率高达51.8%,差异有统计学意义著(P<0.05),显示年龄是精神分裂症患者发生颈动脉粥样硬化的高危因素。
近年来,研究表明,MS与动脉粥样硬化关系密切[7-8]。但以往的研究大多探讨MS中某一组分如高血压、糖尿病等单因素对于颈动脉等大血管结构与功能的损害,而实际上大血管病变往往是多重危险因素综合作用的结果。本研究以应用抗精神病药物治疗的住院精神分裂症患者为研究对象,颈动脉粥样硬化与代谢异常的单因素相关分析显示,中心性肥胖、IFG、高血压、低HDL-C、代谢异常聚集各指标与颈动脉硬化显著相关。有无MS患者之间颈动脉IMT、颈动脉硬化和颈动脉斑块的发生率差异有统计学意义,证明颈动脉硬化与MS紧密相关,两者有共同的危险因子。MS是多种代谢组分异常的病理生理状态,是包含中心性肥胖、高血压、高脂血症、IFG等导致全身动脉粥样硬化危险因素的综合征。其中,中心性肥胖是MS存在的基础,而MS的核心是胰岛素抵抗(insulin resistance, IR),IR是MS发生的主要病理生理基础[9-10],与MS患者的高血压、糖脂代谢异常等密切相关。IR可通过肾脏储钠,激活交感神经系统及改变血管平滑肌细胞内钠、钙离子的转动等途经引起血压升高,动脉壁平滑肌细胞增殖,加速动脉粥样硬化的发生和发展。糖脂代谢紊乱与动脉粥样硬化密切相关,是导致冠状动脉疾病的重要危险因素,IR能导致一系列代谢问题,这些问题都或多或少地对人体动脉粥样硬化产生加速推进作用,因此机体存在MS,心脑血管疾病的发生率大大增加。但同时说明积极控制机体的异常代谢,减少颈动脉硬化发生率,对预防心血管疾病发生具有重要作用。
越来越多的研究发现,抗精神病药物与患者的体质量增加、高血压、糖脂代谢紊乱有关[11],并可导致心脑血管疾病。但本研究不管是将药物分成经典组和非典型抗精神病药、氯氮平奥氮平组和其他药物组、单一用药组和合并用药组比较都未能发现服药情况与颈动脉粥样硬化的发生有密切关系,造成结果不一致的原因可能为: (1) 本研究总的调查人数较少,而其中部分药物(例如喹硫平、奋乃静、帕利哌酮等)的样本量更小,无法统计结果;(2) 无法完全澄清患者用药以前的代谢指标(如: 血糖、血脂、体质量等);(3) 入组患者有相当部分系长期住院者,故无法去除住院本身因素(如: 活动量减少、饮食习惯改变等)对患者代谢的影响。
在单因素相关分析的基础上,采用logistic回归模型进行与颈动脉硬化关系的多因素分析结果显示,年龄和代谢异常聚集是影响颈动脉硬化发生的独立危险因素,进一步证实代谢异常组分聚集对动脉粥样硬化的协同作用,异常组分越多对心血管的损害作用就越明显,提示MS各组分间存在共同的病理基础,多个危险因素聚集具有危险度叠加的作用。国外研究显示,有4个或更多MS组分的人群与无任何MS组分的人群相比,临床心血管病发生率增加5倍以上[12]。
总之,精神疾病患者心血管疾病的发生是多因素作用的结果,MS是心血管病的多种危险因素在个体内的集结状态,伴MS患者颈动脉粥样硬化明显,随着年龄增大,颈动脉粥样硬化程度加重。彩色多普勒超声通过检测颈动脉内膜-中层厚度可以直接观察动脉壁病变,对于预测精神病患者的心血管疾病风险,评价疗效和预后具有重要的临床价值。为了有效控制精神疾病患者MS的发生率,应定期监测患者的体质量及糖脂代谢指标,采取降压、降脂、控制血糖及体质量治疗,控制代谢紊乱,可延缓动脉粥样硬化的发生与发展,有效防止精神病患者心血管疾病的发生。
[1] McEvoy JP, Meyer JM, Gof DC, et al. Prevalence of the metabolic syndrome in patients with schizophrenia baseline results from the clinical antipsychotic trials of intervention effectiveness(CATIE) schizophrenia trial and comparison with national estimates from NHANESⅢ[J]. Schizophrenic Res, 2005,80(1): 19-32.
[2] Osby U, Corriera N, Brandt L, et al. Time trends od schizophrenia in stockholm county, Sweden: cohort study[J].BMJ, 2000,321,(1): 19-26.
[3] Dropinski J, Szczeklik W, Wegrzyn W. Increased carotid artery intima-media thickness as an indicator of the onset of atherosclerosis in patients with connective tissue systemic diseases[J]. Kardiol Pol, 2003,12: 475-483.
[4] 陈丽,杨贵刚,张兴理,等.长期住院精神分裂症患者伴发代谢综合征情况[J].临床精神医学杂志,2011,21(4): 272-274.
[5] 王秀丽,杨靖,刘娜,等.住院精神分裂症患者伴发代谢综合征的调查分析[J].医药论坛杂志,2011,32(11): 35-37.
[6] 岳德华,刘丽华,范勇,等.精神分裂症患者伴发代谢综合征的调查[J].临床精神医学杂志,2011,21(5): 326-328.
[7] Skolton MR, Moulin P, Serusclat A, et al. A comparison of the NCEP-ATPⅢ,IDF and AHA/NHLBI metabolic syndrome definitions with relation to early carotid atherosclerosis in subjects with hypercholesterolemia or at risk of CVD: evidence for sex-specific differences[J]. Atherosclerosis, 2007,190: 416-422.
[8] Lakka HM, Laaksonen DE, Lakka TA, et al. The metabolic syndrome and total and cardiovascular disease mortality in the middle-aged men [J]. JAMA, 2002,288( 21 ): 2709-2716.
[9] Ferrannini E. Is insulin resistance the cause of the metabolic syndrome [J]. Ann Med,2006,38(1): 42-51.
[10] Eckel RH, Grundy SM, Zimmet PZ. The metabolic syndrome [J]. Lancet, 2005,365 (9468): 1415-1428.
[11] 王从杰,张志珺,孙静,等.氯氮平和经典抗精神病药的长期治疗对患者体重、糖代谢及血脂的影响[J].中国神经精神疾病杂志, 2008,34(2): 65-68.
[12] Klein BE,Klein R, Lee KE. Components of metabolic syndrome and the risk of cardiovascular disease and diabetes in beaver dam[J]. Diabetes Care, 2002,25: 1790-1794.
Relationship between carotid artery intima-media thickness and metabolic syndrome in schizophrenic patients
ZHUJing-xin1,2,QUShen3
(1. School of Medicine, Tongji University, Shanghai 200092, China;2. Shanghai Fengxian Mental Health Center, Shanghai 201418, China;3. Dept. of Endocrinology, Tenth People’s Hospital, Tongji University, Shanghai 200072, China)
Objective To investigate the relationship between carotid atherosclerosis(AS)and metabolic syndrome(MS) in schizophrenic inpatients. Methods Abdominal circumference(AC), blood pressure(BP), fasting blood glucose(FPG), total cholesterol (TC), triglyceride (TG), high density lipoprotein cholesterol (HDL-C), low density lipoprotein (LDL), B-ultrasonography in carotid artery were examined in 150 inpatients with schizophrenia. Results The prevalence of MS in schizophrenic inpatients was 34.7%. The carotid intima-media thickness(IMT)of schizophrenia patients with MS was greater than those without MS (P<0.01),and the occurrence of carotid AS and carotid plaques were higher in patients with MS than those without MS (P<0.01). The prevalence of carotid AS in schizophrenic inpatients was 42%. The age, disease duration, AC, SBP, FBG, TC, LDL of patients with carotid AS were significantly greater than those without carotid AS (P<0.05), but there were no significant differences in length of hospital stay, DBP, TG, HDL-C between two groups (P>0.05). The prevalence of central obesity, impaired fasting glucose(IFG), hypertension, low HDL-C, metabolic abnormalities aggregation were significantly higher than those without carotid AS (P<0.05), but there was no significant difference in prevalence of high TG (P>0.05). Age and metabolic abnormalities aggregation might be the risk factors of carotid AS in this population (β=1.339 and 1.971 respectively). Conclusion The prevalence of MS and carotid AS is high in schizophrenia inpatients, MS and carotid AS is closely related,the components of MS often coexists, and play an important role in the development of AS.
schizophrenia; metabolic syndrome; atherosclerosis
10.16118/j.1008-0392.2015.04.018
2014-10-16
朱景新(1982—),男,主治医师,硕士.E-mail: 52614895@qq.com
曲 伸.E-mail: qushencn@hotmail.com
R 749.3
A
1008-0392(2015)04-0090-06
