海岛地区NA治疗无良好应答CHB患者HBV P区耐药突变分析
2015-07-07何剑营周吉航竺王玉陈冬冬黄燕燕李世波
何剑营,周吉航,竺王玉,陈冬冬,黄燕燕,李世波
(浙江省舟山医院:1.细胞分子生物学实验室;2.感染科,舟山316021)
海岛地区NA治疗无良好应答CHB患者HBV P区耐药突变分析
何剑营1,周吉航1,竺王玉1,陈冬冬1,黄燕燕1,李世波2
(浙江省舟山医院:1.细胞分子生物学实验室;2.感染科,舟山316021)
目的分析舟山地区经核苷类似物(NA)治疗无良好应答的慢性乙型肝炎(CHB)患者乙型肝炎病毒(HBV)P区耐药突变模式。方法收集2011年10月至2013年11月188例于浙江省舟山医院接受NA治疗无良好应答的CHB患者血清,采用直接测序法检测患者HBV P区基因突变状态。结果188例经NA治疗无良好应答的CHB患者HBV P区基因突变率为71.28%(134/188),主要模式:rtL180M+rtM204V/I/S突变率为26.12%(35/134),rtM204V/I/S突变率为25.37%(34/134),rtM181T/V/S突变率为16.42%(22/134);其中113例服用单种NA无良好应答患者有73例发生耐药变异(73/113,64.60%),多位点(3个及以上耐药位点)突变率为12.33%(9/73);75例服用多种NAs无良好应答患者有61例发生变异(61/75,81.33%),多位点突变率为16.39%(10/61),多药使用者发生耐药突变率明显高于单药使用者,差异有统计学意义(Χ2=6.631,P<0.05)。结论在NA治疗无良好应答CHB患者中耐药变异发生率高,且长期服用多种NAs易发生多点突变;监测HBV P区耐药突变可为NA耐药CHB患者用药提供依据。
肝炎病毒,乙型;肝炎,乙型,慢性;核苷类;DNA突变分析;药物耐受性
乙型肝炎病毒(hepatitis B virus,HBV)感染是全世界范围内的重大公共卫生问题,但不同地区HBV流行趋势差异很大,我国是全球HBV感染最为严重的地区之一。目前,乙型肝炎患者遇到的最大问题是药物治疗效果不理想,其很大原因是病毒产生了耐药性。研究证实,HBV耐药与HBV P区突变存在着密切关系[1-2]。本研究选择对核苷类似物(nucleoside anologue,NA)治疗无良好应答的慢性乙型肝炎(chronic hepatitis B,CHB)患者为研究对象,分析其感染HBV P区的变异情况及NA类药物使用情况,以期为临床合理使用NA类药物提供依据。
1 资料与方法
1.1 一般资料 收集并筛选2011年10月至2013年11月在本院接受NAs[拉米夫定(LAM)、阿德福韦酯(ADV)、替比夫定、恩替卡韦(ETV)]单药或联合用药治疗1年以上且无良好应答的CHB患者188例,诊断均符合《慢性乙型肝炎防治指南》[3]标准。其中男151例,女37例;平均年龄(45.8±11.1)岁。
1.2 方法
1.2.1 HBV核酸提取与DNA定量检测 采集受检者空腹静脉血1 mL,注入1.5 mL无菌离心管中,于室温静置2 h,转入4℃静置1 h,8 000 r/min离心5 min,吸取200μL上清液转入另一1.5 mL无菌EP管中,-20℃保存待测;采用上海申友生物技术有限公司HBV DNA检测试剂盒抽提HBV DNA后,在ABI7500荧光定量PCR仪上进行定量检测。操作严格按照试剂盒说明书进行。
1.2.2 HBV P区耐药基因突变检测 采用上海申友生物技术有限公司HBV DNA检测试剂盒抽提HBV DNA,美国BIO-RADMyCyclerTMthermalcycler扩增DNA,反应条件为42℃5 min、94℃5 min后,94℃10s、55℃30 s、72℃40 s,共45个循环。用1.5%M/V琼脂糖凝胶鉴定扩增产物。取阳性扩增产物3 μL,加入虾碱性磷酸酶(SAP)2 μL进行酶解后,取酶解产物3 μL、测序试剂bigdye 1 μL和测序引物2 μL进行测序PCR反应,反应条件:96℃1 min,96℃10 s,50℃5 s,60℃4 min,共25个循环。将测序产物用乙醇/EDTA-Na2法进行纯化,高度去离子甲酰胺(Hidi)10 μL溶解后,ABI 3130XL测序仪(美国ABI公司)直接测序,数据收集和分析软件分别为3 130 xl Data Collection SW V3.1和Sequencing Analysis V5.4。
1.3 统计学处理 将患者HBV DNA水平(U/mL)转化为对数结果(lg U/mL)进行分析。应用SPSS17.0统计软件进行数据分析,计量资料以±s表示,采用方差分析或t检验;计数资料以率或构成比表示,采用Χ2检验或Fisher精确检验,P<0.05为差异有统计学意义。
2 结 果
2.1 NA治疗无良好应答CHB患者HBV P区基因突变模式 188例经NA治疗无良好应答的CHB患者HBV P区基因突变率为71.28%(134/188),其中主要有3种突变模式:rtL180M+rtM204V/I/S模式突变35例,占26.12%(35/134),rtM204V/I/S突变34例,占25.37%(34/ 134),rtA181T/V/S突变22例,占16.42%(22/134)。其他小于3例的突变模式共17种,共计23例。单点突变模式共6种,共计66例,占49.25%(66/134)。见表1。
2.2 NA治疗无良好应答CHB患者用药情况比较 188例经NA治疗无良好应答的CHB患者中,单一NA用药113例,检测出耐药突变73例,突变率为64.60%,其中多位点(3个及以上耐药位点)突变9例(9/73,12.33%);多NAs用药75例,检测出耐药突变61例,突变率为81.33%,其中多位点突变10例,占16.39%(10/61)。多NAs用药突变率明显高于单一NA用药,二者比较,差异有统计学意义(Χ2=6.631,P<0.05)。见表2。

表1 NA治疗无良好应答CHB患者HBV P区基因突变模式
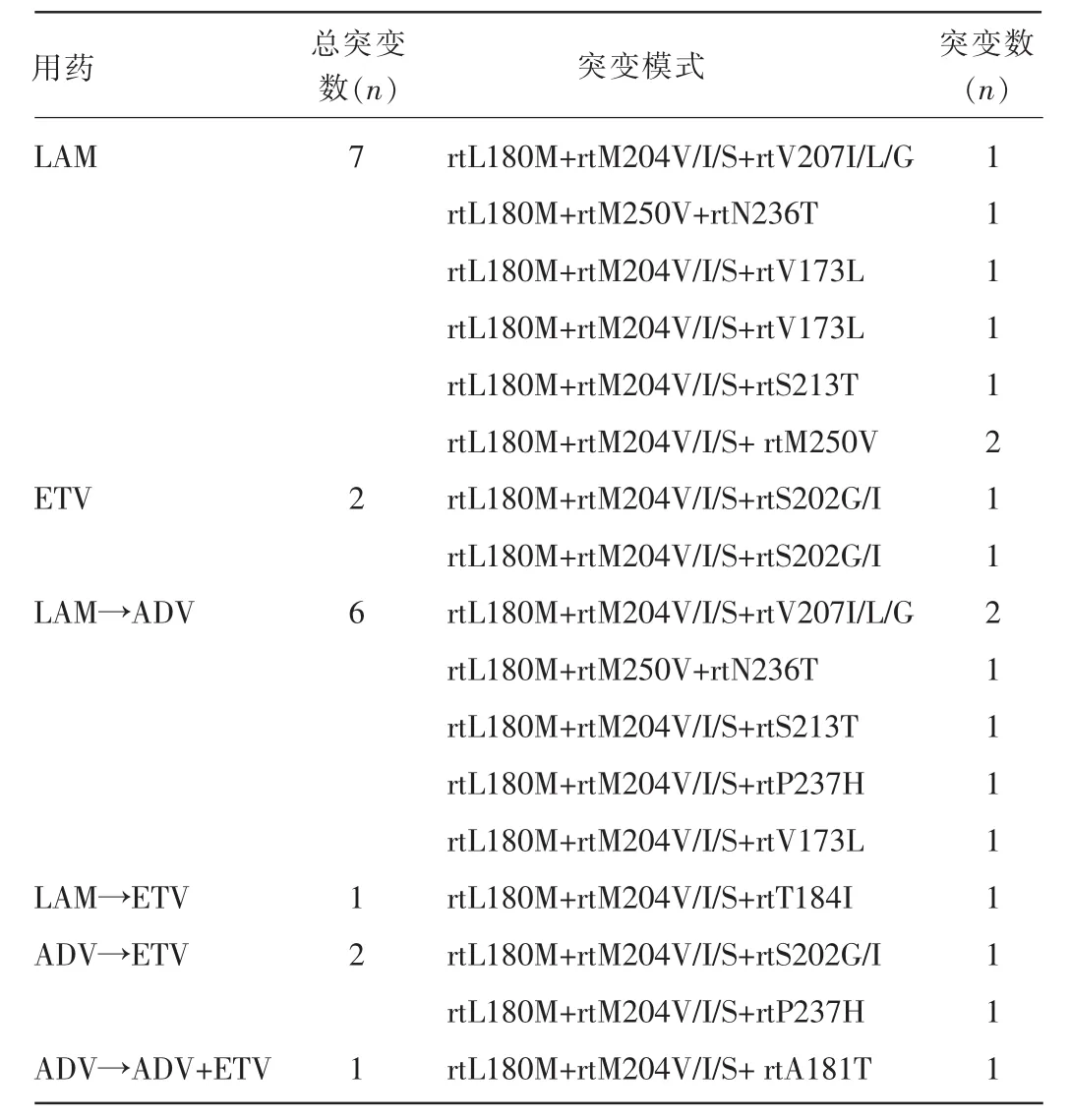
表2 HBV P区基因多位点耐药患者用药情况
3 讨 论
有研究发现,HBV对NA耐药性的产生与HBV P区变异密切相关[3]。本研究对188例服用NAs治疗1年以上且无良好应答的CHB患者进行基因耐药检测发现134例出现突变,突变率(71.28%)显著提高,提示NAs治疗后产生耐药突变是CHB患者对NAs治疗无良好应答的重要原因。
本研究主要检测到的突变模式为rtL180M+rtM204V/ I/S、rtM204V/I/S、rtA181T/V/S,这与LAM和ADV的耐药位点相匹配,可能与临床主要应用这两类药物有关。其中最主要的两类突变模式rtL180M+rtM204V/I/S和rtM204V/I/S为LAM耐药的HBV P区突变模式[4-5],提示本组患者以LAM耐药的CHB患者为主。有研究认为,rtV173L突变不足以导致LAM的耐药,但可作为补偿性的突变提高rtM204位点突变病毒的复制能力[6],本研究中也检测到rtV173L联合突变3例,说明这一突变在CHB患者中可与其他突变伴随出现,但此类突变是否可致患者免疫功能缺陷有待进行大样本的针对性研究证实。另外,LAM治疗发生耐药的CHB患者少见有rtV207I/L/G突变的报道,但在本研究中可见rtV207I/L/G突变11例(其中单纯rtV207I/L/G 5例),提示此类突变应在NA耐药的CHB患者中引起重视。本研究结果显示,ADV耐药突变点以rtA181V/T/S单点突变为主,可见N236T联合A181T及rtV214A单点突变,但未见N236T联合A181V突变,这可能与LAM长期应用出现rtA181T变异有关[7]。相对于LAM,ADV的应用相对较少,出现耐药的概率也较低。此外,无论是单一形式还是组合形式,rtM204V/I/S突变率均最高,提示应对这一位点加以保护[8-9]。
多NAs用药患者耐药位点突变率及多位点突变率均高于单一NA用药组,提示应用多种药物并不能根本解决耐药问题,相反,可能导致多药耐药[10]。本研究结果显示,LAM耐药后改用ADV易发生多位点突变。且已有研究证实,对LAM耐药的患者,改用ADV比加用ADV更易导致多重耐药变异[11],提示对未用过ADV患者LAM耐药后应加用ADV。
综上所述,目前通过对乙型肝炎患者进行HBV突变检测来指导临床用药越来越受到重视,本研究总结了NA治疗无良好应答CHB患者HBV P区突变特点,初步揭示了CHB患者中存在的各类HBV P区突变模式及与NAs用药之间存在的关联,提示对于初治及长期应用NA类药物无良好应答的患者更换药物之前均应进行基因耐药检测,根据用药史及临床特点,合理选择药物,实行个体化治疗,尽量避免因用药不当而产生耐药的情况。
[1]Sheldon J,Soriano V.Hepatitis B virus escape mutants induced by antiviral therapy[J].J Antimicrob Chemother,2008,61(4):766-768.
[2]许利军,潘晨,李勤光,等.拉米夫定治疗无良好应答患者乙型肝炎病毒P区突变与基因型的关系[J].中华肝脏病杂志,2010,18(3):181-183.
[3]中华医学会肝病分会,中华医学会感染病学分会.慢性乙型肝炎防治指南(2010年版)[J].中华肝脏病杂志,2011,3(1):40-56.
[4]张继明.乙型肝炎病毒对拉米夫定的耐药性及防治[J].中国实用内科杂志,2007,27(11):894-897.
[5]汤佳良,周建康.拉米夫定耐药慢性乙型肝炎患者HBV P区基因突变模式与基因型的关系[J].中华实验和临床病毒学杂志,2011,25(5):342-344.
[6]Xiong X,Yang H,Westland CE,et al.In vitro evaluation of hepatitis B virus polymerase mutations associated with famciclovir resistance[J].Hepatology,2000,31(1):219-224.
[7]Yeh CT,Chien RN,Chu CM,et al.Clearance of the original hepatitis B virus YMDD-motif mutants with emergence of distinct lamivudine-resistant mutants during prolonged lamivudine therapy[J].Hepatology,2000,31(6):1318-1326.
[8]张征,胡小宣.拉米夫定耐药患者乙型肝炎病毒P区变异及其特点[J].医学临床研究,2012,29(9):1743-1744.
[9]曹亦菲,何平,谭晓华.1012例乙肝病毒患者HBV P区基因位点变异分析[J].健康研究,2011,31(1):17-20.
[10]Michailidis E,Kirby KA,Hachiya A,et al.Antiviral therapies:focus on hepatitis B reverse transcriptase[J].Int J Biochem Cell Biol,2012,44(7):1060-1071.
[11]徐玲娟,盛秀胜.核苷(酸)类药治疗慢性乙肝患者HBV逆转录酶区基因耐药的变异分析[J].温州医学院学报,2011,41(5):435-438.
Analysis on drug resistance mutation of HBV P region in CHB patients without good response to NA treatment in island area
HeJianying1,ZhouJihang1,Zhu Wangyu1,Chen Dongdong1,Huang Yanyan1,Li Shibo2
(1.Laboratyory of Cellular and Molecular Biology;2.Department of Infection,Zhejiang Zhoushan Hospital,Zhoushan 316021,China)
ObjectiveTo analyze the drug resistance mutation patterns of the HBV P region in CHB patients without good response to the nucleoside analogues(NA)treatment in Zhoushan area.MethodsSera were collected from the chronic hepatitis B (CHB)patients without good response to the NA treatment in our hospital from October 2011 to November 2013 and detected the gene mutation status of the HBV P region by using the direct sequencing method.ResultsIn 188 CHB patients without good response to the NA treatment,the gene mutation rate of HBV P region was 71.28%(134/188),the main patterns included rtL180M+ rtM204V/I/Sin35 cases(35/134,26.12%),rtM204V/I/Sin34cases(34/134,25.37%)and rtM181T/V/S in 22 cases(22/134,16.42%);among 113 CHB patients without good response to single NA treatment,73 cases(73/113,64.60%)developed the drug resistance mutation,the incidence rate of multi-site(three ormore sites)mutations was 12.33%(9/73);in 75 cases of multiple NAs without good response,61 cases(61/75,81.33%)developed the variation,the multiple site mutation rate was 16.39%(10/61),the drug resistance rate in the cases of multiple NAs was significantly higher than that in the cases of single NA,the differences was statistically sig nificant(Χ2=6.631,P<0.05).Conclusion The CHB patients without good response to the NA treatment have higher drug resistance mutation rate,moreover long term taking multiple NAs is easy to generate the multi-site drug resistance mutation;monitoring the drug resistance mutation of HBV P region can provide the basis for the medication in the patients with NA-resistant CHB patients.
Hepatitis B virus;Hepatitis B,chronic;Nucleosides;DNA mutational analysis;Drug tolerance
10.3969/j.issn.1009-5519.2015.16.001
A
1009-5519(2015)16-2409-03
2015-05-19)
本刊欢迎各类基金课题论文
为了更快地传播、交流医学科学技术领域的新成果、新技术,本刊特别欢迎各类基金课题论文,基金课题论文包括国家自然科学基金、国家各部委及各省、市、自治区的各种基金课题所产生的论文。本刊将以优惠价格,优先安排发表,鼓励基金课题作者踊跃投稿。基金项目需写明基金名称及编号,并附单位证明,否则无效。
本刊编辑部
浙江省科技厅项目(2011C37030、2013C37079)。
何剑营(1986-),男,浙江舟山人,主要从事临床分子诊断、基因组学研究;E-mail:hjyncmcstudent@163.com。
李世波(E-mail:lsb0398@126.com)。
