钆掺杂TiO2的制备及其光催化降解乙酰甲胺磷的研究
2015-07-02于田田李晓玲李沙沙李雪莲
朱 军,于田田,李晓玲,李沙沙,李雪莲
宿州学院化学化工学院,安徽宿州,234000
钆掺杂TiO2的制备及其光催化降解乙酰甲胺磷的研究
朱 军,于田田,李晓玲,李沙沙,李雪莲
宿州学院化学化工学院,安徽宿州,234000
采用溶胶-凝胶法制备了钆掺杂TiO2催化剂,并通过X射线衍射仪(XRD)、扫描电镜(SEM)等手段对催化剂进行表征,研究了不同TiO2的加入量、光照时间、钆离子掺杂量对乙酰甲胺磷农药降解性能的影响。结果表明:掺杂一定量Gd3+的TiO2对乙酰甲胺磷农药有明显的降解作用,当二氧化钛用量为0.6 g/L、降解时间为1 h时,Gd3+掺杂量为1.2%,对乙酰甲胺磷的降解率达到92.56%。
二氧化钛;钆;乙酰甲胺磷;光催化;降解
目前,对于消除残留农药问题的研究主要表现在微生物降解和光催化降解两方面。微生物降解方法存在难操作、降解不彻底等问题,而光催化技术以其高效、易操作、稳定性好、应用范围广、降解彻底、无二次污染等优点,引起了国内外学者的普遍关注[1]。其中,TiO2光催化降解技术表现出活性高、稳定性好、对机体无害、过量使用也不会产生污染等优点[2-5],已被广泛用于环境污染预防和治理中。
但TiO2在实际应用中仍存在一些缺陷,如光催化的带隙宽度较大,只能被波长较短的紫外光激发,故对太阳能的利用率很低;如光激发产生的电子与空穴很容易复合,导致光量子效率极低,极大地限制了TiO2在各方面的应用[6]。因此,如何更好地提高降解率成了研究热点,目前已有研究关于利用稀土掺杂TiO2等来解决降解率低的问题,如Bzunova-Bujnova等[8]利用热喷射法制备La掺杂二氧化钛,以亚甲基蓝为降解物进行光催化降解实验。
本文利用溶胶-凝胶法制备掺杂钆的TiO2,探究有无光照、光照时间、TiO2的用量以及掺杂不同比例Gd3+对乙酰甲胺磷降解的影响,以此来探寻稀土掺杂TiO2降解乙酰甲胺磷的可行性。
1 实验部分
1.1 实验仪器及药品
主要仪器:DX-2600型X射线衍射分析仪(丹东方圆仪器有限公司)、SU1510扫描电子显微镜(日本日立有限公司)、傅里叶变换红外光谱仪(370ThermoNicolect)、2950纳米粒度及Zeta电位分析仪(英国马尔文仪器有限公司)、TU-3310型紫外可见分光光度计(日本日立有限公司)。
主要药品:钛酸四丁酯(国药集团化学试剂有限公司)、无水乙醇(安徽安特食品股份有限公司)、冰乙酸(安徽安特食品股份有限公司)、硝酸钆(国药集团化学试剂有限公司)、乙酰甲胺磷(国药集团化学试剂有限公司)等,所有试剂均为分析纯。
1.2 实验步骤
1.2.1 掺杂钆的TiO2催化剂制备
取17 mL钛酸四丁酯与60 mL无水乙醇混合搅拌30 min至均匀为A液,将5.0 mL 0.1 mol/L的硝酸钆溶液与15 mL冰乙酸、42.5 mL95%乙醇充分搅拌30 min至均匀为B液。边搅拌边将A液加入B液中,继续搅拌1 h后形成胶体,在室温下放置48 h后将该胶体放置95℃烘箱中12 h后,将其研磨后放马弗炉中,在500℃下煅烧2 h形成掺杂的TiO2催化剂(掺杂量1.2%)[9]。采用同法制备0.6% Gd3+-TiO2和1.8% Gd3+-TiO2。
1.2.2 掺杂钆的TiO2催化剂的表征
采用XRD、SEM、FT-IR、纳米粒径仪对催化剂进行表征。
1.3 乙酰甲胺磷的光催化降解实验
原理:在降解条件下,有机磷农药中的磷酸酯键易水解,转变成磷酸盐。磷酸盐在一定的酸度条件下,能和钼酸铵发生反应,生成磷钼杂多酸,加入还原剂,磷钼杂多酸可转变成蓝色络合物,即为钼蓝。据钼蓝的颜色深浅可以判断有机磷农药的残留量[10]。
1.3.1 磷标准工作液的标准曲线
分别量取0.00 mL、1.00 mL、2.00 mL、3.00 mL、4.00 mL、5.00 mL、6.00 mL、7.00 mL工作液于50 mL比色管中,加水稀释到25 mL处,然后依次加入2.0 mL钼酸铵溶液(26 μg/L)、1.0 mL抗坏血酸溶液(100 g/L),再加水到50 mL处,混合均匀,在45℃下显色10 min,在波长895 nm下分别测量溶液吸光度, 数值如表1。

表1 不同浓度磷标准工作液的吸光度
由表1可知,磷标准工作液在0~160 μg/L范围内,作图得质量浓度与吸光度A具有良好的线性关系。拟合的标准曲线方程为C=0.0058*A+0.0108,相关系数R2=0.9988。
1.3.2 乙酰甲胺磷的光催化降解实验
量取20 mL的乙酰甲胺磷标准液,分别加入一定量纯的TiO2、Gd3+-TiO2与乙酰甲胺磷标准液混合,边搅拌边在紫外灯下照射约1 h,取出溶液经离心分离。因为需要将清液中有机磷转换为无机磷,需要采用文献[11]中酸消解法进行消解溶液。依据上述方法测定有机磷农药残留量。
按照下式计算出乙酰甲胺磷的降解率。
式中,C1为乙酰甲胺磷的起始浓度,C2为t时间乙酰甲胺磷的浓度。
2 结果与讨论
2.1 掺杂钆的TiO2催化剂表征
2.1.1 掺杂钆的TiO2催化剂XRD
图1是纯TiO2及掺杂不同比例Gd3+-TiO2的XRD。由图可知,在2θ约为25°时有明显的晶面衍射峰出现,对照标准谱图库[7]得到衍射角为25.3°、37.8°、48.0°等分别属于锐钛矿的(101)、(009)、(200)的衍射峰,因此可推断所制备的催化剂中晶型主要是以锐钛矿TiO2形式存在。依据锐钛型计算公式[12]:
锐钛型%=1/(1+1.265IB/IA)
其中,IA为锐钛型最强衍射峰的强度,IR为金刚石最强衍射峰的强度。
由图1(b)至(d) 可以计算出,随着Gd3+掺杂的增加(101)晶面衍射峰的强度减弱。

图1 纯TiO2及掺杂不同比例Gd3+-TiO2的XRD
2.1.2 掺杂钆的TiO2催化剂SEM
图2为掺杂不同比例Gd3+-TiO2的SEM。由图2(a)至(c)可以看出,图2(b)中分散颗粒粒度较好,团聚相对较少,独立分散出来的物质相对较多;图2(a)与(c)相对(b)表面分散颗粒不均匀,没有图2(b)好。因此,百分比为1.2%Gd3+团聚相对较少,独立分散出来的物质相对较多。

图2 掺杂不同比例Gd3+-TiO2的SEM
2.1.3 1.2%La3+-TiO2与1.2%Gd3+-TiO2的EDS
图3是1.2%Gd3+-TiO2的能谱图,表2是1.2%Gd3+-TiO2不同元素含量百分比的EDS。由表2可以看出Gd3+掺杂的较好。

图3 1.2% Gd3+-TiO2的能谱图
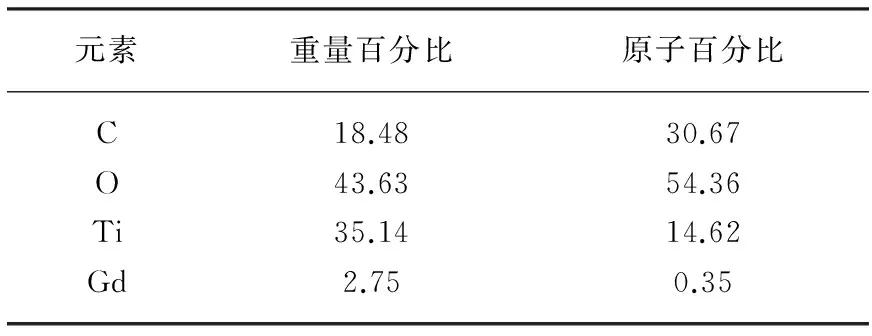
元素重量百分比原子百分比C18.4830.67O43.6354.36Ti35.1414.62Gd2.750.35
2.1.4 掺杂钆的TiO2催化剂FT-IR
图4为纯TiO2与掺杂不同比例Gd3+-TiO2的FT-IR。由图4(a)、(b)、(d)可以看出Ti-O键的弯曲振动峰随掺杂量强度增加减弱[13],在Gd3+掺杂量为1.2%时,演变成为一个宽而平的吸收带,表明该条件Gd3+-TiO2的光催化性能较好。

图4 纯TiO2与掺杂不同比例Gd3+-TiO2的FT-IR
2.1.5 掺杂钆的TiO2催化剂纳米粒径
图5是掺杂不同比例Gd3+-TiO2的纳米粒径的变化图。由图5(a)至(d)可以得出结论:稀土钆掺杂的TiO2催化剂属于纳米级范围。

图5 纯TiO2与掺杂不同比例Gd3+-TiO2的纳米粒径
2.2 掺杂钆的TiO2催化剂催化性能研究
2.2.1 不同光照对乙酰甲胺磷降解的影响
通过以下两种方式探究了不同光照对乙酰甲胺磷降解效果的影响:一组为有紫外灯照射60 min,无催化剂;另一组为有催化剂在自然光下放置60 min,测定其降解率。所得结果分别为5.8%和1.3%,表明比乙酰甲胺磷在紫外光照、有催化剂的条件下降解率较高。
2.2.2 光照时间对乙酰甲胺磷降解的影响
图6为光照时间对降解率的影响。光照时间对乙酰甲胺磷的降解起到非常重要作用。取0.6 g/L TiO2,紫外灯照射下,分别在10、20、30、40、50、60、70、80、90 min,研究它们对乙酰甲胺磷降解的影响,结果如图6所示。由图6可知,随着时间的增加,乙酰甲胺磷降解率在不断变化,到60 min时,降解率为78.35%,达到最大;当随着时间的继续增加,降解率又呈下降趋势,说明最适宜时间为60 min,因此以下实验选择光照时间为60 min。

图6 光照时间对降解率的影响
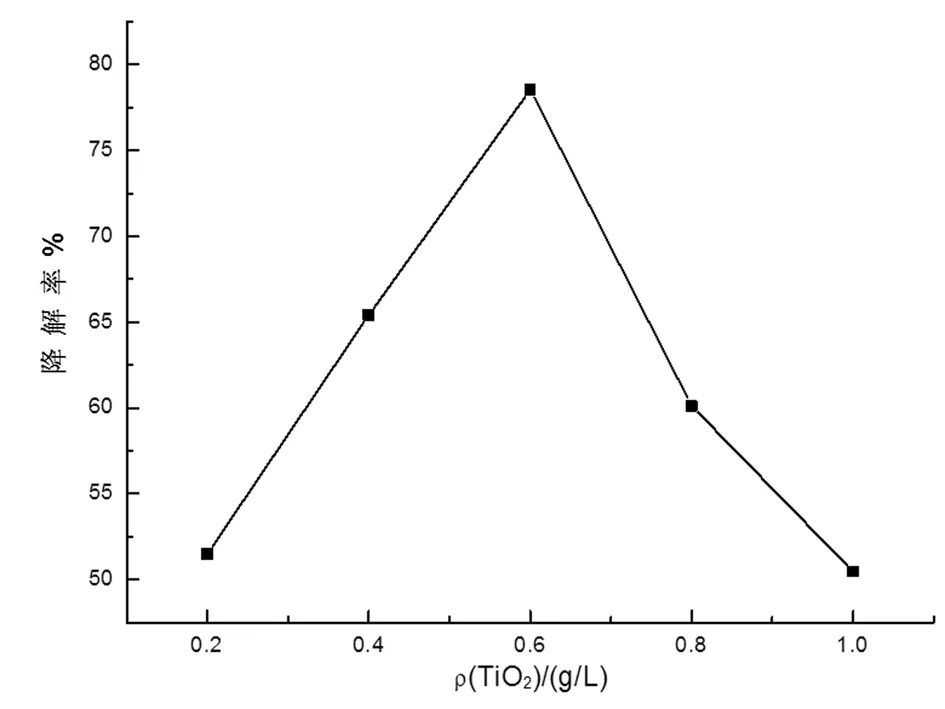
图7 二氧化钛用量对乙酰甲胺磷降解的影响
2.2.3 纯TiO2加入量对乙酰甲胺磷降解的影响
图7为TiO2加入量对乙酰甲胺磷降解的影响情况。在ρ=0.02 μg/L,紫外灯光照下,时间为60 min,分别取0.2、0.4、0.6、0.8、1.0 g/L TiO2,测吸光度,研究对乙酰甲胺磷降解的影响,结果如图7所示。TiO2的用量对乙酰甲胺磷降解具有很大影响并存在最大值,此最大值点在TiO2用量为0.6 g/L处,当TiO2用量增加时,乙酰甲胺磷的降解率没有增加,反而下降。说明催化剂的用量对乙酰甲胺磷降解率的影响存在一个最佳值,即随着催化剂的增加,降解率升高,当到达一定值时,随着催化剂继续增加而降低。
2.2.4 钆掺杂量对乙酰甲胺磷降解率的影响
图8为Gd3+的掺杂量对乙酰甲胺磷降解的影响。在ρ=0.02 g/L,紫外灯照射下,在T=60 min分别取0.6%Gd3+-TiO2、1.2%Gd3+-TiO2、1.8%Gd3+-TiO2各0.6 g/L测定吸光度,结果如图8所示。由图8可知,乙酰甲胺磷的降解率和Gd3+的掺杂量有关,刚开始随掺杂量的增大而增加,当超过某一值时,降解率下降。从本实验看出, Gd3+的掺杂量为1.2%时,乙酰甲胺磷的降解率较高。

图8 Gd3+的掺杂量对乙酰甲胺磷降解的影响
3 结 论
本实验采用溶胶-凝胶法制备了钆掺杂TiO2催化剂,当Gd3+掺杂量为1.2%时,在500℃煅烧2 h制备的催化剂的主要晶型为锐钛矿型;当催化剂的用量为0.6 g/L,紫外光照射下,降解时间60 min时,对乙酰甲胺磷的降解率达到92.56%。
[1]徐悦华,古国榜,李新军.光催化降解甲胺磷影响因素的研究[J].华南理工大学学报,2001,29(5):68-71
[2]Xie Y B,Yuan C W.Characterize ion and photo catalysis of Er3+TiO2sol in the hydrosol react ion system[J].Materials research bulletin,2004,39:533-543
[3]梁春华,李芳柏.稀土铒掺杂TiO2光催化剂的吸附和光催化活性研究[J].环境科学与技术,2008,31(7): 25-31
[4]岳林海.稀土元素掺杂二氧化钛催化剂光降解久效磷的研究[J].上海环境科学,1998,17(9):17-19
[5]王琰,王敬国,胡林.农药光催化降解研究进展[J].西北农林科技大学学报,2008,36(9):162-166
[6]柴瑜超,林琳,赵斌.稀土掺杂二氧化钛光催化剂的研究进展[J].材料导报,2013,27(1):38-43[7]Liang C H,Liu C S,Li F B,et al.The effect of Praseodymium on the adsorption and photo-catalytic degradation of a zodye in 2009,147:219-225
[8]梁春华.铒掺杂二氧化钛光催化降解甲胺磷农药的研究[J].吉林农业大学学报,2012,34(5):536-539
[9]殷晓梅,王欣,雷磊.磷钼蓝分光光度法测定有机磷农药残留量的改进[J].食品与发酵工业,2011,37(7):171-175
[10]GB/T 6913-2008.锅炉水和冷却水分析方法磷酸盐的测定[S].北京:中国标准出版社,2008:1-6
[11]邢磊,张前程,简丽,等.La,Pr,Nd掺杂对纳米TiO2光催化性能的影响[J].人工晶体学报,2010,39(3):724-729
[12]Xie Y B.Rare-earthion modified TiO2sols for photo catalysti sap plication under visible light excitation[J].Rare Metals,2004,23:20-26
(责任编辑:刘小阳)
10.3969/j.issn.1673-2006.2015.08.031
2015-02-26
安徽省教育厅自然科学研究自筹项目“二氧化钛/碳纳米管/壳聚糖复合材料的制备及应用”(KJ2013Z315);自旋电子与纳米材料安徽省重点实验室开放课题“二氧化钛/碳纳米管/壳聚糖复合材料的制备及应用研究”(2012YKF02);宿州学院一般科研项目“头孢类药物及纳米材料与蛋白质相互作用的研究”(2014yyb09);宿州学院教学研究项目“《环境保护》课程实施探究性学习的研究”(SZXYJY200816)。
朱军(1973-),女,安徽宿州人,硕士,副教授,主要研究方向:环境化学。
O611.4
A
1673-2006(2015)08-0103-05
