白藜芦醇对糖尿病肾病大鼠氧化应激反应的影响研究①
2015-07-02张志全刘莹男李君实尹芳革刘中柱
张志全,高 辉,刘莹男,李君实,尹芳革,刘中柱
(1.佳木斯大学附属第一医院,黑龙江 佳木斯 154003;2.93212部队,辽宁 普兰店 116200;3.佳木斯市中心医院,黑龙江 佳木斯 154002;4.佳木斯市妇幼保健院,黑龙江 佳木斯 154003)
白藜芦醇对糖尿病肾病大鼠氧化应激反应的影响研究①
张志全1,高 辉2,刘莹男3,李君实4,尹芳革4,刘中柱1
(1.佳木斯大学附属第一医院,黑龙江 佳木斯 154003;2.93212部队,辽宁 普兰店 116200;3.佳木斯市中心医院,黑龙江 佳木斯 154002;4.佳木斯市妇幼保健院,黑龙江 佳木斯 154003)
目的:研究白藜芦醇对实验用糖尿病肾病大鼠氧化应激指标及血管通透性因子VPF表达的影响。方法:雄性Wistar大鼠,随机分为正常对照组Ⅰ、糖尿病肾病模型组Ⅱ、白藜芦醇治疗组Ⅲ。Ⅱ组与Ⅲ组动物制备糖尿病肾病模型成功。Ⅲ组进行白藜芦醇灌胃干预,100mg/kg·d,其他两组灌胃等量生理盐水。分别在4w、8w、12w,常规检测尿蛋白含量,并检测血糖、血肌酐和尿素氮。在4w、8w、12w取肾脏标本制病理切片,用PAS法制片观察糖原沉积,用免疫组化法标记VPF表达。在12w末用化学比色对照法检测氧化应激指标MDA,T-SOD,GSH-PX的表达情况情况。结果:Ⅱ组大鼠血糖、血肌酐、尿素氮和尿蛋白明显升高(P<0.05)。Ⅱ组肾脏病理组织VPF表达阳性度高于Ⅰ组,Ⅲ组低于Ⅱ组表达;Ⅱ组大鼠血糖、血肌酐、尿素氮和尿蛋白明显升高;Ⅱ组肾脏病理组织VPF表达阳性度高于Ⅰ组,而Ⅲ组又低于Ⅱ组表达;氧化应激各项指标通过对照比较,Ⅲ组与Ⅱ组比较MDH降低,T-SOD、GSH-px均升高。结论:白藜芦醇有效降低了糖尿病肾病大鼠血糖、肌酐、尿蛋白等生化指标,并有有效改善了MDH、T-SOD、GSH-px等氧化应激指标,降低了血管通透性因子VPF的表达,起到了肾脏修复作用。
糖尿病肾病;氧化应激;血管通透性因子
糖尿病肾病是糖尿病人群重要代表性的并发症之一,现已成为终末期肾脏病的第二原因,仅次于各种肾小球肾炎,发病率呈上升势头。由于代谢功能失调呈现变化多样性,所以终末期肾脏病甚至比其他肾脏疾病治疗更加困难。糖尿病肾病的发病机制受多种因素影响,氧化应激的作用尤显突出,因为糖尿病肾病时氧化应激的存在,导致肾脏组织中抗氧化酶裂解氧化,所以抗氧化能力明显降低。白藜芦醇一种具有天然生物学活性物质的抗氧化剂,其毒副作用较低,既往有研究表明可改善糖尿病肾病大鼠的氧化损伤并提高抗氧化酶的活性,抑制损伤因子的活性[1~3],白藜芦醇可能通过影响氧化应激/NF-kB通路改善糖尿病视网膜病变发展[4]。本试验研究白藜芦醇通过多种机制改善糖尿病大鼠体内高血糖、肌酐、尿素氮产生保护治疗效应,并探讨其通过干预影响糖尿病肾病氧化应激反应而起到对肾脏保护效果。
1 材料和方法
1.1 实验材料
实验选用2月龄,体重(160±20)g,Wistar大鼠60只,均为雄性大鼠(购自长春亿斯动物实验中心)。适应性喂养1周后,随机进行分组;Ⅰ正常对照组;Ⅱ糖尿病模型组;Ⅲ白藜芦醇治疗组,每组20只。各组大鼠饲养环境一致,饮用水为自来水、饲料和垫料均已消毒。肾病组模型与白藜芦醇组模型禁食后一次性腹腔注射stz(溶于新鲜配制的0.1mol/L的柠檬酸缓冲液,pH4.5)60mg/mg。静脉采血测空腹血糖并测尿蛋白值,确定判断肾病模型建立达到成功。
1.2 实验方法
1.2.1 肾病模型建立后适应性喂养7d,白藜芦醇治疗组肾病糖尿病模型进行灌胃干预100mg/kg·d,其他两组灌胃等量生理盐水。分别在4w、8w、12w采血检测血肌酐尿素氮,并分别于4w、8w、12w末各取24h尿样标本测尿蛋白含量。
1.2.2 用化学比色对照法测MDA,T-SOD,GSH-PX,取12w末各模型组4只动物标本,麻醉状态下行肾脏切除术,制作肾皮质组织匀浆清夜。
1.2.3 HE染色肾脏组织病理观察,模型组各随机选4只动物,按4w、8w、12w末以50mg/kg苯巴比妥麻醉切除肾脏术,以观察各模型组肾小球系膜细胞,血管以及肾小球基底膜厚度和细胞外基质蓄积情况。
1.2.4 PAS检测观察肾脏组织糖原类物质。
1.2.5 免疫组织化学分析法镜下观察AFP、P53表达。
1.3 统计学方法
2 结果
见表1~3,图1~3。
表1 4周,8周,12周,各组大鼠血糖,肌酐,尿素氮测定
*与Ⅰ组比较,P<0.05,#与Ⅱ组比较,P<0.05。

表2 尿蛋白,4周,8周,12周测定
*与Ⅰ组比较,P<0.05,#与Ⅱ组比较,P<0.05。

表3 各组模型12周末氧化应激指标
*与Ⅰ组比较,P<0.05,#与Ⅱ组比较,P<0.05。
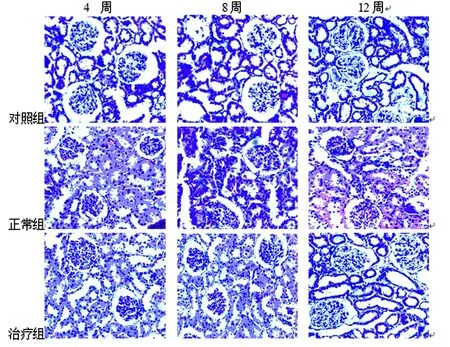
图1 模型病理组织HE染色切片镜下改变

图2 模型病理组织PAS染色切片镜下改变
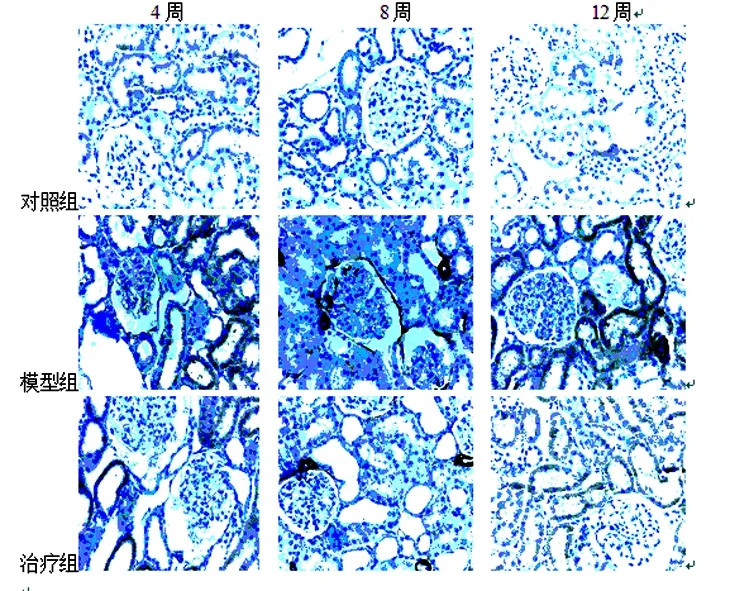
图3 模型病理组织免疫组织化学标记VPF镜下表达
3 讨论
白藜芦醇,又称芪三芬,存在于葡萄、桑椹、花生、虎杖等植物和果实中的多酚化合物,葡萄中含量最高,是一种天然抗氧化剂并具有生物学活性。实验已证明白藜芦醇对超氧阴离子有强烈抑制作用,具有羟自由基清除活性和抑制氧化剂的活性,目前研究表明,白藜芦醇可抑制氧化应激对糖尿病肾病肾脏起保护作用,但其作用机制没有较权威的深入研究。现有研究结果显示白藜芦醇通过保护膜脂从而保护细胞膜而起作用,增强机体抗氧化能力,且其抗氧化效果强于维生素E等微量元素,优点是副作用很小。白藜芦醇同时又抗炎、抗氧化、抗癌、调血脂,治疗心肌缺血等作用。本实验研究通过建立糖尿病肾病大鼠模型,观察肾功能和氧化应激个指标变化,对白藜芦醇减轻糖尿病肾病损伤作用进行探讨[5,6]。
糖尿病肾病是糖尿病病人最重要的合并症之一。随着生活水平提高、膳食习惯改变在中国发病率呈上升趋势,目前已成为终末期肾脏病的第二位原因,仅次于各种肾小球肾炎。由于存在复杂多变的代谢功能紊乱,发展到终末期肾脏病往往比其他肾脏疾病治疗恢复更加棘手。因此及时防治对于延缓糖尿病肾病的意义巨大。遗传因素、血流动力学异常、代谢异常、高血压、活性物质代谢异常都是糖尿病肾病的发病诱因。糖尿病肾病发病可通过肾小球滤过率改变,蛋白尿出现,持续蛋白尿,终末期肾衰改变等不同临床体征表现。临床治疗依据开展不同病期针对性治疗,控制血糖血压、终末期肾脏替代治疗、器官移植[7]。
氧化应激损伤导致肾脏血流动力学异常改变,表现为肾小球高灌注、高滤过、血流量、GFR升高,诱发肾组织局部糖代谢紊乱、非酶糖基化、多元醇通路激活、已糖胺通路代谢异常GBM增厚;细胞外基质蓄积,出现肾小球结节样病变和微血管玻璃样改变,并发生肾小球滤过膜蛋白屏障功能严重损害。氧化应激直接导致肾脏组织内的不饱和脂肪酸收到ROS攻击,产生丙二醛导致肾脏细胞膜的各项生理平衡严重破坏,生物膜通透性增加,血浆蛋白成分大量透过内皮细胞产生沉淀物,蓄积肾小球基底膜,并使其增厚;红细胞膜过氧化反应,降低膜的流动性,提高对内皮细胞黏附作用;脏成肾组织细胞线粒体DNA破坏。间接损伤发生于肾小球系膜细胞,如转录因子NF-kB和AP-1发生磷酸化后被活化,启动不同种细胞因子转录(内皮素-1、肿瘤坏死因子-a、单核细胞趋化蛋白-1)[8]。
通过本实验可以看到,糖尿病肾脏模型组MDA值高于正常对照组,白藜芦醇治疗组低于糖尿病肾脏模型组,糖尿病肾病模型组T-SOD、GSH-px低于对照正常组,白藜芦醇治疗组高于糖尿病肾病模型组。糖尿病肾病大鼠模型组存在明显的氧化应激损伤,白藜芦醇用药组,MDA含量降低,T-SOD活力、GSH-px活力上升,明显改善了应激损伤。
白藜芦醇治疗糖尿病肾病大鼠模型,与未治疗组相比,其氧化应激指标明显改观,提高T-SOD、GSH-px活性,抑制MDA含量,对肾脏氧自由基代谢起到了积极有效的调节作用,通过镜下观察细胞外基质糖原成分显著下降,达到改善肾内血流动力学、减少蛋白尿排出、抑制系膜细胞、成纤维细胞、巨噬细胞活性;改善滤过膜通透性使内生肌酐清除率下降等作用保护肾脏功能。观察模型组4w、8w、12w病理组织HE染色下肾小球单位改变,对照组肾小球单位均无特异性改变,肾小球单位完整,境界清楚。肾病模型组4w开始出现肾小球改变,镜下表现为毛细血管基底膜增厚,系膜细胞增生,简直细胞体积增大,呈弥漫性系膜增生性改变,到8w、12w镜下改变更加明显符合糖尿病肾病病理学特点,较典型改变时可出现出现细动脉玻璃样变及食酸性空泡样变。观察模型组4w、8w、12w大鼠肾脏病理组织PAS法染色下肾小球单位及糖原沉积性改变,如镜下所示对照组肾小球单位均无特异性改变,肾小球单位完整,境界清楚。很少有免疫球蛋白的沉积。肾病模型组4w开始镜下出现毛细血管基底膜增厚伴随连续的颗粒状沉积分布PAS反应阳性,系膜区呈边界清楚的颗粒状沉积,但沉积物强度较弱,系膜增宽(+),细胞中度增生,到8w末时肾脏病理组织镜下沉积物强度明显增高累及小于80%呈阶段性分布,到12w末时呈连续性弥漫性分布颗粒沉积面积大于80%。系膜细胞增生和系膜区糖原符合物的沉积也较突出,毛细血管团位于肾小囊内但血管腔变窄,间质细胞体积增大。治疗组组织镜下改变,4w毛细血管基底膜增厚出现非连续性颗粒状沉积分布,从8w镜下改变开始到12w镜下所见,基底膜增厚不明显,颗粒状沉积信号较弱可视为阴性表达。白藜芦醇干预情况显示,改善了肾小球基底膜的滤过作用,糖原沉积减少,达到了积极良好的干预效果。
由上可见,白藜芦醇本试验中糖尿病肾病大鼠模型起到了有效的干预修复效果,血清生化指标、肾功均得到积极改善,通过对氧化应激反应过程中MDA含量降低,T-SOD、GSH-px活力得到提高,免疫组化VPF表达情况改善了肾小球血管滤过功能,综合各方面实验结果证实,白藜芦醇通过有效抑制氧化应激而达到了保护肾脏功能的功效,而对糖尿病肾病联合多效配伍干预治疗也成为未来探索方向。
[1]张青.护理干预对糖尿病肾病患者生活质量的影响[J].黑龙江医药科学,2010, 33(2):53
[2]赵芳芳,王季猛,程灿.糖尿病肾病发病机制研究进展[J]. 现代生物医学进展,2010,10(24):4796-4798
[3]张晓波,姚海涛,杨子安,等. 有机铬对实验性糖尿病大鼠胰腺保护作用的观察[J].黑龙江医药科学,2004,27(5):1-2
[4]张笃贞,王大丽,杨笑天,等.白藜芦醇对实验性糖尿病大鼠视网膜氧化应激/NF-κB通路的干预作用[J]. 黑龙江医药科学,2014,37(1):105-107
[5]郜海燕,于震宇,陈杭君,等.白藜芦醇功能和作用机理研究进展[J].中国食品学报,2006,6(1):411-416
[6]姜丽,胡明燕.白藜芦醇的研究进展[J]. 安徽农业科学, 2013,41(19):8427,8436
[7]丁洪成,程长明,廖勇敢.白藜芦醇对糖尿病大鼠肾脏内氧化应激的影响[J].成都中医药大学学报, 2009,32(1):62-65
[8]郑美玲,樊均明.氧化应激对糖尿病肾病时细胞、细胞外基质及血管通透性的影响机制[J]. 中国组织工程研究与临床康复,2007,11(25):4988-4991
张志全(1980~)男,黑龙江佳木斯人,在读硕士研究生。
刘中柱(1964~)男,黑龙江佳木斯人,学士,教授,硕士研究生导师。E-mail:liuzhongzhu64@163.com。
R285.1;R287.1
A
1008-0104(2015)01-0088-03
2014-05-10)
