铁粉吸氧腐蚀系列实验的设计及应用
2015-06-18徐泓朱敏魏明贵
徐泓+朱敏+魏明贵
摘要:依据铁的吸氧腐蚀原理,使用铁粉、碳粉、食盐水等试剂和常规玻璃仪器以及数字实验技术,开发了空气中氧气含量的测定、铁氧化过程的能量变化、铁粉的吸氧腐蚀、影响化学反应速率因素等系列实验设计,并应用于教学实践,可充分发挥吸氧腐蚀的教育价值及其教学功能。
关键词:铁粉;吸氧腐蚀;系列设计;实验探究
文章编号:1005–6629(2015)4–0063–04 中图分类号:G633.8 文献标识码:B
吸氧腐蚀是生活中最常见的金属腐蚀形式,其存在一方面对生活中金属资源(尤其是铁)造成大量浪费,在建筑、医疗等许多方面给人类带来很多不利的影响;另一方面利用吸氧腐蚀原理研发的食品脱氧剂、暖宝宝等产品,又给人类生活带来了安全和便捷。中学化学教学中有很多内容涉及吸氧腐蚀,本文从正面、积极的视角,利用铁的吸氧腐蚀开发出空气中氧气含量的测定、铁氧化过程中的能量变化、铁粉的吸氧腐蚀、影响化学反应速率因素等几个系列实验,通过教师在教学中的实践应用,充分发挥这一教学资源的教育价值和实验教学的功能。
1 空气中氧气含量的测定
利用红磷燃烧测定空气中氧气含量的实验一直是我国初中化学教材中的经典实验,但该实验在原理上由于当红磷在密闭容器中不再燃烧时,仍会有3.45%~7.6%的氧气残留[1,2],即红磷燃烧不能完全耗尽空气中的氧气;在操作上由于当燃着的红磷在伸入瓶中的一瞬间,瓶内空气膨胀,会排出相当一部分空气,影响测量的科学性和准确性[3]。而文献显示[4,5,6]:以还原铁粉为主的脱氧剂,短时间内可除去密闭容器中氧气,使食品处于无氧状态(O2浓度0.01%以下),说明铁的吸氧腐蚀几乎能耗尽密闭装置中的氧气。因此,可利用脱氧剂吸收氧气的原理,即铁的吸氧腐蚀设计实验以测量空气中氧气含量。
1.1 实验设计及过程
连接装置如图1所示,检验气密性。实验时先将滤纸裁成长方形,大小以刚好能附着在250mL广口瓶内侧一圈为宜,用胶头滴管吸取约4mL 1 mol/L NaCl溶液使滤纸浸润并粘附在广口瓶内侧。烧杯中倒入与广口瓶净容积相当的水,打开止水夹,用洗耳球使导管内充满水,并夹紧止水夹。称取2.0g还原铁粉、2.5g活性炭粉(本实验使用的是上海申鹤化学品有限公司生产的分析纯还原铁粉和启东申鹤化学品有限公司生产的化学纯活性炭,下同),并搅拌均匀。将广口瓶横放,一边转动,一边将铁粉和碳粉混合物倒入广口瓶内壁,尽可能使其较均匀地附着在广口瓶内壁的滤纸上,并迅速塞紧瓶塞。约4分钟后打开止水夹,会看到水迅速进入广口瓶,稍后可观察到烧杯内水的体积减少约1/5,可得出氧气约占空气体积的1/5。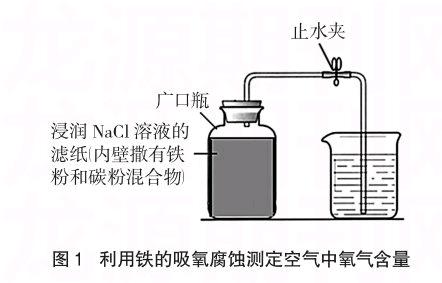
1.2 实验优点
(1)原理科学,利用铁的吸氧腐蚀能几乎耗尽体系中的氧气的原理。
(2)装置简单,与现行初中化学教材中红磷燃烧实验装置基本相似。
(3)原料易得,都为中学化学实验中常见药品,且用量少。
1.3 应用说明
本实验可应用于初中化学“空气中主要成分”相关内容的教学中,可用于演示实验,也可用于学生课后探究(自制食品脱氧剂)。教学中可先通过食品脱氧剂创设教学情境,说明脱氧剂的主要成分和作用,以此开展实验教学引导学生得出空气中氧气含量的结论,最后用铁的生锈简化其原理为[7]:4Fe+3O2=2Fe2O3,既不违背其科学性,也符合学生认知水平。
2 铁的氧化过程中的能量变化
能量观是中学化学的核心观念之一,通过放热反应和吸热反应说明化学反应中伴随能量变化是高中化学的必修内容。现行教材中的有关放热反应是利用金属镁或铝与盐酸反应实验开展教学的,现象虽较明显,但实验的趣味性不强。笔者利用还原铁粉、碳粉组成的吸氧腐蚀系统设计如下实验。
2.1 实验设计及过程
称取2.0g还原铁粉、2.5g活性炭粉,搅拌均匀,用滤纸包好。滴入约1mL 1 mol/L NaCl溶液使滤纸包润湿,此时用手轻轻搓揉滤纸包,明显感觉滤纸包发烫。用温度计或温度传感器测量得到随时间变化而温度发生变化的曲线,如图2(笔者实验时环境温度即起始温度为20.8℃)所示,最高温度可接近70℃。
2.2 实验优点
(1)操作简单,现象明显,尤其是温度变化给学生较强的冲击力。
(2)数字化实验的应用使实验从定性到半定量化。
(3)密切联系生活,能说明暖宝宝的工作原理,引导学生选择使用合格产品以防止使用过程中可能造成的烫伤。
2.3 应用说明
本实验可应用于高中化学必修2模块中有关“化学反应与能量变化”的教学,可用于演示实验,也可用于学生课后探究(自制“暖宝宝”)活动。教学中可从生活中暖宝宝的使用引入,利用上述实验帮助学生感知放热反应及其应用,同时通过温度传感器帮助学生初步认识从定性到半定量的研究方法,加深对铁与氧气、水反应过程中能量变化的认识:2Fe(s)+3/2O2(g)+xH2O(l)=Fe2O3·xH2O(s),ΔH<0。其中图2中A点是对滤纸包轻轻搓揉后,使结块的混合物松散增大了反应物接触面积所致。若不断搓揉滤纸包,曲线会更不规则,但能使反应温度上升更高。本实验还可渗透情感态度价值观的教育。
3 铁粉的吸氧腐蚀
吸氧腐蚀是学生学习过程中的一个难点,尤其是对在中性或弱酸性条件下,由铁、碳组成的原电池的正极电极反应难以理解,大多数学生常常认为是H2O中H+参与得电子,即发生析氢腐蚀。为增强实验的直观性,突出氧气参与反应这一特点,设计如下实验。
3.1 实验设计及过程
装置如图3所示,用胶头滴管吸取约4mL 1 mol/L NaCl溶液使滤纸浸润并粘附在广口瓶内侧。称取2.0g还原铁粉、2.5g活性炭粉,搅拌均匀,倒入广口瓶并迅速放入氧气传感器探头并塞紧瓶塞,轻轻转动广口瓶,使铁粉和碳粉混合物尽可能均匀附着在广口瓶内壁。同时开始采集氧气含量数据,约3分钟后瓶内氧气含量降至0.5%以下,约5~6分钟即可使瓶内氧气含量降至0.1%,10分钟左右降为零,随时间变化氧气含量变化如图4中带“▲”的曲线。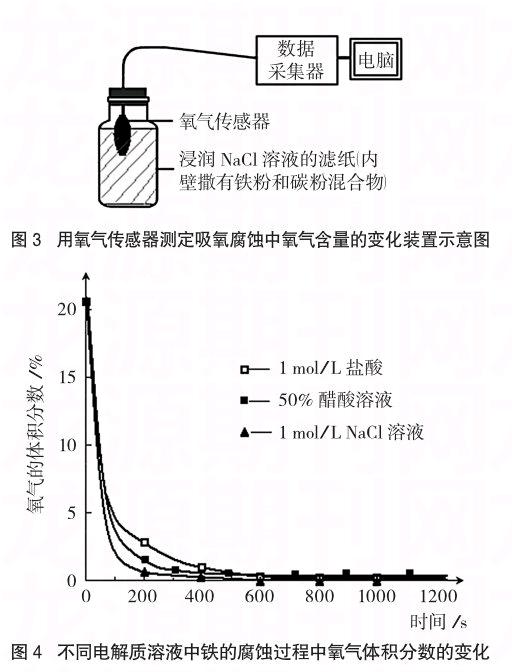
3.2 实验优点
(1)现象直观,便于学生认识到氧气在中性或弱酸性条件下均参与了正极反应,即发生:O2+2H2O+4e-=4OH-。
(2)探究味更浓,有利于学生在实验中学会控制变量,如铁粉和碳粉不变,仅改变电解质溶液,探究不同条件下铁的腐蚀。
(3)趣味性更强,让学生感受数字实验带来的便捷。图4曲线显示,无论是在中性介质(NaCl溶液)中,还是弱酸性介质(稀盐酸或稀醋酸)中,装置内氧气含量均减少,说明铁均可以发生吸氧腐蚀。
3.3 应用说明
本实验可应用于高中化学选修4“化学反应原理”模块中有关“金属的腐蚀”教学,可用于课堂演示或学生课后的探究活动,如用1 mol/L盐酸和50%醋酸溶液代替氯化钠溶液同样显示氧气含量下降(如图4中分别带“□”和“■”的曲线),且用压强传感器测出此时瓶内压强减小,排除氧气含量下降并非由于产生H2所致,说明在该酸性条件下铁仍然以发生吸氧腐蚀为主。还可以继续探究在Na2CO3溶液、NaHCO3溶液等其他电解质溶液中是否会加快金属的腐蚀?是否也会发生吸氧腐蚀?多大pH条件下主要发生析氢腐蚀。实验有助于帮助学生理解中性或弱酸性条件下金属发生吸氧腐蚀这一教学难点,让学生体会实验技术的进步对于化学学科学习和发展的促进作用。
4 影响化学反应速率的因素
利用上述3.1实验中铁的吸氧腐蚀实验还可进一步探究影响化学反应速率(铁的腐蚀速率)的因素。
4.1 实验设计及过程
先完成上述3.1实验,得到如图5中曲线①(横坐标为时间,纵坐标为氧气含量)。其他条件不变,将称量并混合好的铁粉、碳粉用滤纸包好,以减小其与瓶中空气的接触面积,用1 mol/L NaCl溶液浸润滤纸包再放入相同广口瓶中,同时开始采集氧气含量数据,得到如图5中曲线②。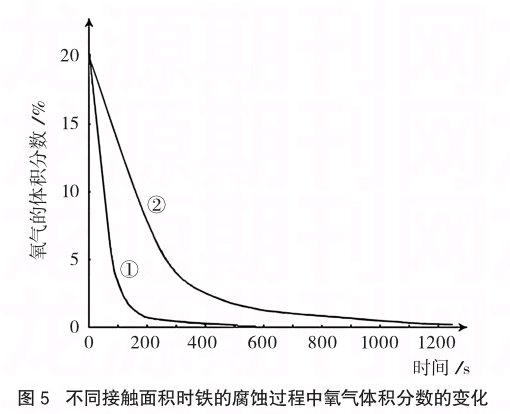
4.2 实验优点
(1)图示形式直观,有助于学生感受到接触面积和氧气浓度等因素对铁的腐蚀速率的影响,进而形成相关认知。
(2)有利于体现宏观、符号、曲线等表征元素在本节内容教学中的价值,加强学生对非连续文本的理解。
(3)有利于教师在教学中应用POD(预测-观察-解释)教学策略,即先让学生预测不同接触面积时铁发生吸氧腐蚀时氧气含量的变化快慢,再通过数字实验观察现象,最后解释并形成结论,同时渗透控制变量的研究方法。
4.3 应用说明
本实验可应用于高中化学选修4“化学反应原理”模块中有关“化学反应速率的影响因素”教学。首先让学生预测在铁粉和碳粉混合物以不同方式放入瓶内后,瓶中氧气含量的变化曲线;再借助于数字化实验手段形成图形并对比;最后进行分析解释,得出结论。同时,同一曲线的变化趋势也体现了氧气浓度对腐蚀速率的影响,即随反应时间的增长,曲线越来越平缓,说明反应速率越来越慢。
此外还可以通过上述实验设计编制相应探究性试题,以电化学、化学反应速率、金属性质、化学反应能量变化等知识为考查内容,突出对学生实验能力和科学探究能力的考查。已有很多老师编制出相关内容的优质试题[8,9],其中2014年安徽省高考理综第28题在借鉴PISA试题编制理念的基础上,以金属的腐蚀为情境[10],设计的科学探究题较为经典。
参考文献:
[1]章永军.利用传感器分析空气中氧气含量测定的误差[J].化学教与学,2011,(7):92~93.
[2]杨承印等.密闭容器中残余氧含量测定的思考[J].化学世界,2010,(11):652~655.
[3]朱华英,刘怀乐.空气里氧气含量的测定实验值得改进[J].教学仪器与实验,2005,(7):25.
[4]吴建文等.脱氧剂量的研究和应用[J].食品科学,2002,(5):148.
[5]赖轩.脱氧剂在食品保鲜中的作用机理、应用与开发[J].广东科技,2008,(5):60.
[6]徐泓.利用“食品脱氧剂”测定空气中氧气含量的系列设计[J].化学教育,2010,(11):71~72.
[7] Just Breathe: The Oxygen Content of Air [J]. Journal of Chemical Education,2001,(4):512A~512B.
[8]谭宗俊,张莉.钢铁吸氧腐蚀速度的探究题[J].化学教学,2010,(9):79~80.
[9]但世辉,李斌.一道关于“铁的吸氧腐蚀”的原创题[J].化学教学,2012,(5):61~63.
[10]夏建华. PISA科学评价对编制化学科学探究题的启迪[J].化学教学,2014,(9):67.
